2010年肺癌治療領域10大進展
劉 喆
(首都醫科大學附屬北京胸科醫院腫瘤內科,北京 101149)
在2010年的肺癌治療領域,隨著一些臨床實驗結果的揭曉,出現了新的數據及結果,這些積極的循證醫學的結果必將在今后影響肺癌診治的現狀。綜合國外各個相關協會的推薦結果,總結2010年肺癌治療領域的10大進步,倒序排列如下。
1 2010年肺癌治療領域的10大進步
第10位,在肺癌立體定向的放療方面,有更多SBRT(體部立體放射治療)的數據支持。對有些肺癌患者來講,SBRT的治療相當于胸外科的肺楔形切除手術的效果。
這是源于發表在2010年2月JCO上的文章[1]。2003~2008年8月在美國William Beaumont醫院選擇124例無法接受肺葉切除的T1-2N0的NSCLC患者參加了研究,69例患者接受了肺楔形切除手術,58例(95%無法手術,5%拒絕手術)患者接受了圖像引導的SBRT治療。接受SBRT治療的患者在局部病變復發率、PFS以及OS等指標上取得了比肺葉楔形切除的患者相當或更好的數據。而作者認為這項研究也有幾項不足之處:SBRT組是一項前瞻性的Ⅱ期研究,而手術組資料是回顧性的,而且兩組患者在幾項臨床特征上未達到完全匹配,接受手術的患者分期是病理分期,而SBRT組是臨床分期等原因。但是,這項研究的結果顯示,隨著計算機技術和放療設備及技術的進步,精準的圖像引導的體部立體放射治療對于特定的肺癌人群的局部治療療效可能會達到與胸外科手術媲美的結果。
第9位,初步數據顯示索拉非尼(sorafenib Nexavar)可能對KRAS突變的NSCLC患者有效,而這部分患者往往對EGFR-TKI的治療效果不理想。
約10%~30%的非小細胞肺癌存在KRAS突變,其中以吸煙者為主而且預后不佳;RAS信號通路位于細胞表面的EGFR信號通路的下游,KRAS的突變可以阻斷EGFR信號的傳導,KRAS可能參與EGFR-TKI的耐藥。眾所周知,美國M.D.Anderson腫瘤中心發起的BATTLE臨床試驗[2],即利用粗針穿刺的病理組織,進行有關EGFR、KRAS、VEGF、Cycling D的檢測,并根據檢測結果讓患者分別接受厄羅替尼、索拉非尼、凡德他尼以及厄羅替尼聯合貝沙羅汀的治療(見圖1)。索拉非尼對有KRAS突變的NSCLC患者有較好的療效。Egbert F.S.在2010年5月JTO雜志發表的索拉非尼對有KRAS突變的晚期NSCLC患者治療的文章中報道了10例接受了1~4線治療的NSCLC患者,9例接受索拉非尼的患者疾病得到控制,僅1例疾病進展[3]。上述結果初步顯示索拉非尼對KRAS突變的NSCLC患者治療的療效。
第8位,德國勃林格殷格翰公司的產品Afatinib(BIBW-2992,Tomtovok或Tovok,)是第二代EGFR-TKI不可逆的抑制劑,對EGFR突變的患者有肯定的療效。
在去年公布的一項Afatinib治療既往接受過化療和第一代EGFR-TKI治療的晚期NSCLC患者的IIB期臨床試驗結果(見圖2)。Afatinib顯示了第二代EGFR-TKI及與EGFR受體不可逆結合的優勢,在經過驗證后的部分緩解率PR(7%:0.5%)及疾病控制率(51%:18%)上顯示了優勢;雖然在總生存OS上未得到統計學的差異,但在無疾病生存期PFS上取得了3.3月對1.1月的優勢;Afatinib初步顯示其作為新一代EGFR-TKIs的特點[4]。當然,后續的臨床試驗包括一線治療EGFR基因突變的優勢人群的臨床試驗正在進行中。

圖1 BATTLE臨床試驗設計流程
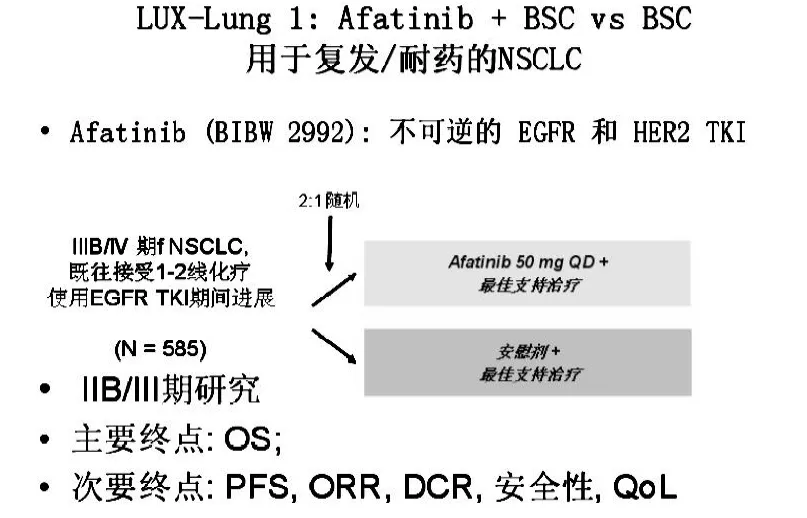
圖2 Afatinib的LUX-Lung1 臨床研究的流程圖
第7位,針對c-MET口服小分子的抑制劑如ARQ-197和PF-299顯示了對肺癌治療的初步的效果。
目前,T790M突變和Met的活化與EGFR基因敏感性突變的NSCLC患者出現EGFR-TKI類藥物治療后的耐藥密切相關。在一項隨機的Ⅱ期臨床試驗比較c-MET抑制劑ARQ-197聯合特羅凱或安慰劑治療既往接受過化療(但未使用過EGFR-TKI)的167例晚期NSCLC患者的臨床試驗中[5],ARQ-197顯示了PFS的延長和OS延長的趨勢。另一個類似的藥物PF-299804在一項包含188例患者與特羅凱頭對頭比較的臨床試驗中顯示了優于特羅凱的勢頭;目前,擴大人群的臨床試驗正在進行中。見圖3。
第6位,還是有關c-MET抑制劑即Met-MAb:作用于Met的單克隆抗體的Ⅱ期臨床試驗的結果。見圖4。
在一項美國發起有128例患者參加的Met-MAb聯合特羅凱與Met-MAb聯合安慰劑比較既往接受過1~2線化療(未接受過EGFR-TKI)的晚期NSCLC臨床試驗中,60%為男性,90%為高加索人群,25%為鱗癌,16%為不吸煙人群,大多數患者提供了病理標本。在分層分析中發現,在免疫組化Met高表達的這部分患者有更好的PFS和OS;而在免疫組化Met低表達的這部分患者似乎應用Met-Mab的結果更差[6]。Met-Mab的初步結果似乎揭示了臨床這組特殊人群未來治療的選擇。
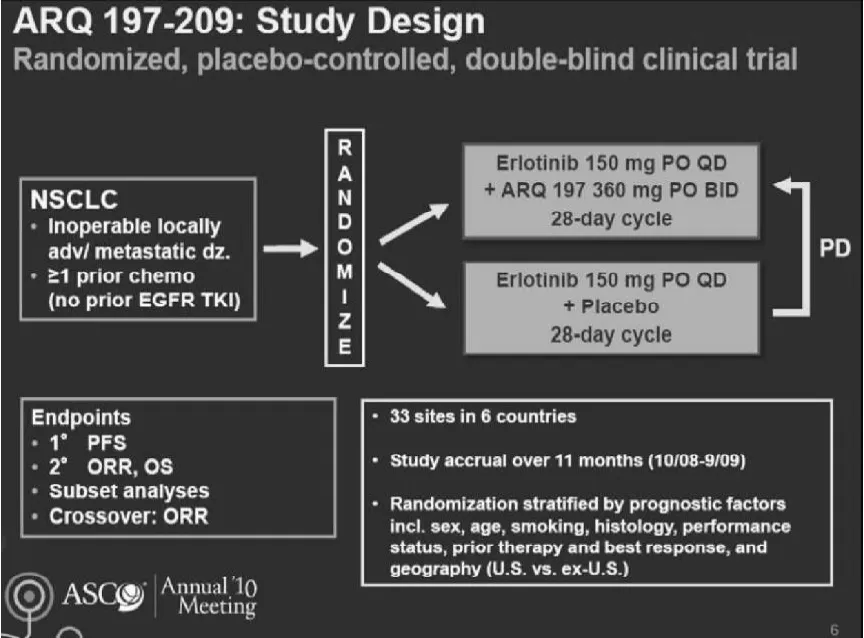
圖3 c-MET口服小分子的抑制劑與特羅凱聯合治療晚期NSCLC患者的流程圖
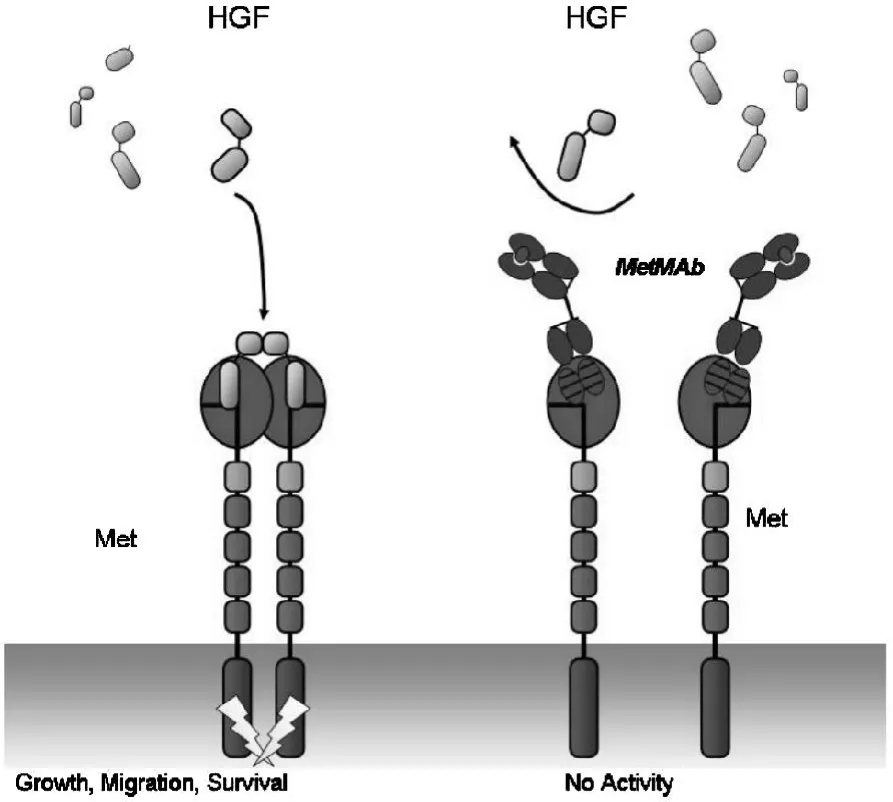
圖4 Met-Mab的結合位點模式圖
第5位,2010年出現了更多的數據支持維持治療的理念。
目前NSCLC維持治療主要用于一線治療后至少穩定的患者,主要有兩種維持治療的模式:(1)將原方案中的一種藥物作為維持治療的藥物。(2)使用一線治療中未曾用過的藥物作為維持治療藥物;美國FDA批準了力比泰和特羅凱可以作為維持治療的藥物選擇。一項由法國Dr.Perol發起的臨床試驗將834例接受4周期一線健擇順鉑化療后病情穩定的464例患者按照1:1:1的比例分為健擇維持治療、特羅凱維持治療和安慰劑對照三組。入組人群中38%為不吸煙者,2/3病理為腺癌。結果顯示健擇和特羅凱維持治療同安慰劑比較在PFS上有顯著性優勢;健擇在降低疾病進展風險上比特羅凱更有優勢(45%:19%)[7]。
第4位,EML4-ALK融合基因(echinoderm microtubule associated protein like 4 anaplastic lymphoma kinase)的TKIs PF-02341066(Crizotinib)Ⅱ、Ⅲ期臨床試驗。
眾所周知,肺癌最相關的誘因是吸煙。但全球肺癌患者約10%為終生不吸煙或者小于100支煙。在亞洲,不吸煙的患者占30%~40%。不吸煙的肺癌患者的病理類型及腫瘤的生物學特性均與吸煙的肺癌不同。在不吸煙的這組特殊肺癌患者中存在的EGFR突變、EML4-ALK表達的分子信號通路的發現,給肺癌的這一特殊亞組的臨床研究注入了新的活力。
EML4-ALK融合基因的表達約占NSCLC患者的3%~7%,對亞裔患者,這部分比例可能還要大一些,EML4-ALK表達陽性的患者對EGFR-TKI的治療往往是無效的。2010年由韓國Dr.Bang教授牽頭的EML4-ALK抑制劑PF-02341066(Crizotinib)治療EML4-ALK表達陽性的NSCLC患者(大多數患者既往接受過化療)的Ⅰ期臨床試驗中,Crizotinib取得了總治療反應率(ORR)為57%以及87%的疾病控制率(圖5)[8-9]。正是由于Ⅰ期臨床試驗的療效,美國FDA直接批準該藥進行Ⅲ期臨床試驗(PROFILE1005和1007),這也反映在目前靶向藥物治療的時代,傳統的藥物審批和藥物臨床試驗程序已經受到挑戰。Crizotinib對既往接受過不同治療方案ALK陽性的NSCLC患者的治療效果疾病控制率DCR(截止至8周時,CR+PR+SD):87%(95%CI:77.93%)。

圖5 CrizotinibⅠ期臨床試驗的結果
第3位,2010年ASCO報道的TORCH研究清楚的表明靶向藥物與標準化療方案在使用的先后順序上對結果的影響非常重要。
在一項由未經選擇的歐洲和北美人群參加的Ⅲ期臨床試驗中,患者被隨機分到一線GC方案化療(標準治療組)和一線特羅凱治療(試驗組)兩組,一線治療后病情進展,則進入二線治療。二線治療將兩組治療藥物交換,即標準治療組一線GC方案化療后接受二線特羅凱的治療,試驗組一線特羅凱治療后接受二線GC方案化療(圖6)[10]。因為初步數據分析顯示試驗組患者在客觀有效率、PFS、總生存等數據上明顯比標準治療組差,所以此項研究被中途叫停了。試想此項研究如果事先篩選患者或者此項研究在亞裔人群中進行,可能結果會不同,此項試驗的結果進一步證實了靶向藥物治療是有其特定的優勢人群的。

圖6 TORCH研究設計的流程圖
第2位,對于有EGFR突變的晚期NSCLC患者,一線治療采用EGFR-TKI相對于傳統標準化療方案有更長的PFS和更好的治療反應率RR。來自日本研究者類似于IPASS研究的資料證實對于EGFR有突變的晚期NSCLC患者一線接受吉非替尼治療相對于化療有更好的PFS和延長總生存的趨勢[11]。在這篇發表在新英格蘭醫學雜志的文章中,日本學者篩選了EGFR活性突變的230例患者,隨機分為一線吉非替尼治療和一線TC方案化療;雖然大部分患者在一線治療失敗后又交叉到其他治療中,結果顯示在PFS上,一線吉非替尼治療組比化療組患者有更長的時間(P值有顯著性差異),OS有延長的趨勢但P值未達到統計學差異。
亞裔人群EGFR的突變率是其他人種的3倍,所以近期有很多類似結果的研究證實有EGFR突變的晚期NSCLC患者,一線治療采用EGFR-TKI相對于傳統標準化療方案有更好的臨床結果。
第1位,在肺癌的篩查方面,美國NCI發起的一項全國肺癌篩查研究(NLST)顯示:在肺癌高危人群的篩查方法中,使用低劑量螺旋CT組患者的生存比常規X線胸片組患者提高20%。

圖7 肺癌篩查研究(NLST)流程圖
這項研究始于2002年,共包含了53000名既往有吸煙史(30包年)的55~75歲的患者,隨機接受平掃的低劑量螺旋CT(未增強的)和常規X線胸片的檢查,每年一次,連續檢查3年(圖7)。追蹤隨訪的結果子顯示,CT篩查組中有354例患者死于肺癌,而X線胸片組中有442例患者死于肺癌,CT篩查組死于的患者比X線胸片組低20.3%;另外CT篩查組患者的死亡率較(除肺癌外也包括)其他各種原因疾病的死亡率低7%[12]。
2 討論
本項研究結果提示對于年齡在55~75歲的高危人群(每年30/包),常規的低劑量螺旋CT檢查,相對于普通X線胸片檢查,更能發現早期肺癌患者。降低肺癌患者的死亡率和早期肺癌的篩查一直是大家感興趣的研究領域,從各個專業協會評出的2010年腫瘤領域的突破或進步都包括此項研究的結果,也說明專業研究人員對肺癌篩查的積極結果的期待。此項研究提示應該進一步研究低劑量螺旋CT作為肺癌篩查的方法的長期結果;除此之外,大家的共識是為更好的延長肺癌患者的生存,最主要的還是需要在肺癌治療領域上的突破,不管是在新藥的研發還是現有治療方法學上的進步方面,治療領域的進步可能才能帶給患者更長的生存。
縱觀2010年肺癌領域的突破或進步,不難發現,除一項研究與肺癌早期篩查有關,另一項研究與放療技術的進步有關外,10項中的8項進步,都與肺癌的藥物治療相關,特別是與分子靶向藥物相關。這也從一個側面說明當今肺癌和腫瘤藥物治療的熱點;隨著對腫瘤分子信號傳導通路研究的深入,會有越來越多的分子靶向藥物進入臨床研究,而這種與傳統細胞毒藥物作用機制完全不同的分子靶向藥物(多數更是口服的藥物),會對有些特殊病理類型的肺癌患者有效;雖然目前化療仍是晚期肺癌治療的基石,但如何讓現有的治療方法與分子靶向藥物有機的組合來最大限度的發揮藥物的治療作用,是擺在肺癌基礎和臨床研究工作者面前的緊迫任務。相信隨著更多前瞻性臨床研究數據的獲得,在肺癌治療領域會帶來更多的意外和驚喜;也期待今年會有更多的突破帶給肺癌治療領域的臨床醫生,造福肺癌的患者。
[1] Grills IS,Mangona VS,Welsh R,et al. Outcomes after stereotactic lung radiotherapy or wedge resection for stage I non small-Cell lung cancer[J]. J Clin Oncol,2010,28(6):928-935.
[2] Kim ES,Herbst RS,Lee JJ,et al. Phase Ⅱ randomized study of biomarker-directed treatment for non-small cell lung cancer(NSCLC):The BATTLE(biomarker-Integrated approaches of targeted therapy for lung cancer elimination)clinical trial program[J]. J Clin Oncol,2009,27(15):8024.
[3] Smit EF,Dingemans AC,Thunnissen FB,et al.Sorafenib in patients with advanced non-small cell lung cancer that harbor k-Ras mutations[J].J Thor Oncol,2010,5(5):719-720.
[4] Miller VA,Hirsh V,Cadrane J,et al. Phase Ⅱb/Ⅲ double-blind randomized trial of BIBW 2992,an irreversible inhibitor of EGFR/HER1 and HER2+ best supportive care(BSC)versus placebo+ BSC in patients with NSCLC failing 1-2 lines of chemotherapy and erlotinib or gefitinib(LUX-Lung1)[J] .Annals of Oncology,2010,21(8):1-12.
[5] Schiller JH,Akerley WL,Brugger W,et al. Results from ARQ 197-209:a global randomized placebo-controlled phase Ⅱ clinical trial of erlotinib plus ARQ 197 versus erlotinib plus placebo in previously treated EGFR inhibitor-naive patients with locally advanced or metastatic non-small cell lung cancer(NSCLC)[J]. J Clin Oncol,2010,28(15):7502.
[6] Spigel D,Ervin T,Ramlau R,et al. Randomized multicenter doubleblind placebo controlled phase Ⅱ study evaluating MetMAb,an antibody to met receptor,in combination with erlotinib,in patients with advanced nonsmall cell lung cancer[J]. Ann Oncol,2010,21(9):viii7.
[7] Perol M,Chouaid C,Milleron BJ,et al. Maintenance with either gemcitabine or erlotinib versus observation with predefined second-line treatment after cisplatin-gemcitabine induction chemotherapy in advanced NSCLC:IFCT-GFPC phase Ⅲ study[J]. J Clin Oncol,2010,28(15):7507.
[8] Bang Y,Kwak EL,Shaw AT,et al. Clinical activity of the oral ALK inhibitor PF-02341066 in ALK-positive patients with non-small cell lung cancer(NSCLC)[J]. J Clin Oncol,2010,28(15):53.
[9] Kwak EL,Bang YJ,Camidge DR,et al. Anaplastic lymphoma kinase inhibition in non-small-cell lung cancer[J]. N Engl J Med,2010,363(7):1693-1703.
[10]Gridelli C,Ciardiello F,Feld R,et al. International multicenter randomized phase Ⅲ study of first-line erlotinib(E)followed by second-line cisplatin plus gemcitabine(CG)versus first-line CG followed by secondline E in advanced non-small cell lung cancer(aNSCLC):the TORCH trial[J]. J Clin Oncol,2010,28(15):7508.
[11]Maemondo M,Inoue A,Kobayashi K,et al. Gefitinib or Chemotherapy for Non Small-Cell Lung Cancer with Mutated EGFR[J]. N Engl J Med,2010,362(3):2380-2388.
[12] National Lung Screening Trial Research Team. The National Lung Screening Trial:Overview and Study Design[J]. Radiology,2011,258(1):243-253.

