硫酸鋇比濁法測定皂角多糖修飾物中硫酸基的研究
張亞男
(泰山學院化學與環境科學系,山東 泰安 271021)
多糖是生物有機體內普遍存在的一類生物大分子,既以游離的形式參與生命過程,又與蛋白質、肽及脂質等組成聚合物的形式;它不僅參與組織細胞骨架的構成,而且是多種內源性生物活性分子的重要組成成分;它在生理機能的平衡與穩定過程中發揮重要的調節作用,同時廣泛參與細胞的各種生命活動而產生多種生物學功能[1-2].某些植物多糖特別是其修飾物具有抗血栓、調節血脂、抗腫瘤、抗病毒、增強細胞免疫和機體免疫功能、抗氧化、對機體細胞的保護等作用[3-10].活性多糖的研究已成為當今研究的一個熱點,它的重要特征是在多糖鏈上具有硫酸基,而且其活性與分子中硫酸基的含量有著直接關系,硫酸基含量越高,其抗HIV病毒的作用越強[11].因此,準確測定硫酸基含量是十分重要的.
1 實驗部分
1.1 儀器與試劑
紫外分光光度計,PHAMACIA UV2000.
硫酸基標準儲備液:精密稱取105℃干燥至恒質量的Na2SO488.6 mg溶于1mol/L的鹽酸中(SO24-濃度為0.6 mg/mL);明膠:分別配制成0.25%、0.50%、0.75%的溶液,冷藏保存;氯化鋇:1 g氯化鋇溶于100 mL明膠溶液中;三氯乙酸:2%、3%、5%的水溶液.
1.2 實驗方法
通過鹽酸水解從皂角多糖修飾物中釋放硫酸基,與BaCl2生成硫酸鋇,SO24-含量與其吸光度呈線性關系,用分光光度計在360nm處,測定其吸光度值,計算出硫酸基的含量.以線性關系相關系數和回收率為指標考察試劑用量和水解條件對檢測方法的影響,確定最優的實驗條件,確定硫酸鋇比濁法檢測皂角多糖硫酸基含量的準確性.
1.2.1 皂角多糖修飾物樣品(以下簡稱樣品)的處理
稱取樣品100 mg,用1 mol/L HCl溶液(鹽酸濃度為考察條件之一)溶解,于100℃水浴中水解,冷卻后,加鹽酸溶液補至刻度線,用濾紙過濾,除去不溶物質,即得粗樣品,保存備用.
1.2.2 紫外光譜的測定
取Na2SO4標準品和樣品溶液各0.2 mL,加三氯乙酸溶液3.8 mL和氯化鋇溶液1mL,將其混勻,進行紫外光譜測定.結果表明,Na2SO4和樣品均在360nm處有最大吸收峰.
1.2.3 標準曲線的繪制
準確吸取標準Na2SO4標準溶液0.02mL,0.06mL,0.08mL,0.10mL,0.12mL,0.14mL,0.16mL,0.20mL,以鹽酸溶液補至0.2mL,以0.2 mLHCl溶液作為空白,加入三氯乙酸3.8 mL及氯化鋇溶液1.0 mL,搖勻,室溫靜置15 min,于360 nm測吸光度A1;以1.0 mL明膠溶液代替氯化鋇溶液,測吸收度A2;以硫酸基質量濃度(μg/mL)為橫坐標,吸光度(A1-A2)為縱坐標,得標準曲線,確定線性范圍及線性關系.其中每點做三個平行樣品,取平均值.
1.2.4 回收率試驗
精密吸取標準儲備液和樣品溶液按比例搖勻,取0.15ml按硫酸基含量測定方法測定SO2-4含量,計算回收率及相對標準偏差RSD%[12].
2 結果與討論
2.1 明膠濃度的影響
通過繪制Na2SO4與不同濃度明膠混合反應的標準曲線并且測定回收率,考察明膠濃度對線性關系的影響[13-14],確定硫酸比濁法中適宜的明膠濃度.
按標準曲線繪制方法操作,控制C(SO2-4)在0~60μg/ml(HCl補足至0.5 ml),3%三氯乙酸加入量3.5ml,分別用0%(超純水代替)、0.25%、0.5%、0.75%的明膠配制的1%的BaCl2加入量1ml.標準曲線檢測結果見表1,不同濃度明膠的回收率結果見表2.
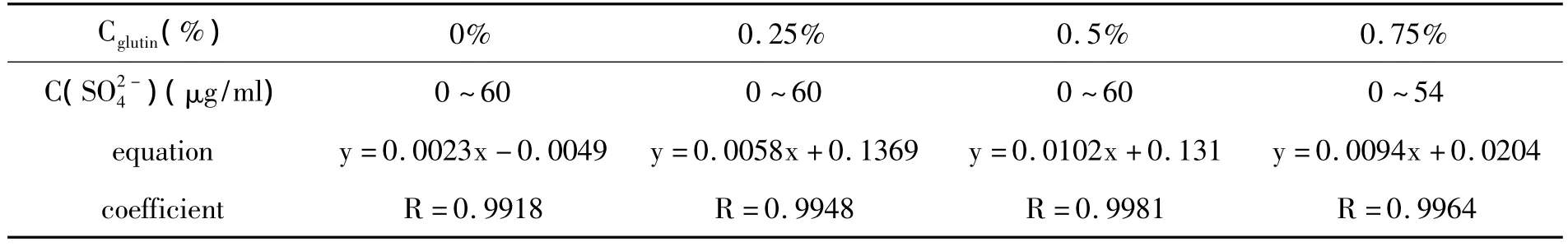
表1 不同明膠濃度的線性關系考察結果

表2 不同濃度明膠的回收率
由表1可以看出明膠濃度對線性關系影響很小,去除相關系數最小的0%的明膠,其他濃度范圍內,標準曲線線性關系良好,相關系數R都高于0.994.用回收率考察明膠的影響結果(表2)可以看出0.25%的明膠線性關系雖然很好,但是平均回收率非常低.明膠濃度為0.5%和0.75%的標準曲線線性關系和回收率都比較好,其中明膠濃度為0.5%時平均回收率為98.47%,RSD%為3.42%;明膠濃度為0.75%時平均回收率為100.97%,RSD%為4.33%,綜合看明膠濃度為0.75%時測得的回收率更好,故適宜的明膠濃度為0.75%.
2.2 三氯乙酸濃度的影響
取0.75%的明膠作為溶劑配制1%的BaCl2.控制三氯乙酸加入量3.5ml,1%的BaCl2加入量1 ml的條件下,考察不同濃度三氯乙酸對線性關系的影響,操作步驟同標準曲線.實驗結果見表3,不同濃度三氯乙酸的回收率結果見表4.

表3 不同三氯乙酸濃度的線性關系考察結果

表4 不同濃度三氯乙酸下的回收率
由表3可以看出三氯乙酸濃度對線性關系影響很小,三氯乙酸濃度0%~5%范圍內,標準曲線線性關系良好,相關系數都高于0.99.由表4可以看出三氯乙酸濃度為0%和2%時回收率較低,三氯乙酸濃度為3%時回收率的平均值為98.47%,RSD%為6.52%,三氯乙酸濃度為5%時回收率的平均值為101.59%,RSD%為9.35%,結合兩者看出3%的三氯乙酸測定結果更好,因此測定過程中三氯乙酸濃度宜為3%.
2.3 水解時間對檢測結果的影響
選取三氯乙酸濃度為3%,明膠濃度為0.75%,按標準曲線進行操作.稱取的微量樣品用1molHCl以1mg/ml溶解好之后,放進超級恒溫器水解,控制水解溫度100℃,取出不同時間的樣品溶液測吸光度,并分別計算硫酸基質量濃度C(SO2-4)、硫的質量濃度Cs及硫的質量百分含量s%,以s%為指標,考察水解時間對檢測結果的影響,測定結果見表5、圖1.
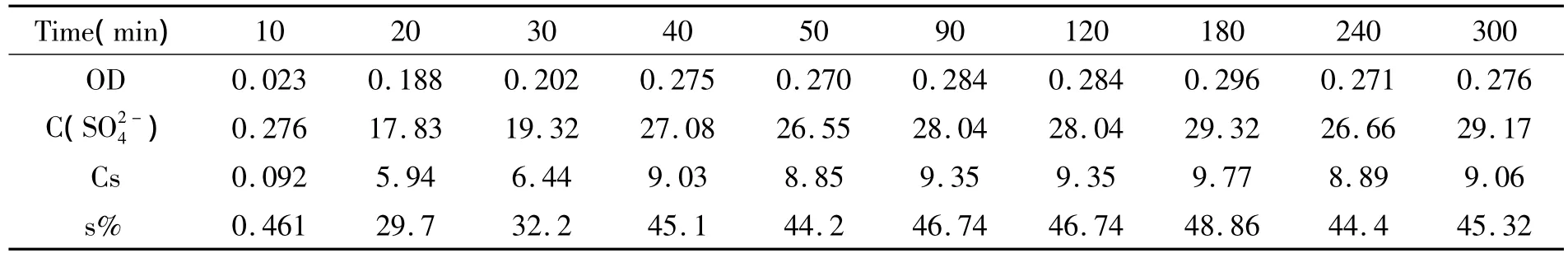
表5 水解時間對檢測結果的影響
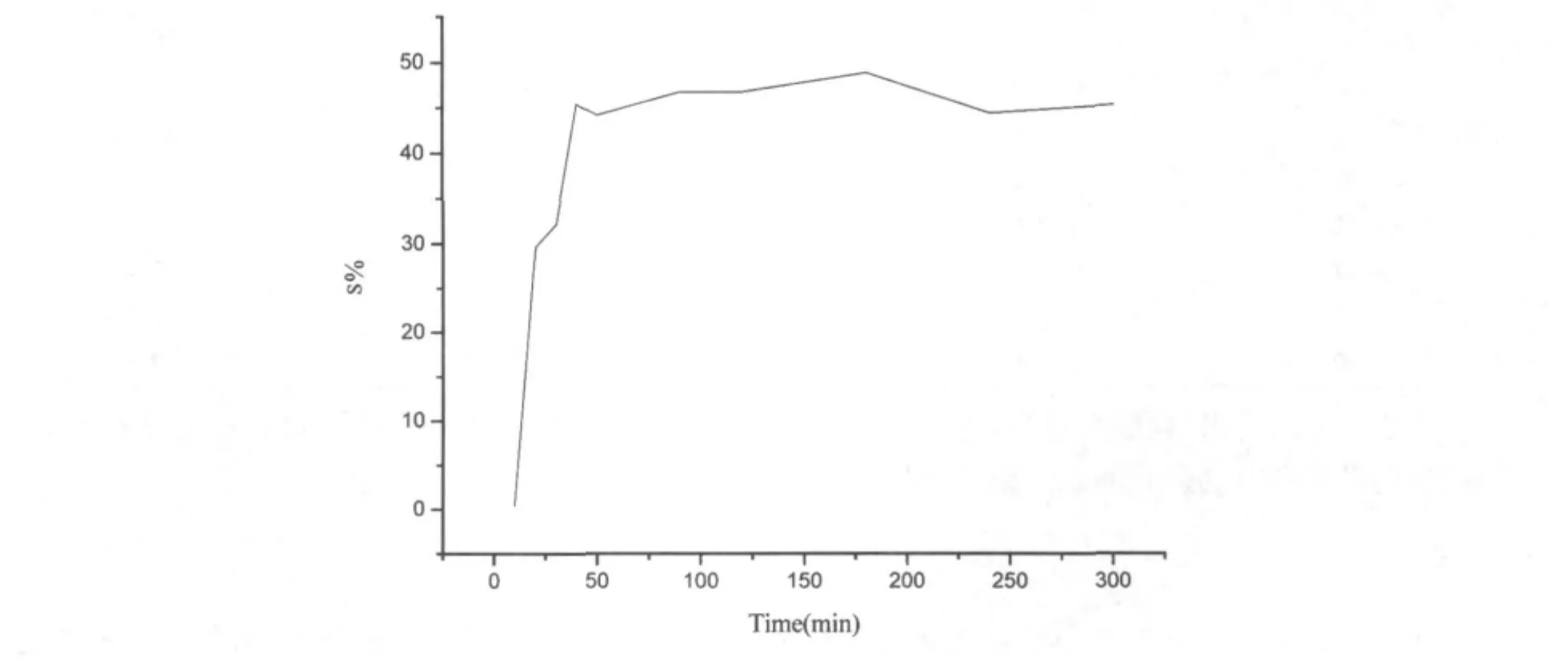
圖1 水解時間對檢測結果的影響
由表5和圖1可以看出在加熱水解180分鐘時,吸光度和硫的質量百分含量S%測定值最高,說明在180分鐘時樣品水解完全,硫酸根游離出來,而水解時間過長時可能會導致反應系統發生一些變化影響檢測結果,所以水解時間宜控制180分鐘,水解條件確定為100℃、3小時.
2.4 水解時鹽酸濃度對檢測結果的影響
保持樣品溶液質量濃度為1mg/mlHCl,改變鹽酸濃度,檢測用不同濃度鹽酸溶解的樣品在水解條件為100℃、3小時下的吸光度,并分別計算硫酸基質量濃度C(SO2-4)、硫的質量濃度Cs及硫質量百分含量s%,以s%為指標,確定適宜的鹽酸濃度.
為了使檢測結果更加準確,應消除鹽酸中可能含有的硫的影響,以及考慮在加熱過程中鹽酸易揮發特性的影響,將未加入樣品的鹽酸管與加入樣品的鹽酸管一同在100℃下水解三小時,以便使兩者鹽酸的揮發量比較相近,空白與待測樣品測定時濃度較一致,使測量值更準確.實驗結果見表6.
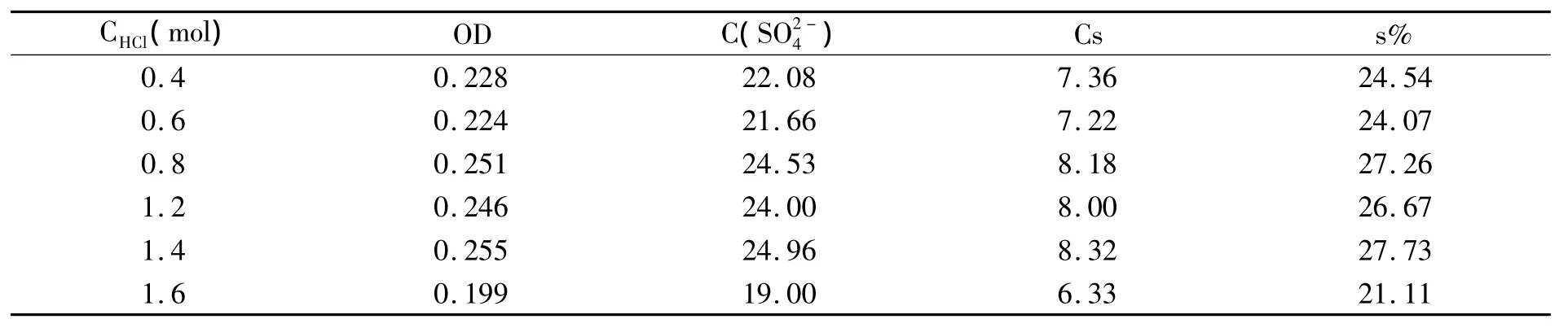
表6 鹽酸濃度對檢測結果的影響
由表6可以看出,鹽酸濃度在0.8~1.4mol/L之間時s%較大并且穩定,說明在此條件多糖完全水解,過高的鹽酸濃度1.6mol會影響檢測結果,因此較適宜的鹽酸濃度是0.8~1.4mol/L,為了方便起見選擇濃度為1mol/L的鹽酸溶解樣品,進行水解.
2.5 水解時鹽酸用量對檢測結果的影響
保持樣品用1mol/L的HCl溶解,改變鹽酸的用量,檢測不同質量濃度的樣品在相同水解條件為100℃、3小時下的吸光度,計算硫的質量百分含量s%.以s%為指標,考察鹽酸用量對檢測結果的影響.同2.4操作步驟,將未加入樣品的鹽酸管與加入樣品的鹽酸管一同在100℃下水解三小時,測量結果見表7.
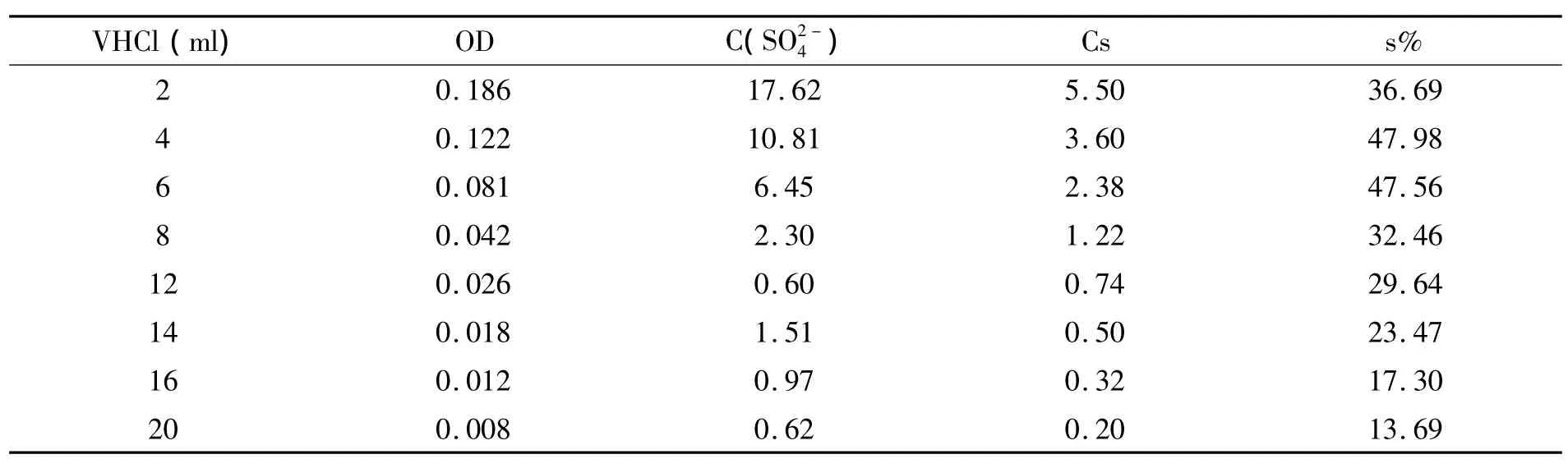
表7 鹽酸用量對檢測結果的影響
由表7可以看出,鹽酸用量在4~6ml之間時s%較穩定,說明此時多糖完全水解,硫酸根游離出來,而鹽酸用量較高時會影響測定結果.所以選擇用5ml鹽酸溶解樣品去加熱水解.
3 結論
通過對硫酸鋇光電比濁法測定皂角硫酸多糖中硫含量的各種影響因素進行研究,得到相關的適宜測定條件.確定溶解氯化鋇的明膠濃度為0.75%,三氯乙酸濃度為3%,樣品溶液水解時間為3小時,溶解樣品的鹽酸濃度為1mol/L,每溶解1mg樣品鹽酸用量為5ml.對于該方法測定準確性等內容將在后續實驗中進一步研究.
[1]張樹政.糖生物學與糖生物工程[M].北京:清華大學出版社,2002.
[2]諸葛健.功能性多糖的構效關系[J].無錫輕工業大學學報,2002,(3):209-212.
[3]邱芳萍,張玲,于健.硫酸鋇比濁法對鹿茸多糖中硫酸基含量的測定[J].長春工業大學學報,2005,26(4):268-270.
[4]Ruperez P,Ahrazem O,Leal JA.Potential antioxidant capacity of sulfated polysaccharides from the ediblemarine brown seaweed Fucus vesiculosus[J].J.Agic.Food Chem,2002,50(4):840.
[5]馬茜.硫酸鋇吸光比濁法測定大蒜中大蒜素含量[J].光譜實驗室,2007,24(3):345-347.
[6]易鳳英,劉素純,李佳蓮,等.茶多糖的提取方法及其生理功能研究進展[J].安徽農業科學,2010,38(6):2911-2913.
[7]蔡為榮,孫元琳,湯堅.果膠多糖結構與降血脂研究進展[J].食品科學,2010,31(5):307-311.
[8]毛健,馬海樂.靈芝多糖的研究進展[J].食品科學,2010,31(1):295-299.
[9]孫運峰,李海娜,周長征,等.鼠尾草屬藥用植物多糖的研究進展[J].食品與藥品,2010,12(3):138-141.
[10]Jiang RW,Lau K M,Hon PM,et al.Chemistry and biological activities of caffeic acid derivatives from salviamiltiorrhiza[J].Curr Med Chem,2005,12(2):237-246.
[11]李運龍.一種抗艾滋活性植物多糖制備工藝的研究[D].昆明:昆明理工大學,2004.
[12]馬巍,戰義鵬.加標回收率計算方法的探討[J].黑龍江醫藥科學,1999,22(1):88.
[13]叢建波,王長振,李妍,等.褐藻硫酸多糖硫酸基含量測定——硫酸鋇比濁法研究[J].解放軍藥學學報,2003,19(3):181-183.

