p16在大鼠腎臟隨增齡表達的變化
常 明 劉書馨 劉 焱 王志宏 付 瑤 (大連市中心醫院腎內科,遼寧 大連 116033)
近年來的研究表明,p16基因(細胞周期蛋白激酶抑制物基因)不僅是一種抑癌基因,也是人類細胞衰老的主導基因。它在衰老細胞中的表達比年輕細胞高10~20倍,是細胞衰老的標志物之一。抑制p16基因表達,不僅細胞衰老速度減慢,壽命延長,而且端粒長度縮短也減慢;反之,增加p16基因表達,不僅細胞衰老速度加快,壽命縮短,端粒長度縮短也加快,提示調控p16的表達直接影響某些細胞的壽命〔1〕。腎臟功能隨年齡增長逐漸下降。腎臟衰老在病理上表現為腎小球硬化、腎間質纖維化和腎動脈硬化,但缺乏特征性改變和特異性標志物,限制了腎臟衰老機制的研究。鑒于p16在細胞衰老中的重要作用,我們推測p16可能是腎臟衰老的標志之一。因此,本研究以p16為切入點,從基因和蛋白質水平觀察p16在大鼠腎臟隨增齡表達的變化,為進一步探討腎臟衰老的機制尋求理想的衰老標志物。
1 材料與方法
1.1 主要試劑與儀器 大鼠p16引物由北京賽百盛公司合成、小鼠p16單克隆抗體(美國Santa Cruz)、辣根過氧化物酶標記的羊抗鼠ⅠgG(美國Santa Cruz)、PCR試劑(TaKaRa生物工程大連有限公司)、ECL顯色試劑(美國 Santa Cruz)、PTC-200 DNA合成儀(美國MJ Research)、SYBR GREENⅠ染料(美國Molecular Probes)、ⅠCYCLER熒光定量PCR儀(美國Bio-Rad)、MⅠNⅠ-PROTEⅠN2 電泳儀(美國 Bio-Rad 公司)、ALPHAⅠMAGER2200凝膠圖像分析系統(美國Alpha公司)。
1.2 實驗動物及標本留取 取1日齡、3月齡和24月齡雄性Wister大鼠(由大連醫科大學動物中心提供)各6只,以2%戊巴比妥(0.1 ml/kg)腹腔注射麻醉,取腹正中切口,分離雙側腎臟,去包膜留取腎組織,腎組織分為2份,1份以10%中性甲醛固定,用于制備石蠟切片,1份置于液氮凍存以提取 RNA和蛋白。
1.3 實時定量PCR檢測不同月齡大鼠腎臟p16的mRNA表達 Trizol一步法提取總RNA。紫外分光光度計測濃度后取2μg RNA,使用Promega公司的反轉錄試劑合成cDNA模板。大鼠p16引物序列為:上游5'-GGTAATAGTGTTTTTAGAGGTG-3',下游 5'-CTACCCTAACTAATCTATCTAC-3',片段長度111 bp。反應條件為:94 ℃變性 5 min,94℃ 30 s、60℃ 30 s、72℃ 30 s、86℃ 15 s(檢測熒光),共40個循環,最后72℃延伸7 min。GADPH作為 RNA內參,引物序列為:上游 5'-TGCACCACCAACTGCTTAGC-3',下 游 5'-GGCATGGAC TGTGGTCATGAG-3',片段長度116 bp。SYBR GREENⅠ作為檢測染料。mRNA表達量用p16拷貝數/GAPDH拷貝數比值表示。
1.4 Western印跡分析檢測不同月齡大鼠腎臟p16蛋白的表達 根據試劑盒說明提取腎組織總蛋白,BCA法測蛋白濃度。取80μg蛋白上樣,進行SDS-聚丙烯酰胺凝膠電泳,半干法轉移至聚氟乙烯膜上,封閉液封閉,加入1∶200稀釋的小鼠p16單克隆抗體,4℃過夜。次日0.05%TBST洗膜3次,加入1∶2 000稀釋辣根過氧化物酶標記的山羊抗小鼠 ⅠgG,室溫搖床1 h,0.05%TBST洗膜3次,ECL顯影。以β-actin的蛋白表達作為內參照,用ALPHAⅠMAGER 2200凝膠圖像分析系統進行半定量分析。
1.5 腎組織p16的免疫組化染色 采用鏈霉親和素-生物素復合物技術(SP)法:腎組織經固定、脫水、石蠟包埋;常規脫蠟至水,PBS浸泡后3%過氧化氫孵育10 min,PBS洗3次,0.05%胰酶室溫修復15 min,5%正常山羊血清封閉10 min后加入1∶50稀釋的小鼠p16單克隆抗體,室溫過夜,PBS洗3次后加入生物素標記的兔抗小鼠二抗,室溫孵育40 min,PBS洗3次后加入辣根過氧化物酶標記的鏈霉卵白素,室溫孵育40 min,PBS洗3次,DAB顯色5 min,充分沖洗后蘇木素復染。400倍視野下觀察p16在腎組織表達。
2 結果
2.1 不同月齡大鼠腎臟p16的mRNA表達結果 實時定量PCR的結果顯示在1日齡大鼠腎臟p16的mRNA表達水平很低,在3月齡大鼠腎臟能夠檢測出p16的mRNA表達,在24月齡大鼠腎臟,p16的 mRNA表達顯著上調(0.31±0.02 vs 1.20±0.17 vs 5.89±0.83,P<0.05)。
2.2 不同月齡大鼠腎臟p16的蛋白表達結果 (1)Western印跡分析檢測發現:在1日齡大鼠p16的蛋白表達水平低,在3月齡大鼠腎臟能夠檢測出p16的蛋白表達,在24月齡大鼠腎臟p16的蛋白表達顯著上調。見圖1。(2)免疫組化結果顯示:在1日齡大鼠腎小球和腎小管幾乎檢測不出p16的蛋白表達;在3月齡大鼠腎小球內細胞核和腎小管上皮細胞核內可見陽性p16表達;在24月齡大鼠腎臟,腎小球內和腎小管上皮細胞核內p16表達顯著上調。見圖2。
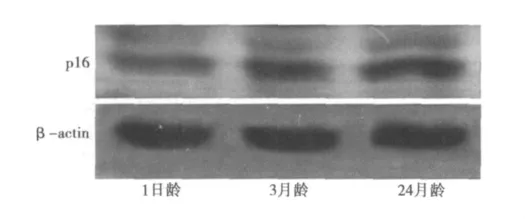
圖1 不同月齡大鼠腎臟p16的Western印跡結果
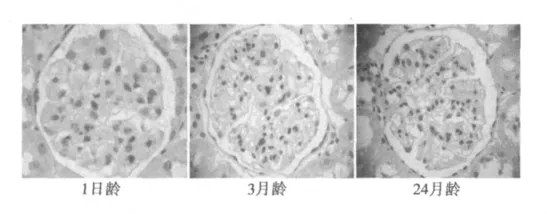
圖2 不同月齡大鼠腎臟p16免疫組化染色結果(×400)
3 討論
衰老是生命活動的普遍現象,其機制至今仍不清楚。腎臟衰老在功能上表現為腎小球濾過率下降,腎臟濃縮稀釋功能受損,對損傷的修復能力減弱,有研究表明,衰老的腎小管上皮細胞在遭受缺血/再灌注損傷后,更易發生壞死和/或凋亡〔2〕。但腎臟衰老缺乏特異性的標志物,大大限制了對腎臟衰老機制的研究。已有大量的體外研究的結果顯示p16在細胞衰老中的重要作用。細胞衰老的關鍵特征是細胞周期停滯。衰老細胞主要含有G1期的DNA含量,因此目前認為衰老細胞停滯于G1期,不能順利進入S期,細胞周期G1/S轉換是衰老的關鍵調控點。近年來的研究發現細胞衰老時,p16基因的mRNA轉錄及蛋白表達水平增高,抑制有絲分裂原刺激發生反應而產生RB蛋白的磷酸化,從而維持了衰老細胞不可逆的生長停滯狀態〔3~5〕。盡管細胞衰老發生不可逆增殖停滯狀態過程中可能發生多種變化,但p16及RB基因的表達及功能的改變可能是細胞周期停滯于G1期的根本原因。p16表達的變化也成為許多細胞如胰島細胞〔6〕、血管內皮細胞〔7〕衰老的標志。
鑒于p16在細胞衰老中的重要作用,我們推測p16可能成為腎臟衰老的良好的分子標志物。也就是說,在腎臟衰老的進程中,p16的mRNA轉錄及蛋白表達水平可能發生顯著變化。我們的研究結果與推測吻合。提示p16是大鼠腎臟衰老的良好的分子標志。
p16在腎臟隨增齡表達上調的機制目前還不完全清楚。Krishnamurthy等的研究顯示正向調控p16表達的轉錄因子Ets1隨增齡表達上調,與p16表達平行,可能是p16隨增齡表達上調的機制之一〔8〕。與此類似,Ressler等〔9〕的研究發現在衰老的皮膚,p16表達的抑制因子Bmi-1水平顯著下調,可能是p16隨增齡表達上調另一原因。p16隨增齡表達上調另一重要機制是氧化損傷,新近的研究發現在造血干細胞,活性氧通過p38-MAPK途徑激活p16表達,從而限制造血干細胞壽命,使造血干細胞喪失自我更新的能力〔10〕。p16在腎臟隨增齡表達上調的機制可能與上述機制有關,但需要進一步的研究闡明。
1 Tsygankov D,Liu Y,Sanoff HK,et al.A quantitative model for age-dependent expression of the p16ⅠNK4a tumor suppressor〔J〕.Proc Natl Acad Sci U SA,2009;106(39):16562-7.
2 丁 瑞,喬 晞,陳香美,等.抗氧化劑和內質網鈣釋放阻滯劑對老年大鼠腎臟缺血/再灌注損傷中凋亡的影響〔J〕.中國老年學雜志,2006;26(6):779-82.
3 Elledge SJ,Harper JW.Cdk inhibitors:on the threshold of checkpoints and development〔J〕.Curr Opin Cell Biol,1994;6(6):847-52.
4 Sherr CJ,Roberts JM.Ⅰnhibitors of mammalian G1 cyclin-dependent kinases〔J〕.Genes Dev,1995;9(10):1149-63.
5 Stein GH,Drullinger LF,Soulard A,et al.Differential roles for cyclin-dependent kinase inhibitors p21 and p16 in the mechanisms of senescence and differentiation in human fibroblasts〔J〕.Mol Cell Biol,1999;19(3):2109-17.
6 林暉榕,陳慎仁,傅玉才,等.不同月齡大鼠胰島細胞衰老及胰島素表達的研究〔J〕.中國病理生理雜志,2009;25(1):180-2.
7 單海燕,白小涓,張偉光,等.AngⅡ誘導血管內皮細胞衰老相關基因表達的研究〔J〕.中國老年學雜志,2008;24(6):1041-6.
8 Krishnamurthy J,Torrice C,Ramsey MR,et al.Ⅰnk4a/Arf expression is a biomarker of aging〔J〕.J Clin Ⅰnvest,2004;114(9):1299-307.
9 Ressler S,Bartkova J,Niederegge R,et al.p16ⅠNK4A is a robust in vivo biomarker of cellular aging in human skin〔J〕.Aging Cell,2006;5(5):379-89.
10 Ⅰto K,Hirao A,Arai F,et al.Reactive oxygen species act through p38 MAPK to limit the lifespan of hematopoietic stem cells〔J〕.Nat Med,2006;12(4):446-51.

