硒酸泥制備粗硒新工藝
李倩,張寶,申文前,楊興文,
(1. 中南大學 冶金科學與工程學院,湖南 長沙,410083;2. 武警天津總隊 第一支隊,天津,300222;3. 江銅集團 貴溪冶煉有限公司,江西 貴溪,335424)
硒屬于稀散元素,在自然界中有工業開采價值的單獨成礦很少。硒有著廣泛的應用領域,但一直是嚴重短缺的金屬資源[1-3]。目前,提取硒[4-7]的主要原料有電解精煉銅的陽極泥、鉛鼓風爐的煙塵、硫鐵礦制酸廠的硒酸泥、煉鋼煙塵、鉛鋅精礦焙燒煙塵、黃鐵礦焙燒渣等。硒酸泥主要含硫、硒、鐵等元素,硫鐵礦原料中的硒在沸騰焙燒過程中大部分以二氧化硒的形式隨 SO2煙氣進入洗滌塔,在洗滌塔中 SeO2溶于水后形成的 H2SeO3被 SO2還原成粗硒隨煙塵一起沉降,形成硒酸泥[8-9]。工業上處理硒酸泥主要采用硫酸化焙燒,硒的回收率達93%以上,但存在嚴重的二氧化硫煙氣問題[9-11];其次,通過溶劑萃取法[12]、真空蒸餾法[13-14]、離子交換法[15]、純堿焙燒法[16]等都可以將硒與其他雜質分離開來。但是,這些方法較適用于處理硒品位較低的物料(硒的品位小于5%),而對于硒含量較高的物料,則需考慮新的方案。本文作者通過多次小型實驗,提出了一種新的生產工藝。
1 實驗
1.1 實驗原料
實驗原料為江西貴溪冶煉廠提供的硒酸泥,干燥后經球磨機磨碎混合均勻,硒酸泥中的主要成分(質量分數)如表1所示。

表1 硒酸泥的主要成分Table 1 Chemical composition of selenium acid mud %
對實驗原料進行X線衍射分析,結果表明:硒酸泥中主要元素硒、鐵和硫分別以單質Se、氧化鐵和單質S的形式存在。
1.2 實驗試劑及儀器
實驗試劑為:煤油,NaClO3,H2SO4,Na2SO3及硫脲等。
實驗儀器為電子恒速攪拌機、601超級恒溫水浴、三頸瓶等。
1.3 實驗原理及工藝流程
硒酸泥中重要成分硫主要以元素硫的形態存在,要用煤油脫除元素硫,首先應該使存在于渣中的硫磺熔化,因此,要求煤油脫除元素硫的溫度達到硫磺的熔點。根據單質硫的性質[17],將正交硫加熱到368.7 K,它不經熔化就可緩慢轉化為單斜硫,從正交硫轉變為單斜硫是一個吸熱過程,當溫度低于368.7 K時,單斜硫又會轉變為正交硫,因此,368.7 K是正交硫與單斜硫的轉變點,只要溫度達到368 K,所處理硒酸泥中的元素硫就會熔化。
在高溫下采用有機溶劑浸取法(又稱固-液萃取),選用溶劑浸漬固體混合物以分離可溶組分和殘渣[18]。實驗選擇煤油作為浸取液,使溶解了單質硫的煤油與硒、鐵分離,熱煤油充分降溫后單質硫從中析出回收,而煤油可循環使用。氧化浸出脫硫渣中的硒,得到的氧化浸出液首先加入硫脲創造還原氣氛,最后加入Na2SO3還原單體硒,主要反應方程式如下:
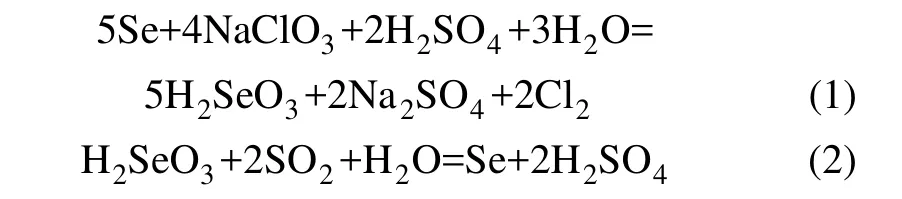
采用的工藝流程見圖1。
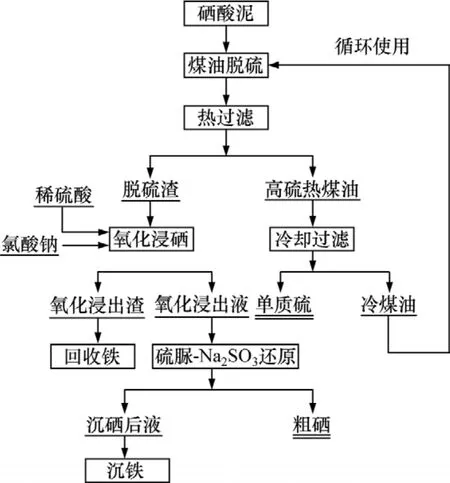
圖1 工藝流程圖Fig.1 Flow sheet of experiment
2 結果及討論
2.1 煤油脫硫實驗
100 g硒酸泥物料在溫度95 ℃、攪拌時間0.5 h、液固比10:1的條件下進行煤油脫硫實驗,得到脫硫渣(76.5 g),其主要成分(質量分數)見表 2;脫硫得到的單質硫和工業硫磺的指標成分(質量分數)如表3所示。

表2 脫硫渣的主要成分Table 2 Chemical composition of desulfurization slag %

表3 工業硫磺的指標成分和單質硫的成分Table 3 Chemical composition of sulfur in industry and product of sulfur %
從表2可見:脫硫渣中硒、鐵得到有效富集;單質硫的脫除率達到97.98%。從表3可見,單質硫中硫的含量達到99.3%,符合工業硫磺的指標。
2.2 NaClO3氧化浸硒條件實驗
2.2.1 NaClO3加入量對Se浸出率的影響
將60 g脫硫渣加入三頸瓶中,在反應溫度為80℃、浸出時間為2 h、H2SO4質量濃度為250 g/L、液固比為5:1的條件下,NaClO3的加入量對Se浸出率η(Se)的影響如圖2所示。
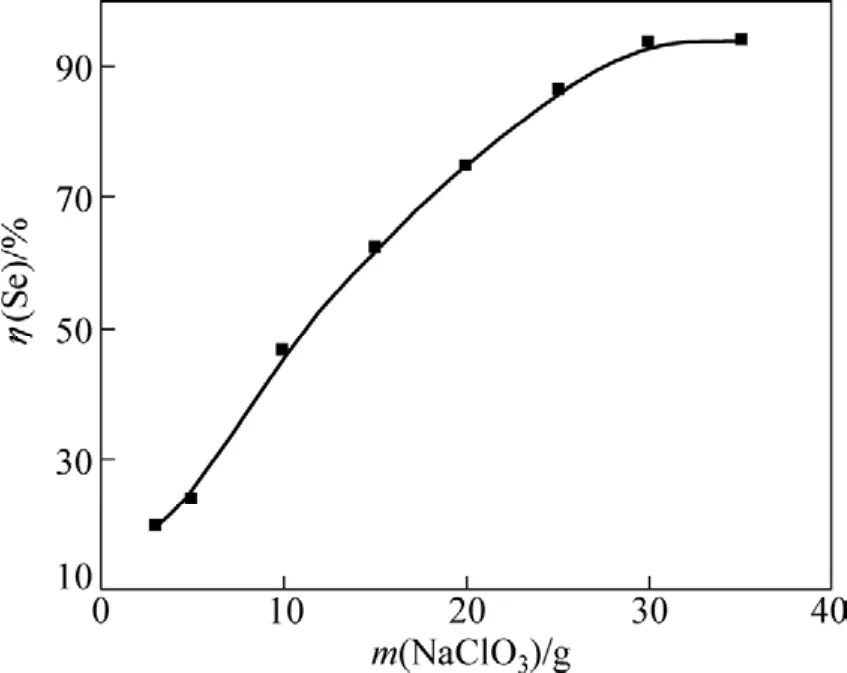
圖2 NaClO3加入量m(NaClO3)對Se浸出率η(Se)的影響Fig.2 Effect of NaClO3 quality m(NaClO3) on Se leaching recovery η(Se)
由式(1)可知:隨著NaClO3加入量的增大,Se的浸出率也隨之增加。由圖2可知:當NaClO3加入量達到 30 g時,硒基本達到浸出平衡。這是因為當NaClO3加入量偏低時,浸出反應速度很慢,在反應時間內不能將硒完全浸出。而當NaClO3加入量達到30 g時,在反應時間內浸出反應進行完全;因此,選擇最佳的NaClO3加入量為30 g,Se浸出率達94.80%。
2.2.2 H2SO4質量濃度對Se浸出率的影響
將60 g脫硫渣加入三頸瓶中,在NaClO3加入量為30 g、反應溫度為80 ℃、浸出時間為2 h、液固比為5:1的條件下,H2SO4質量濃度對Se浸出率的影響如圖3所示。
由式(2)可知:隨著 H2SO4質量濃度的增大,Se的浸出率也隨之增加。從圖3可以看出,當H2SO4質量濃度達到300 g/L以后,Se浸出率已至97.70%。繼續增加H2SO4質量濃度,Se浸出率基本保持不變;考慮到反應物濃度越高,反應速度越快,最佳的H2SO4質量濃度為300 g/L。
2.2.3 液固比對Se浸出率的影響
將60 g脫硫渣加入三頸瓶中,在NaClO3加入量為30 g,H2SO4質量濃度為300 g/L以及反應溫度為80 ℃、浸出時間為2 h的條件下,液固比對Se浸出率的影響如圖4所示。
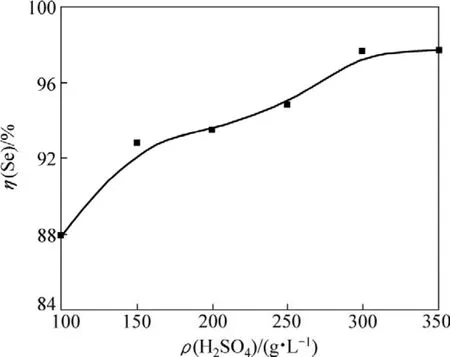
圖3 H2SO4質量濃度ρ(H2SO4)對Se浸出率η(Se)的影響Fig.3 Effect of acidity ρ(H2SO4) on Se leaching recovery η(Se)
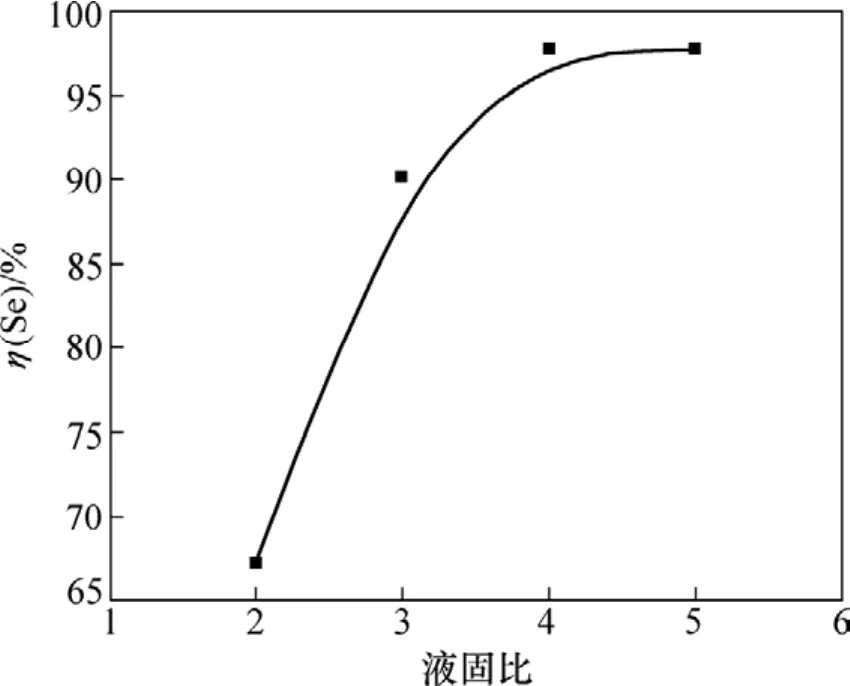
圖4 液固比對Se浸出率η(Se)的影響Fig.4 Effect of the liquid to solid ration on Se leaching recovery η(Se)
圖4表明:隨著液固比的增加,Se浸出率隨之增加。這是因為液固比的增加能增加Se在酸性溶液中的溶解,渣漿黏度減小從而改善了擴散條件。最佳的液固比為5:1。
2.2.4 浸出時間對Se浸出率的影響
將60 g脫硫渣加入三頸瓶中,在NaClO3加入量為30 g,H2SO4質量濃度為300 g/L以及液固比為5:1、反應溫度為80 ℃的條件下,浸出時間對Se浸出率的影響如圖5所示。
圖5表明:隨著浸出時間的延長,Se浸出率上升。浸出時間達到2 h時,Se已基本浸出。考慮到隨著浸出時間的延長,溶液的濃度逐漸降低,反應速度逐漸減小,Se基本完全浸出,因此,最適宜的浸出時間為2 h。
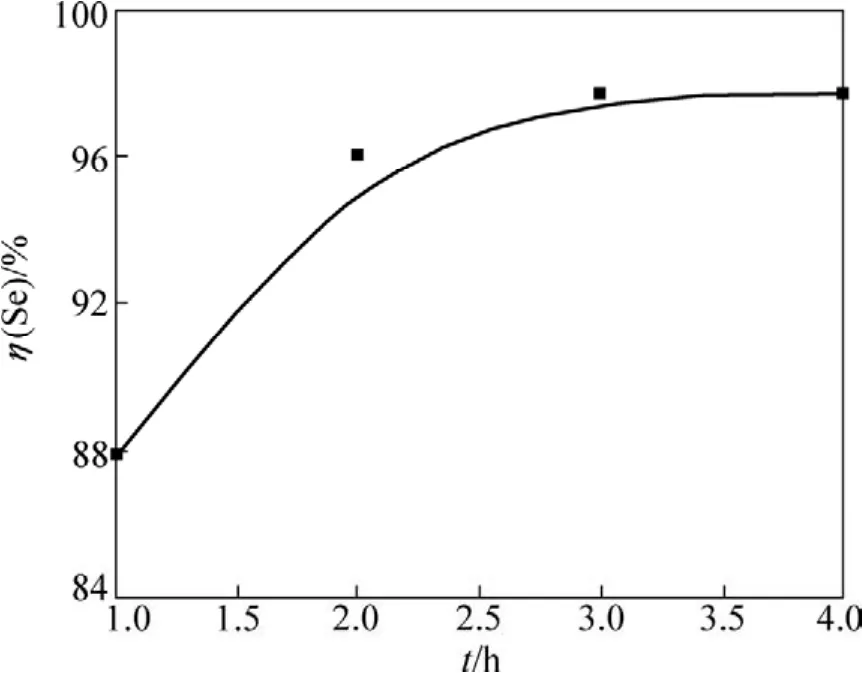
圖5 浸出時間t對Se浸出率η(Se)的影響Fig.5 Effect of leaching time on Se leaching recovery η(Se)
2.2.5 浸出溫度對Se浸出率的影響
將60 g脫硫渣加入三頸瓶中,在NaClO3質量為30 g、H2SO4質量濃度為300 g/L、液固比為5:1、浸出時間為2 h的條件下,浸出溫度對Se浸出率的影響如圖6所示。
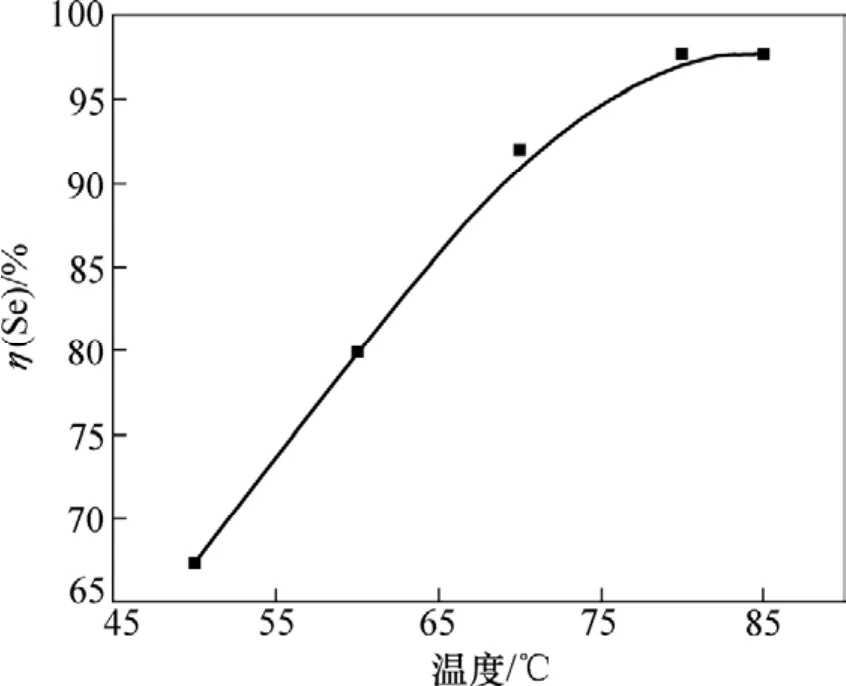
圖6 浸出溫度對Se浸出率η(Se)的影響Fig.6 Effect of leaching temperature on Se leaching recovery η(Se)
圖6表明:當溫度比較低時,隨著開始反應溫度的增加,反應速度加快,浸硒率隨之增加。這是因為隨著溫度的升高,HSeO3-的生成的穩定區域擴大。并且溫度越高,生成的二氧化氯越容易揮發,再提高溫度已沒有多大意義。因此,浸出溫度宜為80 ℃。
2.3 NaClO3氧化浸硒綜合條件實驗
60 g脫硫渣在最優化條件(NaClO3加入量為30 g、H2SO4質量濃度為300 g/L、液固比為5:1、反應溫度為 80 ℃、浸出時間為 2 h)下進行實驗。結果如表 4所示。

表4 氧化浸出渣和氧化浸出液的主要成分Table 4 Chemical composition of leaching slag and oxidative leaching solution
由表4可知:氧化浸出渣為鐵的富集物,其中,鐵的含量為 68.69%;氧化浸出液中硒的質量濃度為42.18 g/L,鐵的質量濃度為9.55g/L;應繼續回收其中的鐵。該過程中硒的浸出率為97.76%。
2.4 硫脲-Na2SO3還原提硒條件實驗
2.4.1 硫脲加入量對沉硒率的影響
常溫下,將50 mL氧化浸出液加入錐形瓶中,在酸度為100 g/L、Na2SO3加入量為4 g、陳化時間為10 h的條件下,硫脲加入量對沉硒率的影響如圖7所示。
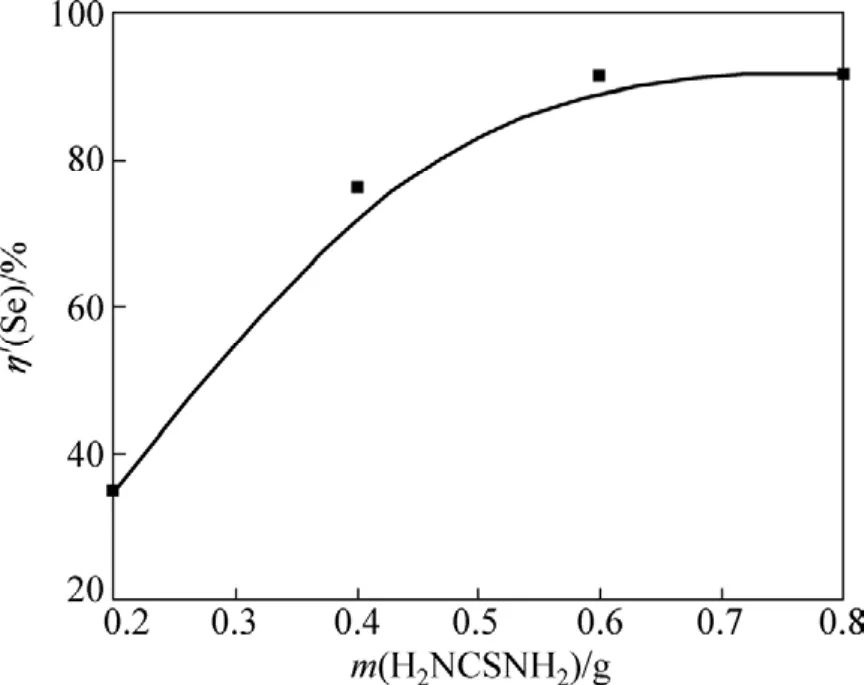
圖7 硫脲加入量m(H2NCSNH2)對沉硒率η′(Se)的影響Fig.7 Effect of H2NCSNH2 quality m(H2NCSNH2)on Se deposition rate η′(Se)
從圖7可以看出,隨著硫脲加入量的增大,沉硒率也隨之增加。硫脲加入量繼續增加,沉硒率保持不變。這是因為硫脲的加入量過少時,亞硫酸鈉會發生副反應,還原其他雜質離子,導致沉硒率偏低。如果硫脲過量會發生副反應,隨著靜置時間的延長,單體硫從沉硒液中析出,影響硒的品位。故選擇硫脲加入量為0.60 g。
2.4.2 氧化浸出液的酸度對沉硒率的影響
常溫下,將50 mL氧化浸出液加入錐形瓶中,在硫脲加入量為0.60 g,Na2SO3加入量為4 g和陳化時間為 10 h的條件下,氧化浸出液的酸度對沉硒率 η′的影響如圖8所示。

圖8 氧化浸出液酸度ρ對沉硒率η′(Se)的影響Fig.8 Effect of acidity on Se deposition rate η′(Se)
從圖8可以看出,隨著酸度的增大,開始時沉硒率基本保持不變,當酸度達到150 g/L以后沉硒率迅速減小。這是因為當溶液酸度比較低時,產生SO2的速度比較慢,反應比較充分,因此,SO2利用率比較高,但當溶液酸度達到150 g/L以后,SO2產生的速度過快,SO2氣體在溶液中溢出量增加,使反應不能充分進行,導致SO2利用率下降。考慮到反應物濃度越低,反應速度越慢,最佳的酸度為150 g/L。
2.4.3 Na2SO3加入量對沉硒率的影響
常溫下將50 mL氧化浸出液加入錐形瓶中,在酸度為150 g/L、硫脲加入量為0.60 g、陳化時間為10 h的條件下,Na2SO3加入量對沉硒率η′的影響如圖9所示。
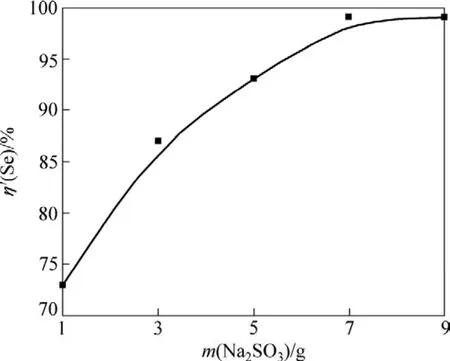
圖9 Na2SO3加入量m(Na2SO3)對沉硒率 η′(Se)的影響Fig.9 Effect of m(Na2SO3) on Se deposition rate η′(Se)
從圖9可以看出:隨著亞硫酸鈉加入量的增加,沉硒率逐漸增大,并且增幅較大,說明體系中仍存在沒被還原的硒離子;當Na2SO3加入量比較低時,產生SO2的速度比較慢,SO2利用率比較高;當Na2SO3加入量達到7 g時,沉硒率已至99.70%;此時體系中的硒離子很少,還原過程速率減慢,故隨亞硫酸鈉用量的繼續增加,硒還原率變化不大。因此,7 g為最佳的Na2SO3加入量。
2.4.4 陳化時間對沉硒率的影響
常溫下,將50 mL氧化浸出液加入錐形瓶中,在硫脲加入量為0.60 g、Na2SO3加入量為7 g、酸度為150 g/L的條件下,陳化時間對沉硒率η′的影響如表5所示。
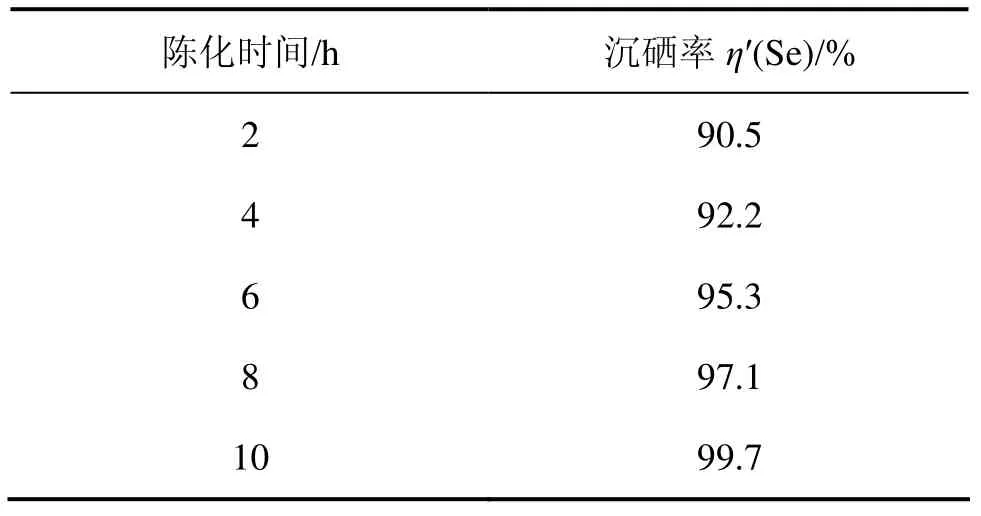
表5 陳化時間對沉硒率η′(Se)的影響Table 5 Effect of aging time on Se deposition rate η′(Se)
從表5可知:隨著陳化時間的延長,沉硒率逐漸增加;這是因為滴定完后的溶液體系中仍存在未反應完全的硒離子。當陳化時間達到10 h時,沉硒率已至99.70%,此時溶液中的硒離子已基本反應完全。因此最適宜的陳化時間為10 h。
2.5 Na2SO3-硫脲還原提硒綜合條件實驗
常溫下,50 mL氧化浸出液在最優化條件(硫脲加入量0.60 g、Na2SO3加入量7 g、酸度150 g/L、陳化時間10 h)下進行實驗。0.165 L沉硒后液中,硒和鐵的質量分數分別為 0.038%和 2.780%。產物粗硒的組成(質量分數)見表6。
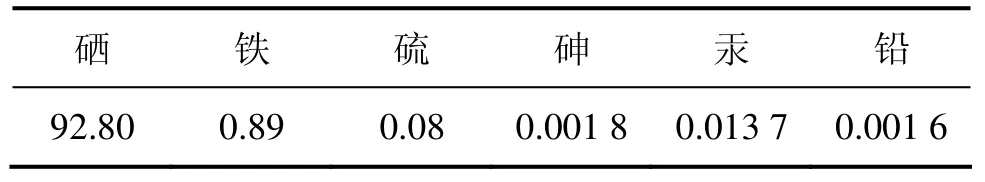
表6 產物粗硒的組成(質量分數)Table 6 Chemical composition of crude selenium %
3 結論
(1) 采用煤油脫硫-氧化浸出-還原沉硒處理硒酸泥是可行的。硫以硫磺回收,脫除率大于97%,且達到工業硫磺的指標;硒的回收率大于97%,粗硒的品位大于92%。這對改造傳統火法冶煉硒酸泥的工藝具有潛在優勢。
(2) 在脫硫渣中硒、鐵以單質硒、氧化鐵的形態存在,與硒酸泥中硒、鐵存在形態一致。鑒于氧化浸出液中硒、鐵含量的差別,可從硫脲-Na2SO3中還原提硒制備粗硒。
[1] 葛清海, 陳后興, 謝明輝, 等. 硒的資源、用途與分離提取技術研究現狀[J]. 四川有色金屬, 2005, 9(3): 7-15.GE Qing-hai, CHEN Hou-xing, XIE Ming-hui, et al. Selenium resources application and the studying situation on separation and abstraction technology[J]. Sichuan Nonferrous Metals, 2005,9(3): 7-15.
[2] 馮彩霞, 劉家軍, 劉燊, 等. 硒資源及其開發利用概況[J]. 地質與資源, 2002, 11(3): 152-156.FENG Cai-xia, LIU Jia-jun, LIU Shen, et al. An outline of selenium resources and its exploitation and utilization[J].Geology and Resources, 2002, 11(3): 152-156.
[3] 彭大明. 中國硒礦資源概述[J]. 化工礦產地質, 1997, 19(1):37-42.PENG Da-ming. Selenium resources of China: An outline[J].Geology of Chemical Minerals, 1997, 19(1): 37-42.
[4] 季金華, 陳禮寬. 濕法提取陽極泥中硒的探索性試驗[J]. 江蘇地質, 1998, 22(2): 88-90.JI Jin-hua, CHEN Li-kuan. Preliminary test of the Se extracting from anode mud with trial wet method[J]. Jiangsu Geology, 1998, 22(2): 88-90.
[5] 楊長江, 張旭, 藍德均. 銅陽極泥脫硒工藝現狀和趨勢[J]. 四川有色金屬, 2005(1): 22-25.YANG Chang-jiang, ZHANG Xu, LAN De-jun. Present situation and trend of selenium removal technique from copper anode slime[J]. Sichuan Nonferrous Metals, 2005(1): 22-25.
[6] 周犇, 趙忱. 陽極泥處理工藝優化實踐[J]. 有色金屬, 2003(1):26-28.ZHOU Ben, ZHAO Chen. Plant practice of process optimizing for treating anode slime[J]. Nonferrous Metals, 2003(1): 26-28.
[7] 余真榮. 銅陽極泥濕法處理工藝的技術改造[J]. 黃金, 1999,20(4): 34-37.YU Zhen-rong. The technological remoulding of wet treatment of copper anode mud[J]. Gold, 1999, 20(4): 34-37.
[8] 湯家道, 楊曉明. 云銅粗硒生產工藝沿革[J]. 云南冶金, 2008,37(4): 31-33.TANG Jia-dao, YANG Xiao-ming. Evolution of crude selenium production process in yunnan copper Co. Ltd[J]. Yunnan Metallurgy, 2008, 37(4): 31-33.
[9] 尹善繼, 劉世武, 張德杰. 提高銅陽極泥中硒回收率的實踐[J]. 中國有色冶金, 2008(3): 28-29.YIN Shan-ji, LIU Shi-wu, ZHANG De-jie. Practice of increasing selenium recovery rate from copper anode sludge[J]. China Nonferrous Metallurgy, 2008(3): 28-29.
[10] 姚淑華, 石中亮, 宋守志. 有色金屬礦物中硫資源的回收及綜合利用[J]. 中國資源綜合利用, 2003(8): 17-18.YAO Shu-hua, SHI Zhong-liang, SONG Shou-zhi. Recovery and comprehensive utilization of sulpher from nonferrous metal mineral[J].China Resources Comprehensive Utilization, 2003(8):17-18.
[11] 蔡世兵. 從高品位硒、碲廢料中分離回收硒和碲[J]. 濕法冶金,2008, 27(1): 35-37.CAI Shi-bing. Separation and recovery of selenium and tellurium from high grade waste material[J]. Hydrometallurgy of China, 2008, 27(1): 35-37.
[12] 衛芝賢, 徐春彥. 以N503從鹽酸溶液中萃取四價硒的研究[J].華北工學院學報, 1996, 17(4): 319-322.WEI Zhi-xian, XU Chun-yan. Solvent extraction of Se(Ⅳ) from HCl solution[J]. Journal of North China Institute of Technology,1996, 17(4): 319-322.
[13] Mandrino D UHV. Se evaporation source: Room-temperature deposition on a clean V (110) surface[J]. Institute of Metals and Technology, 2003, 71(3): 267-271.
[14] 黃占超, 楊斌, 戴永年, 等. 硒渣真空蒸餾研究[J]. 云南冶金,2002, 31(6): 27-29.HUANG Zhan-chao, YANG Bin, DAI Yong-nian, et al. Study on vacuum distillation of selenium residue[J]. Yunnan Metallurgy,2002, 31(6): 27-29.
[15] 楊文斌, 王靖芳, 王建民. 離子交換法從銅陽極泥中提取純硒[J]. 稀有金屬, 1989, 13(4): 300-303.YANG Wen-bin, WANG Jing-fang, WANG Jian-min. Ion exchange from copper anode slime extract pure selenium[J].Chinese Journal of Rare Metals, 1989, 13(4): 300-303.
[16] 鄒家炎, 周令治. 稀有分散金屬及其化合物[M]. 北京: 科學出版社, 1995: 15-50.ZOU Jia-yan, ZHOU Ling-zhi. Rare dispersed metals and their compounds[M]. Beijing: Science Press, 1995: 15-30.
[17] 無機化學叢書編委會. 無機化學叢書[M]. 北京: 科學出版社,1996: 10-35.Inorganic Chemistry Series Editorial Board. Inorganic chemistry series[M]. Beijing: Science Press, 1996: 10-35.
[18] 李振華, 王吉坤. 閃鋅礦氧壓酸浸渣中硫的回收研究[J]. 礦業工程, 2008, 6(6): 31-33.LI Zhen-hua, WANG Ji-kun. Study of sulphur recycling from the leaching slag of oxygen pressure leaching of sphalerites[J].Mining Engineering, 2008, 6(6): 31-33.

