二氯喹啉酸誘導煙草保護酶活性的動態變化
陳澤鵬,鄧建朝,陳偉明,萬樹青*
(1.廣東省煙草公司,廣州 510600;2.華南農業大學農藥與化學生物學教育部重點實驗室,廣州 510642)
二氯喹啉酸(Quinclorac)是由德國巴斯夫公司開發的新型喹啉酸類激素型除草劑,主要用于水稻插秧前后的稗草和其他雜草的防除,是我國稻田使用的主要除草劑[1-3]。由于二氯喹啉酸在土壤中的殘留時間較長,不易降解,因而對許多后茬敏感作物的生長造成一定的影響。
1999—2002年,廣東省部分煙區出現煙草畸形生長現象,結果造成烤煙品質下降,受害嚴重的煙田無煙葉可收。后經分析,致畸原因為土壤中殘留二氯喹啉酸[4-6]。作者經多次深入田間觀察發現,凡畸形生長的煙草田塊,很難找到受其他病害侵襲的煙株。為了弄清原因,在開展致畸機理研究的同時,對畸形煙葉的耐病性因子也展開了一些探索。在二氯喹啉酸化學脅迫下,檢測煙草體內保護酶特別是SOD和POD活性的變化,試驗設計了二氯喹啉酸不同濃度、不同時間處理后煙草體內 SOD活性和POD活性動態變化,以了解煙草畸形生長與保護酶活性變化的關系,對深入了解二氯喹啉酸對煙草毒害效應的機理以及誘導抗病性具有重要意義。
1 材料與方法
1.1 供試材料
供試煙草(Nicotiana tabacumL.)品種為 K326。溫室播種,育苗,于3~4片真葉期移栽。
供試藥劑為50%二氯喹啉酸可濕性粉劑,由江蘇新沂中凱農用化工有限公司生產。采用盆栽法,在土中分別混入 0(CK)、1.04×10-3、2.08×10-3、4.17×10-3、8.33×10-3和 1.67×10-2mg/kg 二氯喹啉酸。
1.2 試驗方法
1.2.1 超氧化物歧化酶(SOD)活性的測定 參照植物生理學實驗指導方法[7],稍作改動。酶液制備:取第4片展開煙草葉片,去中脈,準確稱取0.30 g(共3份)于預冷的研缽中,加入預冷的提取介質1.5 mL(分3次加入,1次研磨,2次沖洗),在冰浴中研磨成勻漿,轉移至1.5 mL離心管中,-4 ℃13 000 rpm下冷凍離心20 min,上清液即為SOD粗提液。
顯色反應:取透明度好、質地相同的試管,樣品測定管和對照管(一支遮光,2支照光),按表1加入試劑。

表1 顯色反應試劑配置Table 1 The formula of color reaction reagent
混勻后,給1支對照管罩上比試管稍長的雙層黑色硬紙套遮光,與其他各管同時置于4 000 lx紫外燈下反應 5 min(要求各管照光情況一致,反應溫度控制在 25~35 ℃之間,視酶活性高低適當調整反應時間)。
樣品超氧化物歧化酶活性的測定:
至反應結束后,用黑布罩蓋上試管,終止反應。以遮光的對照管作為空白,分別在560 nm波長下測定各管的吸光度,按下式計算SOD活性。
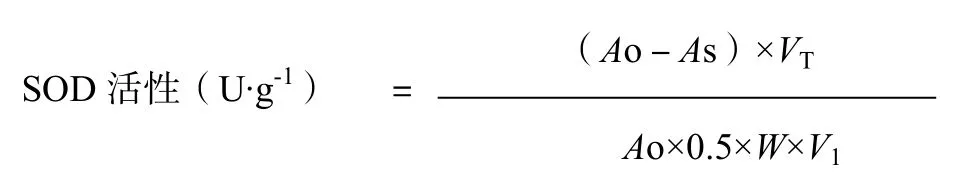
式中:SOD總活性以每克鮮重酶單位表示。A0—照光對照管的光吸收值,As—樣品管的光吸收值,V1—樣液總體積(mL),VT—測定時樣品用量(mL),W—樣品鮮重(g)。
1.2.2 超氧化物歧化同工酶的測定 參照參考文獻[7]的方法。采用聚丙烯酰胺垂直板電泳技術。分離膠濃度為10%,濃縮膠為3%。電極緩沖系統pH 7.8磷酸緩沖液,酶的進樣量30 μL,電泳是在4 ℃的冰箱中進行,電泳時間為 4h。0顯色后照相,測量各酶帶的Rf值。

1.2.3 過氧化物酶(POD)活性測定 參照參考文獻[8]的方法。準確稱取所測葉片0.3 g于預冷的研缽中,加入預冷的Tris2HCl緩沖液(pH 8.5)1.5 mL,冰浴中研磨成勻漿,轉移至1.5 mL 離心管中,-4℃,13 000 r/min 下離心20 min,取上清液分析。反應體系中加入2.8 mL含18 mmol/L愈創木酚的磷酸緩沖液和0.1 mL的酶提液(對照用0.1 mL的磷酸緩沖液代替);最后再加入0.1 mL的1%雙氧水溶液。按酶活性連續記錄法用1 cm比色皿測定反應體系在470 nm處的吸光度OD470;每個樣品重復3次,酶活性以單位鮮重葉片在單位時間內光密度的變化值表示(OD/g?min)。根據處理和對照所測的酶活力的變化,計算酶活力影響率,即:酶活力抑制或激活率/%=[(對照酶活力-處理酶活力)/對照酶活力]×100。若所得值為負值,表明為激活效應。
1.2.4 過氧化物同工酶測定 參考鄒琦的方法[7],采用聚丙烯酰胺凝膠垂直平板電泳技術。濃縮膠濃度為3%,分離膠濃度7.5%,電極緩沖系統pH 8.3(Tris甘氨酸緩沖液),上樣量每孔30 μL,穩壓電泳,在開始電泳時,調節電壓80 V,0.5 h后變為100 V。整個電泳過程在冰箱中進行,歷時3~4 h。顯色后照相,測量各酶帶的Rf值。
1.3 數據統計與分析
本研究的數據采用Microsoft Excel 2000軟件處理,并用SAS國際通用統計軟件包分析數據,對試驗結果用鄧肯氏新復極差多重比較法(Duncan,s Muitiple Range Test,DMRT)進行差異顯著性分析。
2 結 果
2.1 二氯喹啉酸對煙草超氧化物歧化酶活性的影響
從圖1可以看出,移栽后14 d,二氯喹啉酸濃度為 1.04×10-3、2.08×10-3、4.17×10-3、8.33×10-3、1.67×10-2mg/kg處理煙草SOD活性較對照有升高趨勢,分別較對照提高9.21%、32.60%、109.36%、136.16%、151.94%。移栽后 21 d,處理與對照差異不顯著。

圖1 二氯喹啉酸對煙草葉片SOD活性的動態變化Fig.1 Dynamic reaction of SOD in tobacco treated with quinclorac
2.2 二氯喹啉酸對煙草超氧化物歧化同工酶的影響
從圖2看出,煙草的超氧化物酶帶有4條,相對遷移率 Rf分別為 0.49(Rf1)、0.55(Rf2)、0.58(Rf3)、0.63(Rf4)。不同濃度二氯喹啉酸處理煙草30 d的超氧化物酶活性較對照差異不顯著。

圖2 二氯喹啉酸處理煙葉30 d的超氧化物歧化酶凝膠電泳圖Fig.2 The electrophoretogram of SOD in tobacco treated with quinclorac after 30d
2.3 二氯喹啉酸對煙草過氧化物酶活性的影響
從圖3看出,當移栽后28 d,不同濃度處理的煙草葉片酶活力達到一個峰值,對照和二氯喹啉酸濃度分別為 1.04×10-3、2.08×10-3、4.17×10-3、8.33×10-3和1.67×10-2mg/kg處理的煙草,其過氧化物酶活力分別為17.47、29.61、23.73、30.33、41.00、57.73 OD/(g?min-1),各處理的煙草葉片中過氧化物酶活性比對照分別提高69.47%、35.80%、73.61%、134.69%、230.45%。35 d所測結果表明,除1.67×10-2mg/kg濃度的煙草酶活力略有降低外,其他均呈上升趨勢(圖3),表明煙草經二氯喹啉酸處理后,過氧化物酶的活力有所提高。

圖3 二氯喹啉酸對煙草葉片POD活性的動態變化Fig.3 Dynamic reaction of POD in tobacco treated with quinclorac
2.4 二氯喹啉酸對煙草過氧化物同工酶的影響
從圖4看出,二氯喹啉酸不同處理與對照相比,煙根酶帶形態存在一定的差異。凡處理的煙草根共顯現9條酶帶,相對遷移率Rf分別為0.09(Rf1)、0.13(Rf2)、0.19(Rf3)、0.24(Rf4)、0.31(Rf5)、0.35(Rf6)、0.37(Rf7)、0.63(Rf8)、0.66(Rf9)。二氯喹啉酸處理的煙根與對照相比還新增一條酶帶 Rf1,且二氯喹啉酸處理后的酶帶顏色較對照明顯加深。隨著二氯喹啉酸施用量的增加,酶帶變寬,顯色加重,說明酶活性有所上升。二氯喹啉酸處理的煙葉誘導過氧化物同工酶活性與根所表現的活性趨于一致,不同的是誘導同工酶酶帶為10條[9]。

圖4 二氯喹啉酸處理煙草根的過氧化物酶凝膠電泳圖Fig.4 The electrophoretogram of POD in tobacco root treated with quinclorac
3 討 論
水稻與煙草輪作煙區,由于水田施用二氯喹啉酸防除稗草,殘留土壤中的二氯喹啉酸可引起后茬煙草出現畸形生長[4]。從畸形的形態分析,煙草葉面向內褶,葉色加深,嚴重時葉面僅存葉脈而無葉肉組織。盆栽試驗也表明,在不同濃度和時間下,二氯喹啉酸對煙草葉長和葉寬具有顯著的抑制效應,這些癥狀表明,二氯喹啉酸對煙草致畸作用是與抑制細胞分裂有關。但這種畸形植株不會枯萎死亡,而同樣條件下的靶標植物稗草可出現枯萎死亡現象。兩種植物對二氯喹啉酸表現出不同的中毒反應,表明煙草對二氯喹啉酸有一種解毒機制。通過檢測二氯喹啉酸對煙草兩種保護酶的反應表明,在二氯喹啉酸長時間的脅迫條件下,能誘導激活煙草保護酶的活性,測得不同濃度下,二氯喹啉酸隨著濃度升高,POD活性提高,在1.67×10-2mg/kg下,移栽28 d后可提高230%。SOD的活性在移栽后14 d達到峰值。由于保護酶具有清除自由基毒害的功能,在一定范圍內減輕由此產生的氧自由基給機體造成的損傷,使之維持煙草生活的狀態,POD和SOD在一定程度上活性都有升高,從而在清除煙草體內自由基中起到重要的作用。
試驗中二氯喹啉酸的化學脅迫使得煙草內保護酶系(SOD和 POD)活性提高,而且畸形煙草幾乎未發現感染真菌和細菌病害。由此可以得出推論,二氯喹啉酸的化學脅迫可以誘導畸形煙草內SOD和POD酶活性提高,同時增強了煙草抗病的能力。當然保護酶系還包括苯并氨酸解氨酶(PAL),多酚氧化酶(PPO)等,要具體明確二氯喹啉酸與誘導抗病效應之間的關系,還需要進一步對二氯喹啉酸對PAL和PPO酶活性的影響進行研究。該研究對于尋找誘導煙草抗病物質,提高植物潛在的抗病能力給了我們新的啟示。
[1]Kibler E,Menck B H,Rosebrock H,et al.Quinclorac-a new echinochloa-herbicide for rice and an excellent partner for broad spectrum rice herbicides[J].Proceedings 11th Asian Pacific Weed Science Society Conference,1987 (1):89-97.
[2]Grossmann K,Schmulling T.The effects of the herbicide quinclorac on shoot growth in tomato is alleviated by inhibitors of ethylene biosynthesis and by the presence of an antisense construct to theaminocyclopropane-1-carboxylic acid (ACC) synthase gene in transgenic plants[J].Plant Growth Regulation,1995,16(2):183-188.
[3]Lopez-Martinez N,Shimabukuru R H,Pradu R,et al.Effect of quinclorac on auxin induced growth,thansmembrane proton gradient and ethylene biosynthesis inEchinochloasp[J]Australian Journal of
[4]陳澤鵬,王靜,萬樹青,等.廣東部分地區煙葉畸形生長的原因及治理的研究[J].中國煙草學報,2004,10(3):34-37.
[5]王靜,陳澤鵬,萬樹青,等.二氯喹啉酸在煙草水培液中的消解動態及對煙苗生長的影響[J].廣東農業科學,2007(2):59-61.
[6]陳澤鵬,王靜,萬樹青,等.煙區土壤殘留二氯喹啉酸的消解動態[J].農藥,2007,46(7):479-480.Plant Physiology,1998,25(7):851-857.
[7]鄒琦.植物生理生化實驗指導[M].北京:中國農業出版社,1995:97-99.
[8]張志良.植物生理學實驗指導[M].北京:高等教育出版,1990:154-155.
[9]鄧建朝,萬樹青,陳澤鵬,等.二氯喹啉酸誘導煙草過氧化物酶活性的動態分析[J].植物保護學報,2006,33(3):303-306.

