菟絲子醇提液對(duì)衰老模型大鼠肝細(xì)胞p16和cyclinD1基因表達(dá)的影響
孫 潔 李 晶 歐 芹 魏曉東 樸金花 葛堂棟 王迪迪
(佳木斯大學(xué)基礎(chǔ)醫(yī)學(xué)院生物化學(xué)教研室,黑龍江 佳木斯 154007)
細(xì)胞在周期時(shí)相的變遷中進(jìn)入增殖、分化、衰老和死亡等生理狀態(tài)。細(xì)胞周期運(yùn)轉(zhuǎn)沿著G1期、S期、G2期和M期有序進(jìn)行。近年來研究表明,細(xì)胞周期調(diào)控的核心為細(xì)胞周期蛋白依賴性激酶(CDK)的活性表達(dá)與調(diào)控和不同周期時(shí)相之間的轉(zhuǎn)變的生物學(xué)意義,其中以G1/S、G2/M關(guān)卡的調(diào)節(jié)最為重要〔1〕,而細(xì)胞周期的完成依賴于一系列正負(fù)調(diào)節(jié)因子的相互作用順利渡過G1/S、G2/M兩個(gè)關(guān)卡的轉(zhuǎn)變。菟絲子常用作補(bǔ)益中藥,藥理學(xué)研究表明其具有補(bǔ)腎壯陽(yáng)、提高機(jī)體免疫能力、調(diào)節(jié)內(nèi)分泌、抗氧化等作用〔2~4〕。本實(shí)驗(yàn)旨在觀察細(xì)胞調(diào)控因子p16和cyclinD1的表達(dá),研究菟絲子醇提液的抗衰老機(jī)制。
1 材料與方法
1.1 藥品及實(shí)驗(yàn)動(dòng)物 選用 Wistar大鼠50只,雌雄各半,體重180~220 g。由佳木斯大學(xué)實(shí)驗(yàn)動(dòng)物中心提供(許可證號(hào):SYXK黑20030014)。菟絲子購(gòu)自佳木斯寶泰醫(yī)藥,由本校生藥教研室鑒定。以8倍乙醇回流提取,旋轉(zhuǎn)蒸發(fā)器回收乙醇,將菟絲子制成生藥濃度為0.15/ml的菟絲子醇提物水溶液,采用鹽酸-鎂粉實(shí)驗(yàn)鑒定菟絲子醇提液中所含成分。
1.2 動(dòng)物分組及處理 50只大鼠隨機(jī)分為青年組10只;衰老模型組10只;給藥組30只,又分15 d、30 d和45 d組,每組各10只,雌雄各半。各組正常飲食,衰老模型組和給藥組按48 mg/kg注射 D-gal,連續(xù)注射45 d后,衰老模型組按0.5 ml/100 g體重灌服溫開水;給藥組按0.8 g/kg體重灌服菟絲子醇提液。連續(xù)給藥后分別于灌服后第 15、30、45天處死動(dòng)物,提取肝組織,液氮保存?zhèn)溆谩?/p>
1.3 指標(biāo)的測(cè)定 采用Trizol法提取肝組織RNA,核酸蛋白分析儀測(cè)定RNA濃度及純度。采用電泳凝膠成像系統(tǒng)觀察mRNA表達(dá)量。RT-PCR法檢測(cè)p16、cyclin D1 m RNA表達(dá)水平:cDNA反應(yīng)體系:引物選擇Oligo d T18-Adaptor Primer,5×RNA PCR buffer 5 μ l,無 RNA 酶水 6.5 μ l,dNTP 混 合物 4 μ l,RNA 酶抑 制劑 0.5 μ l,AMV 逆 轉(zhuǎn)錄 酶 1 μ l,Oligo-dT 引 物 1 μ l,RNA 樣 品2 μ l,混勻,移入 PCR 儀,42℃ 60 min;95℃ 5 min;1 次循環(huán)。PCR反應(yīng):采用GAPDH和 β-actin作內(nèi)參,GAPDH引物5'-CTGAATTCGGGCTCTCCAGAACATCAT C-3',5'-CAGGATCCC CAGCGTCAAAGGTGGA-3'(擴(kuò)增產(chǎn)物 300 bp);β-actin引物5'-CTACAATGAGCTG CGCGTGGC-3′,5'-CAGGTCCAGACGCAGGATGGC-3'(擴(kuò)增產(chǎn)物242 bp);p16引物5'-GATGATGGGCAACGTCAAA-3',5'-AGAGTAGATACCGCAAATACCG-3'(擴(kuò)增產(chǎn)物248 bp);cyclinD1引物5'-GGAGCAGAAGTGCGAAGA-3',5'-GGGTGGGTTGGA AAT GAA-3'(擴(kuò)增產(chǎn)物394 bp)。94℃5 min,1循環(huán),94℃40 s,55℃45 s,72℃45 s;35個(gè)循環(huán),72℃7 min。PCR產(chǎn)物經(jīng)瓊脂糖電泳分離后以凝膠成像系統(tǒng)掃描,測(cè)定光密度值,并計(jì)算p16/GAPDH和cyclinD1/β-actin光密度比值。采用免疫組化SABC法檢測(cè)p16和cyclinD1蛋白的表達(dá)。
1.4 統(tǒng)計(jì)學(xué)處理 采用SPSS12.0統(tǒng)計(jì)分析軟件,實(shí)驗(yàn)數(shù)據(jù)用±s表示,進(jìn)行方差分析,q檢驗(yàn)。
2 結(jié) 果
2.1 菟絲子醇提液對(duì)衰老模型大鼠肝組織p16基因表達(dá)的影響 擴(kuò)增后得到GAPDH 300 bp和p16 248 bp兩個(gè)片段,GAPDH和p16擴(kuò)增條件完全一致。圖像分析結(jié)果(見表1,圖1,圖2)顯示:與青年組相比衰老模型組及各給藥組大鼠p16 m RNA及蛋白表達(dá)顯著增高(P<0.01);與衰老模型組比較,菟絲子30 d、45 d給藥組mRNA及蛋白表達(dá)明顯降低(P<0.01),并且兩給藥組間相比較表達(dá)無差別(P>0.05)。
2.2 菟絲子醇提液對(duì)衰老模型大鼠肝組織cyclinD1基因表達(dá)的影響 擴(kuò)增后得到 β-actin 242 bp和cyclinD1 394 bp兩個(gè)片段,β-actin和cyclinD1擴(kuò)增條件完全一致。圖像分析結(jié)果(見表2,圖3,圖4)顯示:與青年組比較,模型組及各給藥組 cyclinD1 mRNA及蛋白表達(dá)顯著降低(P<0.05);與模型組比較,菟絲子15 d、30 d、45 d給藥組 cyclin D1 mRNA及蛋白表達(dá)明顯升高(P<0.05),并且各給藥組間相比較表達(dá)有差別(P<0.05)。
表1 菟絲子醇提液對(duì)衰老模型大鼠肝組織p16基因表達(dá)的影響( ±s,n=10)

表1 菟絲子醇提液對(duì)衰老模型大鼠肝組織p16基因表達(dá)的影響( ±s,n=10)
與青年組比較:1)P<0.01;與模型組比較:2)P<0.01;給藥30 d、45 d組間比較:3)P<0.05;下表同
組別 p16/GAPDH 陽(yáng)性細(xì)胞數(shù)(%)青年對(duì)照組 0.82±0.05 8.62±4.69衰老模型組 1.32±0.09 1) 53.70±6.951)給藥15 d組 1.25±0.06 1) 48.13±5.151)給藥30 d組 1.06±0.071)2) 36.23±4.911)2)給藥45 d組 1.04±0.101)2) 32.17±7.871)2)
表2 菟絲子醇提液對(duì)衰老模型大鼠肝組織cyclinD1基因表達(dá)的影響(±s,n=10)

表2 菟絲子醇提液對(duì)衰老模型大鼠肝組織cyclinD1基因表達(dá)的影響(±s,n=10)
組別 cyclinD1/β-actin 陽(yáng)性細(xì)胞數(shù)(%)青年對(duì)照組 1.22±0.10 48.45±7.39衰老模型組 0.71±0.141) 9.40±3.141)給藥15 d組 0.96 ±0.121)2) 26.39 ±5.251)2)給藥30 d組 1.03 ±0.141)2)3) 29.40±5.34 1)2)3)給藥45 d組 1.15 ±0.131)2)3) 44.34±4.57 1)2)3)
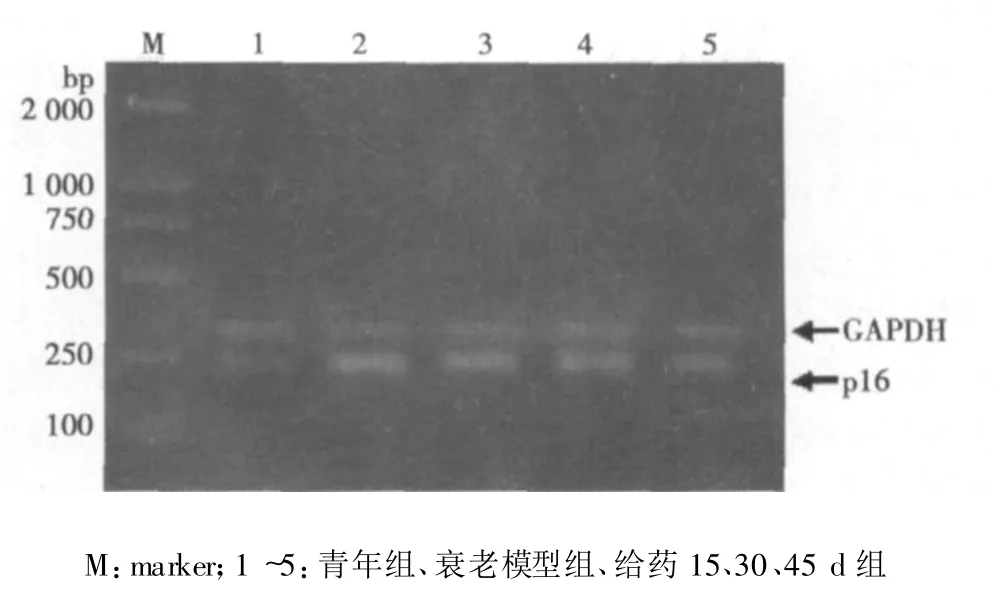
圖1 各組大鼠肝組織p16 mRNA的表達(dá)

圖2 肝細(xì)胞p16蛋白表達(dá)(×400)
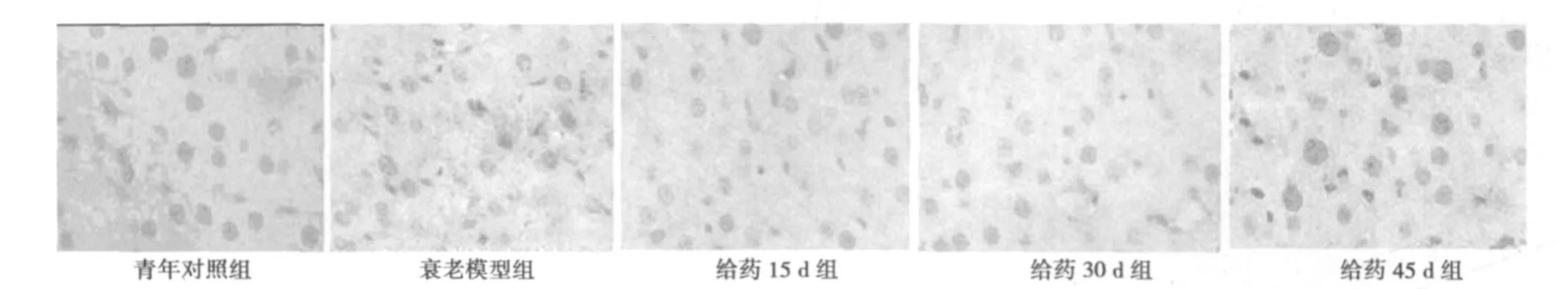
圖3 各組肝細(xì)胞cyclinD1蛋白表達(dá)(×400)
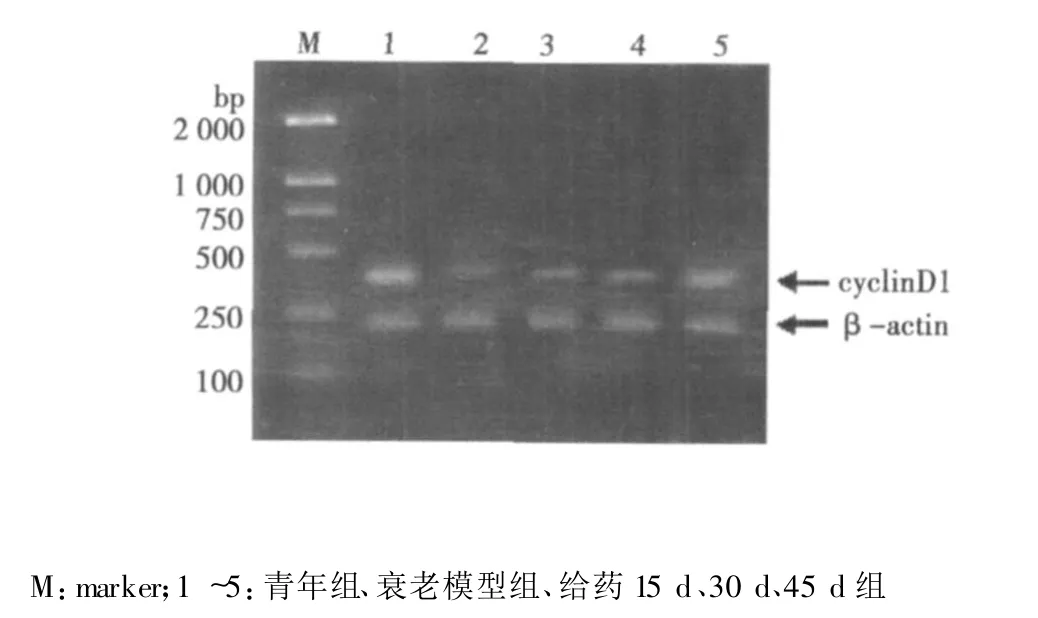
圖4 各組大鼠肝組織cyclinD1 mRNA的表達(dá)
3 討 論
目前研究發(fā)現(xiàn)哺乳動(dòng)物cyclin有9大類,主要有 cyclinA、B(1、2)、C、D(1、2、3)和 E 等,其中以 D1 的作用最為重要〔5〕,是大多數(shù)組織增殖所必需的。關(guān)于CyclinD1與衰老的關(guān)系已成不爭(zhēng)的事實(shí),它通過與CDK結(jié)合成復(fù)合物,在細(xì)胞周期各相應(yīng)時(shí)期發(fā)揮調(diào)節(jié)作用。本實(shí)驗(yàn)研究結(jié)果說明D半乳糖衰老模型大鼠cyclinD1的表達(dá)水平明顯降低,而各菟絲子組則較模型組顯著提高。多數(shù)學(xué)者研究發(fā)現(xiàn),細(xì)胞周期停滯是細(xì)胞衰老的一個(gè)關(guān)鍵特征,衰老細(xì)胞主要停滯于G1期,不能順利進(jìn)人S期。Cyclin D1作用于G1/S期轉(zhuǎn)換過程,促使細(xì)胞從G1期進(jìn)入S期。在G1期,cyclinD與 CDK4/CDK6結(jié)合,使后者激活,活化的CDK4可使Rb磷酸化,特別是磷酸化組蛋白R(shí)b。在細(xì)胞的G1期,Rb與 E2F-DP1雜二聚體結(jié)合,在cyclin D-CDK作用下,磷酸化的Rb與雜二聚體分離,結(jié)合狀態(tài)的E2F變成游離狀態(tài)即可發(fā)揮啟動(dòng)DNA合成的作用,從而促使細(xì)胞由 G1期進(jìn)入S期〔6~10〕。衰老時(shí) cyclin D1表達(dá)的下降,可能通過減少 CDK4活化,進(jìn)而抑制Rb的磷酸化,從而減少E2F的游離,減慢細(xì)胞從G1進(jìn)入S期,菟絲子醇提液通過上調(diào)cyclinD1的表達(dá)而增加cyclinD1的表達(dá),可能通過 CDK4/CDK6的活化,催化 Rb磷酸化而加速 E2F與Rb分離,促使細(xì)胞進(jìn)入 S期,而發(fā)揮延緩細(xì)胞衰老的作用。
p16是細(xì)胞周期依賴性激酶抑制因子(CDKI),是細(xì)胞周期的負(fù)調(diào)節(jié)因子,通過抑制CDK的活性使Rb正常地行使G1期阻滯功能,使細(xì)胞周期停止,阻斷細(xì)胞增殖〔11~13〕。衰老時(shí)的p16表達(dá)增加,可通過與cyclin D競(jìng)爭(zhēng)性結(jié)合CDK4/CDK6,P16-CDK復(fù)合物不能使Rb磷酸化,抑制cyclin D1-CDK復(fù)合物的活性,使細(xì)胞阻滯在G1期。而菟絲子醇提液可以通過降低p16的表達(dá),減少其與Cyclin D競(jìng)爭(zhēng)結(jié)合CDK,而使cyclin D1激活CDK4的過程不受抑制,從而促進(jìn)細(xì)胞從G1進(jìn)入S期,發(fā)揮延緩衰老的作用。
1 Nielson NH,Loden M,Cajander J,et al.G1-S transition defects occur in most breast cancers and predict outcome〔J〕.Breast Cancer Res,1999;56(2):105-12.
2 柯江維,王建紅,趙 宏 .菟絲子黃酮對(duì)心理應(yīng)激雌性大鼠海馬-下丘腦-垂體-卵巢軸性激素受體的影響〔J〕.中草藥,2006;37(1):90-2.
3 楊 欣,丁彩飛,張永華,等 .菟絲子水提物對(duì)人精子頂體和超微結(jié)構(gòu)的保護(hù)作用〔J〕.中國(guó)中藥雜志,2006;31(5):422-5.
4 樸金花,歐 芹,王 昭,等 .生菟絲子、鹽菟絲子對(duì)D-半乳糖所致衰老模型小鼠免疫功能影響〔J〕.中國(guó)老年學(xué)雜志,2005;25(2):452-3.
5 Grana X,Heddy EP.Cell cycle control in mammalian cells:role of cyclins,cyclin dependent kinases(CDKs),growth suppressor genes and cyclin-dependent kinase inhibitors(CKIs) 〔J〕.Oncogene,1995;11(1):21-9.
6 Serrano M,Hannon GJ,Beach D.A new regulatory modify in cell cycle control causing specific inhibitor of cyclinD/CDK4 〔J〕.Nature,1999;366:704.
7 Dreyling MH,Bullinger L,Ott G,et al.Alteration of the cyclinD1/p16-pRb pathway in mantle cell lymphoma〔J〕.Cancer Res,2005;57:4608-14.
8 Easton J,Wei T,Lahti JM,et al.Disruption of the cyclinD/cyclin-dependent kinase/INK4 l retinoblastoma protein regulatory pathway in human neuroblastoma〔J〕.Cancer Res,1998;58:2624-32.
9 Fong LY,Nguyen VT,Farber JL,et al.Early deregulation of the pl6ink4a-cyclinD1/cyclin-dependent kinase 4-retinoblastoma pathway in cell proliferation-driven esophageal tumorigenesis in zinc-deficient rats〔J〕.Cancer Res,2000;60(16):4589-95.
10 Serrano M,Gregory J,Hannon S,et al.A new regulatory motif in cell-cycle control causing specific inhibition of cyclinD/CDK4〔J〕.Nature,2004;366:704-7.
11 鄭文婕,童坦君,張宗玉 .細(xì)胞衰老的重要通路:p16INK4a/Rb和p19ARF/p53/p21cip1信號(hào)途徑〔J〕.生命的化學(xué),2002;22(4):314.
12 Rues M,Peters C.The p1611 NK4a/CDKN2.4 tumor suppressor and its relatives〔J〕.Biochim Biophys Acta,1998;14:115-77.
13 Geradts J,Kratzke RA,Niehans GA,et al.Immunohistochemical detection of the cyclin-dependent kinase inhibitor2/multiple tumor suppressor gene1(CDKN2/MTS1)product p16ink4a in archival human solid tumors:correlation with retinoblastoma protein expression〔J〕.Cancer Res,2005;55:6006-11.

