人參總皂苷和枸杞多糖的溶解特性與脂質體包封率的關系研究
郭偉英,吳 迪(遼寧醫學院藥學院,錦州市 121001)
人參總皂苷為人參的主要有效組分之一,是人參根的主要生理活性物質。人參總皂苷有抗皮膚衰老、改善記憶、抑制細胞凋亡、抑制腫瘤生長和降糖降脂等藥理活性[1,2]。
枸杞屬植物枸杞Lycium barbarumL.為多棘刺落葉小灌木,抗旱能力很強,其漿果枸杞子在《神農本草經》中引為上品。枸杞多糖對機體具有非特異性免疫調解功能[3],可調節機體免疫力,抑制腫瘤生長和細胞突變,延緩衰老,提高適應能力,并具有抗疲勞和加速消除疲勞作用[4]。
脂質體作為靶向給藥的載體已被廣泛研究。人參總皂苷和枸杞多糖制成脂質體有利于其藥理活性及生物利用度的提高。在脂質體的制備中,影響包封率的因素有原料的種類和用量、制備方法以及藥物性質等,其中藥物性質中溶解特性最為重要,因為它決定藥物是否適合制成脂質體。本研究在其他因素固定的條件下,制備2種不同性質的藥物以期找出藥物的溶解性質對脂質體包封率的影響,這方面在國內研究得較少。本研究可為人參總皂苷和枸杞多糖是否適合制成具有高包封率的脂質體提供試驗數據,并為在試驗前判斷其他藥物是否適合制備成脂質體提供參考依據。
1 儀器與試藥
RE-52A型旋轉蒸發儀(上海亞榮生化儀器廠);JY96-I1型超聲波細胞粉碎儀(寧波新芝科學儀器研究所);XS205DV型電子天平(瑞士梅特勒-托利多公司);UV-2450型紫外分光光度儀(日本島津公司);G-50葡聚糖凝膠柱(上海保曼生物科技有限公司)。
人參皂苷Rbl對照品(中國藥品生物制品檢定所,批號:110704-200820);人參總皂苷原料藥(遼寧鑫泰藥業有限公司,人參總皂苷含量≥80%,批號:20081120);枸杞多糖原料藥(西安易楊生物技術有限公司,批號:20080610);葡萄糖標準品(上海楚柏試驗室有限公司,含量≥98%);大豆磷脂(上海金伴藥業有限公司,批號:20080904);膽固醇(天津東方試劑廠);G-50葡聚糖凝膠(上海化學試劑廠);乙醇(天津市科密歐化學試劑有限公司);水為雙蒸水,其他試劑均為分析純。
2 方法與結果
2.1 藥物基本理化性質的考察
2.1.1 溶解度的考察 按2010年版《中國藥典》(二部)凡例項下規定操作,取藥物適量,于(25±2)℃一定量溶劑中,每隔5 min強力振搖30 s,觀察30 min內的溶解情況,在看不到溶質顆粒時,即認為已完全溶解。考察藥物在常用溶劑水、甲醇、乙醇、氯仿、丙酮、乙醚中的溶解情況,詳見表1。
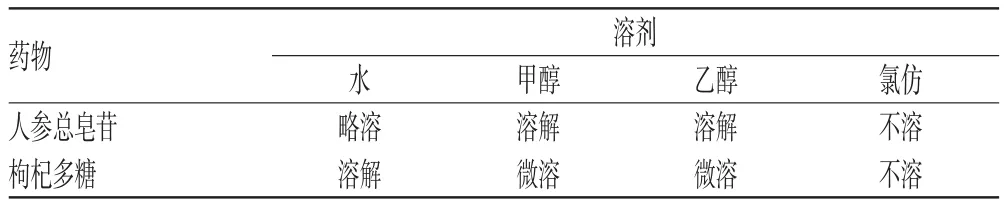
表1 藥物在常用溶劑中的溶解情況Tab1 Dissolution of drugs in common solvents
2.1.2 油水分配系數(P)的測定 將溶有定量藥物的飽和溶液和經水飽和過的正辛醇溶液各10 mL,裝入三角瓶中,在一定強度下渦旋振蕩24 h,靜置15 min后兩相分層,分離出水相,將水相以3 000 r·min-1離心10 min,用高效液相色譜(HPLC)法分別測定人參總皂苷和枸杞多糖濃度(CW)。將水相中原來藥物濃度定為C0,則分配后油相中藥物濃度為C0-CW,P=(C0-CW)/CW。結果,LogP人參總皂苷=0.45(正辛醇-水,n=3)、LogP枸杞多糖=0.98(正辛醇-水,n=3),表明人參總皂苷的P為0.45,枸杞多糖的P為0.98。
2.2 處方優化
選取對水溶性藥物包封率影響較大的4個因素,即大豆磷脂與膽固醇重量比(A)、超聲時間(B)、溫度(C)、藥液濃度(D)為考察對象。每個因素各取3個水平,用L9(34)正交表安排試驗,每組重復3次。因素水平見表2。

表2 因素水平Tab2 Factors and levels
2.3 制備工藝
采用逆相蒸發法制備。按表1中的比例將大豆卵磷脂和膽固醇溶于氯仿后,轉移到圓底燒瓶中;在不同溫度下進行減壓旋轉蒸發,使瓶內壁形成一層脂質薄膜,加入6 mL乙醚薄膜溶解,再加入2 mL水相,超聲乳化,置于旋轉蒸發儀上旋轉蒸發并負壓抽吸至乙醚揮發盡,即得到脂質體懸液。人參總皂苷脂質體和枸杞多糖脂質體均按此法制備。
2.4 包封率的測定
2.4.1 標準曲線的制備 (1)人參總皂苷的標準曲線:精密稱取已干燥至恒重的人參皂苷Rb1對照品6.4 mg,置于50 mL容量瓶中,將蒸餾水加至刻度,制成人參皂苷Rb1貯備液。分別從此貯備液中吸出6、7、8、9、10 mL,分別定容至10 mL。用紫外分光光度計于232 nm波長處,以蒸餾水為空白,測定各吸光度。以吸光度(A)為縱坐標,人參皂苷Rb1檢測濃度(c)為橫坐標,制備標準曲線,得回歸方程為A=1.084 2c-0.050 1(r=0.986 6,n=5)。結果表明,人參總皂苷Rb1檢測濃度在0.076 8~0.128 0 mg·mL-1范圍內與吸光度呈良好的線性關系。(2)枸杞多糖的標準曲線:采用苯酚-濃硫酸顯色法。精密稱取已干燥至恒重的葡萄糖標準品50 mg,置于50 mL容量瓶中,加水至刻度。吸出0.5、1.0、1.5、2.0、2.5 mL,置于25 mL容量瓶中,加水至刻度,各取1 mL置于10 mL試管中,加5%苯酚1 mL,迅速加入5 mL濃硫酸,冷水浴冷卻至室溫;水同法為空白,在450~500 nm波長范圍內測定吸光度。以吸光度(A)為縱坐標,枸杞多糖檢測濃度(c)為橫坐標,制備標準曲線,得回歸方程為A=0.871 9c-0.012 1(r=0.998 8,n=5)。結果表明,枸杞多糖檢測濃度在0.01~0.12 mg·mL-1范圍內與吸光度呈良好的線性關系。
2.4.2 不同藥物的脂質體紫外吸收結果 (1)取適量人參皂苷Rb1對照品、人參總皂苷脂質體和空白脂質體,將人參皂苷脂質體和空白脂質體用無水乙醇破乳后,在200~400 nm波長范圍內進行光譜掃描。由波譜圖可知,人參皂苷Rb1對照品、人參總皂苷脂質體在232 nm波長處均有吸收,故選擇232 nm為檢測波長。(2)取適量枸杞多糖標準品、枸杞多糖脂質體和空白脂質體,將枸杞多糖脂質體和空白脂質體用無水乙醇破乳后,在300~700 nm波長范圍內進行光譜掃描。由波譜圖可知,枸杞多糖標準品、枸杞多糖脂質體均在485 nm波長處有吸收,故選擇485 nm為檢測波長。
2.4.3 包封率的測定 取同批脂質體共2份,每份1 mL,一份置25 mL量瓶中,用乙醇破乳;另一份上G-50葡聚糖凝膠柱,流速為1 mg·min-1,收集洗脫液,將分離得到的脂質體置于25 mL量瓶中,用乙醇破乳,2份樣品用乙醇定容。然后分別測定2份樣品的吸光度,計算出藥物總量(W總)和包進脂質體內的藥物量(W包),按下式計算包封率:包封率(%)=W總/W包×100%。
2.5 正交試驗結果
按表2中各因素水平進行試驗,以包封率為評價指標,優選工藝。人參總皂苷脂質體的正交試驗結果見表3;人參總皂苷脂質體的方差分析結果見表4;枸杞多糖脂質體的正交試驗結果見表5;枸杞多糖脂質體的方差分析結果見表6。
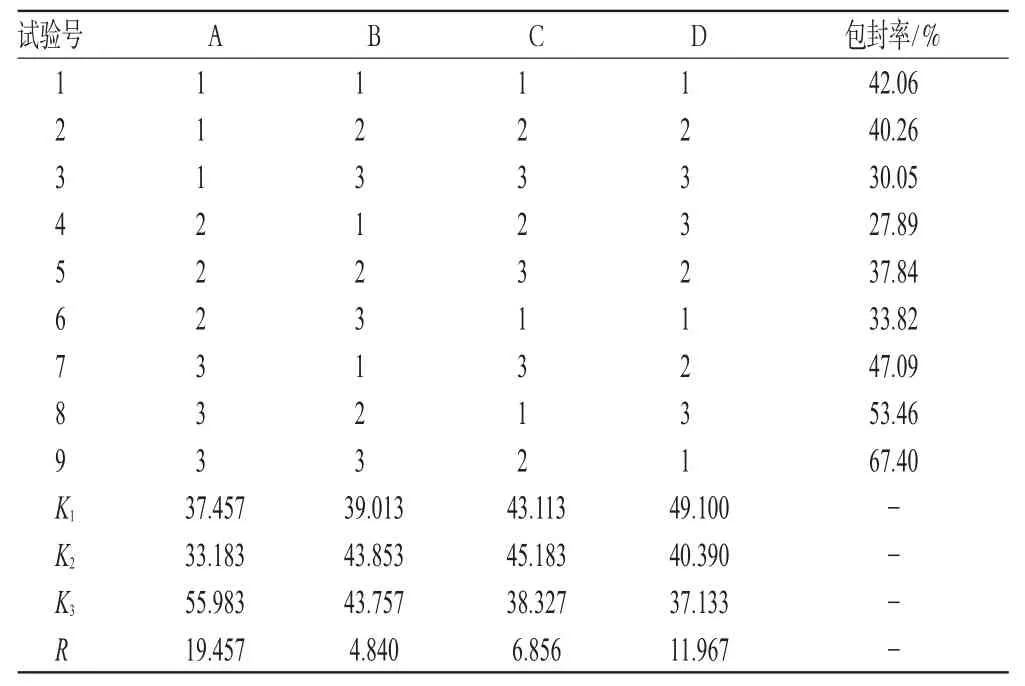
表3 人參總皂苷脂質體的正交試驗結果Tab3 Results of orthogonal experiment of ginsenoside
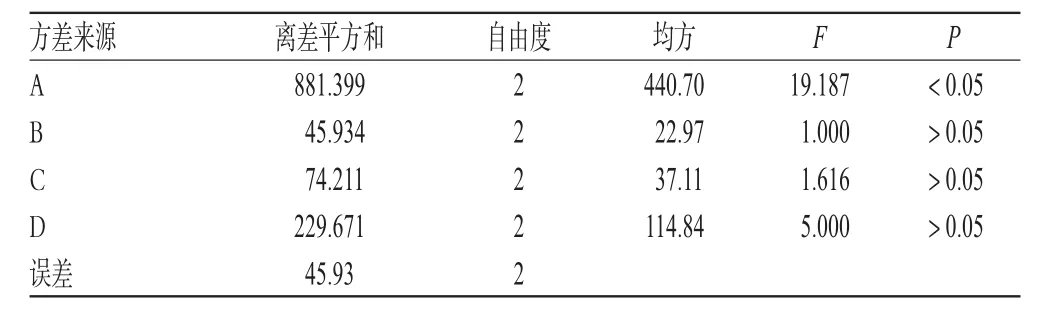
表4 人參總皂苷脂質體的方差分析結果Tab4 Analysis of variance of ginsenoside liposome
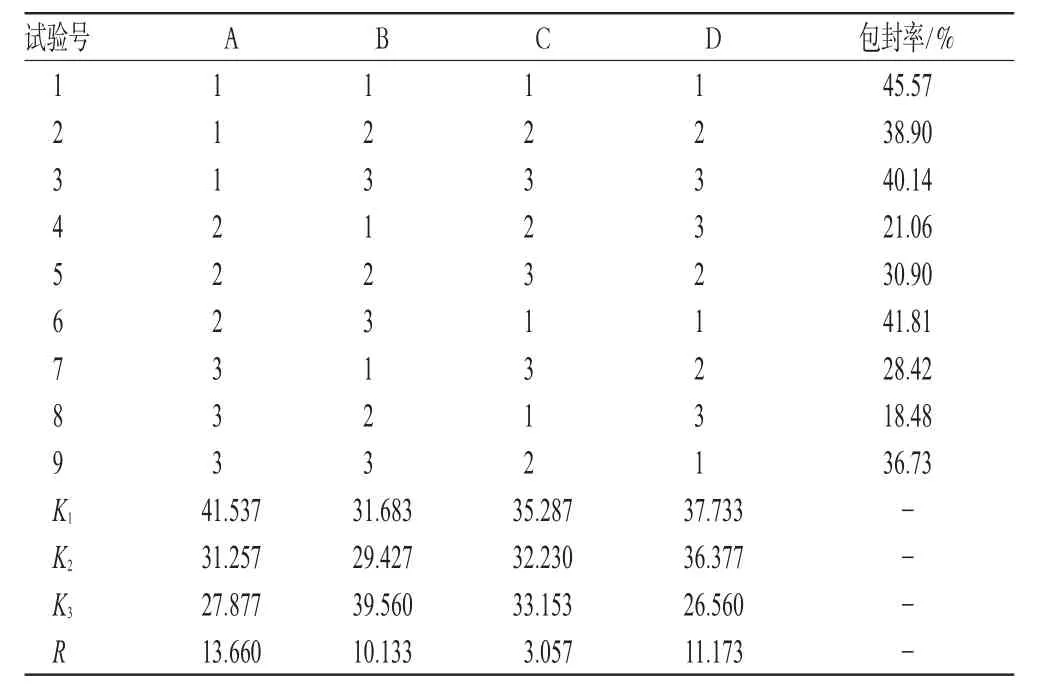
表5 枸杞多糖脂質體的正交試驗結果Tab5 Results of orthogonal experiment of LBPliposome
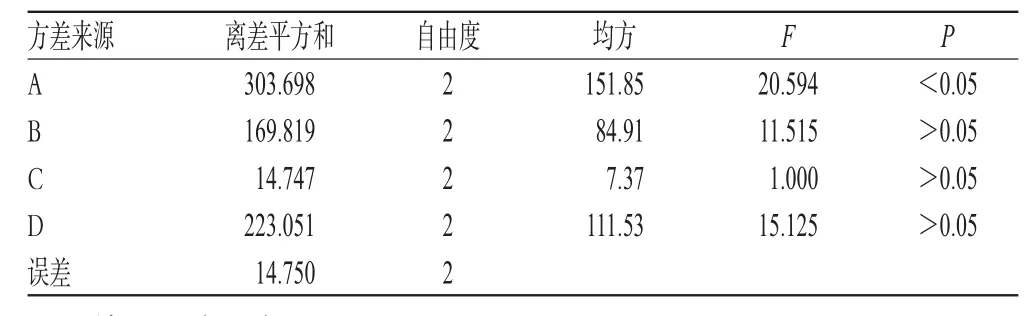
表6 枸杞多糖脂質體的方差分析結果Tab6 Analysis of variance of LBPliposome
由表3、表4可知,大豆磷脂與膽固醇重量比對人參總皂苷脂質體包封率的影響顯著,其次是藥液濃度、超聲溫度,反應時間影響較小;最優工藝為A3B2C2D1,即大豆磷脂與膽固醇重量比是1∶3,超聲時間8 min,反應溫度35℃,藥液濃度6 g·L-1。
由表5、表6可知,大豆磷脂與膽固醇重量比對枸杞多糖脂質體包封率的影響顯著,藥液濃度、超聲時間、反應溫度影響較小;最優工藝為A1B3C1D1,即大豆磷脂與膽固醇重量比是1∶1,超聲時間10 min,反應溫度25 ℃,藥液濃度6 g·L-1。
2.6 統計學分析
按優化的工藝分別制備3批人參總皂苷脂質體和枸杞多糖脂質體,按“2.4”項下方法測定包封率,結果見表7。

表7 包封率測定結果Tab7 Results of entrapment efficiency
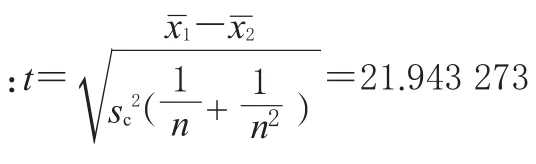
3 討論
本研究是對制備脂質體條件的探討,而人參總皂苷含量測定只是作為規律探索的一個中間指標,并不作為定量測定項,故只用了人參皂苷Rb1為對照測定含量。
本研究采用了相同的輔料和方法(經典的逆向蒸發法)制備2種藥物的脂質體。結果,人參總皂苷脂質體包封率為59.06%,枸杞多糖脂質體包封率為47.61%,因此可知2種藥物脂質體的包封率存在明顯差異。由于2種藥物的制備方法、試驗試劑用品和實驗室條件及人員等其他條件完全相同,因此這種差異是由藥物本身性質引起的。首先人參總皂苷在水中略溶,在甲醇和乙醇中溶解,且在甲醇中的溶解度大于在乙醇中溶解度,人參總皂苷在水相和油相中均具有一定溶解度。枸杞多糖在甲醇和乙醇中微溶,溶解度比人參總皂苷低。溶解度對微粒載藥量、包封率的影響顯著,藥物溶解度越高,其脂質體包封率就越高[5]。
文獻報道[6],脂質體的包封率與該藥物的P有密切關系。若脂溶性特別好或水溶性特別好,一般使用藥物在正辛醇-水相中的LogP來表示這種性質,只有LogP>4.5的脂溶性藥物或者LogP<0.3的水溶性藥物才能包封成具有較高包封率且穩定的脂質體;而對于LogP具有中間值(0.3<LogP<4.5)的藥物,即使包封脂質體后,藥物也會迅速滲漏[7]。其原因是親脂性或親水性強的藥物分布在脂質體的油相或水相,容易得到高的包封率;而兩親性的藥物,由于在脂質體的油相和水相都有一定的溶解度,故容易穿膜而發生泄漏。人參總皂苷和枸杞多糖都屬于兩親性藥物,包封率都不高,然而人參總皂苷LogP更接近于臨界值0.3,處于邊界處,因此人參總皂苷脂質體的包封率比枸杞多糖脂質體的包封率略高。因而,藥物的溶解性質對脂質體的包封率具有重要影響,而藥物的其他性質對包封率的影響也值得進一步的研究。
[1]李泰平.人參皂苷藥理活性的研究進展[J].生物學教學,2003,28(4):1.
[2]王紅麗,吳 鐵,吳志華,等.人參皂苷抗皮膚衰老作用試驗研究[J].廣東藥學院學報,2003,19(1):26.
[3]張意靜.食品分析[M].北京:中國輕工業出版社,2002:181-183.
[4]方建國,丁水平,田庚元.枸杞多糖藥理作用與臨床應用[J].醫藥導報,2004,23(7):484.
[5]吳俊珠,王成軍,金 拓.賴諾普利微粒載藥量與包封率影響因素研究[J].大理學院學報,2010,9(2):6.
[6]鄧英杰,史淑芬,顧學裘.油酸多相脂質體(139)注射液包封率測定方法的研究[J].藥學學報,1988,23(7):539.
[7]陳新梅,朱家壁.人參皂苷Rg1的溶解特性與脂質體包封率關系的研究[J].中國藥房,2007,18(1):41.

