結核性胸膜炎合并組織細胞壞死性淋巴結炎一例
黃 玲,王開綠,鄭曉鳳,李文軍,劉艷群,劉 藺,蒙 琴
組織細胞壞死性淋巴結炎 (histocytic necrotizinglymphadenitis,HNL) 又 稱Kikuchi病[1]或 Kikuchi-Fujimato病,是一種由多種病因所致的非腫瘤性淋巴結疾病,好發于青年人,伴高熱、淋巴結腫大,以頸部淋巴結腫大多見,外周血白細胞計數正常或下降,紅細胞沉降率 (血沉)加快、C反應蛋白升高。臨床上常誤診為淋巴結結核、淋巴瘤等,誤診率約40%[2]。本例患者在結核性胸膜炎的治療過程中出現發熱、頸部淋巴結腫大,免疫學檢查異常,經淋巴結活檢病理診斷為HNL,給予抗結核及糖皮質激素治療后痊愈,隨訪2年未復發。提示結核性胸膜炎、HNL及免疫學異常之間可能存在某種內在聯系,結核菌感染可能是HNL及免疫學異常的誘因。
1 病例簡介
患者,男,27歲,因“潮熱、盜汗2個月,胸悶、氣促1個月”入院。患者入院前2個月不明誘因出現潮熱、盜汗,伴乏力、納差,偶有咳嗽,咳少許白色泡沫痰,無胸痛、咯血等不適,未予特殊處理。入院前1個月出現胸悶、氣促,無心悸、水腫等。患者患病以來精神較差,體質量下降約5 kg。入院時查體:體溫37℃,無力體型,全身淺表淋巴結未捫及腫大,右胸第4肋以下叩診濁音,呼吸音消失。血常規:白細胞計數 5.81×109/L,中性粒細胞分數 0.650,淋巴細胞分數0.170,血紅蛋白121 g/L,血小板216×109/L;結核菌素試驗 (PPD)(+);血結核抗體 (TBAb)弱陽性;痰涂片抗酸染色 (-);血沉61 mm/h;C反應蛋白61.3 mg/L;胸腔積液常規:李凡他 (Rivalta)試驗 (++),白細胞計數6×106/L,胸腔積液生化:蛋白 (TP)53.2 g/L,腺苷脫氨酶 (ADA)33 U/L,乳酸脫氫酶 (LDH)274 U/L;胸腔積液涂片抗酸染色 (+);胸腔積液脫落細胞學檢查 (-)。胸部CT:右側胸腔積液。胸腔B超:右側胸腔中量積液。給予異煙肼0.3 g,1次/d;利福平0.45 g,1次/d;吡嗪酰胺1.5 g,1次/d;乙胺丁醇0.75 g,1次/d,并行胸腔穿刺抽出胸腔積液730 ml。抗結核治療10 d后,患者潮熱、盜汗、氣促減輕,但仍感乏力、納差。治療13 d后,患者出現發熱,體溫36.4~39.6℃,多在夜間出現,為弛張熱型。加用潑尼松40 mg/d,臨時使用柴胡、安痛定,體溫下降后又升高。治療18 d后,患者出現雙側頸部淋巴結腫大伴壓痛。查人類免疫缺陷病毒 (HIV)(-);瘧原蟲 (-);肥達氏-外斐氏試驗 (-);血培養 (-);復查血常規:白細胞計數3.35×109/L,中性粒細胞分數0.373,淋巴細胞分數0.445;免疫學檢查:IgG 23.9 g/L,IgA 3 130 mg/L,IgE 776.08 U/ml,循環免疫復合物(CIC)0.16 OD,抗核抗體 (ANA)+1∶100斑點型,抗干燥綜合征A抗體 (抗SSA)(++),抗干燥綜合征B抗體 (抗SSB)(+)。取左側頸部淋巴結活檢,病理學檢查示:HNL(見圖1)。給予甲潑尼龍80 mg,2次/d,連用3 d,改為琥珀氫化可的松100 mg,2次/d,連用3 d,再改為琥珀氫化可的松150 mg,1次/d,連用3 d,后改為潑尼松40 mg/d,逐漸減量停藥,糖皮質激素總療程35 d。患者體溫恢復正常,腫大淋巴結消失。抗結核治療3個月后,患者潮熱、盜汗、氣促、乏力、納差消失,體質量增加,復查胸部CT:右側少量胸腔積液;胸部B超:右側少量胸腔積液。繼續抗結核治療至9個月,復查胸部CT:右側胸膜增厚,停抗結核治療。隨訪頸部淋巴結、血常規、胸部CT兩年無異常發現,患者拒絕免疫學復查。
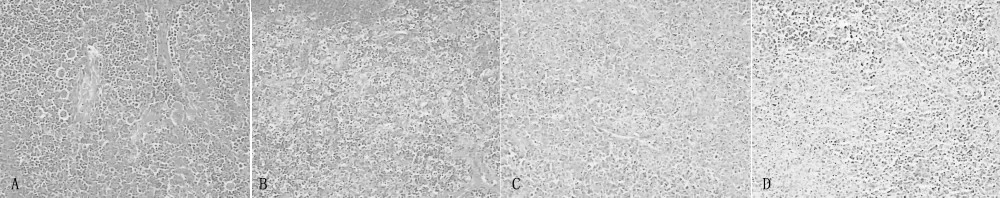
圖1 左頸部淋巴結活檢病理學檢查低倍放大 (HE染色)Figure1 Pathological results of left cervical lymph node
2 討論
本例患者以潮熱、盜汗、胸悶、氣促入院。入院時體溫正常,消瘦,全身淺表淋巴未捫及腫大,右側胸腔積液征。白細胞計數正常,PPD皮試 (+),血TBAb弱陽性,血沉加快、C反應蛋白升高。胸部影像學檢查示:右側胸腔積液。胸腔積液檢查提示滲出液,胸腔積液涂片抗酸染色 (+),診斷結核性胸膜炎,予抗結核治療,患者潮熱、盜汗、氣促減輕。之后患者出現發熱,復查血常規白細胞計數下降,淋巴細胞百分數增高,進行一些相關檢查無陽性發現,考慮類赫氏反應,加用口服潑尼松并于臨時對癥處理,體溫下降后又升高。此后患者出現雙側頸部淋巴結腫大伴有壓痛。行左側頸部淋巴結活檢術,病理學檢查示:HNL。予甲潑尼龍、琥珀氫化可的松靜脈使用,后改為潑尼松,逐漸減量停藥,患者體溫恢復正常,腫大淋巴結消失。繼續服用抗結核藥物至9個月,復查胸部CT病變消失,停抗結核治療,隨訪2年無異常發現。從該患者臨床經過來看,結核性胸膜炎合并HNL的診斷是成立的。
該病例有以下幾個方面值得探討:(1)該患者在抗結核治療的過程中出現發熱、淋巴結腫大,按照一元論的原則首先考慮類赫氏反應或淋巴結核,但淋巴結活檢病理學檢查未提示毛細血管擴張滲透性增加、中性粒細胞滲出、巨噬細胞、淋巴細胞聚集成結節等類赫氏反應的表現及干酪樣壞死、類上皮樣細胞、郎漢斯巨細胞或查見結核桿菌等淋巴結核的表現,不支持類赫氏反應或淋巴結核。故在結核性胸膜炎的病程中若出現發熱、淋巴結腫大等,除考慮類赫氏反應、淋巴結核、淋巴瘤等,還應考慮合并HNL,盡早行淋巴結活檢以明確。據報道,HNL是一種免疫相關疾病,其病因除了病毒感染以外,還可能與包括結核在內的分枝桿菌感染有關[3-4]。本病例可能是該學說的又一個例證。(2)本病例免疫學檢查異常。楊佩珍等[5]報道結核感染可引起自身免疫性疾病。其機制可能為機體感染結核菌后,菌體釋放可溶性結核蛋白,激活機體細胞和體液免疫,產生抗核抗體、循環免疫復合物等,出現免疫學異常。HNL病因尚不清楚,鐘英強等[6]研究發現可能與感染病毒、弓形蟲、結核桿菌等引起超敏反應或自身免疫性反應有關,多數預后良好,但亦可與各種自身免疫性疾病相關聯,如系統性紅斑狼瘡 (SLE)、結節硬化癥、多發性關節炎等。林瑩等[7]報道1例SLE合并 HNL;巫斌[8]報道1例 HNL演變為SLE,亦有報道稱若抗核抗體陽性,則可能發展為SLE。本例患者結核性胸膜炎、HNL診斷明確,免疫學檢查IgG、IgA、IgE、循環免疫復合物增高,ANA、抗SSA抗體、抗 SSB抗體陽性,故推測結核性胸膜炎、HNL與免疫學異常/自身免疫性疾病在發病機制上可能有某種聯系,就本例患者而言,推測結核菌感染為HNL與免疫學異常的病因。由于目前少見有報道,故對于診斷為結核性胸膜炎、HNL或兩者合并存在的患者有必要行免疫學檢查及加強隨訪,以觀察患者的轉歸。(3)本例患者出現發熱、淋巴結腫大等表現,使用口服潑尼松后癥狀緩解不明顯,后靜脈給予甲潑尼龍、琥珀琥珀氫化可的松,以上癥狀很快消失,再改為潑尼松口服,逐漸減量停藥,癥狀未再復發。本例患者治療經過表明,結核性胸膜炎并HNL,且又伴有 ANA陽性的患者,全身炎癥反應較重,選用作用較強的糖皮質激素靜脈使用,可較快緩解病情。當然,本例僅為個案,尚需較大的樣本量來研究證實。
1 Kikuchim.Lymphadenitis showing focal reticulum cell hyperplasia with nuclear debris and phagocytosis[J].Nippon Ketsueki Gakkai Zasshi,1972,35(3):379-380.
2 Menasce LP,Banerjee SS,Edmondson D,et al.Histiocytic necrotizing lymphadenitis Kikuchi-Fujimoto disease:continuing diagnostic difficulties[J].Histopathology,1998,33(3):248-254.
3 廖新波,莊恒國,林華歡,等.組織細胞壞死性淋巴結炎[J].臨床與實驗病理學雜志,2001,17(2):117-119.
4 丁順利,趙天如,張乃鑫,等.結核性淋巴結炎:組織細胞性壞死性淋巴結炎樣變型[J].天津醫藥,1997,25(3):166.
5 楊佩珍,閔偉琪,鄭錫銘,等.結核感染與自身免疫疾病[J].中華結核和呼吸雜志,1993,16(5):261.
6 鐘英強,黃花榮,李海剛.組織細胞性壞死性淋巴結炎的臨床和病理特征[J].美國中華健康衛生雜志,2000,3(10):15-18.
7 林瑩,鐘英強,李海剛.SLE合并組織細胞壞死性淋巴結炎1例報告[J].新醫學,2002,33(7):425-427.
8 巫斌.組織細胞壞死性淋巴結炎演變為系統性紅斑狼瘡伴曲霉菌感染1例[J].福建醫科大學學報,2005,39(2):120.

