三種阿爾茨海默病小鼠模型的建立和比較
程 欣 馬劉紅 徐建兵 陳 彥 羅煥敏 (暨南大學醫學院組胚系,廣東 廣州 50632)
阿爾茨海默病(Alzheimer's disease,AD)是一種與衰老相關、以認知功能下降為特征的漸進性腦退行性疾病。AD患者大腦皮質彌散性萎縮,神經元丟失,突觸減少,細胞外β淀粉樣蛋白(amyloid β-protein,Aβ)沉積形成老年斑(senile plaque,SP)和細胞內tau蛋白異常磷酸化導致神經原纖維纏結(neurofibrillary tangle,NFT)形成是其特征性病理變化。由于AD是多因素引起的、涉及多種病理機制的多因異質性疾病,建立精準復制AD病理特征和臨床癥狀的動物模型有一定困難,從而影響AD的深入研究。模型是評價實驗結果的重要依據,因此,確立合適的AD模型是實驗的基礎。本實驗分別采用側腦室注射Aβ25-35、AlCl3和海馬物理損傷三種方法復制出不同的AD小鼠模型,旨在建立并比較這幾種常用模型的特點。
1 材料與方法
1.1 實驗動物 SPF級雌性昆明小鼠90只,體重25.0~30.0 g,購自廣東省醫學實驗動物中心,合格證2009A022。
1.2 試劑和儀器 Aβ25-35(Sigma,Cat:A4559)。Aβ25-351 mg溶于 100 μl滅菌生理鹽水中,濃度為 10 μg/μl,4℃ 冰箱保存,使用前封口置于37℃孵育96 h。AlCl3(天津市福晨化學試劑廠)。2.5 g AlCl3溶解于100 ml滅菌生理鹽水中,4℃冰箱貯存備用。兔抗 β1-40多克隆抗體、SABC免疫組化試劑盒(均Boster),DAB(福州邁新)。自制針頭(取9號注射針頭,于距針尖1 mm處彎折90°)。通用型Morris水迷宮自動實驗記錄儀器(上海吉量公司),DY-1型腦立體定位儀(天津市醫療器械研究所),微量注射器(寧波市鎮海玻璃儀器廠)。
1.3 方法
1.3.1 動物分組 90只小鼠分6組,每組15只。①正常對照組:動物未經任何處理。②Aβ25~35損傷模型組:小鼠經3%戊巴比妥鈉(40 mg/kg)腹腔注射麻醉,固定于腦立體定位儀,暴露前囟,參照小鼠腦立體定位圖譜,每只小鼠右側腦室注射3 μl Aβ25-35(濃度2 μg/μl);坐標為前囟后1.2 mm,矢狀縫右側旁開1.2 mm,即為側腦室的體表部位(圖1),進針深度為顱骨表面向下3.2 mm;注射時進針1 μl/min,注射后留針8 min,拔針時速度為1 mm/min,動物清醒后歸籠飼養。③AlCl3損傷模型組:小鼠右側腦室內注射3 μl AlCl3溶液(濃度2.5%),注射坐標、方法同上組。④海馬物理損傷模型組:小鼠固定于腦立體定位儀,坐標為前囟后2.4 mm,矢狀縫右旁開2.0 mm,使用自制尖端彎曲的9號針頭垂直插入兩側海馬,順時針轉一周,進針深度為顱骨表面向下3 mm。⑤空白對照組:注射部位、方法同②,注射等體積的無菌生理鹽水。⑥假手術組:小鼠固定于腦立體定位儀,坐標同④,使用自制尖端彎曲的9號針頭垂直插入兩側皮層,進針深度為顱骨表面下1.5 mm,不旋轉,插入即拔出(排除皮層損傷對小鼠行為學的影響)。
1.3.2 行為學檢測 術后14 d,水迷宮檢測小鼠學習記憶能力。Morris水迷宮直徑100 cm、高50 cm,水深30 cm。水溫(24±1)℃。池壁標記 E、S、W、N 4個入水點,在 E、S象限中央、距池壁約30 cm處,放置一高約29 cm、直徑9 cm的水下平臺。測試共5 d,包括:①定位航行試驗(place navigation training):將小鼠依次從4個入水點面向池壁放入水中,記錄小鼠從入水至找到并爬上平臺的時間即逃避潛伏期。測試時間60 s,上臺15 s后系統自動關閉。60 s內小鼠未找到平臺,逃避潛伏期記錄為60 s,隨后將小鼠置于平臺上停留15 s。室內安靜、參照物位置固定。完成4個象限測試為1次,每天上下午各訓練1次,連續4.5 d,統計第5天上午的逃避潛伏期,逃避潛伏期越短說明其學習記憶能力越好。②空間探索試驗(spatial probe training):第5天下午撤平臺,將小鼠于S點置于水中,記錄其90 s內穿越原平臺所在位置的次數,穿臺次數越多說明小鼠學習記憶能力越好。
1.3.3 組織學切片觀察海馬形態 實驗用小鼠完成水迷宮測試后,4%多聚甲醛灌注固定,取小鼠全腦,后固定24 h后梯度蔗糖脫水,OCT包埋,海馬區冠狀連續冰凍切片,片厚20 μm,每3張取1張裱片,HE染色,觀察各組小鼠海馬結構變化。
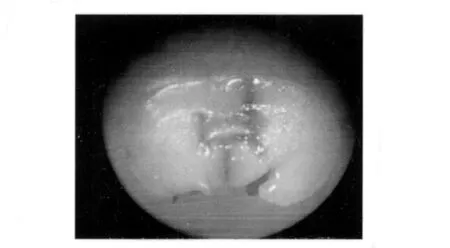
圖1 側腦室注射染料后體視鏡圖(×10),依此確定側腦室的體表體置
1.3.4 Aβ1-40免疫組化染色 海馬區冠狀連續切片每3張取1張行Aβ免疫組化染色。切片抗原微波修復10 min,一抗為兔抗 Aβ1-40多克隆抗體(1∶200),4℃冰箱過夜,DAB 顯色,蘇木素復染。
1.4 統計學處理 行為學檢測結果用SPSS16.0處理,采用單因素方差分析。方差齊同用LSD檢驗各組間顯著性差異,方差不齊用Tamhane's法。數據以±s表示,α=0.05。
2 結果
2.1 不同造模方法對小鼠學習記憶的影響 定位航行和空間探索實驗結果顯示(表1):與正常對照組、空白對照組和假手術組比較,海馬物理損傷組小鼠逃避潛伏期顯著延長、穿越平臺次數明顯減少(P<0.01),AlCl3側腦室注射組小鼠逃避潛伏期也延長、跨越平臺次數也減少(P<0.05),但均不及海馬物理損傷組明顯,Aβ25-35側腦室注射組小鼠逃避潛伏期和穿越平臺次數變化不明顯(P>0.05)。3個模型組間比較,Aβ25-35注射組小鼠逃避潛伏期和穿臺次數與海馬物理損傷組和AlCl3注射組均有顯著性差異(P<0.05)。可見海馬物理損傷組、側腦室注射AlCl3組小鼠空間學習記憶能力受到一定影響,但一次性側腦室注射Aβ25-35對小鼠空間學習記憶影響不大。側腦室注射生理鹽水及傷及皮層的物理損傷對小鼠的學習記憶能力無影響。見表1。
2.2 各組小鼠海馬Aβ1-40免疫組化染色結果 正常對照組、空白對照組、假手術組和海馬物理損傷模型組小鼠海馬Aβ1-40反應均呈陰性;側腦室注射AlCl3和Aβ25-35模型組的小鼠,在海馬區和皮層都可見呈Aβ1-40弱陽性反應的細小的棕黃色斑塊,陽性反應物積聚在神經元胞體和突起的周圍,以星星點點的“彌散狀斑塊”為主,未見較大的陽性斑塊聚集。其中側腦室注射AlCl3組Aβ1-40陽性物略多。見圖2。
表1 各組小鼠第5天定位航行與空間探索實驗結果比較(± s,n=15)
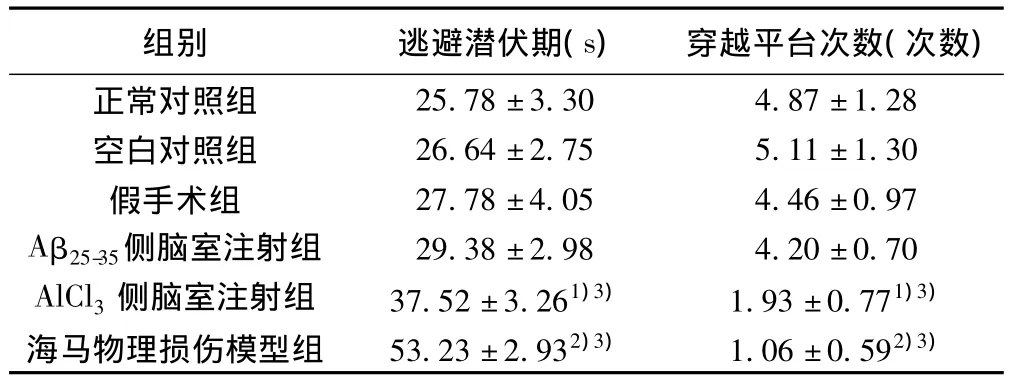
表1 各組小鼠第5天定位航行與空間探索實驗結果比較(± s,n=15)
與正常對照組、空白對照組和假手術組比較:1)P<0.05;2)P<0.01;與Aβ25-35側腦室注射組比較:3)P<0.05
組別 逃避潛伏期(s) 穿越平臺次數(次數)正常對照組25.78±3.30 4.87±1.28空白對照組 26.64±2.75 5.11±1.30假手術組 27.78±4.05 4.46±0.97 Aβ25-35側腦室注射組 29.38±2.98 4.20±0.70 AlCl3側腦室注射組 37.52±3.261)3) 1.93±0.771)3)海馬物理損傷模型組 53.23±2.932)3) 1.06±0.592)3)
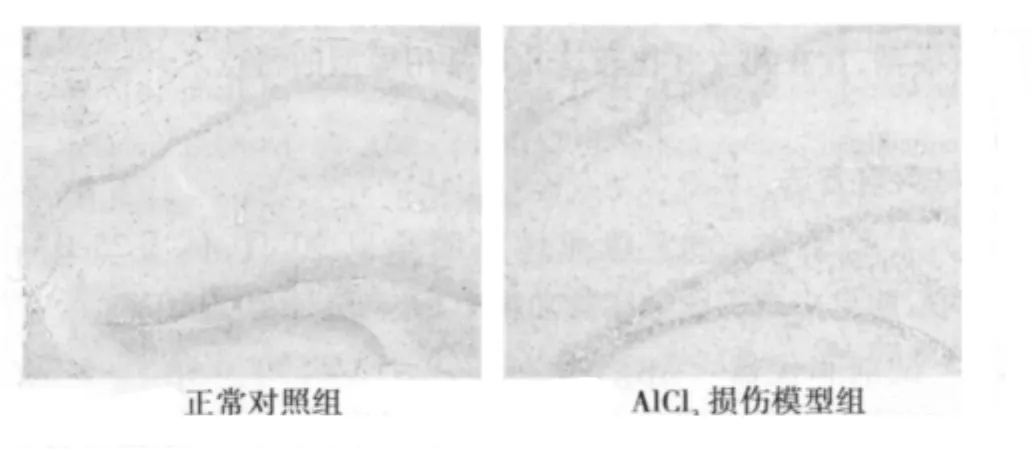
圖2 各組小鼠海馬Aβ1-40免疫組化染色結果(×100)
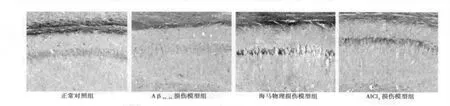
圖3 各組小鼠海馬CA1區病理學改變(HE,×200)
2.3 各組小鼠海馬形態學變化 如圖3所示,正常對照組小鼠海馬CA1區錐體形神經元有1~3層,細胞形態規則,層次清晰,排列整齊密集,胞核淺染、核仁清楚。海馬物理損傷模型組小鼠海馬CA1~CA3區的錐體形神經元及DG顆粒神經元數量明顯減少,CA1區神經元多為單層分布,排列松散,有些部位細胞層不連續,細胞間有空隙。有的細胞核濃染,出現核固縮,有些細胞核有水腫。手術進針的皮層表面有組織缺損,針道附近可見較明顯的毛細血管增生。AlCl3損傷模型組海馬CA1區形態介于正常對照組和海馬物理損傷模型組之間,但更接近正常組,神經元排列較整齊,有些部位偶見細胞稀疏、核固縮、核內染色體邊集等現象。側腦室注射Aβ25-35模型組海馬區結構與正常對照組差異不明顯,有些部位神經元層次結構松散。空白對照組和假手術組小鼠海馬形態同正常對照組無差異,假手術組小鼠皮層表面尚見淺凹形缺損。
3 討論
理想的AD模型應具備以下條件:①記憶和認知功能障礙;②能復制引起損傷的病理特點:SP、NFT及神經元丟失;③膽堿能系統功能低下。一個動物模型如能反映出上述3個方面,可認為是成功的AD動物模型。動物模型是藥物研究的前提,選擇合適的模型對藥物臨床前研究的成敗至關重要。目前常把學習和記憶障礙的動物模型作為AD的動物模型。
Aβ是SP的主要成分,但Aβ注射制作AD模型的可行性報道差別較大。Aβ常見注射部位有Meynert核、海馬等,造模方式有一次性注射致急性中毒和持續性注射致慢性中毒〔1~4〕。基于AD是腦組織彌漫性損傷性疾病,經側腦室給予更利于Aβ彌散而造成較大范圍的損害,同時依據Aβ神經毒性的特點,本實驗采用Aβ核心毒性片斷25-35肽段側腦室注射制作AD模型。結果顯示Aβ25-35一次性側腦室注射后第3周末,小鼠穿越平臺次數和逃避潛伏期與對照組均無明顯差異,即對小鼠記憶能力無影響。此與上述文獻結果有差異,究其原因可能與Aβ蛋白的活性受溫度、pH、濃度、分子構象等多因素影響有關;并且本實驗選用Aβ25-35,有可能因片段較短致使毒性降低而損傷較輕。由于小鼠機體本身存在自凈和修復作用,一次性給予Aβ有可能可制備記憶損傷模型,但損傷持續時間較短,且未形成明顯形態學改變。因此,支持Aβ注射造模需多次注射的觀點,如多次給藥一般需要埋管處理,顯著增加造模難度和成本。
鋁毒性作用在AD形成中引起高度關注。流行病學資料顯示:長期高鋁暴露致認知能力下降,尸檢結果也發現AD患者大腦中Al含量為正常人的1.5~3.0倍,提示Al和AD發病的潛在關聯〔5〕。慢性鋁中毒可導致小鼠神經原纖維變性,出現膽堿能系統損傷癥狀,大腦皮質萎縮、端腦皮質和海馬神經元損傷丟失等,這些變化與AD病理改變有一定相似性〔6〕。慢性鋁中毒致AD模型多采用腹腔或皮下注射,鑒于經驗,長期腹腔或皮下注射易感染,反復灌胃給藥也易引發胃黏膜損傷嚴重甚至穿孔,同時影響動物食欲致體重明顯降低,故本實驗采用了側腦室一次性注射AlCl3的方法。文獻報道鋁積聚激活反應性星形膠質細胞,引發炎性反應,促使Aβ以不溶形式沉積于腦組織,形成老年斑〔7〕。本實驗觀察到造模后小鼠海馬和皮層呈Aβ1-40免疫組化陽性反應,而Aβ1-40是老年斑的主要成分,與報道一致;另有研究表明鋁可與鈣調蛋白結合,改變該蛋白結構,影響鈣調蛋白依賴的各種蛋白激酶活性,從而影響體內磷酸化和去磷酸化的過程及信號轉導,如PKC異常激活導致tau蛋白異常磷酸化〔8〕,因此本模型能較好地模擬AD的特征性病理改變。該模型的優點有:①模擬AD程度高,造模成功率高;②價格低廉,造模成本低。缺點在于:由于酸堿度、AlCl3的神經毒性等原因,動物體重下降明顯。
1970年代人們發現AD患者腦內Ach含量低于正常水平,提出膽堿能缺陷學說,認為突觸末端膽堿能缺損是導致記憶障礙的主要原因之一。Meynert核是前腦皮層Ach的重要來源,其產生的Ach經穹窿轉移至海馬被利用,而海馬在維持記憶方面扮演重要角色。針對這條通路產生各種記憶損傷模型,如真空抽吸、橫斷、電灼傷等物理方法。Xuan等〔9〕在前囟定位后插進刀片并反復抽提,離斷SD大鼠一側穹窿-海馬傘外側緣纖維,復制出癡呆大鼠模型。筆者在預實驗中發現:實驗動物的選擇對結果有一定影響,應用該方法制備小鼠AD模型,操作中因橫切抽動出血量大,術后動物死亡率高、造模成功率低;同時很難保持每次提拉刀片時進刀角度和深度一致,極易損傷周邊腦組織。此法造模后行為學測試結果確有記憶減退,但難以說明完全是由損傷膽堿能通路所致。針對這點,筆者采取旋轉的辦法特異性地破壞海馬組織,操作中容易定位,損傷強度和范圍相對易于控制,小鼠術后存活率高。與上述2種化學損傷模型相比,物理損傷模型的優勢在于:①造模時間短,記憶下降明顯,持續時間久;②造模成本低;③損傷機制清楚;④無藥物殘留,若用于藥物治療研究,不會造成造模藥物與治療藥物相互影響,造模后短時間內即可給藥。劣勢有:①損傷局限,無全腦彌漫性損傷,模擬AD程度低,無特征性病理改變形成;②操作難度大,損傷范圍有時不易控制;③水迷宮中發現物理損傷后不游泳或游泳不靈活小鼠增加,可能與術后未完全康復有關。
因AD發病機制復雜,目前所有動物模型只能模擬其部分特征,且各種模型雖均可使動物記憶下降或出現行為學改變,機制卻不盡相同。多因素復合損傷制作的AD模型,同樣存在技術復雜、損傷機制不甚清楚等缺陷。研究AD模型的意義是為探明其發病機制和藥物治療提供平臺,本實驗使用的3種造模方法,旨在制作急性記憶下降的模型,可用于研究急性或亞急性指標的改變,或用于AD的預防給藥及治療藥物的臨床前研究。在不同的實驗研究中,只有選擇最合適的模型,才可達到事半功倍的效果。
1 Fabrício AP,Pablo P,Filipe SD,et al.Altered emotionality leads to increased pain tolerance in amyloid β (Aβ1-40)peptide-treated mice〔J〕.Behav Brain Res,2010;212:96-102.
2 張曉裕,何利明,侯軍代,等.去癡靈對AD模型小鼠學習記憶及腦內突觸體素表達的影響〔J〕.中國老年學雜志,2010;30(2):495-8.
3 Amaral FA,Resk Lemos MT,Dong KE,et al.Participation of kinin receptors on memory impairment after chronic infusion of human amyloid-β 1-40 peptide in mice〔J〕.Neuropeptides,2010;44:93-7.
4 姚柏春,袁 華,趙涓涓.Aβ25-35誘導阿爾茨海默病模型大鼠海馬神經元HSP70的表達〔J〕.中國老年學雜志,2005;6(25):680-2.
5 Perl DP,Moalem S.Aluminum and Alzheimer's disease,a personal perspective after 25 years〔J〕.J Alzheimers Dis,2006;9(3 Suppl):291-300.
6 Kaizer RR,Corrêa MC,Spanevello RM,et al.Acetylcholinesterase activation and enhanced lipid peroxidation after long-term exposure to low levels of aluminum on different mouse brain regions〔J〕.J Inorg Biochem,2005;99(9):1865-70.
7 Lin R,Chen X,Li W,et al.Exposure to metal ions regulates mRNA levels of APP and BACE1 in PC12 cells:blockage by curcumin〔J〕.Neurosci Lett,2008;440(3):344-7.
8 Walton JR.An aluminum-based rat model for Alzheimer's disease exhibits oxidative damage,inhibition of PP2A activity,hyperphosphorylated tau,and granulovacuolar degeneration〔J〕.J Inorg Biochem,2007;101(9):1275-84.
9 Xuan AG,Luo M,Ji WD,et al.Effects of engrafted neural stem cells in Alzheimer's disease rats〔J〕.Neurosci Lett,2009;(450):167-71.

