H3反應勢能面的構建
——計算化學實驗設計*
袁汝明 傅鋼 韓國彬
(廈門大學化學化工學院 福建廈門 361005)

教學內容包含基本原理的講解,Gaussian03W、Gaussview5.0、Origin等軟件的使用,實際的上機操作,以及數(shù)據(jù)處理和分析,問題思考等。
1 基本原理
簡單地講,勢能面就是把分子的能量表示為幾何坐標的函數(shù)。值得一提的是,根據(jù)量子力學原理, 勢能面并不是理所當然的, 而是建立在波恩-奧普海默(Born-Oppenheimer)近似的基礎上,即將原子核運動與電子運動分開處理。對于N原子反應體系,體系的能量E是3N-6(非線形分子)或3N-5個(線形分子)內坐標的函數(shù),可寫為[2]:
E=f(R1,R2,…,R3N-6 or 3N-5)
(1)
若用幾何圖形表示該函數(shù),其圖像為3N-6或3N-5維空間的超曲面,即勢能面[2]。對于3原子相互作用體系,變量數(shù)為3N-6=3,通常用兩個核間距RAB,RBC以及其夾角θ作為變量,此時能量函數(shù)可表示為:
E=f(RAB,RBC,θ)
(2)
由式(2)得到的勢能面為四維空間曲面,故難以直觀地畫出其圖形。如果固定其中一個變量(常固定夾角θ),此時體系只剩兩個獨立變量RAB和RBC,能量函數(shù)可簡化為:
E=f(RAB,RBC)
(3)
以E為縱坐標,RAB、RBC為平面上的兩個坐標,則得到一個三維曲面。這種曲面很像起伏的山巒, 也有山峰、山谷和洼地。分子體系的勢能面可以決定分子的諸多性質。分子的穩(wěn)態(tài),如反應物和產物,對應于勢能面上的極小點;而反應過渡態(tài)對應于連接極小點的山谷中的最高點,即勢能面上的一級鞍點。當過渡態(tài)確定后, 根據(jù)它和穩(wěn)態(tài)的能量差以及斷面的形狀可以計算反應速率。還可以將極小點附近的勢能面簡化為二維,在諧振子近似下計算體系的振動頻率和零點能。
勢能面函數(shù)一般無解析的形式, 但可通過量子化學方法計算出給定結構的能量,并通過相應的軟件(如Gaussview或Origin等)繪制出來。常見的計算方法有半經驗方法(AM1,PM3), HF方法,密度泛函方法(如B3LYP),后自洽場方法(如CCSD,MPn系列,QCISD等)。需要注意的是,各種計算方法實際上都或多或少引入了近似,因此它們所描述的勢能面也有一定的差異。
2 軟硬件設備
計算軟件:Gaussian03W(并行版)[3],收費軟件,廈門大學授權。
作圖軟件:Gaussview5.0[4], 收費軟件,廈門大學授權;Origin6.0以上版本或Excel。
計算硬件:PC服務器(本文使用的是雙路四核xeon5345服務器)。
3 上機部分
3.1 計算內容
采用Gaussian03W中的QCISD(T)方法,結合6-311++G(2d,2p)基組,計算H3反應勢能面。
① 共線碰撞的勢能面(θ=180°),RAB和RBC的初始長度設為0.58?,步數(shù)為20,步長為0.09?,共計算441個點(21×21)。輸入文件(通常以gjf或com為后綴名)和說明如下[5]:
%nproc=8 //并行CPU數(shù)
%chk=h3.chk //checkpoint文件
# QCISD(T)/6-311++G(2d,2p) scan //任務類型
//空白行
H+H2 -> H2 + H PES Scan //文件說明項
//空白行
0 2 //電荷 自旋多重度
H //H3體系內坐標
X 1 1.0 //贗原子,常用于構建共線體系的內坐標
H 1 RAB 2 90.0
H 1 RBC 2 90.0 3 180.0
RAB 0.58 20 0.09 //鍵參數(shù) 初始鍵長 掃描步數(shù) 掃描步長
RBC 0.58 20 0.09
② 計算θ=180°,掃描RAB=RBC時的能量變化,初始長度設為0.88?,步數(shù)為90,步長為0.002?。輸入文件略。
③ 改變①中的鍵角,分別設θ=150°、120°、90°,可和①同時進行。建議可將每個實驗組分成4個小組,考察不同鍵角下勢能面變化(輸入文件略)。
④ 計算反應物(產物)能量,對比不同計算方法預測的反應能壘Eb。
3.2 結果輸出
用文本編輯器打開Gaussian輸出程序(通常以log或out為后綴名),就可得到勢能面掃描的結果(θ=180°),截取其中的部分數(shù)據(jù)列于表1。

表1 勢能面掃描的數(shù)據(jù)結果(部分)*
*其中體系能量單位為kJ·mol-1。
值得一提的是,采用QCISD(T)方法計算時,Gaussian03W還可以同時輸出HF(即SCF),MP2,MP3和QCISD的能量。因此,我們還可以方便地比較不同計算方法描述的勢能面之間的差異。
3.3 數(shù)據(jù)處理
① 在GaussView5.0中,用File→Open命令打開輸出文件,用Result→Scan命令打開一個繪有3D勢能面的新窗口(圖1)。在GaussView5.0下,按鼠標左鍵可以旋轉圖形,可以從各個角度觀察H3勢能面;按Shift+鼠標左鍵可平移圖形;滾動鼠標滾輪可以縮放圖形,方便觀察特定區(qū)域。
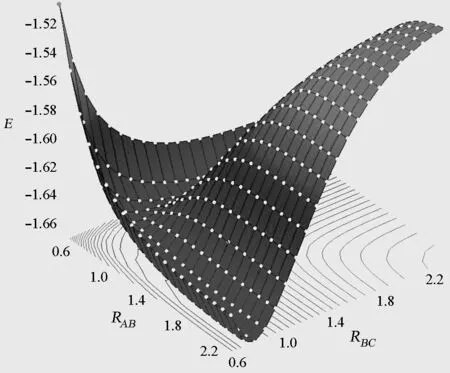
圖1 H3體系(H+H2→H2+H(θ=180°))的勢能面
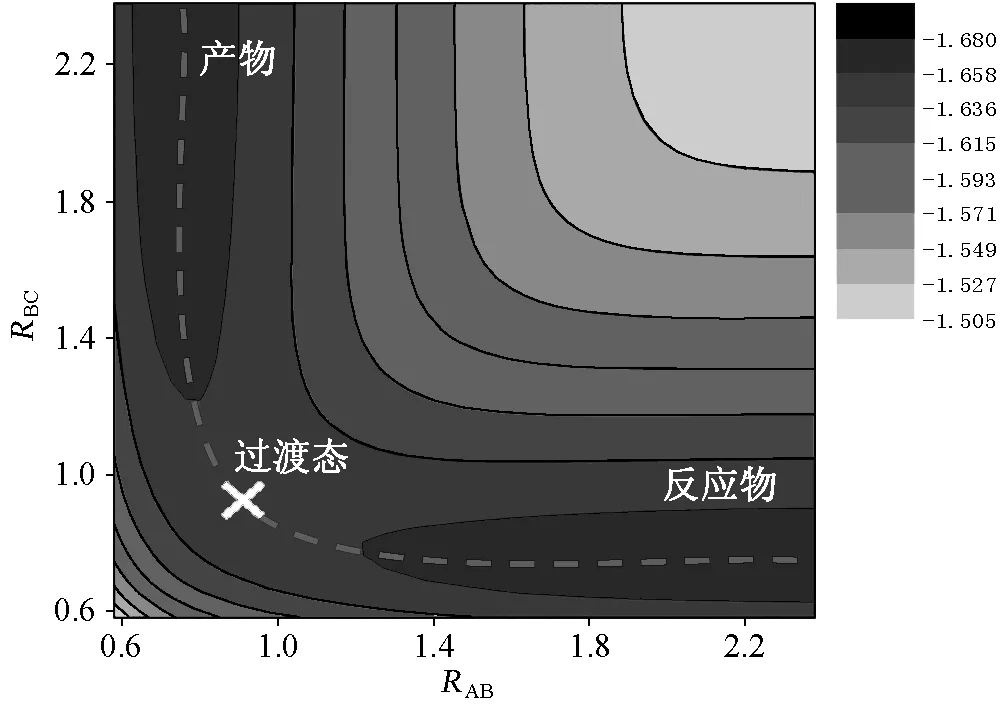
圖2 H3體系(θ=180°)的勢能等高圖
② 為了得到更平滑的勢能面,可用Origin程序中非線性內插的方法。將數(shù)據(jù)增加至50×50,繪制不同H3體系的勢能等高圖(圖2)。由圖2可見,反應物和產物分別位于圖中的右下角和左上角;連接反應物, 過渡態(tài)和產物的山谷就是反應路徑(虛線所示);反應路徑中的最高點為反應的過渡態(tài)。
③ 根據(jù)勢能面的對稱性,對過渡態(tài)附近的區(qū)域進行重點構筑,見計算內容②。根據(jù)定義,反應路徑上的最高點能量和反應物能量之差,即反應能壘Eb,列入表2,并對比不同θ下能壘的高低。

表2 不同θ下反應能壘
由表2可見,θ越小,活化絡合物中RAB(BC)的鍵長越長,H3反應所需克服的反應能壘也越高。因此,H原子進攻的最有利方式是共線碰撞。
3.4 問題思考
① 勢能面掃描得到的活化能壘是否可以直接和實驗活化能進行比較?(提示:還需考慮零點校正和溫度校正。)
② 不同理論方法(如HF,MP2,QCISD和QCISD(T)等)計算得到的活化能壘是否相同?(提示:不同。各種計算方法均引入了近似,通常認為后自洽場方法所描述的勢能面較為合理。)
③ 研究反應的勢能面是計算化學的核心問題。能否結合近年來的研究進展,舉一個或幾個例子談談勢能面在預測反應機理中的作用,以小論文的形式提交。
4 時間安排
本實驗是為大三下學期或大四上學期學生所設計的物理化學探索性實驗,需用時兩天。具體的實驗安排見表3。在教學過程中,我們對于各種計算方法的細節(jié)不作過多的講解,而注重培養(yǎng)學生的興趣,即如何應用成熟的計算化學軟件去探索一個具體的反應過程。

表3 實驗安排
通過上機練習和數(shù)據(jù)分析,可以得到不同θ角的H3反應勢能面,并可通過Gausview程序進行360°全方位觀察,有利于學生對過渡態(tài)理論的理解和掌握。此外,學生還可以熟悉各種計算相關的應用程序,如量子化學程序包(Gaussian03),圖形界面分子構建工具(GaussView5.0)以及數(shù)據(jù)處理程序(Origin)等。這種密切結合物理化學教學的計算機實驗設計,不僅可以將前沿的科研手段融入教學中,提高教學內容的創(chuàng)新性,而且有助于學生將物理化學的基本概念運用到科學研究中。
參 考 文 獻
[1] 傅獻彩,沈文霞,姚天揚.物理化學.第4版.北京:高等教育出版社,1990
[2] 夏少武.活化能及其計算.北京:高等教育出版社,1993
[3] Frisch M J,Trucks G W,Schlegel H B,etal.Gaussian03W,Rev.E01.Wallingford CT:Gaussian Inc,2004
[4] Gaussview 5.0.Wallingford CT:Gaussian Inc,2008
[5] Frisch ?,F(xiàn)risch M J,Trucks G W.Gaussian03 User′s Reference.Wallingford CT:Gaussian Inc,2003

