Cu/SiO2兩步法催化甘油氫解制備1,2-丙二醇
顧 斌,王 紅,卯福林,周小平
(南京工業(yè)大學(xué)生物與制藥工程學(xué)院,江蘇 南京 211816)
研究開發(fā)
Cu/SiO2兩步法催化甘油氫解制備1,2-丙二醇
顧 斌,王 紅,卯福林,周小平
(南京工業(yè)大學(xué)生物與制藥工程學(xué)院,江蘇 南京 211816)
采用兩步法從甘油制備1,2-丙二醇,首先甘油在催化劑上進(jìn)行脫水反應(yīng)生成丙酮醇,然后丙酮醇在催化劑上進(jìn)行加氫反應(yīng)生成1,2-丙二醇。兩個反應(yīng)應(yīng)用的催化劑都是采用浸漬法制備的Cu/SiO2催化劑。催化劑制備簡單,成本較低且綠色無污染。結(jié)果表明:加氫反應(yīng)在反應(yīng)溫度為180 ℃,催化劑相對原料用量為10%,反應(yīng)時間為30 h,反應(yīng)壓力為4 MPa,10%Cu負(fù)載量的催化劑上具有最高的轉(zhuǎn)化率(>96%)和選擇性(>96%)。該催化劑為雙功能催化劑既具有酸中心又具有金屬活性位點。研究結(jié)果表明催化劑上單質(zhì)銅粒徑的大小是影響催化劑活性的主要因素;催化劑表面銅物種與載體間較弱的相互作用使活性物種易于發(fā)生聚集,從而導(dǎo)致催化劑失活。制備的催化劑采用BET、XRD等進(jìn)行了表征。
甘油;催化加氫;1,2-丙二醇
把生物質(zhì)轉(zhuǎn)化為高附加值的化學(xué)產(chǎn)品是綠色化學(xué)的一個重要研究方向[1-2]。綠色化學(xué)所追求的目標(biāo)是化學(xué)反應(yīng)的原料具有可再生性、化學(xué)過程不產(chǎn)生污染,實現(xiàn)高效的化學(xué)反應(yīng)[3]。甘油作為一種理想的可再生原料,以其為平臺可以提供一條綠色且經(jīng)濟(jì)的生產(chǎn)大宗化學(xué)產(chǎn)品的途徑。它作為生物柴油的副產(chǎn)物產(chǎn)量大,每生產(chǎn)9 kg生物柴油就有1 kg粗甘油生成[4-5]。隨著對生物柴油需求的持續(xù)增長,尋找和開發(fā)利用甘油的新用途,將其作為原材料加工成其它產(chǎn)品,不但可以降低生物柴油的生產(chǎn)成本和提高綜合經(jīng)濟(jì)效益,而且還可以解決甘油的生產(chǎn)過剩問題。
甘油所富含的羥基易被官能化或降解,進(jìn)而合成許多需要經(jīng)過復(fù)雜的石油化工路線才能得到的化學(xué)品,其中選擇性氫解可以得到各種二醇 ,包括乙二醇、1,2-丙二醇和 1,3-丙二醇等[6]。近年來,有關(guān)甘油催化氫解合成1,2-丙二醇的研究情況國外已有較多報道,而國內(nèi)卻鮮有報道。報道的催化劑一般是含 Rh[7-9]、Ru[8,10]、Pt[11-13]、PtRu[14]、AuRu[14]等貴金屬以及Ni[15]基和Cu[7,10,16-17]基催化劑。
含有Pt、Pd、Ru、Rh等的活性炭負(fù)載貴金屬催化劑在催化氫解中的研究較多,其中 Ru/C是研究最多、效果最好的一種貴金屬催化劑。Ru/C催化劑由 Ru(NO)(NO3)3水溶液與較低比表面積的活性炭混合蒸發(fā)去除溶劑后在393 K下干燥12 h制得。其特點是:①具有較低比表面積且含較少的氧化性官能團(tuán)的活性炭制備的催化劑催化效果較好;②催化劑活性與顆粒粒徑大小無關(guān)。③催化劑在573 K下用30 cm3/m in的氬氣進(jìn)行預(yù)處理后使用效果更好;④Ru在甘油氫解反應(yīng)中表現(xiàn)了很好的活性,但過多的Ru常促進(jìn)C—C鍵的過分?jǐn)嗔眩狗磻?yīng)進(jìn)一步分解而得較多的碳?xì)浠衔铮ㄖ饕羌淄椋话?% Ru/C催化甘油的轉(zhuǎn)化率及生產(chǎn)1,2-丙二醇的選擇性最好[18]。Perosa等[15]采用Raney-Ni催化劑,在1.0 MPa H2、190 ℃下,反應(yīng)20 h轉(zhuǎn)化率達(dá)到63%,1,2-丙二醇選擇性達(dá)到77%。Werpy等[19]發(fā)現(xiàn)Ni、Re/C雙金屬催化體系可催化合成1,2-丙二醇,在8.2 MPa H2、230 ℃下反應(yīng)4 h,1,2-丙二醇產(chǎn)率為44%、選擇性高達(dá)88%。反應(yīng)受溫度影響明顯,穩(wěn)定性較差,低溫時效果好,但反應(yīng)時間長,不利于實現(xiàn)工業(yè)化。Dasari等[16]利用 Cu/Cr催化劑催化氫解甘油生產(chǎn)1,2-丙二醇的選擇性可達(dá) 95%以上,甘油的轉(zhuǎn)化率接近100%。但是該催化體系中的Cr對環(huán)境污染較大。研究表明在各種金屬催化劑當(dāng)中,對甘油催化氫解生成1,2-丙二醇效果最好的是含Cu的催化劑。銅系催化劑對C—C鍵氫解的反應(yīng)活性較低,而對C—O鍵的氫解活性較高[20-21],具有較高的1,2-丙二醇選擇性。
本研究采用浸漬法制備了Cu/SiO2催化劑,使用兩步法制備1,2-丙二醇,其中較溫和的反應(yīng)條件有利于第一步的脫水反應(yīng),而第二步的加氫反應(yīng)需要較高的溫度和壓力。兩步法工藝可以分別控制反應(yīng)的工藝參數(shù)使兩步反應(yīng)都處在更佳的反應(yīng)條件從而獲得更高的收率以及降低反應(yīng)成本。作者主要研究了第二步反應(yīng),即:以甘油在催化劑上進(jìn)行脫水反應(yīng)生成的丙酮醇為原料加氫制備 1,2-丙二醇的工藝研究及催化劑設(shè)計。結(jié)果表明,該催化劑具有較高的反應(yīng)活性及選擇性,其制備簡單并且綠色無污染,有良好的工業(yè)應(yīng)用前景。
1 實驗部分
1.1 催化劑的制備
載體 SiO2的制備:將 136 g 的四乙氧基硅(TEOS)和20 g的去離子水加入燒杯中混合,然后放進(jìn)油浴鍋中在70 ℃下攪拌,并加入75.4 g稀硝酸[稀硝酸用 500 g去離子水和 37 g 濃硝酸(65%~88%)配制而成],后用保鮮膜封口,攪拌大約2 h,待形成凝膠后在120 ℃下干燥12 h。干燥后所得的固體在馬弗爐中于300 ℃焙燒3 h得催化劑,制成10~50目的顆粒備用。
Cu/SiO2催化劑的制備:取 7.4 g 的Cu(NO3)2·3H2O,加入50 g的蒸餾水,待完全溶解后,倒入制備好的SiO2顆粒中,攪拌后浸漬24 h,放入120 ℃干燥箱干燥12 h,最后用馬弗爐在450℃煅燒3 h,待降溫后取出,使用10~50目的篩子過篩后得到成型的催化劑。
1.2 催化劑的表征
催化劑的比表面積是在 ASAP 2020(美國M icromeritics公司)型物理吸附儀上測定的,采用N2作吸附劑。樣品經(jīng)過300 ℃抽真空6 h預(yù)處理后,再進(jìn)行比表面積測定。
樣品的 X射線衍射(XRD)分析是在 D8 Advance型X射線衍射儀(德國Bruker公司)上進(jìn)行的,采用Cu靶Kα射線作光源,掃描速度為5°/m in,掃描范圍為2θ=10°~70°,管電壓為40 kV,管電流為40 mA。
1.3 催化劑的活性評價
催化劑性能評價是在自行設(shè)計的反應(yīng)裝置上進(jìn)行的。甘油脫水制丙酮醇的反應(yīng)是在固定床反應(yīng)器(長135 cm,內(nèi)徑3 cm)中進(jìn)行的,在管式反應(yīng)器內(nèi)填充有500 g催化劑(位于反應(yīng)管中部),反應(yīng)管兩端裝填25~45目的石英砂。反應(yīng)用25%的甘油水溶液以0.5 m L/min的流速泵入反應(yīng)器中。產(chǎn)物收集于反應(yīng)器后面的容器中。
丙酮醇加氫制1,2-丙二醇的反應(yīng)是在反應(yīng)釜中進(jìn)行的。秤取10.0 g第一步反應(yīng)的產(chǎn)物(丙酮醇的水溶液及少量副產(chǎn)物)和1.0 g Cu/SiO2催化劑加入高壓反應(yīng)釜中。擰緊反應(yīng)器,通過氫氣鋼瓶向釜內(nèi)充入適量氫氣壓力至2 MPa,關(guān)閉氫氣鋼瓶閥門和反應(yīng)釜閥門。觀察反應(yīng)釜半小時,如果釜內(nèi)壓力無變化,可以確定反應(yīng)裝置不漏氣。排出釜內(nèi)氣體,再進(jìn)行一次同樣的排氣操作。基本可以排空釜內(nèi)的空氣,然后開始加熱至溫度達(dá)到預(yù)設(shè)值。打開氫氣鋼瓶閥門,把壓力調(diào)節(jié)到反應(yīng)所需的壓力,再打開反應(yīng)釜閥門使得釜內(nèi)壓力達(dá)到反應(yīng)所需壓力,打開磁力攪拌器調(diào)節(jié)到適當(dāng)?shù)霓D(zhuǎn)速進(jìn)行反應(yīng)。觀察反應(yīng)過程中壓力的變化,壓力每減少0.1 MPa就需要補氣一次,確保反應(yīng)在設(shè)定的壓力下進(jìn)行。反應(yīng)結(jié)束后,等待反應(yīng)釜冷卻到室溫再打開閥門放出氣體,收集產(chǎn)物。產(chǎn)物用氣相色譜儀(島津GC-2010)進(jìn)行分析,采用內(nèi)標(biāo)法計算各物質(zhì)的百分含量。氣相用氫氣為載氣,在色譜柱Stabilwax-DA上進(jìn)行分析,氣象色譜的檢測器是熱導(dǎo)檢測器。液相產(chǎn)物用GC-MS進(jìn)行分析,其副產(chǎn)物主要為乙二醇、甲醇、異丙醇、正丙醇、丙酮醇等。
2 結(jié)果與討論
反應(yīng)中用恒流泵將 25%的甘油水溶液以 0.50 m L/min的流量注入固定床反應(yīng)器進(jìn)行反應(yīng),反應(yīng)溫度為220 ℃。在甘油脫水反應(yīng)中,甘油的轉(zhuǎn)化率大于99%,丙酮醇的選擇性大于96%。這一反應(yīng)的結(jié)果表明,10%Cu/SiO2是一個有效的甘油脫水催化劑,甘油幾乎達(dá)到100%的轉(zhuǎn)化率。該產(chǎn)物丙酮醇的水溶液沒有經(jīng)過進(jìn)一步提純,在本研究工作中作為下一步反應(yīng)的原料,進(jìn)行丙酮醇的加氫反應(yīng)。
2.1 載體對催化劑性能的影響
載體的選擇對催化劑的性能影響較大,選擇合適的載體不僅有利于提高反應(yīng)活性而且對提高目的產(chǎn)物的選擇性也很重要。銅基催化劑常用的載體是SiO2和 Al2O3。選用現(xiàn)有的幾種常用載體,采用浸漬法制備了催化劑,考察了這些催化劑在丙酮醇?xì)浣夥磻?yīng)中的催化性能,結(jié)果見表1。
表1表示以Cu 為活性組分時載體SBA-15、堇青石、3A型分子篩、4A型分子篩、活性炭及SiO2)對催化性能的影響,活性組分的負(fù)載量為10%。由表1可以看出,載體對丙酮醇的轉(zhuǎn)化率和 1,2-丙二醇的選擇性影響較大。根據(jù)1,2-丙二醇的收率可以得出不同載體制備出的催化劑活性大小依次為 Cu/SiO2>Cu/活性炭>Cu/3A型分子篩>Cu/SBA-15 >Cu/堇青石>Cu/4A型分子篩。因此,選取SiO2作為催化劑的載體。
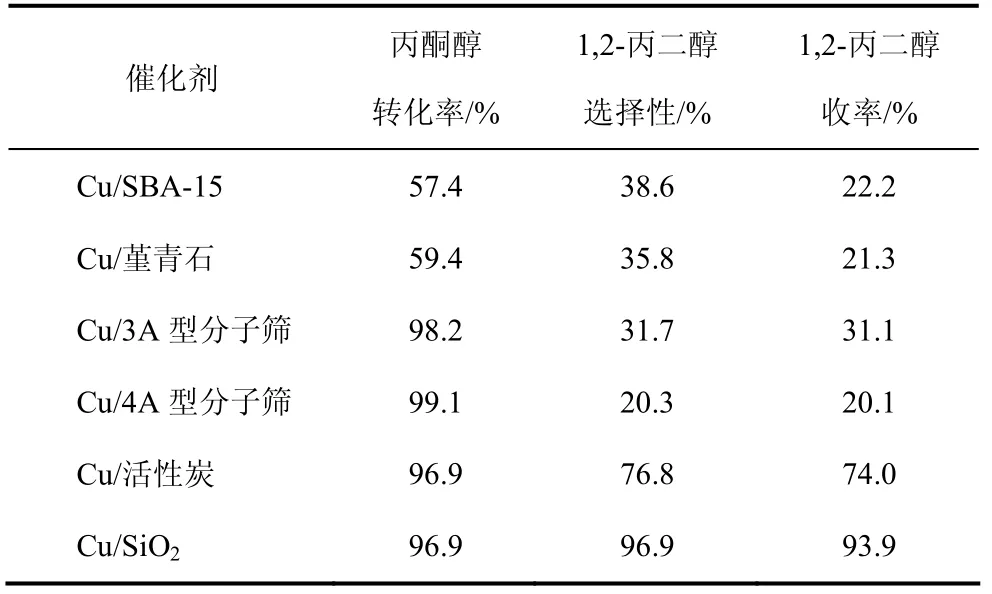
表1 不同載體對催化劑性能的影響
2.2 Cu負(fù)載量對催化劑性能的影響
對負(fù)載型催化劑而言,活性物種的負(fù)載量是影響催化活性的一個重要因素。
采用浸漬法制備了不同銅負(fù)載量的 Cu/SiO2催化劑,考察銅含量對丙酮醇?xì)浣饣钚院椭鳟a(chǎn)物1,2-丙二醇選擇性的影響。催化劑都在250 ℃下用氫氣還原2 h預(yù)處理。催化劑的 XRD 圖譜如圖1所示。由圖1可知催化劑3%Cu/SiO2、5%Cu/SiO2、8%Cu/SiO2和 10%Cu/SiO2中沒有出現(xiàn) CuO和Cu0的衍射峰,表明此時CuO或/和Cu0是高度分散在載體表面的非晶態(tài)物質(zhì)。當(dāng)銅負(fù)載量大于10%時,從圖譜中可以觀察到 Cu0的特征衍射峰(2θ=43.4°),隨著銅負(fù)載量的增加衍射峰加強,說明催化劑中有Cu0晶相存在。
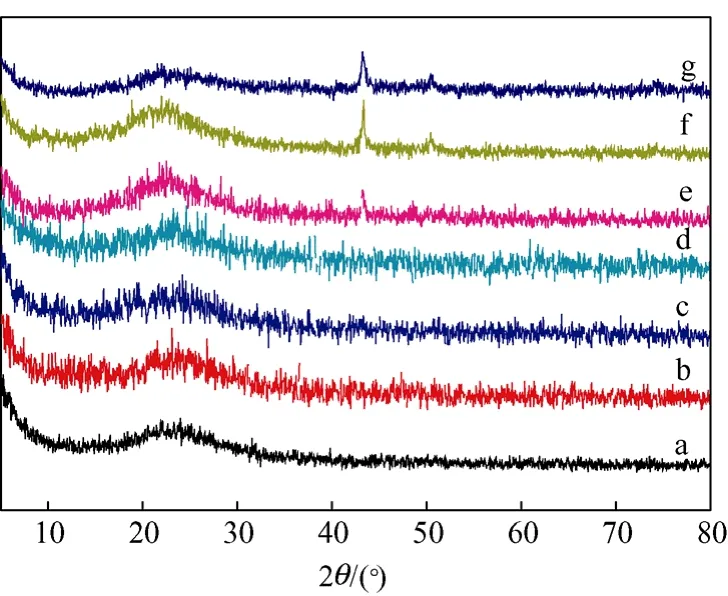
圖1 不同銅含量催化劑反應(yīng)前的XRD圖譜
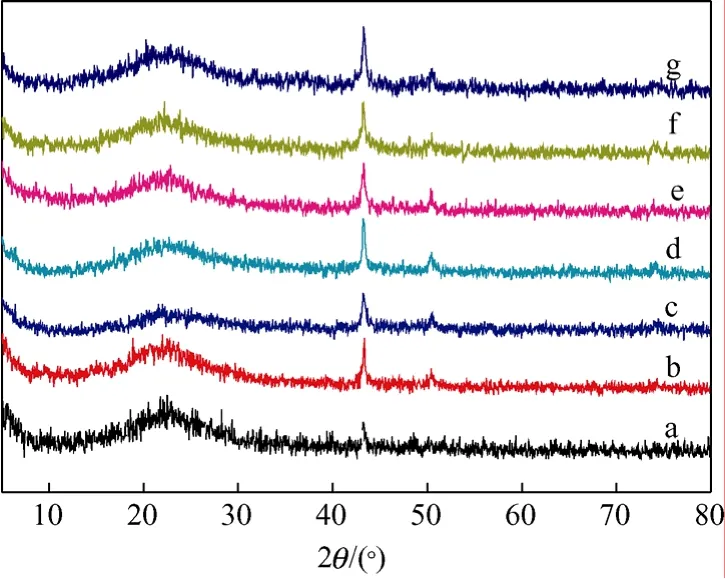
圖2 不同銅含量催化劑反應(yīng)后的XRD圖譜
圖2為反應(yīng)后的Cu/SiO2催化劑的XRD圖譜。從圖中可以看出,沒有SiO2的峰出現(xiàn)表明它仍然是非晶態(tài)。在2θ=43.4°處有明顯的金屬Cu0的衍射峰,并且峰的強度隨負(fù)載量的增大而增強,這個現(xiàn)象說明在反應(yīng)后的催化劑上發(fā)生了 Cu0的集聚,Cu0的粒徑變大了,催化劑的活性可能會降低。
表2給出了丙酮醇在不同銅含量的催化劑上的加氫反應(yīng)結(jié)果。由表 2可以看出,在 250 ℃和 4 MPa 下,隨著Cu的負(fù)載量從3%增加到20%,丙酮醇的轉(zhuǎn)化率從 58.5%升高至 98.5%。當(dāng) Cu的負(fù)載量從1%增加到10%時,1,2-丙二醇的選擇性從 79.5%增加至 96.9%;Cu的負(fù)載量超過 10%時,1,2-丙二醇的選擇性略有下降,生成了少量的乙二醇和CO2等。對于3%Cu/SiO2催化劑,由于銅的負(fù)載量過低,催化劑表面的活性中心數(shù)量不足,因此丙酮醇的轉(zhuǎn)化率很低。對于 10%Cu/SiO2催化劑,銅的負(fù)載量較 3%Cu/SiO2催化劑提高3倍多,因此丙酮醇的轉(zhuǎn)化率明顯提高。由表2可以看出BET比表面積隨著銅負(fù)載量的增大而減小的現(xiàn)象,說明過高的 Cu負(fù)載量可能使載體表面Cu形成多層負(fù)載,生成較大的Cu0晶體。XRD 的研究結(jié)果表明,當(dāng)銅的負(fù)載量大于 10%時,催化劑上出現(xiàn)金屬Cu0的衍射峰(圖1),并且隨銅含量的增加Cu的衍射峰增強,銅晶體可能長大。本文作者認(rèn)為催化劑表面高度分散的微簇是反應(yīng)的主要活性中心,大晶粒的 Cu0表面可能有催化副反應(yīng)發(fā)生,從而產(chǎn)生了較多乙二醇等副產(chǎn)物。因此,當(dāng)銅負(fù)載量從10%增加到20%時1,2-丙二醇的選擇性下降。
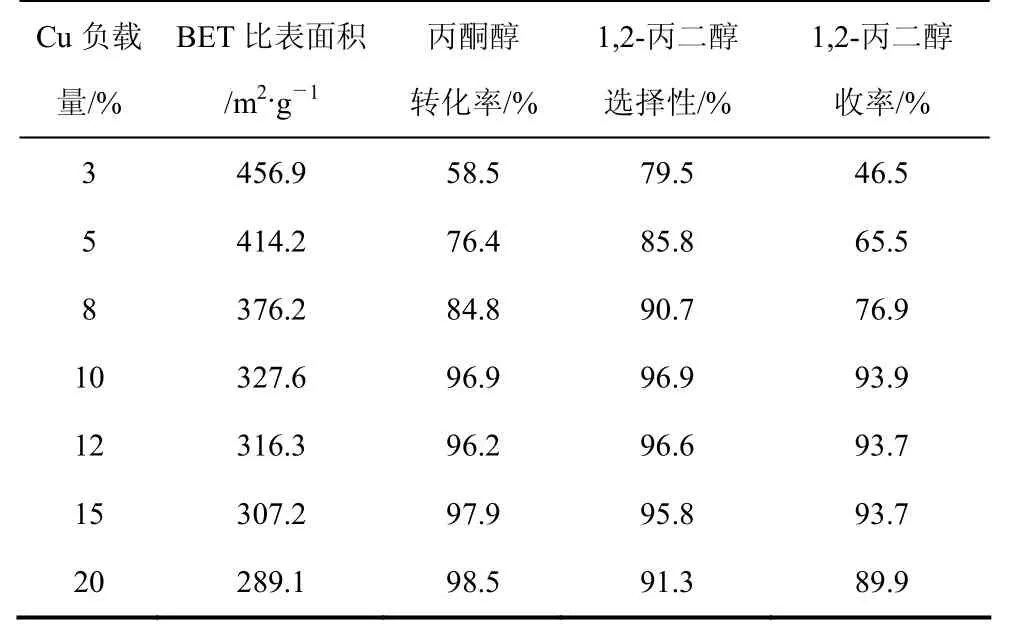
表2 銅負(fù)載量對催化劑性能的影響
2.3 反應(yīng)溫度對催化劑性能的影響
表3給出了在不同反應(yīng)溫度下Cu/SiO2催化劑上丙酮醇?xì)浣馍?1,2-丙二醇反應(yīng)的結(jié)果。由表 3可看出,反應(yīng)溫度對丙酮醇的轉(zhuǎn)化率和生成1,2-丙二醇的選擇性有較大影響。隨著反應(yīng)溫度的升高,丙酮醇的轉(zhuǎn)化率由25.8%提高至 96.9%;1,2-丙二醇的選擇性出現(xiàn)先增加后減少的趨勢,在 200 ℃時,1,2-丙二醇的選擇性達(dá)到 97.6%。1,2-丙二醇的收率在180 ℃時最好,為93.9%。因此,180 ℃為該反應(yīng)的最佳反應(yīng)溫度。在220 ℃時由于水蒸氣重整反應(yīng),1,2-丙二醇的選擇性很低。
2.4 反應(yīng)壓力對催化劑性能的影響
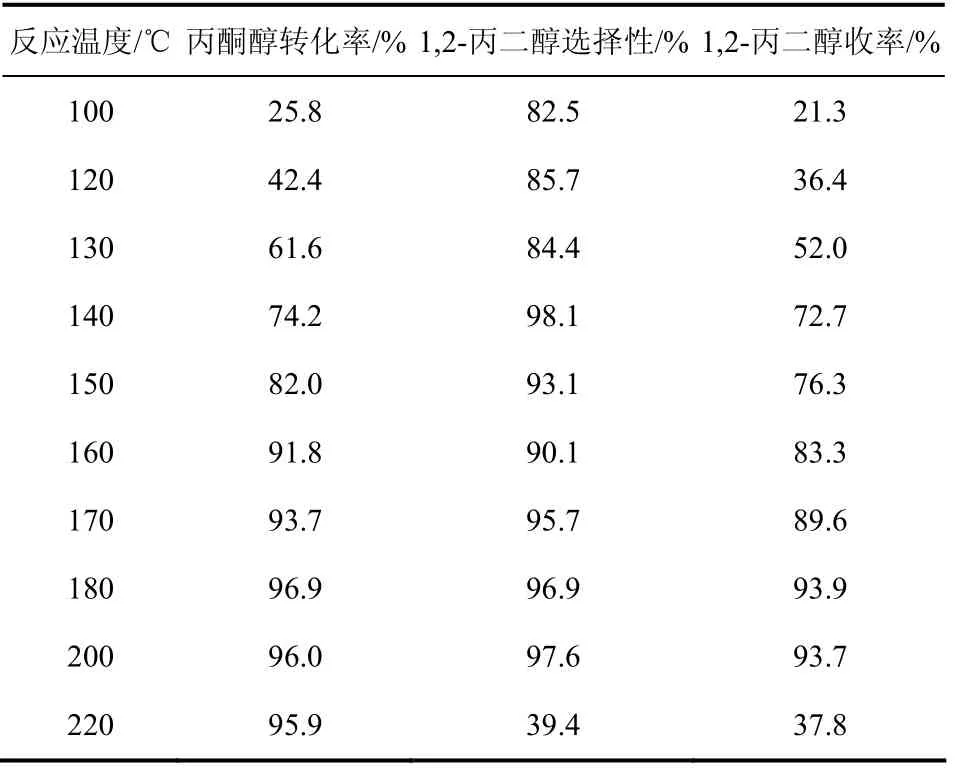
表3 反應(yīng)溫度對催化劑性能的影響
表 4給出了在 180 ℃和不同氫氣壓力下丙酮醇在 Cu/SiO2催化劑上氫解生成 1,2-丙二醇的反應(yīng)結(jié)果。結(jié)果表明,增加反應(yīng)壓力有助于丙酮醇的加氫反應(yīng),但是考慮到反應(yīng)的安全性和工業(yè)化成本,4.0 MPa的反應(yīng)壓力比較合適。
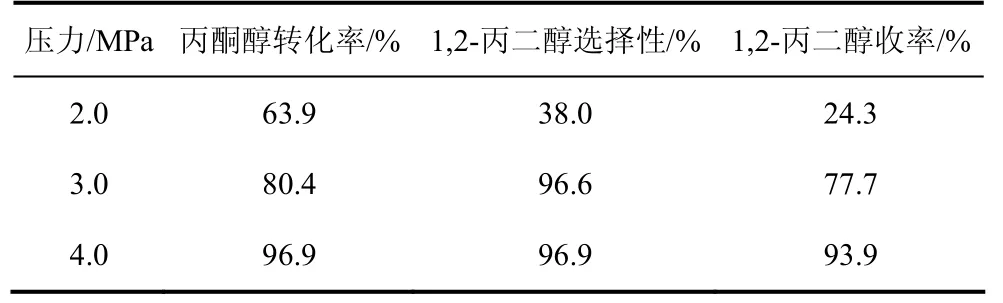
表4 反應(yīng)壓力對催化劑性能的影響
2.5 不同反應(yīng)時間對反應(yīng)的影響
表5給出了反應(yīng)時間對反應(yīng)的影響。隨著反應(yīng)時間的增加,轉(zhuǎn)化率、選擇性、收率都有所增加。但是考慮到反應(yīng)的效率,選取30 h為合理的反應(yīng)時間。
2.6 不同催化劑用量對反應(yīng)的影響
表 6給出了催化劑相對原料用量對反應(yīng)的影響。隨著催化劑用量的增加,1,2-丙二醇的收率出現(xiàn)先升高后下降的趨勢,在15%的時候達(dá)到最大。催化劑相對用量為10%時1,2-丙二醇的收率只是略低于15%時的催化劑相對用量。考慮到反應(yīng)的經(jīng)濟(jì)性,選取10%的催化劑相對原料用量。
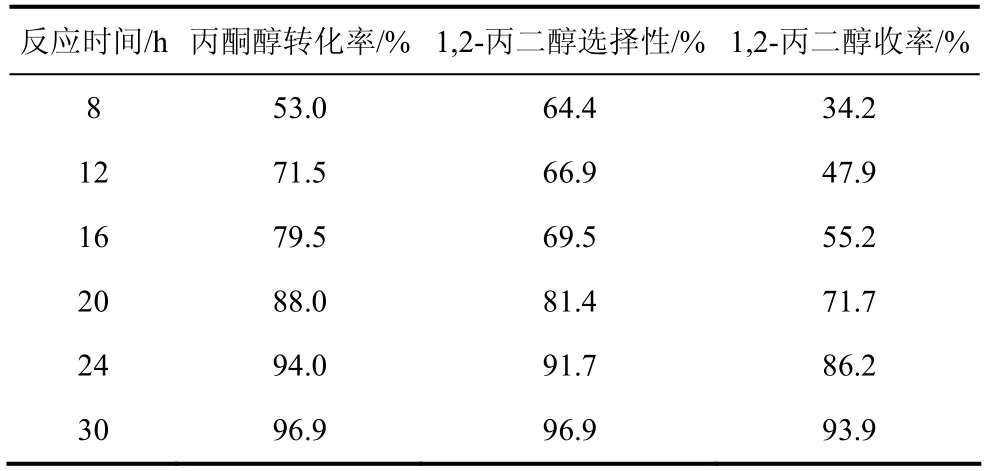
表5 不同反應(yīng)時間對反應(yīng)的影響
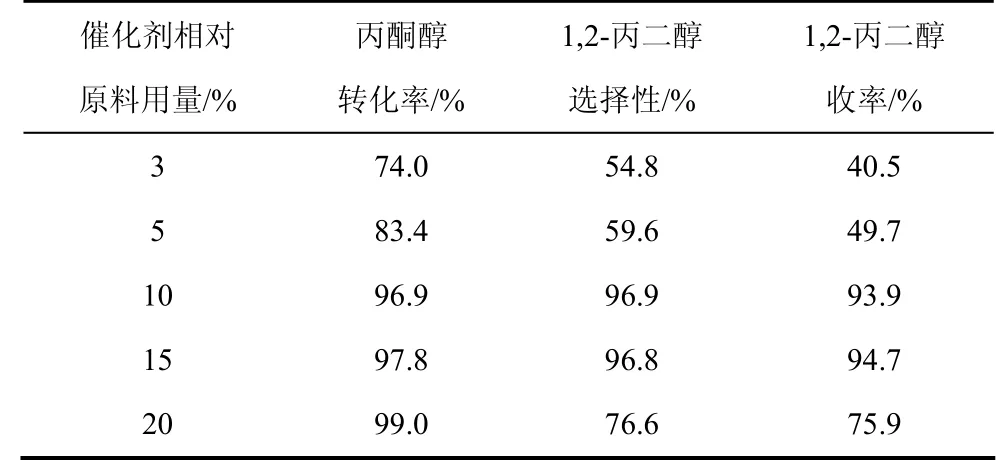
表6 不同催化劑用量對反應(yīng)的影響
2.7 催化劑穩(wěn)定性測試
為了了解催化劑的穩(wěn)定性,考察了Cu/SiO2催化劑在丙酮醇?xì)浣夥磻?yīng)中的性能。如表7所示,隨著反應(yīng)次數(shù)的增加,丙酮醇的轉(zhuǎn)化率和1,2-丙二醇的選擇性均出現(xiàn)下降的趨勢,丙酮醇的轉(zhuǎn)化率由開始的96.9%下降至79.3%,選擇性亦從 96.9%下降至85.3%。
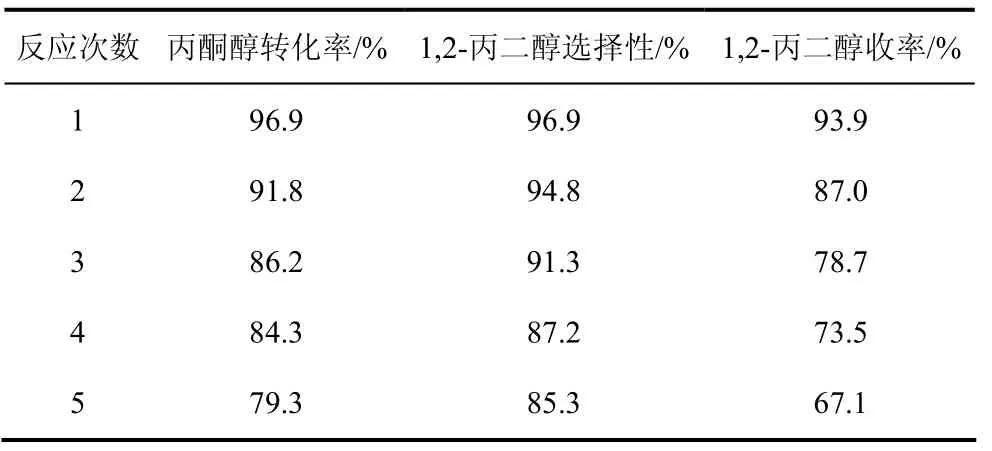
表7 催化劑穩(wěn)定性測試
對比圖1、圖2反應(yīng)前后催化劑的XRD表征結(jié)果可知,反應(yīng)后的催化劑峰強增加,說明在反應(yīng)后,催化劑的活性物種粒徑長大。可能正是因為 Cu0粒徑的增大導(dǎo)致了催化劑失活。也可能是負(fù)載的 Cu0從載體表面脫落造成了催化劑的活性下降。
3 結(jié) 論
采用兩步法從甘油制備1,2-丙二醇,并重點研究了加氫反應(yīng)的工藝參數(shù)。使用浸漬法制備了具有不同銅負(fù)載量的 Cu/SiO2催化劑并考察了催化劑的反應(yīng)性能。此催化劑既有酸性位又有金屬加氫位,是雙功能型催化劑。結(jié)果表明:負(fù)載量 10% Cu/SiO2催化劑表現(xiàn)出了較好的催化性能,在優(yōu)化的反應(yīng)條件下,1,2-丙二醇的收率達(dá)到93.9%。
結(jié)合 XRD 及 BET等表征結(jié)果,可以認(rèn)為催化劑上單質(zhì)銅粒徑的大小是影響催化劑活性的主要因素;催化劑表面銅物種與載體間較弱的相互作用使活性物種易于發(fā)生聚集,從而導(dǎo)致催化劑活性降低。
[1] Clark J H. Green chem istry:Today(and tomorrow)[J].Green Chem.,2006:17-21.
[2] Dale B E. ‘Greening’ the chem ical industry:Research and development priorities for biobased industrial products[J].J.Chem.Technol. Biotechnol.,2003,78:1093-1103.
[3] 閔恩澤.綠色化學(xué)技術(shù)[M].南昌:江西科學(xué)技術(shù)出版社,2001:1-28.
[4] Suppes G J,Dasari M A,Goff M J,et al.Transesterification of soybean oil w ith zeolite and metal catalysts[J].Appl.Catal.A:Gen.,2004,257:213-223.
[5] Plank C,Lorbeer E. Simultaneous determ ination of glycerol,and mono-,di- and triglycerides in vegetable oil methyl esters by capillary gas chromatography[J].J. Chromatogr. A,1995,697:461.
[6] Huang L,Zhu Y L,Zheng H Y,et al. Continuous production of 1,2-propanediol by the selective hydrogenolysis of solvent-free glycerol under m ild conditions[J].J. Chem.Technol.Biotechnol.,2008,83:1670 .
[7] Cham inand J,Djakovitch L A,Gallezot P,et al. Glycerol hydrogenolysis on heterogeneous catalysts[J].Green Chem.,2004,6:359-361.
[8] Lahr D G,Shanks B H. Effect of sulfur and temperature on ruthenium-catalyzed glycerol hydrogenolysis to glycols[J].J. Catal.,2005,232:386-394.
[9] Furikada I,M iyazawa T,Koso S,et al. Catalytic performance of Rh/SiO2in glycerol reaction under hydrogen[J].Green Chem.,2007,9:582-588.
[10] Brandner A,Lehnert K,Bienholz A,et al. Production of biomassderived chemicals and energy:Chemocatalytic conversions of glycerol[J].Top Catal.,2009,52:278-287.
[11] M iyazawa T,Koso S,Kunimori K,et al. Development of a Ru/C catalyst for glycerol hydrogenolysis in combination w ith an ion-exchange resin[J].Appl. Catal. A:Gen.,2007,329:30-35.
[12] Kurosaka T,Maruyama H,Naribayashi I,et al.Production of 1,3-propanediol by hydrogenolysis of glycerol catalyzed by Pt/WO3/ZrO2[J].Catal.Commun.,2008,9:1360-1363.
[13] Yuan Z,Wu P,Gao J,et al.Pt/solid-base:A predom inant catalyst for glycerol hydrogenolysis in a base-free aqueous solution[J].Catal.Lett.,2009,130:261.
[14] Maris E P,Ketchie W C,Murayama M,et al.Hydrogenolysis of glycerol catalyzed by Ru-Cu bimetallic catalysts supported on clay w ith the aid of ionic liquids[J].J. Catal.,2007,251:281-294.
[15] Perosa A,Tundo P. Selective hydrogenolysis of glycerol w ith Raney nickel[J].Ind.Eng.Chem.Res.,2005,44:8535-8537.
[16] Dasari M A,Kiatsimkul P P,Sutterlin W R,et al. Low-pressure hydrogenolysis of glycerol to propylene glycerol[J].Appl.Catal.A:Gen.,2005,281:225-231.
[17] Balaraju M,Rekha V,Prasad P S S,et al.Selective hydrogenolysis of glycerol to 1,2 propanediol over Cu-ZnO catalysts[J].Catal.Lett.,2008,126:119-124.
[18] M iyazawa T,Koso S.Parameters affecting the formation of 1,2-propanediol from glycerol over Ru/SiO2catalyst[J].Appl. Catal. A:Gen.,2007,318:244-251.
[19] Werpy T A,F(xiàn)rye J G,Zacher A H,et al. Hydrogenolysis of 6-carbon sugars and other organic compounds:US,6841085B2[P]. 2005-01-11.
[20] Runeberg J,Baiker A,Kijenski J. Copper catalyzed am ination of ethylene glycol[J].Appl. Catal.,1985,17:309-319.
[21] Montassier C,Giraud D,Barbier J.Polyol conversion by liquid phase heterogeneous catalysis over metals[J].Stud. Surf. Sci. Catal.,1988,41:165-170.
Hydrogenolysis of glycerol to 1,2-propanediol by two steps over Cu/SiO2
GU Bin,WANG Hong,MAO Fulin,ZHOU Xiaoping
(Department of Biotechnology and Pharmaceutical Engineering,NanJing University of Technology,Nanjing 211816,Jiangsu,China)
1,2-propanediol was prepared by hydrogenolysis of glycerol in two steps. Firstly,glycerol was dehydrated over bi-functional catalyst Cu/SiO2into acetol,which was in turn hydrogenated into 1,2-propanediol over the same catalyst. The catalyst Cu/ SiO2was prepared,by the coprecipitation method. The catalyst preparation was simple,of low cost,and environmentally friendly. The prepared catalyst was characterized w ith BET and XRD. The result indicated that the prepared catalyst had comparatively high activity. The best conversion(>96%)and selectivity(>96%)performance of the catalyst was achieved when the Cu loading amount was 10%. This bi-functional catalyst possessed acid site and metal active site as well. The particle size of Cu was the major factor to influence the activity of the catalyst. Deactivation of the catalyst was attributed to interaction of the copper species on the catalyst surface and the carrier,which caused aggregation of the active species.
glycerol;catalytic hydrogenation;1,2-propanediol
TQ 214
A
1000–6613(2011)09–1961–06
2011-02-28;修改稿日期:2011-03-27。
顧斌(1987—),男,碩士研究生。聯(lián)系人:周小平,教授。E-mail hgx2002@hnu.cn。

