鄰二氮菲-Fe3+法測定保健食品中水溶性成分的抗氧化能力
劉 薇,劉雯佳,劉彥霞,趙 建,文 鏡*
(北京聯合大學應用文理學院,生物活性物質與功能食品北京市重點實驗室,北京 100191)
鄰二氮菲-Fe3+法測定保健食品中水溶性成分的抗氧化能力
劉 薇,劉雯佳,劉彥霞,趙 建,文 鏡*
(北京聯合大學應用文理學院,生物活性物質與功能食品北京市重點實驗室,北京 100191)
目的:建立用鄰二氮菲-Fe3+測定保健食品中水溶性成分抗氧化能力的方法。方法:用水相提取保健食品中的水溶性抗氧化成分,使其還原反應體系中的Fe3+,生成的亞鐵離子與鄰二氮菲反應成穩定的橙紅色絡合物,用分光光度計在536nm波長處測定吸光度。以水溶性VE為對照,由此計算樣品水溶性成分中抗氧化(還原性)物質的多少。通過對方法線性關系、最低檢測限、精密度、準確度等指標進行測定,驗證方法的可行性。結果:檢測Trolox在質量濃度0.66~10.53μmol/L范圍內呈現良好的線性關系(R2=0.9999);最低檢測下限為0.54μmol /L;平行性精密度為2.7%;重復性精密度為3.3%;5次重復加標回收率為(99.9±4.6)%。結論:鄰二氮菲-Fe3+法可用于保健食品中水溶性成分抗氧化能力的檢測。
保健食品;抗氧化能力;鄰二氮菲-Fe3+法
隨著人們對自由基研究的日漸深入,發現損害人體健康的自由基幾乎都與活性較強的含氧物質有關,因而把與這些物質相結合的自由基定義為活性氧自由基。活性氧自由基對人體的損害本質是一種氧化過程[1-3]。要降低自由基的損害,就需要抗氧化。抗氧化劑能夠提供電子給自由基,并且在此過程中不會產生具有毒性或能引起自由基鏈式反應的活性產物,從而消除氧自由基,終止鏈式反應[4-7]。體外測定抗氧化物質清除自由基的方法主要包括化學發光法、分光光度法、電子自旋共振法、電化學檢測法,氣相色譜法和熒光法等[8-14]。這些方法中有些儀器試劑昂貴,操作復雜,使其應用受到限制。分光光度法儀器價格便宜,操作簡單,是一般實驗室的常規分析儀器。鄰二氮菲比色法最初是用于檢測樣品中Fe2+含量,其原理是鄰二氮菲可與Fe2+生成穩定的橙紅色絡合物,而這種物質在可見光區有顯著的吸收,利用這一性質可對樣品中的Fe2+進行測定[15-16]。標準的Fenton試劑是由H2O2與Fe2+組成的混合體系,Fe2+可以催化分解H2O2產生羥自由基(·OH),由此出現了對樣品清除自由基的能力進行檢測的鄰二氮菲- Fe2+氧化法[17-18]。本實驗室曾用分光光度計及鄰二氮菲- Fe2+法檢測保健食品的抗氧化能力[19]。該方法雖然具有操作簡單,快速等優點,但由于方法中通過Fenton反應產生的自由基容易受到多方面因素的干擾,使方法的重復性受到影響。本實驗采用分光光度計及鄰二氮菲-Fe3+測定保健食品中水溶性成分抗氧化能力,使保健食品中的水溶性抗氧化成分直接與反應體系中的Fe3+作用,試圖避開額外產生自由基的影響,提高方法的精密度。
1 材料與方法
1.1 材料與試劑
山竹粉 義烏章舸生物工程有限公司;葡萄籽膠囊艾申特生物科技有限公司;保健食品(品名:健康啟程)北京北衛藥業有限責任公司;茶色素 江西綠色制藥有限公司;雅培牌胰肽素軟膠囊 北京北衛藥業有限責任公司。
1,10-鄰二氮菲(分析純) 廣東汕頭市西隴化工廠;水溶性維生素E 美國Sigma公司;磷酸(分析純);磷酸二氫鈉;磷酸氫二鉀;硫酸高鐵銨(分析純);磷酸緩沖液PBS (75mmol/L、 pH7.4)、硫酸高鐵銨(10mmol/L)、鄰二氮菲(1.5mmol/L)、Trolox標準儲備液(0.2g/L Trolox)。
1.2 儀器與設備
HH-4型數顯恒溫水浴鍋 江蘇省金壇市榮華儀器制造有限公司;PP-15專業型pH計 梅特勒-托利多儀器(上海)有限公司;P211D分析天平 北京賽多利斯有限公司;METTLER AE100電子天平 梅特勒-托利多儀器(上海)有限公司;渦旋混勻器 德國IKA公司;TDL-5CENTRIFUGE離心機 上海安亭科學儀器廠;KQ-100B臺式超聲波清洗器 昆山市超聲儀器有限公司;UV-2450 紫外-可見分光光度計 日本Shimadzu 公司。
1.3 方法
1.3.1 鄰二氮菲-Fe3+分光光度法原理
將待測保健食品樣品粉碎,用磷酸緩沖液提取樣品中水溶性抗氧化成分。反應體系中的三價鐵離子(Fe3+)被提取液中的抗氧化成分(還原性物質)還原為Fe2+,亞鐵離子再與反應體系中的鄰二氮菲生成穩定的橙紅色絡合物,其吸光度與Fe2+濃度的關系符合朗伯-比耳定律,可用分光光度計檢測,由此測定出樣品中抗氧化(還原性)物質的多少。以水溶性VE為標準,用每單位抗氧化樣品還原能力相當于水溶性VE的當量作為該樣品的抗氧化能力。
1.3.2 樣品提取
準確稱取樣品(例如葡萄籽膠囊0.025g)用20mL緩沖液溶解后,超聲提取20min, 5000r/min離心10min,將上清移入50mL容量瓶內,沉淀用20mL緩沖液溶解后再提取一次,合并兩次提取液,用緩沖液定容至50mL搖勻,即為待測樣品。
1.3.3 樣品及Trolox的測定
在干凈試管中加入1mL磷酸緩沖液PBS,再加入0.1mL樣品或標準Trolox(分別為樣品管或標準Trolox管),再加入2mL鄰二氮菲和0.5mL硫酸高鐵銨,水浴30min后取出試管再加入0.2mL磷酸,室溫靜置10min;以不加入任何樣品或標準Trolox,其他條件與上述相同的試管為對照管;以只加0.1mL樣品其余體積用磷酸緩沖液PBS補齊,該試管為樣品空白管。在536nm波長處以蒸餾水調零比色測定其吸光度,記錄數值。
反應中Fe3+會被抗氧化劑還原為Fe2+,但未反應完剩余的Fe3+也會與鄰二氮菲生成黃色絡合物,因此當Fe2+和Fe3+共存情況下,Fe3+的干擾是客觀存在且不可忽視的。因此選用磷酸(H3PO4)當掩蔽劑,Fe3+可與H3PO4形成穩定的無色Fe(HPO4)+配離子,從而有效地排除了顯色時Fe3+對Fe2+離子的干擾。H3PO4不具有氧化性,測定時不參與對Fe2+離子的氧化作用。
1.3.4 抗氧化能力計算

式中:抗氧化能力值以Trolox當量(μmol Trolox當量/g)表示,即1g樣品相當于Trolox微摩爾數;A樣品、ATrolox、A對照分別為樣品管、標準管和對照管的吸光度;MTrolox為標準管所含Trolox的微摩爾數;M樣品為樣品管所含樣品的質量。
1.3.5 標準曲線的繪制
取0.2g/L Trolox標準儲備液1mL加1mL磷酸緩沖液稀釋為0.1g/L應用液,再將應用液用磷酸緩沖液稀釋為0.05、0.025、0.0125、0.00625g/L的Trolox標準品溶液。按1.3.3節方法測定。
1.3.6 最低檢測下限
連續測定對照管吸光度10次,根據最低檢測限的計算公式計算結果。
DL=3SD/K
式中:DL為最低檢測限;SD為標準偏差;K為斜率。
1.3.7 平行性精密度實驗
準確稱取山竹粉0.025g 5份,平行操作,用1.3.3節方法提取并測定。
1.3.8 重復性精密度實驗
每天準確稱取山竹粉0.025g 3份,用1.3.3節方法提取并測定。連續測定5 d。
1.3.9 加標回收率實驗
準確稱取0.025g山竹粉2份,其中一份定量加入0.0025g標準Trolox,樣品處理及測定方法同上。重復測定5次。

2 結果與分析
2.1 Trolox標準曲線的繪制

圖1 Trolox標準曲線Fig.1 Troloxst and ardcurve
由圖1可知,Trolox 在質量濃度0.00625~0.1g/L范圍內有較好的線性關系和較低的檢測下限。
2.2 最低檢測下限測定
平行測定10次對照管值,計算可得方法檢測Trolox的最低檢測下限為0.27μmol/L。由于在實際樣品測定時干擾因素較多,因此將這一數值再放大2倍作為本方法的最低檢測下限,即0.54μmol/L。
2.3 平行性精密度實驗
用山竹粉樣品進行平行性精密度實驗,5個平行測定結果為(396±11.0)μmol/g ,變異系數為2.7%,表明方法的平行性精密度良好。
2.4 重復性精密度實驗結果
用山竹粉進行重復性精密度實驗,其5次重復性測定結果為(402±13.2)μmol/g ,變異系數為3.3%,表明方法的重復性精密度良好。
2.5 加標回收率實驗結果
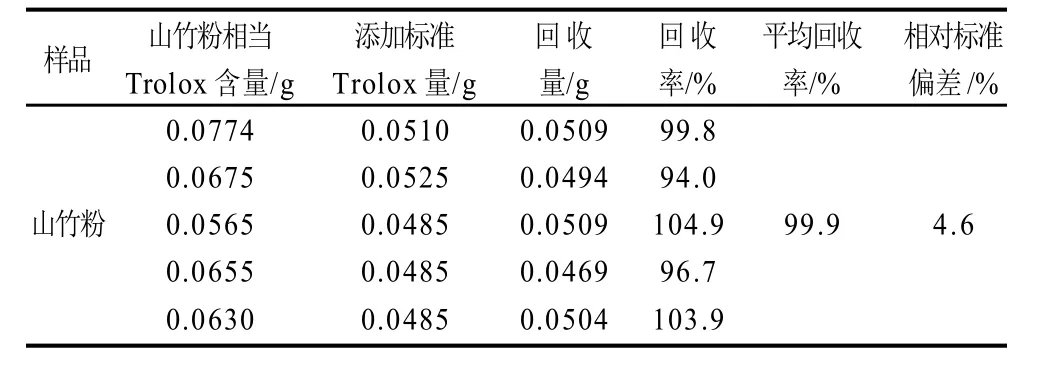
表1 加標回收率實驗結果Table1 Spiker ecoveries for Trolox in mangosteen powder
用山竹粉樣品進行加標回收率實驗(表1),5次重復結果為(99.9±4.6)%,表明方法具有較好的準確度。用鄰二氮菲-Fe2+法測定同一樣品(山竹粉),將鄰二氮菲-Fe3+法與鄰二氮菲-Fe2+法[19]測定結果進比較(表2)。結果表明,鄰二氮菲-Fe3+法測得最低檢測下限有了明顯的下降,這可能與鄰二氮菲-Fe2+法反應體系中有H2O2的有關。當H2O2加量過多,過量的H2O2與樣品中還原性物質反應,還原性物質對Fe2+保護的靈敏性下降,使得檢測下限偏高。另外,鄰二氮菲-Fe3+法重復性精密度明顯好于鄰二氮菲-Fe2+法,其他指標都與鄰二氮菲-Fe2+法相差不大。說明與鄰二氮菲-Fe2+法比較,鄰二氮菲-Fe3+法測定保健食品抗氧化能力有更好的穩定性。

表2 鄰二氮菲-F e2+法與鄰二氮菲-F e3+法方法學對比Table2 Methodological comparisonbetween phenan throline-Fe2+ and phen an throline-Fe3+ methods
2.6 5種樣品抗氧化能力的測定結果

表3 樣品抗氧化能力測定結果(n=5)Table 3 Antioxidant capacity of various commercial functional foods determined by phenanthroline-Fe3+ method (n=5)
用該方法順利測定了山竹粉等5種樣品中水溶性部分的抗氧化能力,結果見表3。重復測定結果的變異系數為2.2%~2.8%,表明用此方法實測樣品,結果具有良好的重復性。
3 討 論
3.1 方法的適用性
由于方法的顯色反應是在水相中進行,因此對于樣品的提取、分離等前處理過程采用磷酸緩沖液,標準參照物也選擇了水溶性VE。保健食品中的抗氧化活性成分可以分為脂溶性和水溶性兩部分。本方法只能檢測到保健食品中水溶性成分的抗氧化能力,樣品中脂溶性成份的抗氧化能力不能被測定出來。 因此此方法適用于檢測不含脂溶性成份或脂溶性成份含量低的保健食品。對于脂溶性成份含量高的保健食品,本方法只能檢測其水溶性成份的抗氧化能力,脂溶性成份的抗氧化能力需采用其他方法檢測。
3.2 方法的局限性
保健食品中的抗氧化成份絕大部分為能夠給出電子將自由基轉變為陰離子的還原劑。常見金屬離子氧化性排列順序如下:K+<Ca2+<Na+<Mg2+<Al3+<Mn2+<Zn2+<Cr3+<Fe2+<Ni2+<Sn2+<Pb2+<(H+)<Cu2+<Hg2+<Fe3+<Ag+<Pt2+<Au2+從這個排列順序可知Fe3+具有很強的氧化性,因此能夠與保健食品中的絕大部分還原劑反應,故采用鄰二氮菲Fe3+法可將這些具有還原性的抗氧化成份檢測出來。但是個別樣品可能會含有一些高氧化還原電位的抗氧化物質,它們不能將Fe3+還原,盡管它們能夠與自由基發生反應但用本方法卻不能將它們檢測出來,這是本方法的局限性。
4 結 論
鄰二氮菲-Fe3+法具有良好的準確度(RSD 2.7%)和精密度(RSD 3.3%);最低檢測下限為0.54μmol/L;在0.66~10.53μmoL/L Trolox濃度范圍內具有較好的線性關系(R2=0.9999)。鄰二氮菲-Fe3+法避開自由基的生成和消耗,簡化了實驗的步驟,與鄰二氮菲-Fe2+法相比具有更好的穩定性,實驗證明鄰二氮菲-Fe3+法適用于保健食品水溶性成份抗氧化能力的檢測。
[1] ABDI S, ALI A. Role of ROS modified human DNA in the pathogenesis and etiology of cancer[J]. Cancer Letters, 1999, 142(1): 1-9.
[2] OLSEN H, SELJEFLOT I, KHLER H, et al. Increased leukocyte levels of reactive oxygen species (ROS) in populations at risk for atherosclerotic disease[J]. Atherosclerosis, 2000, 151(1): 57-59.
[3] ANGELOPOULOU R, LAVRANOS G, MANOLAKOU P. ROS in the aging male: Model diseases with ROS-related pathophysiology[J]. Reproductive Toxicology, 2009, 2(28): 167-171.
[4] 李云. 綜述自由基對人體健康的影響及目前的預防措施[J]. 內蒙古石油化工, 2011(1): 87-89.
[5] 方允中. 自由基生物學的理論與應用[M]. 北京: 科學出版社, 2002: 649-703.
[6] RYAN P, HYNES M J. The kinetics and mechanisms of the complex formation and antioxidant behaviour of the polyphenols EGCg and ECG with iron(Ⅲ)[J]. Journal of Inorganic Biochemistry, 2007, 101(4): 585-593
[7] CASALINO E, CALZARETTI G, SBLANO C, et al. Molecular inhibitory mechanisms of antioxidant enzymes in rat liver and kidney by cadmium[J]. Toxicology, 2002, 179(1/2): 37-50.
[8] 文鏡, 劉璇, 趙建. 熒光法及化學發光法在保健食品抗氧化體外實驗中的應用[J]. 中國釀造, 2009(11): 130-133.
[9] 楊芬, 張瑞萍, 賀玖明, 等. 羥自由基的產生、捕集及檢測方法[J].藥學學報, 2007, 42(7): 692-697.
[10] 陳培榕, 李景虹, 鄧勃. 現代儀器分析試驗與技術[M ]. 北京: 清華大學出版社, 2006,17(11): 65-67.
[11] 叢建波, 孫存普, 莫簡. 自旋捕集短壽命自由基的低溫保存[J]. 生物化學與生物物理進展, 1993, 20(4): 326-327.
[12] 續潔琨, 姚新生, 栗原博. 抗氧化能力指數(ORAC)測定原理及應用[J]. 中國藥理學通報, 2006, 22(8): 1015-21.
[13] 程宏英, 曹玉華. 毛細管電泳-電化學檢測法測定硫酸銅-維生素C反應體系中的羥基自由基和菊花的抗氧化活性[J]. 2007, 25(5): 681-685.
[14] ONOR, ODA T. Measurement of hydroxyl radicals in pulsed corona discharge[J]. Journal of Elect rostatics, 2002, 55: 333-342.
[15] SAYWELL L B, CUNNINGHAM B B. Determination of iron: colorimetric o-phenanthroline method[J]. Analytical Chemistry, 1937, 9(2): 67-69.
[16] TAMURA H, GOTO K, YOTSUYANAGI T, et al. Spectrophotometric determination of iron(Ⅱ) with 1,10-phenanthroline in the presence of large amounts of iron(Ⅲ)[J]. Talanta, 1974, 21(4): 314-318.
[17] 陳勝兵, 何少華, 婁今生, 等. Fenton試劑的氧化作用機理及其應用[J]. 環境科學與技術, 2004, 3(27):105-107.
[18] 金鳴, 蔡亞欣, 李金榮, 等. 鄰二氮菲-Fe2+氧化法檢測H2O2/Fe2+產生的羥自由基[J]. 生物化學與生物物理進展, 1996, 23(6): 553-555.
[19] 文鏡, 劉薇, 王宏君, 等. 鄰二氮菲-Fe2+法測定保健食品的抗氧化能力[J]. 食品科學, 2010, 31(18): 333-337.
Determination of Antioxidant Capacity of Water-soluble Compounds in Functional Food by Phenanthroline-Ferric Ion Method
LIU Wei,LIU Wen-jia,LIU Yan-xia,ZHAO Jian,WEN Jing*
(Beijing Key Laboratory of Bioactive Substances and Functional Foods, College of Arts and Science, Beijing Union University, Beijing 100191, China)
Objective: To establish a colorimetric method to determine the antioxidant capacity of water-soluble compounds in functional food based on the reaction between 1,10-2 phenanthroline and Fe3+to form yellow complexes. Methods: The hydrophilic antioxidants in functional foods were extracted with pH 7.4 PBS buffer solution (75 mmol/L) and allowed to reduce Fe3+to Fe2+. Fe2+was exposed to 1,10-2 phenanthroline to form a stable Fe2+-phenanthroline complex. The absorbance of the complex was determined on a spectrophotometer at 536 nm and used to calculate the antioxidant capacity of water-soluble compounds in functional food using Trolox, a water soluble vitamin E analog, as the reference standard. The accuracy, linearity, repeatability, recovery rate and limit of detection (LOD) of this method were studied, and its feasibility was also verified. Results: This method showed a good linearity over the Trolox concentration of 0.66-10.53 μmol/L (R2= 0.9999). The LOD was 0.54 μmol/L. The replicability and repeatability was 2.7% and 3.3% relative standard deviation (RSD), respectively. The mean spike recovery was (99.9±4.6)% (n = 5). Conclusion: This method is applicable to determine the antioxidant capacity of water-soluble compounds in functional food.
functional food;antioxidant capacity;phenanthroline-Fe3+method
TS207.3
A
1002-6630(2011)16-0261-04
2011-05-16
北京市教委科技發展計劃項目(KM201011417006)
劉薇(1986—),女,助理工程師,主要從事保健食品功能評價研究。E-mail:liuwei4465@sina.com
*通信作者:文鏡(1952—),男,教授,主要從事保健食品功能學評價機理和方法學研究。E-mail:wenjing@ygi.edu.cn

