pH、離子強度、時間和溫度對Cd(Ⅱ)在伊利石上吸附的影響
劉 霞,陳元濤,*,胡 君,張 煒,池亞玲,郭智軍,肖 江
1.青海師范大學 化學系,青海 西寧 810008;2.中國科學院 等離子體物理研究所,安徽 合肥 230031
隨著工業化和城市化的發展,工業廢水中的重金屬造成的環境污染具有不可逆性和長期性,嚴重威脅著全球生態系統及人類健康,各國現已將重金屬元素列為環境中的優先控制污染物。鎘普遍存在于工業廢水中,它是毒性最強、移動性最大的重金屬之一,被美國毒物管理委員會列為第6位危及人體健康的有毒物質。另外109Cd(Ⅱ)是一種高毒性放射性核素。因此,對重金屬復合污染的研究十分必要。黏土礦物作為環境自凈化劑,其吸附性能在治理環境污染的自凈化工程研究中受到了廣泛的關注[1-5]。鎘作為當今重金屬水污染中的主要污染物之一,國內外已利用各種黏土對鎘進行吸附,如:累托石、膨潤土、針鐵石和蒙脫土等[6-9],并均有良好的吸附效果,但用伊利石去除鎘的報道卻很少,本實驗以伊利石為吸附劑,主要研究pH值、離子強度、時間及溫度等因素對Cd(Ⅱ)在伊利石上吸附的影響。
1 實驗材料與方法
1.1 實驗材料
伊利石,購自成明伊利石公司,化學組成為K0.75(Al1.75R)[Si3.5Al0.5O10](OH)2,是一種富含鉀、高鋁的層狀含水硅酸鹽礦物,其層間區域中存在著可交換的水合陽離子和水。實驗所用試劑均為分析純,且所有試劑均用二次蒸餾水配制。
1.2 實驗儀器
AL204型電光分析天平(感量0.000 1 g)、pH-3B型精密pH計,上海梅特勒-托利多儀器有限公司;722型分光光度計,上海光譜儀器有限公司;微量可調移液器,北京青云卓立精密設備有限公司;LG10-2.4A型高速離心機,北京醫用離心機廠。
1.3 實驗方法
1.3.1吸附實驗 實驗采用靜態批式法,在聚乙烯離心管中加入一定量的伊利石懸浮液和Cd(Ⅱ)溶液,分別用0.001、0.01、0.1 mol/L NaClO4調節離子強度,用微量的HClO4或NaOH調節體系的pH至所需值。振蕩24 h,待吸附達到平衡后,在8 000 r/min下離心10 min,取一定體積的上清液,用分光光度法測定上清液中Cd(Ⅱ)的濃度。伊利石吸附Cd(Ⅱ)的量從吸附初始和平衡后兩者的差值計算得到。所有實驗數據都是3次實驗的平均值,數據相對誤差約為5%。
1.3.2數據處理 Cd(Ⅱ)的吸附率(Y)計算公式為:
(1)
式中:c0是Cd(Ⅱ)的初始濃度,mol/L;ce是吸附平衡后上清液中Cd(Ⅱ)的濃度,mol/L。
2 結果與討論
2.1 pH和離子強度對Cd(Ⅱ)吸附的影響
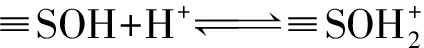

(2)

(3)
(4)
當pH值升高時,Cd(Ⅱ)的水解程度隨著溶液中的OH-濃度增高而增加,Cd(Ⅱ)的吸附率也隨之增加,這表明Cd(Ⅱ)在伊利石表面的吸附主要是由表面絡合反應引起的,而非內層絡合[11-12]。
離子強度是影響Cd(Ⅱ)在伊利石上吸附的另一重要因素。從圖1(a)還可以看出,當pH<7.5時Cd(Ⅱ)的吸附率受離子強度影響較大,可以推斷出在此pH范圍內Cd(Ⅱ)在伊利石上的吸附主要是通過外層絡合或通過與占據了吸附劑表面位的H+或者Na+進行離子交換來實現[13],在此pH范圍內,Cd(Ⅱ)在伊利石上的吸附率緩慢增加,并且在高濃度的NaClO4溶液中Cd(Ⅱ)的吸附率比在低濃度的NaClO4溶液中的要小,這一現象也證明了上面的吸附理論;當pH=7.5~9時,受離子強度影響較小;當pH>9時,吸附率不受影響。
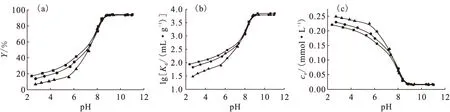
圖1 不同離子強度下pH對伊利石吸附Cd(Ⅱ)的影響
圖1(b)是描述lgKd隨pH變化的曲線,從圖中可以看出:pH<7.5時,lgKd隨pH的升高而增大;當pH>7.5時,lgKd保持不變。由圖1(c)可知,ce隨pH升高而迅速降低,最后保持平衡不變。Kd表達式如下:
(5)
式中:Cs是Cd(Ⅱ)在吸附劑上的平衡濃度,mol/g;V是懸浮液的總體積,mL;m是吸附劑的質量,g。
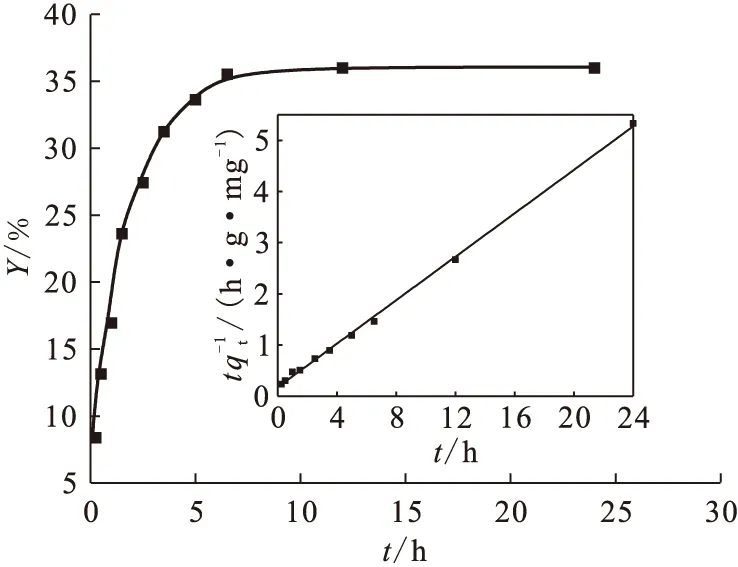
圖2 吸附時間對Cd(Ⅱ)吸附的影響和伊利石吸附Cd(Ⅱ)的準二級動力學模型(內圖)
2.2 反應時間對Cd(Ⅱ)吸附的影響及其動力學特征
反應時間對Cd(Ⅱ)在伊利石上的吸附影響示于圖2。由圖2可知,Cd(Ⅱ)的吸附率隨著反應時間增加而迅速增大,在反應5 h時吸附率達到最大并隨時間增加保持不變。吸附在幾小時內就達到平衡,這表明Cd(Ⅱ)在伊利石上的吸附主要是化學吸附而非物理吸附[14-15]。Cd(Ⅱ)在伊利石上的吸附動力學準二階方程為:
Lagrange準二級動力學模型:
(6)
式中qt和qe分別是吸附t時和吸附平衡時的吸附量,mg/g;t為吸附時間,h;k′為二級吸附速率常數,g/(mg·h)。t/qt-t的線性擬合結果示于圖2內插圖,相關動力學參數可以從公式(6)中求得:qe=4.754 mg/g,k′=0.246 g/(mg·h),r2=0.999,數據表明準二級動力學模型可以很好的擬合Cd(Ⅱ)在伊利石上的吸附動力學。因此,本實驗對混合懸濁液振蕩24 h完全可使吸附實驗達到平衡。
2.3 溫度對Cd(Ⅱ)吸附的影響及其吸附熱力學
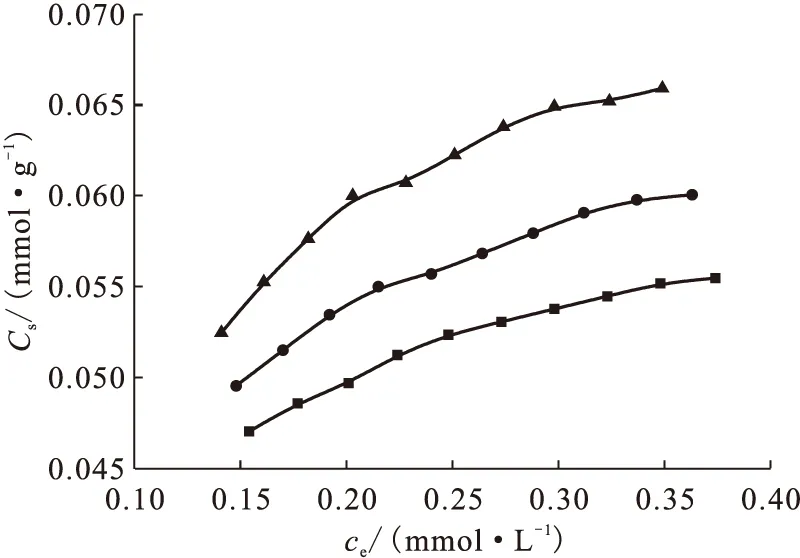
圖3 3種溫度下Cd(Ⅱ)在伊利石上的吸附等溫線
溫度是影響Cd(Ⅱ)在伊利石上吸附的又一重要因素,本實驗分別在288、303、323 K下對其進行研究,實驗條件為:m/V=2.4 g/L,c0(NaClO4)=0.01 mol/L,pH=6.04±0.01。實驗結果示于圖3。由圖3可以看出,Cd(Ⅱ)在伊利石上的吸附率隨著溫度的升高而增大,表明在該實驗條件下升高溫度有利于吸附。為了更好的證明以上觀點,分別用Langmuir、Freundlich和D-R(Dubini-Radushkevich)模型對實驗數據進行擬合,結果示于圖4,擬合的相關參數列于表1。

圖4 3種溫度下Cd(Ⅱ)在伊利石上吸附的3種吸附模型

表1 不同溫度下Langmuir、Freundlich和D-R模型的擬合參數
Langmuir等溫線方程為:
(7)
式中Csmax是單分子層飽和吸附量,mol/g;b是Langmuir常數,L/mol。
由圖4(a)可知,ce/Cs對ce呈線性關系,3種溫度下的r2分別為0.999、0.999、0.998。這表明伊利石對Cd(Ⅱ)的吸附吻合于Langmuir等溫線方程;并且吸附主要發生在伊利石表面的活性區位,屬于單層吸附[16]。
Freundlich等溫線方程為:
(8)
式中:KF(mol1-n·Ln/g)和n是Freundlich常數。
由圖4(b)和表1可知,n值介于0~1之間,表明所選定的吸附條件有利于伊利石對Cd(Ⅱ)的吸附。但圖4(b)r2僅為0.986、0.984和0.964,這說明Langmuir等溫線方程比Freundlich等溫線方程更吻合伊利石對Cd(Ⅱ)的吸附過程。
Dubinin-Radushkevich(D-R)等溫線方程:
lnCs=lnCsmax-βε2
(9)
式中:β是與吸附能有關的常數,mol2/kJ;ε是Polanyi活化能,ε表達式為:
(10)
由圖4(c)可知,r2分別為0.989、0.987、0.976。說明Langmuir等溫線方程比D-R等溫線方程更吻合伊利石對Cd(Ⅱ)的吸附過程。平均吸附自由能E(kJ/mol)表達式如下:
(11)
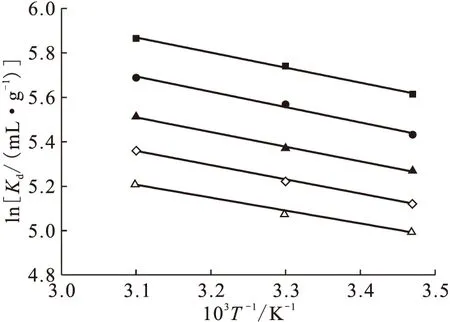
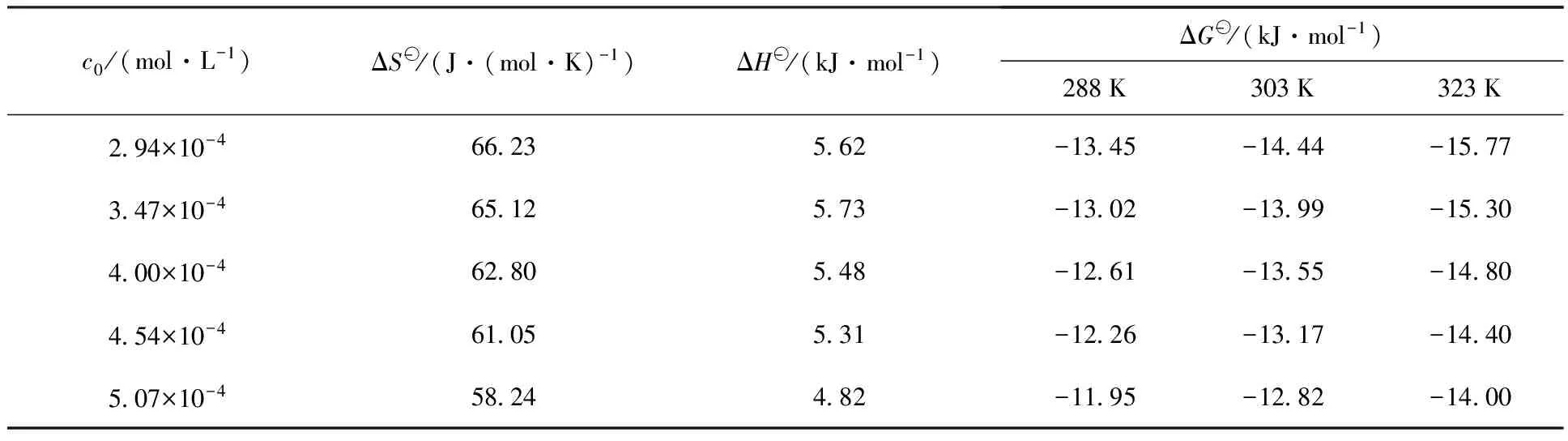
平均吸附自由能E的大小可以反映該機制是物理吸附還是化學吸附。若E<8 kJ/mol,表明該吸附是物理吸附;若8 (12) (13) 圖5 Cd(Ⅱ)在伊利石上吸附的熱力學參數評價 表2 Cd(Ⅱ)在伊利石上的吸附熱力學參數 (1)pH值和離子強度對Cd(Ⅱ)在伊利石上的吸附都有明顯影響,在pH=2~6時,Cd(Ⅱ)的吸附率隨pH的升高而增加,隨離子強度的增強而降低。 (2)Cd(Ⅱ)在伊利石上的吸附在5 h內達到吸附平衡,吸附過程服從準二級吸附動力學模型。 (3)Cd(Ⅱ)在伊利石上的吸附是自發吸熱過程,并且該吸附符合Langmuir等溫線。 [1]Chen L,Yu X J,Zhao Z D,et al.Sorption and Desorption of Co(Ⅱ)on Montmorillonite in Presence and Absence of Fulvic Acid[J].J Radioanal Nucl Chem,2008,275(1): 209-216. [2]EI-Khouly S H.Separation of Europium,Cobalt and Zinc on Zirconium Tungstate Ion Exchanger[J].J Radioanal Nucl Chem,2006,270(2): 391-398. [3]Yu S,Ren A,Cheng J,et al.Comparative Study on Sorption of Radiocobalt to Montmorillonite and Its Alpillared and Cross-Linked Samples: Effect of pH,Ionic Strength and Fulvic Acid[J].J Radioanal Nucl Chem,2007,273(1): 129-133. [4]Davila-Rangel J I,Solache-Rios M.Sorption of Cobalt by Two Mexican Clinoptilolite Rich Tuffs Zeolitic Rocks and Kaolinite[J].J Radioanal Nucl Chem,2006,270(2): 465-471. [5]丁國清,張茂林,吳王鎖.幾種有機物對 Al2O3吸附Eu(Ⅲ)和Am(Ⅲ)的影響[J].核化學與放射化學,2006,28(4):240-243. [6]杜冬云,孫文,揭武,等.鈣基累托石對模擬水中鎘的吸附[J].離子交換與吸附,2004,20(6):519-525. [7]Zhao D L,Chen S H,Yang S B,et al.Investigation of the Sorption Behavior of Cd(Ⅱ)on GMZ Bentonite as Affected by Solution Chemistry[J].Chem Eng J,2011,166(3): 1 010-1 016. [8]Weirich D B,Hari R,Xue H B,et al.Adsorption of Cu,Cd,and Ni on Goethite in the Presence of Natural Groundwater Ligands[J].Environ Sci Technol,2002,36(3): 328-336. [9]Bradbury H M,Baeyens B.Modelling the Sorption of Mn(Ⅱ),Co(Ⅱ),Ni(Ⅱ),Zn(Ⅱ),Cd(Ⅱ),Eu(Ⅲ),Am(Ⅲ),Sn(Ⅳ),Th(Ⅳ),Np(Ⅴ)and U(Ⅵ)on Montmorillonite: Linear Free Energy Relationships and Estimates of Surface Binding Constants for Some Selected Heavy Metals and Actinides[J].Geochimica et Cosmochimica Acta,2005,69(4): 875-892. [10]張暉,張麗鵬,于先進,等.放射性核素60Co(Ⅱ)在伊利石上的吸附行為[J].核化學與放射化學,2011,33(3):167-172. [11]Xu D,Wang X K,Chen C L,et al.Influence of Soil Humic Acid and Fulvic Acid on Sorption of Thorium(Ⅳ)on MX-80 Bentonite[J].Radiochim Acta,2006,94(8): 429-434. [12]Yu S M,Chen C L,Chang P P,et al.Adsorption of Th(Ⅳ)Onto Al-Pillared Rectorite: Effect of pH,Ionic Strength,Temperature,Soil Humic Acid and Fulvic Acid[J].Appl Clay Sci,2008,38(3-4): 219-226. [13]邵大冬,許笛,王所偉,等.pH值和離子強度對放射性核素鎳在MX-80 黏土上的吸附影響和模型研究[J].中國科學B:化學,2008,38(11):1 025-1 034. [14]Liu W X.Modeling Description and Spectroscopic Evidence of Surface Acid-Base Properties of Natural Illites[J].Water Res,2001,35(17): 4 111-4 125. [15]Zhao G X,Li J X,Ren X M,et al.Few-Layered Graphene Oxide Nanosheets as Superior Sorbents for Heavy Metal Ion Pollution Management[J].Environ Sci Technol,2011,45(24): 10 454-10 462. [16]Langmuir I.The Adsorption of Gases on Plane Surfaces of Glass,Mica and Platinum[J].J Am Chem Soc,1918,40(9): 1 361-1 403. [17]Lodeiro P,Barriada J L,Herrero R,et al.The Marine Macroalga Cystoseira Baccata as Biosorbent for Cadmium(Ⅱ)and Lead(Ⅱ)Removal: Kinetic and Equilibrium Studies[J].Environ Pollut,2006,142(2): 264-273. [18]Shirvani M,Shaiatmadari H,Kalbasi M,et al.Sorption of Cadmium on Palygorskite,Sepiolite and Calcite: Equilibria and Organic Ligand Affected Kinetics[J].Colloids Surf A: Physicochen Eng Aapects,2006,287(1-3): 182-190.2.4 伊利石對Cd(Ⅱ)的吸附熱力學特征
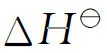
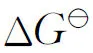
3 結 論

