吡咯烷類二肽基肽酶-Ⅳ抑制劑的最新研究進展
付文卓 吳英婷 張進祿
(首都醫科大學醫學實驗與測試中心,北京100069)
胰高血糖素樣肽1(glucagon like peptide,GLP-1)是一種腸促胰島素,可以促進胰島素分泌、調節血糖、保護胰島β細胞,刺激其分化。但是活化的GLP-1在體內會迅速被二肽基肽酶降解而失去活性。吡咯烷類二肽基肽酶(dipeptidyl peptidase-Ⅳ,DPP-4)抑制劑是一種細胞表面的絲氨酸蛋白酶,主要作用是分解體內的蛋白質,能夠特異地裂解GLP-1的N端末端第2位的脯氨酸或丙氨基殘基[1-2]。
因此DPP-4抑制劑,可以通過抑制DPP-4活性,避免GLP-1快速失活,維持體內GLP-1濃度,進而促進2型糖尿病患者新的β細胞的生成,促進胰島素分泌,達到降血糖的效果,阻止疾病惡化,是近年來治療2型糖尿病的新方向[3]。
許多DPP-4抑制劑已經上市或者進入臨床試驗階段,而且都顯示了很好的治療效果。大量DPP-4抑制劑的構效關系已經被報道[4],根據已知DPP-4抑制劑的結構特點和作用機制分為底物類似的DPP-4抑制劑和非底物類似的DPP-4抑制劑,通過結合方式可分為非共價鍵DPP-4抑制劑和共價鍵DPP-4抑制劑。對于目前已經報道的DPP-4抑制劑,均為雜環小分子化合物,本文就含有吡咯環烷結構的二肽基肽酶-Ⅳ抑制劑的作用機制和結構特點進行綜述。
1 吡咯烷衍生物DPP-4抑制劑的作用機制
人類DPP-4是766個氨基酸跨膜糖蛋白,包括:胞質尾區(1~6位殘基),跨膜區域(7~28位殘基)和胞外區域(29~766位殘基)[5]。幾個重要的作用位點有S1口袋(由Tyr 631,Val 656,Trp 659,Tyr662,Tyr 666和Val711的側鏈組成,疏水性較高,可以高特異性識別脯氨酸或其衍生物),N端識別區(谷氨酸殘基Glu205/ Glu206和Tyr662的表面負電荷區域能與伯胺或仲胺配體形成氫鍵作用)。以脯氨酸為基本結構進行修飾,即含有吡咯環烷類DPP-4抑制劑,具有與DPP-4天然底物相似的結構,可以競爭性結合DPP-4活性部位。DPP-4的催化部位包括酶的S1口袋、N端識別區S2口袋和絲氨酸殘基的共價作用[6]。所以吡咯環烷類DPP-4抑制劑的基本結構特點含有脯氨酸或類似結構,含有堿性的伯胺或仲胺。根據結合的方式,吡咯環烷類DPP-4抑制劑可分為共價和非共價2類。
2 共價鍵結合吡咯環烷類DPP-4抑制劑
這是研究最為廣泛,最為深入的一類DPP-4抑制劑,基本結構包括:氰基吡咯環和含仲胺取代基[7]。諾華公司研發的1(NVP DPP-728)(IC50=22 nmol/ L),如圖1,是第1個含有氰基吡咯環結構的DPP-4抑制劑,能夠占據S1口袋,氰基能與受體產生共價作用。但是氰基容易與堿性氨基發生分子內環合,失去活性。所以對其進行結構修飾,降低分子內環合,大大提高了血漿半衰期[8]。
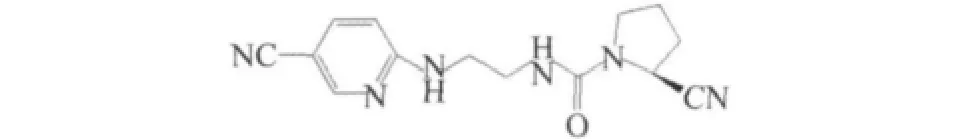
圖1 NVP-DPP-728結構式Fig.1 NVP-DPP-728
1)N端修飾:諾華公司以NVP DPP-728為先導化合物,在氨基引入了大體積取代基,如金剛烷胺,得到維格他汀(vildagliptin)2(IC50=35 nmol/L),見圖2,血漿半衰期明顯延長為3 h,提高了口服生物藥物的利用度(85%)[9]。
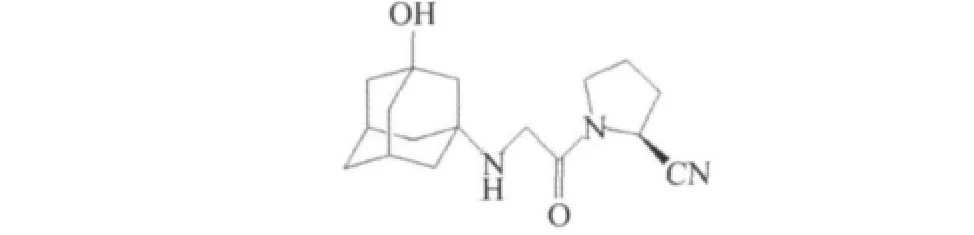
圖2 維格列汀Fig.2 Vildagliptin
K-579(IC50=5 nmol/L),在氨基附近引入2個雜環結構,延長了作用時間,t1/2=0.144 h,可作為長效DPP-4抑制劑[10],見圖3。類似機制的DPP-4抑制劑ASP4000(IC50=2.25 nmol/L),目前已進入臨床前研究階段[11],見圖4。
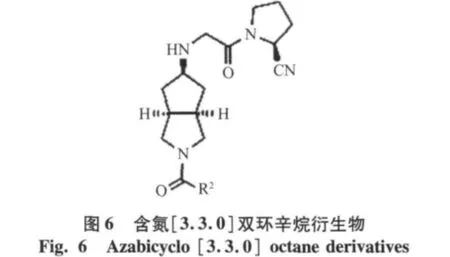
Cho T P等[13]在氨基端引入[3.3.0]雙環辛烷,合成了一系列含有雙環辛烷的衍生物,其中化合物(R1=OMe,R2=H)(IC50=0.008 μmol/L)并體現了對DPP-4較好的選擇性[12],見圖5。Cho T P等[13]以[3.3.0]雙環辛烷衍生物為基礎,繼續合成了一系列[3.3.0]雙環辛烷衍生物DPP-4抑制劑(IC50=0.009 μmol/L),見圖6。其中取代基為N(CH3)2時,并體現了更好的DPP-4的選擇性。目前已經進入到一期臨床研究階段。


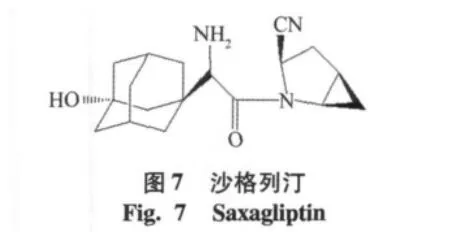
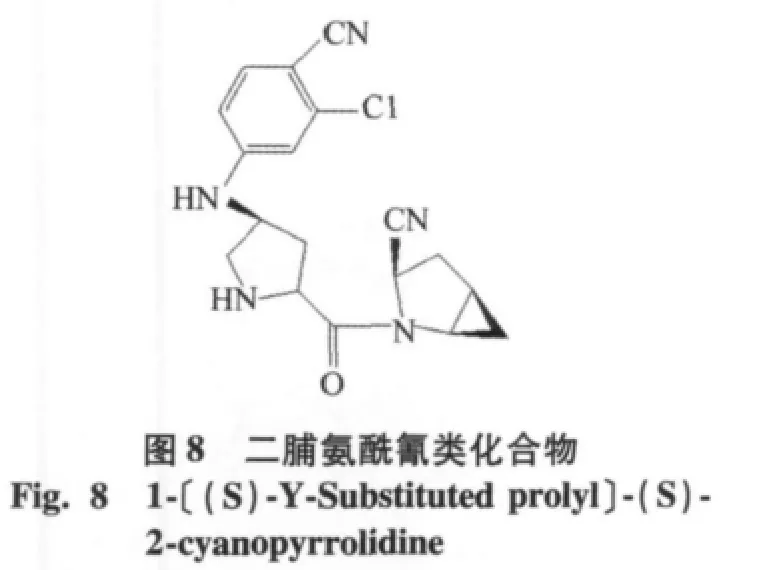
2)C端修飾:在氰基附近引入大體積基團也可以提高氰基吡咯烷類化合物的穩定性,如bristol-myers squibb公司在維格他汀結構的基礎上,在氰基吡咯環上引入環丙基,沙格列汀(saxagliptin,IC50=3.37 nmol/l),增加了穩定性,2009年7月被美國FDA批準上市,生物口服利用度為75%,t1/2=2.1 h[14],見圖7。另一個化合物二脯氨酰氰類化合物(IC50= 0.25 nmol/L),C端引入環丙烷基礎上,在P2上以4位取代的脯氨酸基團取代,見圖8。通過構效分析,引入5環的氨基酸可以提高氰基吡咯烷類DPP-4抑制劑的活性,要優于4環或者6環取代化合物。L-環氨基酸可以立體異構性地與酶的S2口袋結合[15]。
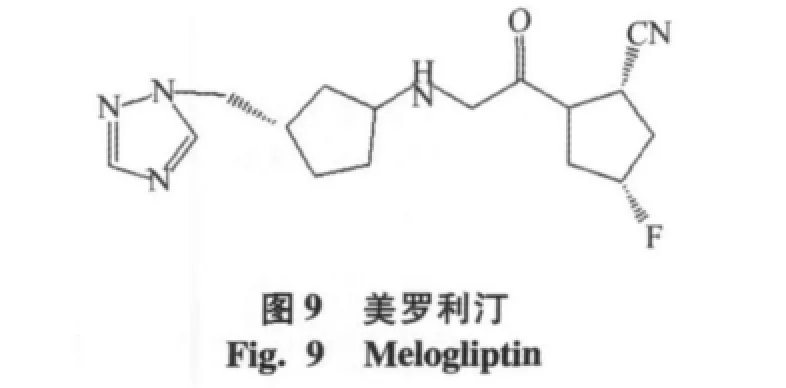
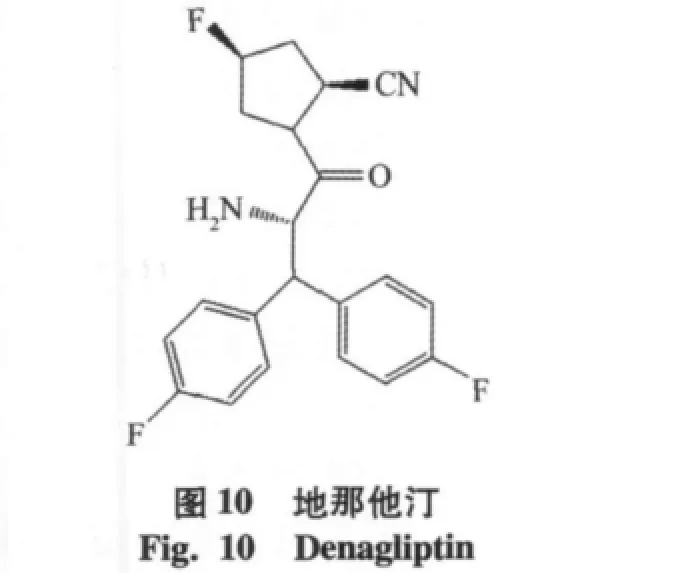
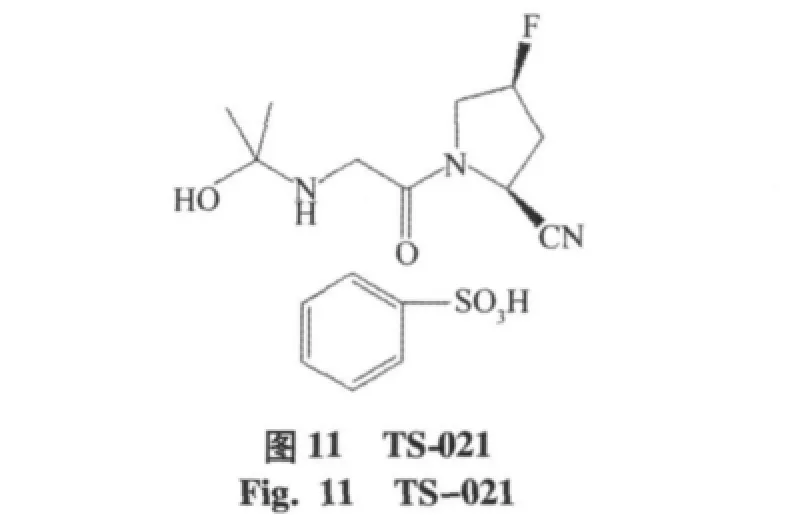
通過實驗[22]表明在吡咯烷環C-4位單氟取代,可以提高穩定性,如Glenmark pharmaceuticals Ltd公司的化合物美羅利汀(melogliptin,IC50=1.61 nmol/ L),目前已經進入到臨床Ⅱ期實驗階段[16]。Glaxosmithkline公司研發的地那列汀(denagliptin,IC50=22 nmol/ L),見圖10,其中結構特征為氟取代吡咯烷環,在N端引入(S)-2-氨基-3,3-二-(4-氟苯基)丙酸,雙氟苯取代基團可以與Phe357和Tyr547殘基的芳環相互作用,已經進入到臨床Ⅲ期實驗階段[17]。另外由Taisho公司研發的TS-021(IC50=5.0 nmol/L),目前處于臨床Ⅰ期的實驗階段[18],見圖11。
雅培公司研發的ABT-279引入乙炔基,見圖12,表現了很好的活性和選擇性〔Ki=1.0 nmol/L(DPP-4),>30 mol/L(DPP-8),>30 mol/L(DPP-9),>30 mol/L(DPP-7)〕,同時也具有很好的臨床前藥理安全性[CYP3A4,CYP2D6,CYP2C9(IC50>30 mol/L)]和毒理研究,給予鼠和狗4周每天大于1 000 mg/kg,均不見其產生明顯的不良反應[19]。

3 非共價鍵結合吡咯環烷類DPP-4抑制劑
在上述氰基吡咯烷類化合物去掉親電子基團氰基,可以直接減少環化的概率,提高穩定性。所以合理設計合成一系列無氰基的吡咯環類DPP-4抑制劑。由于缺少和絲氨酸的共價作用,所以活性中等。如苯基丙氨酸衍生物結構式(IC50=110 nmol/L),見圖13[20]。
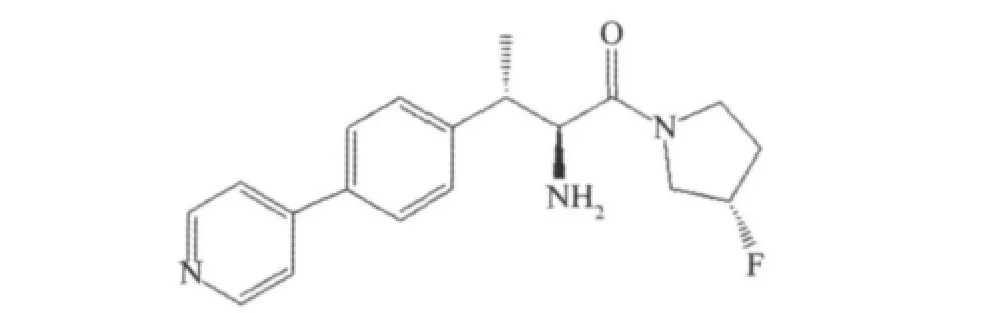
圖13 苯基丙氨酸衍生物Fig.13 Phenylalanine based derivative
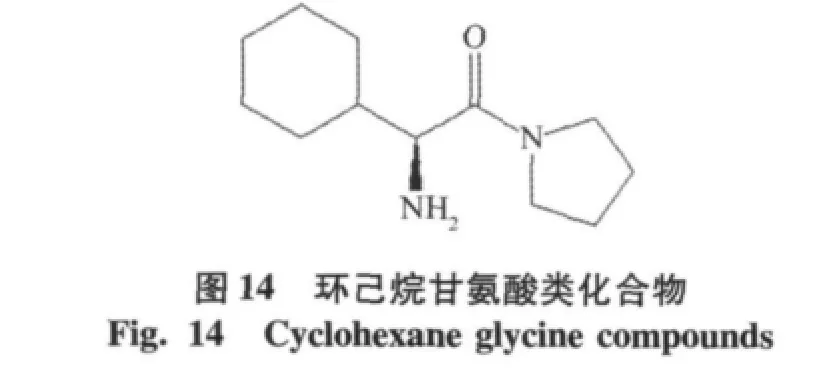
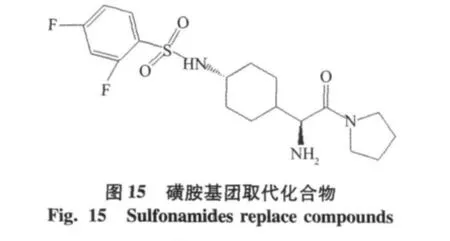
(s)-環己烷甘氨酸類化合物(IC50=320 nmol/ L)[21],不含氰基的吡咯環類抑制劑,后來多以環己烷甘氨酸類化合物為先導化合物,進行結構修飾,獲得更優秀的DPP-4抑制劑。以磺胺基團修飾后磺胺基團取代化合物(IC50=88 nmol/L),活性和選擇性都提高了[22],見圖14。
Tsai T Y等[23]合成了一系列2-(吡咯烷-1-羰基)取代的酰胺類化合物,其中活性最好的是2-(吡咯烷-1-羰基)取代的酰胺類化合物(IC50=0.050 μmol/ L),通過 LC-MS該化合物在水中表現了很好的穩定性。

以氟取代的吡咯環替代環己烷甘氨酸類化合物的吡咯環,設計并合成了一系列衍生物,具有同等或者更好的母體化合物。苯基丙氨酸類衍生物二甲氨基取代苯基丙氨酸衍生物具有DPP-4抑制活性和選擇性,見圖17[24],由于該類化合物的親脂性基團(聯芳基團),其與hERG離子通道結合特性,所以在血漿中IC50值要增加到10倍以上。
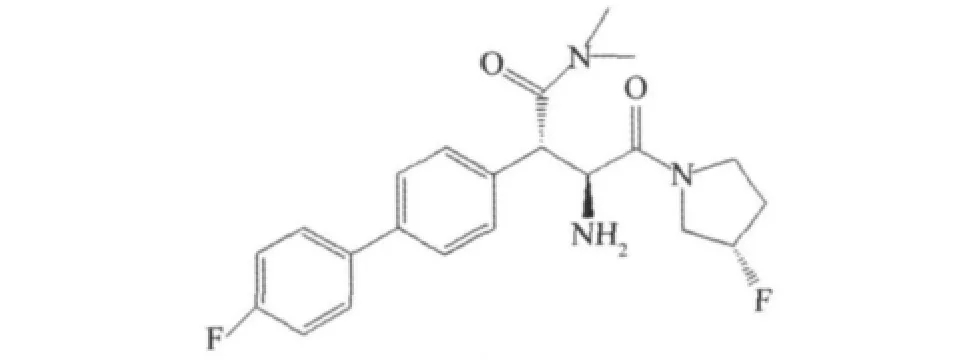
圖17 二甲氨基取代苯基丙氨酸衍生物Fig.17 Dimethylamide substituted phenylalanine derivative
用其他雜環替代二甲氨基取代苯基丙氨酸衍生物中4位氟苯基,得到化合物二甲氨基取代苯基丙氨酸衍生物(IC50=4.3 nmol/L),與hERG的結合能力得到了提高(IC50=86 mol/L),但是因為可能存在經鼠和人的代謝后活化,所以并沒有繼續深入研究[25]。

圖18 二甲氨基取代苯基丙氨酸衍生物Fig.18 Dimethylamide substituted phenylalanine derivative
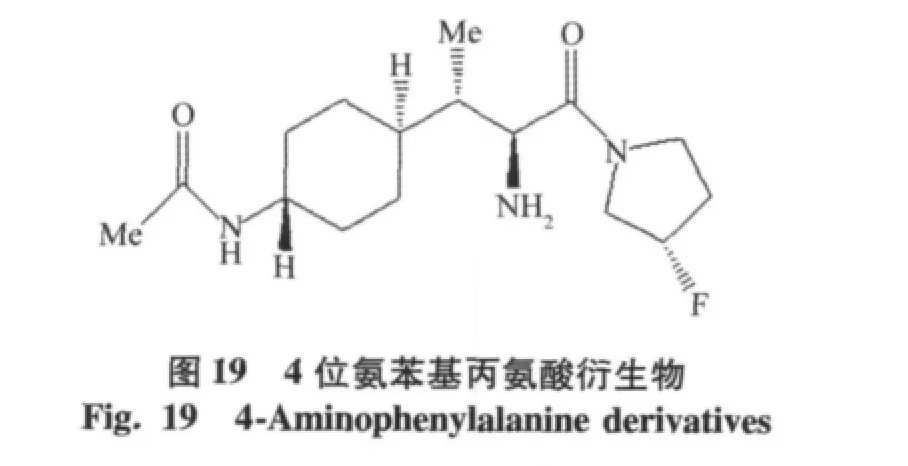
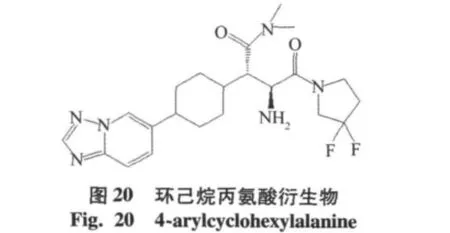
用環己基代替二甲氨基取代苯基丙氨酸衍生物中的苯基,得到的化合物4位氨苯基丙氨酸衍生物(IC50=0.016 μmol/L),具有很好的抑制活性,相對于DPP-8,DPP-9具有高度的選擇性,和離子通道hERG結合性低(IC50>90 μmol/L),但是在嚙齒類動物中的活性沒有達到預期結果[26]。結合化合物二甲氨基取代苯基丙氨酸衍生物和4位氨苯基丙氨酸衍生物得到新的一系列4-芳環己基丙氨酸DPP-4抑制劑,如環己烷丙氨酸衍生物(IC50=0.0048 μmol/L),X-射線晶體,環己烷丙氨酸衍生物的雜環部分與DPP-4的Arg358活性部位以氫鍵結合[27]。
4-氨基環己烷氨基乙酸衍生的 DPP-4抑制劑(IC50=48 nmol/L),沒有親電子基團[28],活性得到顯著提高,但是同時氟代吡咯氨基化合物對DPP-8,DPP-9也有很大的抑制作用DPP-8(IC50=993 nmol/ L),DPP-9(IC50=2 720 nmol/L),所以停止了進一步的研究,見圖21。
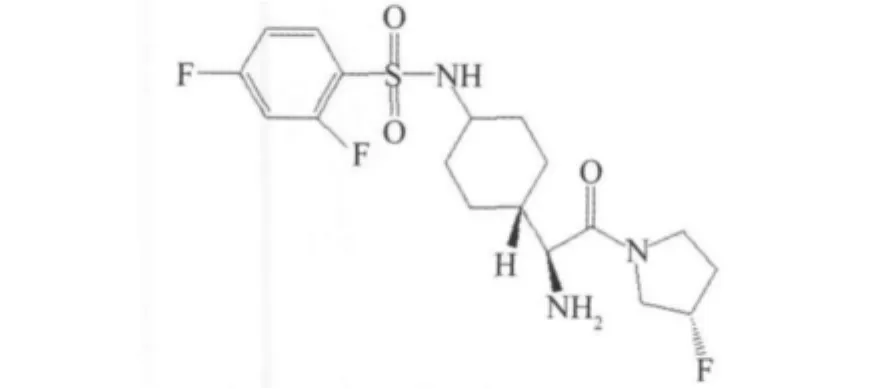
圖21 氟代吡咯氨基化合物Fig.21 Fluoropyrrolidine amides
將圖17中的苯基替代為其他雜環,通過構效關系研究合成了一系列新的惡唑環類DPP-4抑制劑,最優化的是〔IC50=0.019μmol/L(DPP-4),>100μmol/ L(DPP-8),>100 μmol/L(DPP-9)〕,并且體現了很好的選擇性[29],見圖22。通過X射線晶體衍射,二唑基衍生物的伯胺和β-甲基之間有同步性。圖22中的結合方式不同于苯基丙氨酸類衍生物二甲氨基取代苯基丙氨酸衍生物,二甲氨基取代苯基丙氨酸衍生物,環已烷丙氨酸衍生物。惡唑環進入到另一個DPP-4鍵合口袋。但是二唑基衍生物口服半衰期很短,其中鼠的半衰期為 (t1/2=1.3 h),狗的半衰期為(t1/2=1.75 h),所以阻礙了進一步研究。

圖22 二唑基衍生物Fig.22 Oxadiazole-based derivatives
多氟化的吡咯烷類衍生物已成為新的一類DPP-4抑制劑[30],代表性的化合物是四氟取代吡咯烷(Ki=81 nmol/L),表現了較強DPP-4抑制劑活性,見圖23。
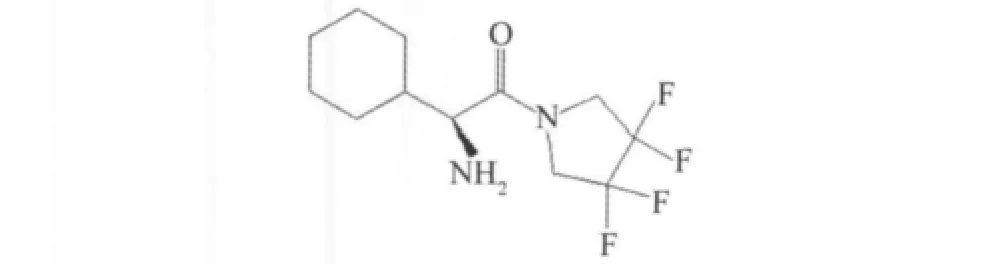
圖23 氟代吡咯氮環丁烷Fig.23 Fluorinated pyrrolidine and azetidine amides
4 結語
2006年首個DPP-4抑制劑成功應用于臨床后,DPP-4抑制劑就備受關注,目前已經有很多DPP-4抑制劑進入了臨床實驗階段。其中吡咯烷類DPP-4抑制劑研究的最為廣泛。通過晶體結構分析,研究了吡咯烷類DPP-4抑制劑的作用機制,通過構效關系研究,對吡咯烷類DPP-4抑制劑進行結構修飾,增加其穩定性的同時提高了DPP-4的抑制活性與選擇性。期望在上述基礎上,進一步研究,可以尋找到更高效,更安全的DPP-4抑制劑。
[1] Pratley R E,Salsali A.Inhibition of DPP-4:a new therapeutic approach for the treatment of type 2用diabetes[J].Curr Med Res Opin,2007,23(4):919-931.
[2] 倪衛惠.2型糖尿病的藥物治療進展[J].藥物生物技術,2010,17(2):185-189.
[3] 李祎亮,王菊仙,吳春玫,等.二肽基肽酶Ⅳ抑制劑的研究進展[J].中國新藥雜志,2008,17(20):1739-1745.
[4] Thornberry N A,Gallwitz B,.Mechanism of action of inhibitors of dipeptidyl peptidase-4(DPP-4)[J].Best Prac Res Clin Endocrinol Metabol,2009,23(4):479-486.
[5] Rasmussen H B,Branner S,Wiberg F C,et al.Crystal structure of human dipeptidyl peptidaseⅣ/CD26 in comp lex with a substrate analog[J].Nat Struct Biol,2003,10 (1):19-25.
[6] Wiedeman P E.DPPIV inhibition:promising therapy for the treatment of type 2 diabetes[J].Prog Med Chem,2007,45:63-109.
[7] Pan Y X,Ren A J,Zheng J,et al.Delayed cytoprotection induced by hypoxic preconditioning in cultured neonatal rat cardio-myocytes:role of GRP78[J].Life Sci,2007,81 (13):1042-1049.
[8] Hughes T E,Mone M D,Russell M E,et al.NVPDPP728(1-〔〔〔2-〔(5-cyanopyridine-2-yl)amino〕ethyl〕amino〕acetyl〕-2-cyano-(S)-pyrrolidine),a slow-binding inhibitor of dipeptidyl peptidaseⅣ[J].Biochemistry,1999,38(36):11597-11603.
[9] Ahrén B,Landin-Olsson M,Jansson P A,et al.Inhibition of dipeptidyl peptidase-4 reduces glycemia,sustains insulin levels,and reduces glucagon levels in type 2 diabetes[J].J Clin Endocrinol Metab,2004,89(5):2078-2084.
[10]Takasaki K,Iwase M,Nakajima T,et al.K579,a slow binding inhibitor of dipeptidyl peptidaseⅣ,is a long-acting hypoglycemic agent[J].Eur J Pharm Acol,2004,486(3):335-342.
[11]Tanaka Amino K,Matsumoto K,Hatakeyama Y,et al.ASP4000,a novel,selective,dipeptidyl peptidase 4 inhibitor with antihyperglycemic activity[J].Eur J Pharm Acol,2008,590(1-3):444-449.
[12]Cho T P,Gang L Z,Long Y F,et al.Synthesis and biological evaluation of bicyclo[3.3.0]octane derivatives as dipeptidyl peptidase4 inhibitors for the treatment of type 2 diabetes[J].Bioorg Med Chem Lett,2010,20(12):3521-3525.
[13]ChoT P,Long Y F,Gang L Z,et al.Synthesis and biological evaluation of azabicyclo[3.3.0]octane derivatives as dipeptidyl peptidase 4 inhibitors for the treatment of type 2 diabetes[J].Bioorg Med Chem Lett,2010,20(12):3565-3568.
[14]Fura A,Khanna A,Vyas V,et al.Pharmacokinetics of the dipeptidyl peptidase 4 inhibitor saxagliptin in rats,dogs,and monkeys and clinical projections[J].Drug Metab Dispos,2009,37(6):1164-1171.
[15]Zhao G,Taunk P C,Magnin D R,et al.Diprolyl nitriles as potent dipeptidyl peptidaseⅣinhibitors[J].Bioorg Med Chem Lett,2005,15(18):3992-3995.
[16]Gupta R,Walunj S S,Tokala R K,et al.Emerging drug candidates of dipeptidyl peptidaseⅣ(DPPⅣ)inhibitor class for the treatment of type 2 diabetes[J].Curr Drug Targets,2009,10(1):71-87.
[17]Kuhn B,Hennig M,Mattei P.Molecular recognition of ligands in dipeptidyl peptidaseⅣ[J].Curr Top Med Chem,2007,7(6):609-619.
[18]Fukushima H,Hiratate A,Takahashi M,et.al.Synthesis and structure-activity relationships of potent 4-fluoro-2-cyanopyrrolidine dipeptidyl peptidaseⅣ inhibitors[J].Bioorg Med Chem,2008,16(7):4093-4106.
[19]Pei Z H,Li X F,Longenecker K,et a l.Discovery,structure-activity relationship,and pharmacological evaluation of (5-substituted-pyrrolidinyl-2-carbonyl)-2-cyanopyrrolidines as potent dipeptidyl peptidaseⅣ inhibitors[J].J Med Chem,2006,49(12):3520-3535.
[20]Jinyou X,Lan W,Robert M,et al.Discovery of potent and selective phenylalanine based dipeptidyl peptidaseⅣinhibitors[J].Bioorg Med Chem Lett,2005,15:2533-2536.
[21]Pei Z,Li X,Longenecker K,et al.Discovery,structureactivity relationship,and pharmacological evaluation of(5-substituted-pyrrolidinyl-2-carbonyl)-2-cyanopyrrolidines as potent dipeptidyl peptidaseⅣinhibitors[J].J Med Chem,2006,49(12):3 520-3535.
[22]Parmee E R,He J,Mastracchio A,et al.4-Amino cyclohexylglycine analogues as potent dipeptidyl peptidaseⅣinhibitors[J].Bioorg Med Chem Lett,2004,14(1):43-46.
[23]Tsai T Y,Coumar M S,Hsu T,et al.Substituted pyrrolidine-2,4-dicarboxylic acid amides as potentdipeptidyl peptidaseⅣ inhibitors[J].Bioorg Med Chem Lett,2006,16 (12):3268-3272.
[24]Edmondson S D,Mastracchio A,Duffy J L,et.al.Discovery of potent and selective orally bioavailable b-substituted phenylalanine derived dipeptidyl peptidaseⅣ inhibitors[J].Bioorg Med Chem Lett,2005,15(12):3048-3052.
[25]Edmondson S D,Mastracchio A,Cox J M,et al.Aminopiperidine-fused imidazoles as dipeptidyl peptidase-Ⅳinhibitors[J].Bioorg Med Chem Lett,2009,19(15):4097-4101.
[26]Joseph D L,Kirk B A,Wang L,et al.4-Aminophenylalanine and 4-aminocyclohexylalanine derivatives as potent,selective,and orally bioavailable inhibitors of dipeptidyl peptidaseⅣ[J].Bioorg Med Chem Lett,2007,17(10):2879-2885.
[27]Kaelin D E,Smenton A L,Eiermann G J,et al.4-Arylcyclohexylalanine analogs as potent,selective,and orally active inhibitors of dipeptidyl peptidaseⅣ[J].Bioorg Med Chem Lett,2007,17(21):5806-5811.
[28]Caldwell C G,Chen P,He J,et al.Fluoropyrrolidine amides as dipeptidyl peptidaseⅣ inhibitors[J].Bioorg Med Chem Lett,2004,14(5):1265-1268.
[29]Xu J,Wei L,Mathvink R J,et.al.Discovery of potent,selective,and orally bioavailable oxadiazole-based dipeptidyl peptidaseⅣ inhibitors[J].Bioorg Med Chem Lett,2006,16(20):5373-5377.
[30]Hulin B,Cabral S,Lopaze M G,et al.New fluorinated pyrrolidine and azetidine amides as dipeptidyl peptidaseⅣinhibitors[J].Bioorg Med Chem Lett,2005,15(21):4770-4773.

