2×2熔錐光纖表面增強拉曼散射實驗
陳振宜, 陳 娜, 胡 玲, 王廷云, 龐拂飛, 劉 琳
(上海大學特種光纖與光接入網省部共建重點實驗室,上海200072)
拉曼光譜因其能夠提供豐富的分子振動信息,已逐漸成為一種物質分析中的有效檢測工具[1].近年來,拉曼光譜在水質污染檢測、奶制品的質量檢驗及有毒有害液體檢測等方面已發揮出越來越重要的作用,并廣泛應用于醫學、食品安全及環境監測等多個領域.利用貴金屬顆粒作為活性基底[2-4]的表面增強拉曼散射(SERS)技術,能夠通過局域電磁場增強等效應,顯著提高目標分子的拉曼散射強度,從而實現對低濃度樣品的檢測.為滿足長距離在線檢測等需求,科研人員又進一步著眼于光纖與SERS技術的結合[5-12],以實現高靈敏度的探測,并研究出了一系列基于錐形光纖[5-9]、D形光纖[10]和光子晶體光纖[11-12]的SERS傳感器.
本研究提出了一種基于2×2熔錐光纖的SERS結構,并自行設計搭建一套熔錐耦合式光纖SERS傳感實驗測量系統(見圖1).該系統利用熔融拉伸光纖錐區透射出的漸逝波作為激發源,結合具有表面增強拉曼散射的金屬溶膠顆粒活性基底,以增強自發拉曼散射強度,從而實現對低濃度待測分子的檢測.

圖1 熔錐光纖SERS傳感實驗測量系統示意圖Fig.1 Experimental test system diagram of fused fiber SERS sensor
1 表面活性基底的制備與表征
1.1 銀溶膠的制備
本研究采用改進的Meisel方法制備銀溶膠活性基底.具體過程如下:將90 mg硝酸銀溶于500 mL去離子水中,加熱至沸騰后,加入1%檸檬酸三鈉10 mL;繼續加熱60 min后,自然冷卻至室溫,可獲得黃綠色的不透明液體;放置一段時間后,由于重力作用,銀顆粒會向容器底部沉積,從而形成高濃度的銀溶膠.
對于銀溶膠溶液中的銀納米粒子,可以通過加入適量凝聚劑來誘導其形成聚集體,以達到活化溶膠和進一步增強拉曼散射強度的目的.本研究選用NaCl來促使銀納米粒子的聚集,由于銀溶膠溶液中的銀納米粒子表面帶有負電荷,彼此之間會相互排斥,因此,它們將獨立地游離在銀溶膠溶液之中.如果在銀溶膠溶液中加入一定量的NaCl,則一方面由于鈉離子帶有正電荷,另一方面,隨著鈉離子濃度的不斷升高,銀粒子所帶的負電荷量會不斷減少,因此,粒子間的排斥力會逐漸降低,從而引起銀納米粒子的聚集.
1.2 銀溶膠的表征
粒徑大小會直接影響納米顆粒的熔點、光學性能、表面活性等特性,本研究對制備的銀溶膠進行了表征.圖2是加入凝聚劑前后銀溶膠的吸收光譜對比.由圖可見,經過離心、超聲后的銀溶膠的吸收峰位于420 nm處.加入NaCl后,其吸收峰向長波長方向偏移,同時半高寬展寬,這表明銀顆粒粒徑分布較分散.
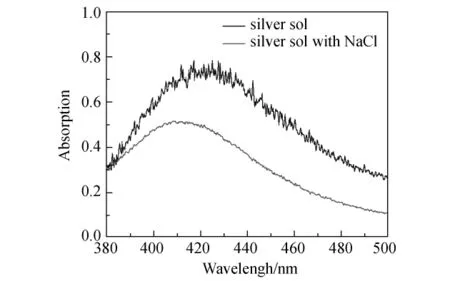
圖2 加入NaCl前后銀溶膠的吸收峰Fig.2 Absorption spectra of silver sols before and after the addition of NaCl
圖3是利用原子力顯微鏡測得的提純后銀溶膠的表面形貌.由圖可見,所制備的銀溶膠顆粒大體呈球狀,粒徑約為40~60 nm,且部分顆粒有團聚現象,團聚后粒徑在100 nm以上.但銀溶膠的吸收峰和表面形貌圖只能粗略地表征銀顆粒的平均大小和粒徑分布,為了表征其拉曼增強效果,本研究進一步測試了銀顆粒與R6G混合溶液的拉曼光譜.

圖3 提純后的銀溶膠表面形貌圖Fig.3 Atomic force microscope(AFM)image of silver sol after purified
1.3 不同濃度的R6G/銀溶膠混合溶液的SERS測試
將上述配制好的銀溶膠溶液分別取1 mL放入3個樣品試管中,再各滴入1 mL濃度分別為10-9,10-11,10-13mol/L的R6G溶液.使其充分混合后,放置24 h,以使其相互吸附、充分團聚.由此制得3種不同濃度的R6G/銀溶膠混合溶液的SERS測試樣品.圖4是實驗測得的不同濃度的R6G/銀溶膠混合溶液的歸一化拉曼光譜.

圖4 不同濃度下R6G/銀溶膠混合溶液的歸一化拉曼光譜Fig.4 Normalized Raman spectra of different concentration R6G solutions with silver sols
圖4中呈現出多個R6G的拉曼特征峰,其拉曼位移分別為 1 309,1 361,1 507,1 536,1 572,1 646 cm-1,但這些特征拉曼峰的強度大小不一,這與相對應分子振動鍵的伸縮強弱有關.除此之外,3種不同濃度的R6G/銀溶膠混合溶液的拉曼光譜疊加有一定強度的熒光背底,該熒光背底是由游離在混合溶液中的R6G分子所產生的.同時,隨著R6G濃度的降低,游離在溶液中的R6G自由分子相對減少,其熒光背底強度也隨之減弱,拉曼信號突顯.
1.4 銀納米粒子聚集對SERS測量的影響
在上述溶液中加入1 mL濃度為10-2mol/L的NaCl溶液后,其拉曼光譜如圖5所示.與未加入NaCl的R6G拉曼光譜相比,加入NaCl后的R6G拉曼光譜的熒光背底強度減弱,拉曼特征峰強度增強了5~6倍.上述現象源于Cl-使銀顆粒凝聚產生多個“熱點分子”,從而增強了拉曼散射強度.與此同時,由于可吸附R6G分子的銀顆粒增多,使得游離的R6G分子相對變少,從而使熒光背底強度進一步減弱,提高了拉曼信號的信噪比.因此,在修飾光纖活性表面之前,可將銀溶膠和NaCl混合使用.

圖5 加入NaCl前后R6G/銀溶膠混合溶液拉曼光譜Fig.5 Raman spectra of R6G solutions with silver sols before and after the addition of NaCl
2 2×2熔錐光纖SERS實驗
2.1 實驗裝置
實驗中,采用波長為532 nm的激光通過2×2熔錐型光纖耦合器的漸逝波激發R6G溶液樣品的拉曼光譜,測試系統如圖6所示.實際測量參數設置如下:曝光時間1 s,入口狹縫寬度10 μm,累加次數70次,1 200線光柵,設定波數范圍為 600~1 800 cm-1(所對應的波長范圍為 549.5~588.3 nm).此外,如圖7所示,所有待測樣品均置于暗室中,以避免外界雜散光對測量的影響.

圖6 拉曼實驗系統照片Fig.6 Photograph of Raman experimental system
2.2 熔錐型光纖耦合錐區直接激發R6G溶液的SERS光譜
實驗中使用的熔錐光纖的參數如下:熔融拉伸長度13.26 mm,拉伸振蕩周期數8個,耦合分光比30∶70,附加插入損耗0.1 dB.測試結果如圖8所示.由圖可見,測得的拉曼譜峰仍然位于1 309,1 360,1 509,1 572,1 596,1 647 cm-1等波數處,與R6G/銀溶膠混合溶液中的測試結果相吻合.由此可見,光纖本身的拉曼不會改變R6G的拉曼峰位.但是,從2×2熔錐光纖耦合錐區激發出的R6G拉曼光譜信噪比較差,拉曼譜峰很不明顯,這是由于此時熔錐光纖耦合錐區尚未涂覆固化上銀納米顆粒SERS活性基底,因此,從石英槽中R6G溶液分子所產生的拉曼散射光的強度較弱,信噪比較差.另外,隨著R6G溶液濃度的降低,其拉曼峰的強度也隨之減弱,從而更加不明顯.

圖7 由2×2熔錐光纖耦合器錐區激發拉曼實驗照片Fig.7 Photograph of Raman experiments excited with 2×2 fused fiber coupling zone
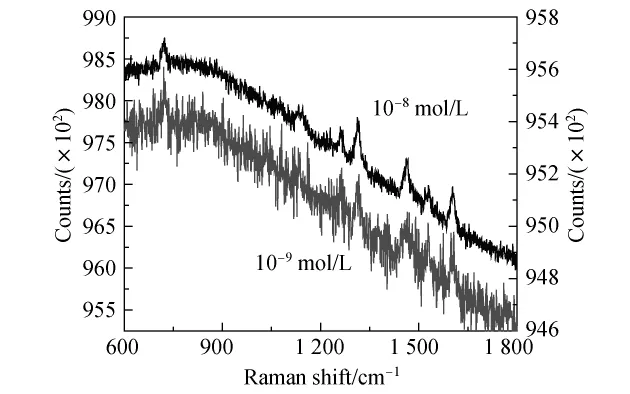
圖8 由2×2熔錐光纖耦合錐區激發的R6G拉曼光譜Fig.8 R6G Raman spectra exited by 2×2 fused fiber coupling zone
2.3 具有表面活性的2×2熔錐光纖耦合錐區激發R6G溶液的拉曼光譜
為獲得修飾光纖的功能化基團,先將2×2熔錐光纖浸入Piranhan溶液(體積比為3∶1的96%濃硫酸和30%過氧化氫的混合溶液)15 min進行羥基化,隨后用去離子水清洗,再浸入硅烷化混合溶液10 min,取出后用甲醇清洗表面;然后,在溫度為110℃的恒溫箱中加熱10 min;最后,浸入銀溶膠溶液中靜置21~24 h.
之后,本研究利用耦合錐區已固化上銀納米顆粒SERS活性基底的熔錐型光纖耦合器進行拉曼光譜測量,與此同時,也可驗證涂覆固化上銀納米顆粒活性基底的光纖耦合器是否具有拉曼增強效果.為此,在已固化上SERS活性基底的光纖耦合錐區滴加濃度為10-8mol/L的R6G溶液.在相同實驗條件下,測得的耦合錐區所激發的R6G溶液分子SERS光譜如圖9所示,其拉曼譜峰位于1 309,1 360,1 509,1 570,1 596,1 647 cm-1等波數處.

圖9 涂覆SERS的2×2熔錐光纖耦合錐區激發的R6G拉曼光譜Fig.9 R6G Raman spectra exited by 2×2 fused fiber coupling zone with SERS coating
由圖8可知,固化上SERS活性基底的光纖耦合錐區激發出的SERS光譜的熒光背景較強,這表明游離在溶液中的R6G分子數量較多,同時也表明固化在光纖耦合錐區表面的銀納米顆粒相對較少.比較圖8和圖9的拉曼光譜可知,圖9所示的拉曼光譜比圖8所示的拉曼光譜具有更好的信噪比,從而驗證了涂覆固化上銀納米顆粒活性基底的光纖熔融耦合錐區具有顯著的拉曼增強效應.
2.4 不同耦合周期條件下光纖錐區測得的SERS光譜
由于拉曼散射強度取決于漸逝波的強度,而熔錐光纖耦合錐區透射出的漸逝波強度隨熔融拉伸長度的變化而變化,為此,本研究在工作波長為1 310 nm的條件下,將不同熔融拉錐耦合周期的光纖耦合器作為傳感頭,用于對R6G溶液的SERS測試,測試結果如圖10所示.由圖可見,光纖熔融拉錐耦合周期越多,耦合越長,透射出的漸逝波也越強,從而由耦合錐區激發出的拉曼散射光也越強.
3 結束語
本研究提出一種基于光纖漸逝波原理,利用2×2熔錐光纖SERS對待測液體進行拉曼檢測的方法.利用熔融拉錐光纖錐區對外界介質敏感的特性,滴加折射率較大的待測溶液,以增強漸逝波,激發待測溶液分子的拉曼散射,從而實現對液體相分子組分的分析與檢測.實驗結果表明,對R6G溶液的最低檢測濃度可達10-8mol/L.

圖10 由不同耦合周期2×2熔錐光纖耦合錐區測得的SERS光譜Fig.10 SERS spectra exited by 2×2 fused fiber coupling zone with different couple period
[1] ZHOUZ H,WANGG Y,XUZ Z.Single-molecule detection in a liquid by surface-enhanced resonance Raman scattering[J].Appl Phys Lett,2006,88:034104.
[2] FLEISCHMANNM,HENDRAP J,MCQUILLANA J.Raman spectra of pyridine adsorbed at a silver electrode[J].Chem Phys Lett,1974,26:163-166.
[3] JEANMAIRED L,VAN DUYNER P.Surface Raman spectroelectrochemisty:part I.Heterocyclic,aromatic,and aliphatic amines adsorbed on the anodized silver electrode [J]. J Electroanal Chem Interfacial Electrochem,1977,84:1-20.
[4] LEEP C,MEISELD.Adsorption and surface-enhanced Raman of dyes on silver and gold sols[J].J Phys Chem,1982,86:3391-3395.
[5] STOKESD L, VO-DINH T. Developmentofan intergrated single-fiber SERS sensor[J].Sensors and Actuators B:Chemical,2000,69:28-36.
[6] GOLDENJ P,GEORGEG P,ANDERSONP.An evanescent wave biosensor:part 2.Fluorescence signal acquisition from tapered fiber optic probes[J].IEEE Trans Biomed,1994,41:585-591.
[7] LUCOTTIA,ZERBIG.Fiber-optic SERS sensor with optimized geometry[J].Sensors and Actuators B:Chemical,2007,121(2):356-364.
[8] VIETSC,HILLW.Comparison of fibre-optic SERS sensors with differently prepared tips[J].Sensors and Actuators B:Chemical,1998,51:92-99.
[9] POLWARTE,KEIRR L,DAVIDSONC M,et al.Novel SERS-active optical fibers prepared by the immobilization of silver colloidal particles[J].Appl Spectrosc,2000,54:522-527.
[10] ZHANGY,GUC.Surface-enhanced Raman scattering sensor based on D-shaped fiber[J].Appl Phys Lett,2005,87:123105.
[11] YANH,GUC.Hollow core photonic crystal fiber surface-enhanced Raman probe[J].Appl Phys Lett,2006,89:204101.
[12] ZHANGY,SHIC,GUC.Liquid core photonic crystal fiber sensor based on surface enhanced Raman scattering[J].Appl Phys Lett,2007,90:193504.

