銅(Ⅱ)摻雜Li3V2(PO4)3/C的結構與性能*
龍云飛,李媚琳,楊克迪,葛 利,呂小艷,文衍宣
(1.廣西大學化學化工學院,廣西南寧530004;2.廣西大學教務處)
研究與開發
銅(Ⅱ)摻雜Li3V2(PO4)3/C的結構與性能*
龍云飛1,李媚琳1,楊克迪1,葛 利1,呂小艷2,文衍宣1
(1.廣西大學化學化工學院,廣西南寧530004;2.廣西大學教務處)
用一步碳熱還原法制備了Li3V2-xCux(PO4)3/C(x=0.00、0.02、0.05、0.08、0.10、0.15)復合正極材料,并研究了摻雜對材料結構、微觀形貌、充放電性能的影響。結果表明摻雜少量銅(Ⅱ)不會影響材料Li3V2(PO4)3的基本結構,但會在Li3V2(PO4)3中形成電子缺陷,提高晶體內部原子的無序化程度,降低極化和電荷轉移電阻。從而改善材料的電化學性能。Li3V1.98Cu0.02(PO4)3/C的10 C放電容量比Li3V2(PO4)3/C提高了20 mA·h/g,具有較好的倍率性能。
鋰離子電池;正極材料;銅(Ⅱ)摻雜
聚陰離子化合物LiFePO4作為鋰離子電池正極材料具有優越的電化學性能,一直受到研究人員的廣泛關注[1]。目前,以聚陰離子磷酸鹽為基礎的LiMPO4(M=Fe、Co、Ni、Mn)[1-2]和Li3M2(PO4)3(M=Fe、V)[3-4]因PO替代了O,一方面可以提高結構的穩定性,另一方面可加快Li+的嵌入-脫嵌速度[5],從而具有較好的電化學、熱力學穩定性及較高的比容量。Li3V2(PO4)3因其高比容量、高工作電壓、快速的離子遷移速率、良好的熱穩定性、使用壽命長、自放電小等[5]優點,有望應用于電動汽車(EVs)和混合電動汽車(HEVs)領域。
NASCION型Li3V2(PO4)3的3D結構雖然穩定,但在此結構中金屬離子相隔較遠,故電子遷移率和導電率都偏低,這也是該材料實際應用中必須要解決的問題。同LiFePO4一樣,通過改性的方法可提高材料的導電能力從而優化Li3V2(PO4)3的電化學性能。根據J.Barker[5]的報道,在完全充電過程中,活性元素釩沒有完全變價,為了有效提高其利用率,有必要利用其他價格低廉的金屬元素以摻雜的形式取代釩的位置。目前金屬離子的摻雜研究主要集中在以Fe3+、Cr3+、Zr4+、Ti4+、Co2+、Mg2+、Al3+等[5-9]替代釩方面。摻雜少量的金屬離子可提高晶體的無序化程度,形成晶格缺陷,進而提高材料內部導電性,改善其電化學性能。筆者采用一步碳熱還原法合成制備了Cu2+摻雜的Li3V2(PO4)3/C,并用XRD、FT-IR、SEM、CV、EIS和恒電流充放電技術研究了Cu2+摻雜對材料結構、形貌和電化學性能的影響。
1 實驗部分
按 Li3V2-xCux(PO4)3/C(x=0.00、0.02、0.05、0.08、0.10、0.15)比例稱取 LiH2PO4(電池級)、V2O5(分析純)和Cu2(OH)2CO3(分析純),以蔗糖為還原劑。原料在無水乙醇中球磨分散5 h,前驅體烘干后,置于管式爐內N2氣氛下于800℃反應20 h,隨爐冷卻至室溫,得到最終產品,分別記為C0、C2、C5、C8、C10、C15。
采用D/Max 2500 V型X射線衍射儀進行XRD測試[Cu靶,Kα輻射,波長λ=0.154 06 nm,管電流為300 mA,管電壓為40 kV,掃描速率為8(°)/min,步長為0.02°,掃描范圍2θ為10~70°];利用Nexus 470型傅立葉紅外光譜儀進行紅外光譜測試分析;采用S-3400N型掃描電鏡觀察樣品形貌、結構、顆粒粒徑大小及分布情況。
將合成好的活性材料、導電劑乙炔黑、黏結劑聚偏四氟乙烯按質量比80∶10∶10置于N-甲基吡咯烷酮中混合均勻,沖片,制備正極材料。以金屬鋰片為負極,Celgard2400型聚丙烯為隔膜,1 mol/L、體積比為1∶1的LiFP6+EC/DEC(碳酸二乙酯)為電解液在SUPER 1220/750型氬氣手套箱中組裝成電池。采用CT2001A型LAND系列電池測試系統在3.0~4.2 V電壓下測量正極材料電化學性能。在PCI 4750電化學工作站上進行循環伏安測試(CV)和阻抗譜測試(EIS),CV測試采用兩電極體系,以含活性物質的正極作為研究電極,負極金屬鋰作為對電極和參比電極,掃描范圍為3.0~4.2 V,EIS測試條件為:交流電壓5 mV,頻率為10-3~105Hz。
2 結果與討論
2.1 XRD和FT-IR分析
圖1為Li3V2-xCux(PO4)3/C復合材料的XRD和FT-IR譜圖。由圖1a可知,Li3V2-xCux(PO4)3/C的晶體結構與摻雜量x的大小有關,當x<0.08時,所得樣品均具有單斜結構,無雜相產生;當x繼續增大時,有雜相產生,且其特征峰的強度隨摻雜量的增加而不斷加強。圖中沒有出現碳的衍射峰,可能的原因是殘余碳是不定形結構或是包覆在Li3V2(PO4)3顆粒的碳層太薄不易被檢測到[10]。
從圖1b可見,Li3V2-xCux(PO4)3/C樣品的紅外光譜變化并不明顯,與文獻[11]所報道的結果一致。在 1 150~1 250 cm-1處為 NASICON結構的磷酸鹽化合物;574.43、1 051.09 cm-1處分別為PO的不對稱伸縮振動 v3和彎曲振動 v4;1 199.83、 1 228.54 cm-1處為PO結構中O=P—O—的伸縮振動譜帶[12],由此可以認為所測樣品的結構均為類NASICON型;634.34 cm-1處為八面體[VO6]中V—O的伸縮振動v1;505.37、634.34、973.32 cm-1處為V3+的特征吸收峰。可知摻雜Cu2+后的樣品依然具有類NASICON結構,此外,FT-IR譜圖中也沒有發現碳的吸收峰。
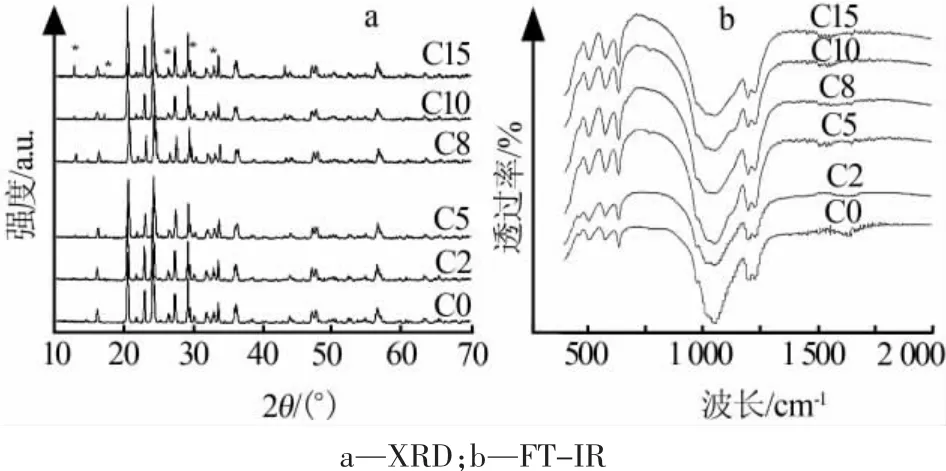
圖1 Li3V2-xCux(PO4)3/C的XRD和FT-IR譜圖
2.2 充放電性能分析

圖2 Li3V2-xCux(PO4)3/C的首次充放電曲線和循環性能
圖2a、b為Li3V2-xCux(PO4)3/C在充放電倍率為0.5 C的首次充放電曲線和循環曲線。從圖2a、b可見,隨著Cu2+摻雜量的增加,樣品的放電比容量先增加后降低,其中C2具有更好的電化學性能。原因是少量Cu2+摻雜占據V位,造成了Li3V2(PO4)3的電子缺陷,提高了晶體內部原子的無序化程度,使電化學性能有所改善。當Cu2+摻雜量繼續增大時,導致了雜質的生成(見圖1),故電化學性能差。C8的放電比容量一直增加直至循環達25次,結合XRD分析結果,可能的原因是該摻雜量下引入的雜質占據了晶體結構的間隙位置,使Li+擴散困難,活化時間延長。
圖2c為C0和C2復合材料在充放電倍率為10C時的循環性能曲線。由圖2c可見,C0和C2的首次放電比容量分別為72.6 mA·h/g和94.8 mA·h/g,循環50次后,容量衰減率分別為5.89%和5.51%。說明摻雜Cu2+的樣品可以有效減少Li3V2(PO4)3復合材料在高倍率下的極化現象,提高材料活性組分的利用率,加快電極反應速率,有效提高Li3V2(PO4)3材料的電化學性能。
2.3 SEM微觀形貌分析
圖3為樣品Li3V2(PO4)3和Li3V1.98Cu0.02(PO4)3/C的SEM照片。從圖3可以看出,兩種樣品顆粒形貌相差不大,粒徑大都在1μm以下。

圖3 Li3V2(PO4)3(a)和Li3V1.98Cu0.02(PO4)3/C(b)的SEM照片
2.4 CV和EIS分析
圖4是Li3V2(PO4)3和Li3V1.98Cu0.02(PO4)3/C在不同掃描速率(mV/s)下的循環伏安曲線。從圖4a可以看出,在較小掃描速率下,所有材料的循環伏安曲線存在3對氧化還原峰,第一、二對氧化還原峰分別對應著Li3V2(PO4)3、Li2.5V2(PO4)3、Li2.5V2(PO4)3、Li2V2(PO4)3的兩相轉變,第三對氧化還原峰對應Li2V2(PO4)3、LiV2(PO4)3兩相轉變,這與其小倍率下的充放電平臺對數及位置一致。但隨著掃描速率的增大,峰形發生變化,第一、二對氧化還原峰幾乎相重疊,這符合Li+在電極溶液界面的動力學過程[13]。掃描速率越大,峰值電流Ip也增大,氧化峰和還原峰分別向右、向左偏移,峰值電位差△V不斷增大,極化急劇增加。這主要是由于固相擴散控制,Li+擴散速率比較小,隨著掃描速率的增大,活性物質未能充分利用,極化也就越大。圖4b是摻雜了少量Cu2+的C2復合材料,由圖4b可見,掃描速率較小時,曲線中均呈現3對氧化還原峰,這與之前充放電曲線電壓平臺對數相吻合;同樣,隨著掃描速率的增加,氧化峰與還原峰均分別向正、負方向移動,但相對而言,二者離平衡電位較近,△V增幅不大,這說明少量的銅離子摻雜可以有效降低脫嵌鋰的極化程度,可逆性相對較好,這也是前文中摻雜銅離子后電化學性能會得到提高的原因。

圖4 Li3V2(PO4)3/C和Li3V1.98Cu0.02(PO4)3/C的CV曲線
圖5為Li3V2(PO4)3和Li3V1.98Cu0.02(PO4)3/C復合材料在25℃下循環1、30次后的電化學阻抗曲線和等效電路,直線部分是依據等效電路利用軟件擬合出來的結果。從圖5a可見,4種電極材料的電化學阻抗曲線均由中、高頻區的半圓弧和低頻區的直線構成,中、高頻區的半圓弧在實軸的截距為溶液電阻和接觸電阻Rel。一般來說,等效電路中電阻和電容并聯,在阻抗曲線中表現為圓弧形,故中、高頻的半圓弧可認為是中頻區的半圓弧和高頻區的半圓弧疊加而成,中頻區的半圓弧對應的是電極表面上的電荷轉移電阻Rct及相應的電容Cd,高頻區的半圓弧所對應的是Li+穿過界面的膜電阻Rs及相應的電容C;低頻區的直線反應了Li+在固相中的擴散,即Warburg阻抗,在等效電路圖中用Zw和Cint表示。Li+在電極中的各元件的擬合值結果見表1。


圖5 Li3V2(PO4)3/C和Li3V1.98Cu0.02(PO4)3/C的等效電路(a)和EIS曲線(b)
由圖5b及表1可以看出,4種樣品的溶液電阻和接觸電阻Rel與膜阻抗Rs阻抗值相對電荷轉移電阻Rct要小的多,在電極過程中,電荷轉移阻抗起主導作用,在阻抗圖上以半圓弧表現出來,半圓直徑越大,電荷轉移阻抗就越大。從圖5b可明顯看出,摻雜了少量離子的樣品的半圓弧均比沒有摻雜的樣品的要小。從表1以可看出,膜阻抗受循環影響小,可能的原因是電極表面的SEI膜在首次充放電過程中已經基本形成。與此相反,電荷轉移阻抗受循環影響顯著。Li3V2(PO4)3電極首次循環時,電荷轉移電阻為360 Ω,第三十次的數值為678.1 Ω;而Li3V1.98Cu0.02(PO4)3電極在第一次和三十次電荷轉移電阻分別為176.8 Ω和499.8 Ω,均高于未摻雜的。這也充分說明Cu2+摻雜能使充放電過程中電荷轉移更加容易,提高反應速率,達到了提高電子離子導電率的目的。

表1 阻抗參數擬合結果
3 結論
采用XRD、FT-IR、SEM、CV、EIS和恒流充放電測試研究了Cu2+摻雜對Li3V2-xCux(PO4)3/C材料的結構、形貌及電化學性能的影響,主要結論如下。
1)銅離子以固溶體的方式進入到晶格內部,Li3V2-xCux(PO4)3/C(x=0.02、0.05、0.08、0.10、0.15)與Li3V2(PO4)3/C均為單斜結構;Cu2+摻雜降低電荷轉移阻抗和電極極化減小,但對材料形貌影響很小。
2)Li3V2-xCux(PO4)3/C的放電比容量和循環性能隨Cu2+摻雜量的增加先增加然后下降。
3)與 Li3V2(PO4)3/C相比,Li3V1.98Cu0.02(PO4)3/C的10 C首次放電容量提高20 mA·h/g,具有較好的倍率性能和循環性能。
[1] 馮國彪,鄧宏.鋰離子電池正極材料磷酸鐵鋰研究進展[J].無機鹽工業,2011,43(3):14-17.
[2] 童孟良,何灝彥,劉絢艷.銅摻雜碳包覆磷酸鐵鋰的微波合成及性能研究[J].無機鹽工業,2011,43(6):27-29.
[3] Huang H,Yin S C,Kerr T,et al.Nanostructured composites:a high capacity,fast rate Li3V2(PO4)3/carbon cathode for rechargeable lithium batteries[J].Adv.Mater.,2002,14(21):1525-1528.
[4] Wang L,Zhang L C.,Lieberwirth I.,et al.A Li3V2(PO4)3/C thin film with high rate capability as a cathode material for lithium-ion batteries[J].Electrochem.Commun.,2010,12(1):52-55.
[5] Barker J,Gover R K B,Burns P.,et al.The effect of Al substitution on the electrochemical insertion properties of the lithium vanadium phosphate,Li3V2(PO4)3[J].J.Electrochem.Soc.,2007,154(4):A307-A313.
[6] Chen Y H,Zhao Y M,An X N.,et al.Preparation and electrochemical performance studies on Cr-doped Li3V2(PO4)3as cathode materials for lithium-ion batteries[J].Electrochimi Acta,2009,54(24):5844-5850.
[7] 劉素琴,李世彩,黃可龍,等.Ti4+離子摻雜對Li3V2(PO4)3晶體結構與性能的影響[J].物理化學學報,2007,23(4):537-542.
[8] Kuang Q,Zhao Y M,An X N.,et al.Synthesis and electrochemical properties of Co-doped Li3V2(PO4)3cathode materials for lithiumion batteries[J].Electrochimi Acta,2010,55(5):1575-1581.
[9] Huang J S,Yang L,Liu K Y.,et al.Synthesis and characterization of Li3V(2-2x/3)Mgx(PO4)3/C cathode material for lithium-ion batteries[J].J.Power Sources,2010,195(15):5013-5018.
[10] Ding N,Xu J,Yao Y X.,et al.Determination of the diffusion coefficient of lithium ions in nano-Si[J].Solid State Ionics,2009,180(2/3):222-225.
[11] 潘文成.NASICON結構鋰離子電池正極材料Na3V2(PO4)2F3和Li3V2(PO4)3的合成及表征[D].長春:吉林大學碩士論文,2010.
[12] Salah A A,Jozwiak P,Garbarczyk J,et al.Local structure and redox energies of lithium phosphates with olivine-and Nasicon-like structures[J].J.Power Sources,2005,140(2):370-375.
[13] 童匯.鋰離子電池正極材料磷酸鐵鋰的制備與性能研究[D].長沙:中南大學碩士論文,2007.
Structure and performance of Cu2+doped Li3V2(PO4)3/C
Long Yunfei1,Li Meilin1,Yang Kedi1,Ge Li1,Lü Xiaoyan2,Wen Yanxuan1
(1.School of Chemistry and Chemical Engineering,Guangxi University,Nanning 530004,China;2.Educational A dministration Department,Guangxi University)
Li3V2-xCux(PO4)3/C(x=0.00,0.02,0.05,0.08,0.10,0.15)composite cathode material had been synthesized by onestep carbothermal reduction technology,and effects of doping on crystalline structure,morphology,and charge-and-discharge performances were investigated.Results showed that a small amount of Cu2+did not affect the basic structure of Li3V2(PO4)3,but they formed electronic defects in Li3V2(PO4)3to improve the degree of the disorder of crystal lattice atoms,and reduced the polarization and charge transfer resistance.So the electrochemical properties of the material were improved.Compared to Li3V2(PO4)3/C,the discharge capacity of Li3V1.98Cu0.02(PO4)3/C increased by 20 mA·h/g at 10 C,exhibiting good rate capability.
lithium-ion battery;cathode materials;Cu2+doping
TQ131.11
:A
:1006-4990(2012)05-0011-04
2011-11-28
龍云飛(1964— ),男,高級工程師,主要研究方向為資源與材料化學工程,已公開發表論文20余篇。
國家自然科學基金(50474092);廣西自然科學基金(2011GXNSFA018015)。
聯 系 人:文衍宣
聯系方式:wenyanxuan@vip.163.com

