制備條件對胺改性納米ZnO光催化性能的影響
張秋紅,宋 華*,柳艷修,牟祖霖
(1. 東北石油大學化學化工學院,黑龍江 大慶 163318; 2. 大連理工大學,遼寧 大連 116023)
ZnO半導體材料因其無毒、成本低廉等優點,在光催化方面有廣泛應用[1-4]。但由于ZnO為寬禁帶(Eg=3.37 eV)半導體材料,在室溫下具有較大的激子束縛能(60 meV)[5],而且光生電子與空穴極易復合,使得光量子利用率較低,難以取得滿意的光催化效果。基于以上原因,可對ZnO進行改性來提高ZnO的光催化性能。目前的研究大多是通過摻雜金屬離子、非金屬[6-8],與其它物質復合[9]抑制光生電子與空穴的復合,從而提高光催化性能。
有機胺類化合物在多種材料的制備過程中都作為改性劑出現。吳建鋒[10]采用聚丙烯酰胺調節并控制了目標晶體的形貌。李梅[11]以辛胺為造孔劑,改變了納米ZnO的孔道分布。這些研究結果表明有機胺作為改性劑,可調節合成材料的微觀結構。但其對催化劑光催化性能的影響并沒有進行研究。本研究采用有機胺化合物對納米ZnO進行了改性,以紫外光照射下的甲基橙降解反應為研究對象,考察了有機胺的加入對ZnO光催化性能的影響。
1 試驗部分
1.1 試劑與儀器
乙酸鋅和無水乙醇,沈陽華東試劑廠;乙醇胺、二乙醇胺、乙二胺、三乙胺、檬酸三銨和草酸,哈爾濱市化工試劑廠。均為分析純。
自制光催化石英反應器,722-分光光度計。
1.2 催化劑的制備
采用溶膠-凝膠法制備了ZnO光催化劑。試驗如下:稱取6.651 5 g乙酸鋅及一定量的有機胺,溶于50 mL蒸餾水中,攪拌均勻。將草酸11.369 0 g,溶于50 mL無水乙醇中,將乙酸鋅溶液,逐滴加到草酸的無水乙醇溶液中,使其形成均勻的溶膠。用氨水調節pH值,80 ℃恒溫水浴加熱一定時間,然后分別用蒸餾水,無水乙醇洗滌,放入真空干燥箱中干燥,將干燥好的催化劑放入馬弗爐中焙燒。
1.3 試驗方法
向50 mL濃度為0.01 g/L甲基橙溶液中添加0.1 g制備的改性ZnO催化劑,先在無光照情況下攪拌吸附0.5 h,之后打開紫外光燈進行光照降解,降解得到的溶液利用分光光度計進行吸光度測定。根據標準曲線和式(1)求降解效率(η):
η=(A0-A)/A0×100%
(1)
式中A0為降解前甲基橙水溶液的吸光度值;A為降解后甲基橙水溶液的吸光度值。
1.4 納米ZnO光催化降解有機物的機理
當以光子能量等于或大于ZnO禁帶寬度能量(3.37 eV)的光照射下,處于價帶上的電子就會激發躍遷到導帶上,從而分別在價帶和導帶上產生高活性的光生空穴(h+)和光生電子(e-),此步驟稱為載流子的產生[12]:
ZnO+hv→e-+h++ ZnO
光生空穴具有氧化性,而光生電子則具有還原性。在一定條件下,分布在ZnO表面的h+則可將吸附在ZnO表面的OH-和H2O氧化成·OH,此步驟稱為載流子的俘獲:
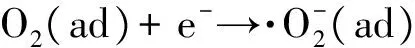
·OH作為強氧化劑[13],可進一步與大多數有機污染物、細菌、病毒及部分無機污染物作用,最終使其氧化分解為CO2和H2O及無機物等無害物質。此外,許多有機物的電位比半導體的價帶電位更負些,因此,有機物直接被h+氧化也是可行的。
而如果光生空穴(h+)和光生電子(e-)發生復合,就會將吸收的光能以熱的形式釋放,使光催化效率降低,稱為載流子復合:
e-+ h+→·△
改性劑的加入也可以改變催化劑微觀結構,抑制光生電子與空穴的復合,從而提高光催化性能。另外在ZnO前驅體的制備過程中加入表面改性劑,表面改性劑在前驅體的生成階段吸附在表面,形成空間阻擋層,使顆粒之間的團聚不易發生,也有利于提高其催化性能[14]。
2 結果與討論
2.1 改性劑的篩選
在n(改性劑)/n[Zn(Ac)2]為0.50,催化劑凝膠溫度為80 ℃,制備時間2 h,600 ℃煅燒3 h的條件下制備催化劑。采用了先無光照攪拌吸附0.5 h后紫外光照10 min的光催化反應降解(下同),考察了不同改性劑對于ZnO光催化性能的影響,結果如表1所示。
所添加的有機胺化合物對ZnO的光催化性能都有增強,甲基橙降解率有不同程度的增強。其中二乙醇胺的效果最好,光照10 min對甲基橙降解率為39.0%,比無添加劑的甲基橙降解率提高了14.1%。在以后的試驗中選定二乙醇胺為改性劑。
2.2 改性劑二乙醇胺量的影響
在催化劑凝膠溫度為80 ℃,凝膠老化時間2 h,600 ℃煅燒3.0 h的條件下制備催化劑。考察了二乙醇胺量對ZnO光催化性能的影響,結果如圖1所示。
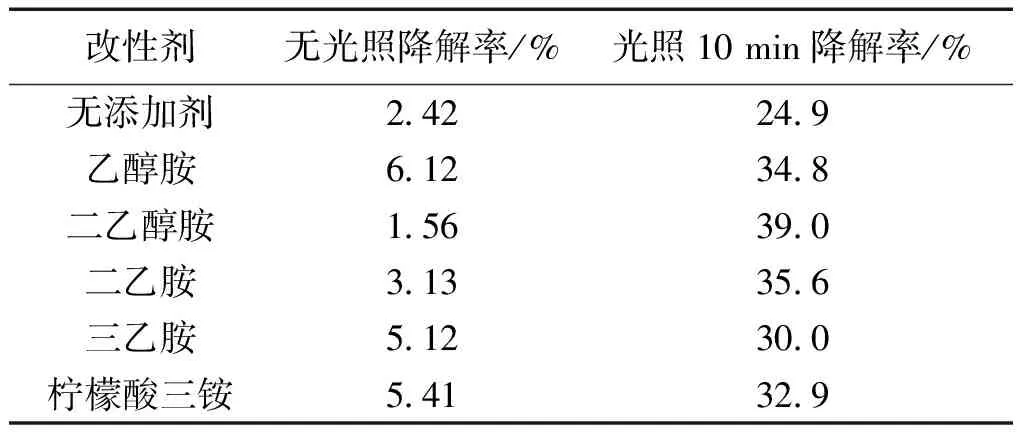
表1 不同改性劑對ZnO光催化性能的影響Table 1 Effect of different modifier on the photocatalytic performance of ZnO
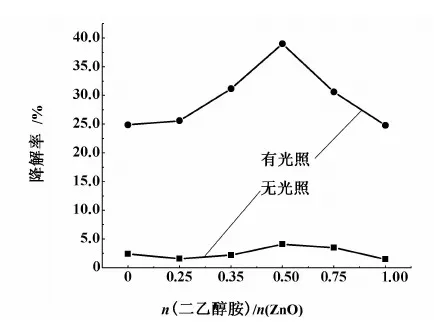
圖1 改性劑的量對光催化降解率的影響Fig.1 Effect of modifier amount on the degradation rate of methyl orange
由圖1可以看出,隨著改性劑用量的不斷增加,甲基橙降解率呈現先增大后下降的趨勢。當n(二乙醇胺)/n(ZnO)為0.50時,ZnO的光催化性能最強。沒有光照的情況下,改性劑用量與去除甲基橙能力規律也是相似的。根據半導體物理學理論,當改性劑濃度增大時,晶格常數增大,晶格膨脹增加,晶格缺陷增加,從而導致氧空位濃度增加,ZnO n型半導體特性變得更加明顯,在紫外光照射下,電子濃度相對增大,直接導致具有高氧化活性的·OH濃度的增加,使得ZnO光催化活性增強。而添加劑用量過大,可能影響了ZnO的形貌,使得其光催化性能下降,甲基橙降解率隨之下降。
2.3 凝膠溫度的影響
在n(二乙醇胺)/n(ZnO)為0.50,凝膠老化時間2 h,600 ℃煅燒3.0 h的條件下制備催化劑。考察了不同凝膠溫度對ZnO光催化性能的影響,結果如圖2所示。
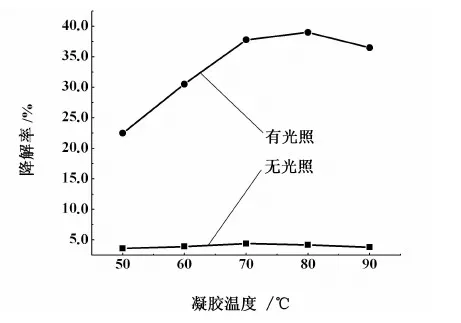
圖2 凝膠溫度對于光催化降解率的影響Fig.2 Effect of gel temperature on the degradation rate of methyl orange
由圖2可以看出,隨著凝膠溫度的逐漸升高,甲基橙的降解率逐漸升高,在80 ℃時達到最高點,隨后略微下降。在80 ℃時制備的ZnO光催化性能最強。這是因為:當溫度較低時,不利于水解的發生,水解速度比較慢,所以降解率較低。當水解反應溫度較高時,一方面水解反應速率較快,成膠的時間就會縮短。但溫度也不宜過高,以免溶劑揮發過快,降低了溶液的黏度,使粒子碰撞機率增大,易引起團聚而影響催化劑性能。
2.4 凝膠老化時間的影響
在n(二乙醇胺)/n(ZnO)為0.50,催化劑凝膠溫度80 ℃和600 ℃煅燒3.0 h的條件下制備催化劑。考察了不同凝膠老化時間對ZnO光催化性能的影響,試驗結果如圖3所示。
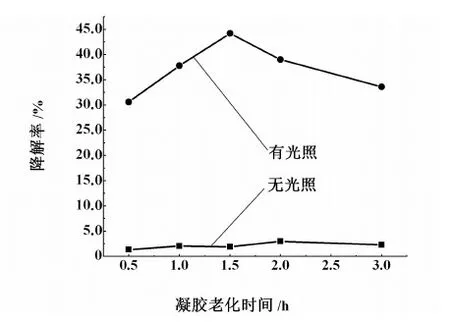
圖3 凝膠老化時間對于光催化降解率的影響Fig.3 Effect of gel time on the degradation rate of methyl orange
由圖3可以看出,隨著凝膠老化時間的加長,甲基橙降解率呈現一個先上升再下降的趨勢。在凝膠老化時間為1.5 h時,ZnO的光催化性能最強。這是因為時間過短,水解反應不完全,不利于后續充分轉變為ZnO的前驅體,而時間過長,又會引起團聚現象,影響催化劑的形貌,使得其光催化性能變差。
2.5 煅燒溫度的影響
在n(二乙醇胺)/n(ZnO)為0.50,催化劑凝膠溫度80 ℃,恒溫時間1.5 h,煅燒3.0 h的條件下制備催化劑。考察了不同煅燒溫度對ZnO光催化性能的影響,試驗結果如圖4所示。
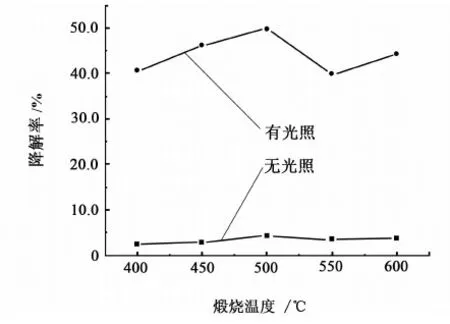
圖4 煅燒溫度對于光催化降解率的影響Fig.4 Effect of calcination temperature on the degradation rate of methyl orange
由圖4可以看出,隨著煅燒溫度的升高,甲基橙的降解率也跟著升高,在500 ℃達到最高點49.8%,與未改性的ZnO相比,甲基橙降解率提高了1倍。繼續升高煅燒溫度,ZnO光催化性能下降。無光照時的降解率與有光照時的規律類似。Ohtani等[15]提出光催化劑催化活性的高低與兩方面因素有關,即比表面的大小和結晶性的高低。較高的比表面,有利于催化劑被有機質的吸附;而較高的結晶性則可以降低光激發的電子與空穴復合的幾率。一方面焙燒溫度的升高提高了產物的結晶性,而另一方面焙燒溫度越高,晶粒長大,產物比表面越低。因此存在一個適宜的溫度使得光催化性能最強。
3 結論
采用溶膠-凝膠法制備了有機胺改性的ZnO光催化劑。在所考察的乙醇胺、二乙醇胺、二乙胺、三乙胺及檸檬酸胺中,二乙醇胺作為改性劑的效果最好。催化劑的制備條件,如改性劑的量、凝膠溫度及時間、煅燒溫度對ZnO的光催化性能均有一定的影響。適宜的催化劑制備條件是:二乙醇胺的摻雜量為n(二乙醇胺)/n(ZnO)為0.50,凝膠溫度為80 ℃,凝膠老化時間1.5 h,煅燒溫度500 ℃。
我們下一步工作將著眼于反應條件的優化及二乙醇胺對提高納米ZnO光催化性能機理方面的深入研究。
參考文獻:
[1]夏昌奎,黃劍鋒,曹麗云,等.微波水熱法制備ZnO納米晶[J].人工晶體學報,2008,37(4):833-838
[2]ZHOU Q.Preparation process of ZnO nanobelts self-assembling generated via polymer[J].Inor Chem Trans,2006,22:1 675-1 678
[3]BONAMALI P,MAHEAHWAR S.Enhanced photocatalytic activity of highly porous ZnO thin films prepared by sol-gel process [J].Materials Chemistry and Physics,2002,76:82 -87
[4]MIKI-YOSHIDA M,COLLINS-MARTINEZ V,AMERZAGA-MADRID P.Thin films of photocatalytic TiO2and ZnO deposited inside a tubing by spray pyrolysis [J].Thin Solid Films,2002,416:60-64
[5]李新華,徐家躍.半導體ZnO單晶生長的技術進展[J].功能材料,2005,36(5):652-654
[6]HANEDA D L.Synthesis of nitrogen-containing ZnO powders by spray pyrolysis and their visible light photocatalysis in gas-phase acetaldehyde decomposition[J].Journal of Photochemistry and PhotobiologyA:Chemistry,2003,155:171-178
[7]HANEDA D L.Photocatalysis of sprayed nitrogen containing Fe2O3-ZnO and WO3-ZnO composite powder using as-phase acetaldehyde decomposition[J].Journal of Photochemistry and Photobiology A: Chemistry, 2003, 160: 203-212
[8]ZHOU P,YU X,YANG L,etal.Simple air oxidation synthesis and optical propenies of S-doped ZnO microspheres[J].Materials Litters,2007,61:3 870-3 872
[9]SAKTHIVEL S, GEISSEN S U, BAHNEMANN D W,etal.Enhancement of photocatalytic activity by semiconductor heterojunctions:α-Fe2O3,WO3and CdS deposited on ZnO[J].Journal of Photobiology A:Chemistry,2002,148:283-293
[10]吳建鋒,張敏,徐曉虹,等.氨和胺在水熱法合成ZnO花簇微晶中的作用[J].武漢理工大學學報,2009,31(10):1-5
[11]李梅,劉秀琳,徐紅燕,等.水和辛胺對ZnO多孔納米塊體孔道結構的影響[J].化學學報,2005,63(16):1 510-1 514
[12]羅菊仙,趙中一. 半導體多相光催化氧化技術在環境保護中的應用研究進展[J].中國地質大學學報,2000,25(5):536-541
[13]劉俊渤,臧玉春,吳景貴,等.納米半導體材料的光催化機理與應用[J].長春工業大學學報:自然科學版,2004,25(3):19-21
[14]李玲.表面改性劑與納米技術[M].北京:化學工業出版社, 2004
[15]OHTANI B,OGAWA Y,NISHIMOTO S I.Photocatalytic activity of amorphousanatase mixture of titanium(IV) oxide particles suspended in aqueous solutions[J].Phys Chem B,1997,101:3 746-3 752

