尿激酶型纖溶酶原激活物及其Ⅰ型抑制劑mRNA在實驗性肌炎肌肉組織中的表達和意義
段 楓
多發性肌炎(polymyositis,PM)是一組以肌肉炎性改變為特征、常伴有肌纖維壞死變性的肌病。目前普遍認為,PM是遺傳易感個體由于環境因素觸發引起的免疫介導過程,其發病機制尚未明了。纖溶系統是非常重要的細胞外基質降解酶,通過降解細胞外基質成分(extracellul-ar matrix,ECM),在許多生理和病理過程中發揮重要作用,包括免疫和炎性反應。特別是uPA系統,參與了巨噬細胞的增殖、黏附和遷移,被認為在炎性反應過程中發揮了重要的作用。目前尚無uPA系統在PM、EAM發病機制中的作用方面的研究。本實驗應用RT–PCR技術研究uPA、PAI-1基因mRNA在EAM和正常豚鼠肌肉組織中的表達,旨在探討纖溶酶原激活系統在EAM發病中的作用,為其治療提供線索。
1 材料與方法
1.1 試劑 兔肌球蛋白5 mg/0.5 ml、完全弗氏佐劑(美國sigma公司)、百日咳毒素(北京天壇生物制品所)、Trizol試劑盒(美國GibcoBRL公司)、反轉錄試劑盒(美國Promega公司)。
1.2 實驗動物和分組 25只健康雌性英國短毛豚鼠(符合二級動物標準),重250~300 g,由解放軍軍醫進修學院實驗動物中心提供。隨機分為:(1)正常組10只,不進行任何處理;(2)EAM組15只,按以下程序進行EAM動物模型誘導。兩組觀察到第4周末后,處死動物,取血及肌肉標本,做進一步研究。
1.3 EAM 動物模型誘導 取0.5 ml,10 μg/ml的兔肌球蛋白與等量福氏完全佐劑(CFA)混合制成1 ml抗原乳劑,分別于第0、7、14、21天背部皮下注射1次,同時于第0、7天給予百日咳毒素2 μg腹腔注射。EAM動物模型成功標準:根據臨床評分、血肌酶變化及肌肉病理綜合判斷模型是否成功,模型成功的動物進行肌肉uPA和PAI-1基因mRNA表達的研究。
1.4 評價指標 每次免疫注射后觀察豚鼠體重、免疫注射局部皮膚、步態、毛色、活躍度。根據動物體重、姿勢、呼吸及活動情況,以Lennon LA法評分。標準:0分,無明顯的肌無力表現;1分,無力咬嚙或鳴叫;2分,休息時隆起體位,頭下垂,前肢屈曲,行走震顫;3分,嚴重肌無力,不鳴叫,體重減輕,甚至肌肉萎縮,呼吸困難,瀕于死亡。癥狀居中者分別評分為0.5、1.5、2.5 分。
1.5 標本制備 (1)動物免疫成功后第4周末水合氯醛麻醉動物后,活體取股四頭肌,分成兩部分,一部分樣本離體30 min內置于液氮冷凍,隨后轉移入-80℃冰箱中保存,備做rt-PCR,另一部分新鮮肌肉標本經異戊烷-液氮速凍,行5 μm冷凍切片,HE染色,光鏡下觀察;(2)心臟取血,測定血肌酶(CK)。
1.6 uPA、PAI-1基因mRNA表達的測定
1.6.1 總RNA的提取和定量 取凍存的標本各100 mg,分別加入1 ml Trizol溶液,提取總RNA,通過測定A260值和A280值分別計算RNA的濃度和純度,1180<A260/A280<2100。
1.6.2 反轉錄反應體系(20 μl) 水 5 μl,加入總RNA 1 μg,混勻,在PCR 儀上保溫,70 ℃ 10 min,4 ℃ 5 min,依次加入M-MLV 5 緩沖液4 μl,dNTP混合物10 mM,2 μl,重組RNA 酶抑制藥0.5 μl,M-MLV 反轉錄酶200 U,隨機引物0.5 μg,加水至終體積20 μl并混勻,在PCR儀上保溫,25℃ 10 min,37 ℃ 120 min,99 ℃ 5 min,4 ℃ 5 min,cDNA 模板-20℃保存備用。
PCR反應體系10PCR 緩沖液10 μl,dNTP10 mM 2 μl,cDNA 模板4 μl,上游引物1 μg,下游引物1 μg,TaqDNA 聚合酶2.5 u,加水至終體積100 μl,混勻。反應條件:uPA預變性94℃,5 min,變性94 ℃,0.5 min,退火53 ℃,0.5 ~1 min,延伸72 ℃ ,1 min,循環數27,終末延伸72℃,7 min。PAI-1:預變性94 ℃ 5 min,變性94 ℃,0.5 min,退火52℃,0.5 ~1 min,延伸72 ℃1 min,循環數28,終末延伸72℃,7min。各引物根據Genebank合成。
uPA上游引物5'CCTACAATGCTCACAGATCCGATGC3',下游引物 5'TCCACTGCCCCAGCTCACAA3',PAI-1上游引物 5'AGCCCTCACTTGCCTCACCC3',下游引物 5'CACTGATATTGAATCCCATAGCATCTT3'。
1.6.3 PCR產物相對定量 PCR產物經瓊脂糖凝膠電泳分離后,溴化乙啶染色,用凝膠掃描儀進行電泳條帶強度分析。以GAPDH作為內參照,將uPA/GAPDH,PAI-1/GAPDH的值作為各自表達水平的參數,在掃描儀上如未發現明顯條帶,則不按上述方法計算,作為陰性表達,參數計為0。
1.6.4 結果判定 有陽性條帶作為陽性表達,計算表達陽性率;表達強度以相對灰度值表示:目的基因相對表達水平=(目的基因灰度值-背景灰度值)/(看家基因灰度值一背景灰度值)。
1.7 統計學處理 所有數據使用SPSS11.0軟件進行統計分析。本研究測定數值用±s表示,兩樣本均數比較用成組t檢驗。兩變量間的相關分析用雙尾Pearson相關檢驗。P<0.05為差異有統計學意義。
2 結 果
2.1 EAM組發病情況 EAM組15只豚鼠免疫注射后兩周開始出現背部皮膚紅腫、破潰,2只豚鼠(5,14)免疫各周活動正常,體重增長,血肌酶正常,肌肉HE染色未見異常;13只動物免疫2周后出現活動減少,體重下降,其中2只豚鼠(7,11)分別于免疫第3、4周死亡,死亡后肌肉病理證實存在肌肉變性壞死及淋巴細胞浸潤,死亡原因考慮為肌炎導致的呼吸功能衰竭;其余11只豚鼠血肌酶明顯增高,肌肉HE染色可見炎性改變;15只動物中有13只物模型成功,11只存活,模型成功率73.3%。正常組豚鼠各周活動正常,體重增長,血CPK值小于696.09 U/L。EAM組豚鼠的LennonLA評分變化及EAM組血清CK值見表1。EAM組的LennonLA評分與血CK顯著正相關(表1)。血CK是反應EAM急性期疾病嚴重程度的客觀指標。
2.2 肌肉病理形態 正常組及EAM組5、14號豚鼠肌肉HE染色(圖1A),EAM組13只臨床發病的豚鼠(2只死亡)肌肉HE染色結果顯示,肌纖維大小不等、變性、壞死、萎縮,肌內衣、肌束衣和間質小血管周圍見淋巴細胞浸潤(圖1B、C、D)。
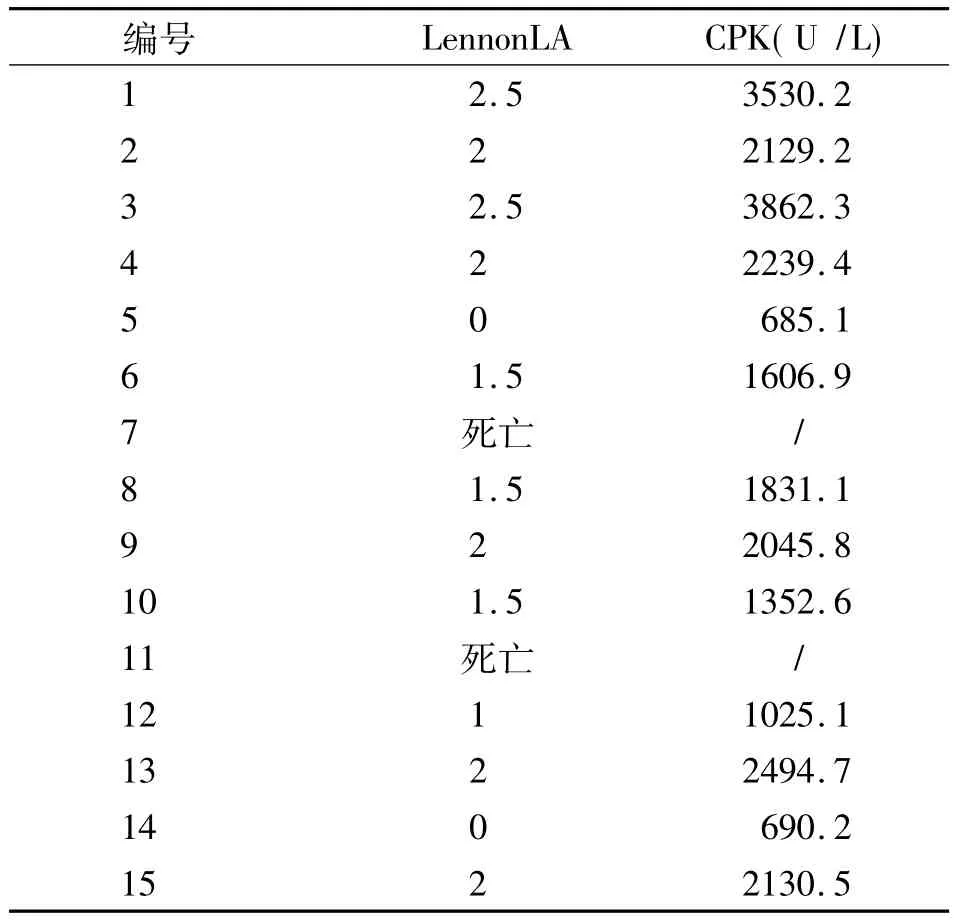
表1 EAM組L ennonLA評分及血CPK值
2.3 正常組和EAM肌肉上uPA、PAI-1基因mRNA的表達 本研究發現,正常組肌肉uPA 1.259±0.064、PAI-1基因mRNA表達水平1.13±0.080,EAM組肌肉uPA42.325±0.041、PAI-1基因mRNA表達水平2.055±0.037,EAM組肌肉uPA、PAI-1基因mRNA表達水平高于正常組(圖2),差異有統計學意義(P<0.01)。同時為了進一步明確EAM發病機制中是否存在uPA/PAI-1失衡的問題,將正常組與EAM組uPA與PAI-1基因mRNA表達的比值(uPA/PAI-1)進行了統計分析,正常組uPA/PAI-1比值平均為1.10±0.023,EAM組uPA/PAI-1比值平均為1.114±0.017,兩組之間無統計學差異(P>0.05)。
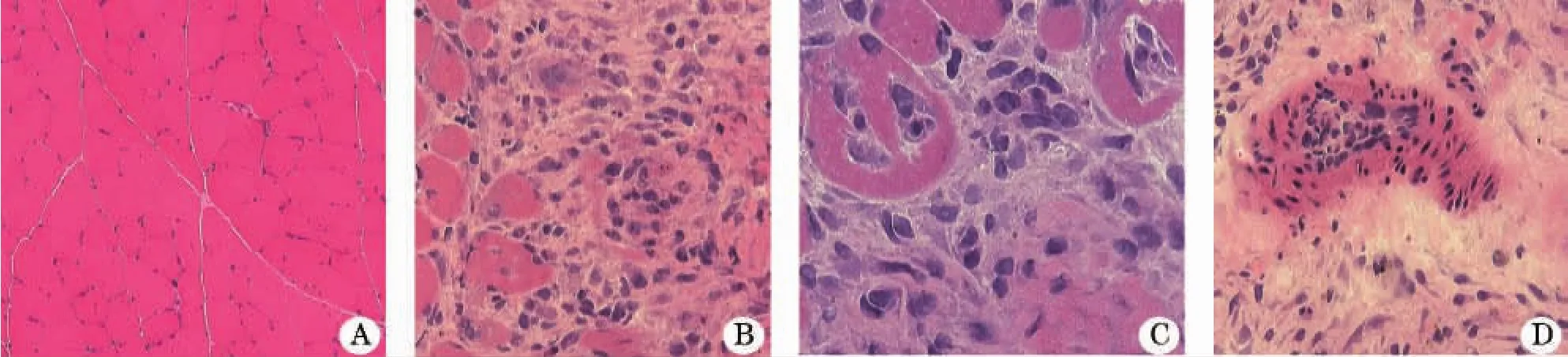
圖1 正常組及EAM組豚鼠肌肉HE染色
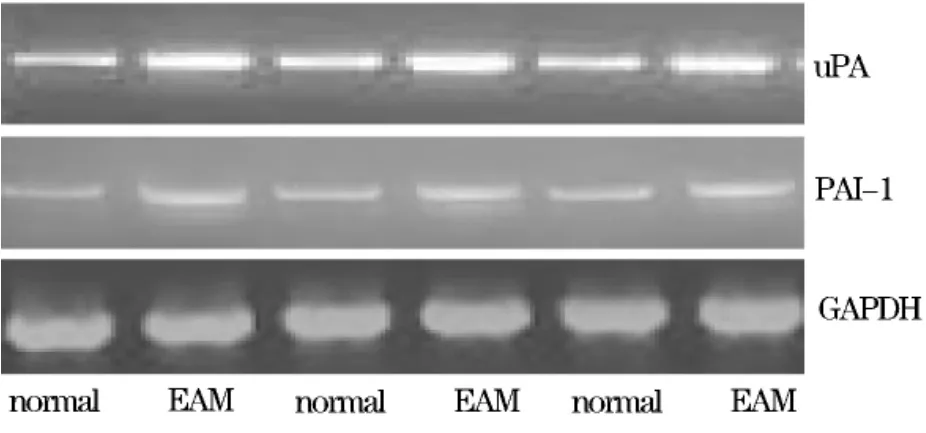
圖2 正常組和EAM肌肉上uPA、PAI-1基因mRNA的表達
3 討 論
uPA是一種絲氨酸蛋白酶,基因定位于10q24,分子量為54ku,以一種滅活的前體(pro-uPA)的形式分泌。在生理條件下,uPA主要來自于腎小管上皮細胞、免疫細胞、內皮細胞等,研究證實uPA也在多種哺乳動物的肌纖維上表達。uPA可以與細胞表面特異性的細胞膜受體(uPAR)結合[1],加速uPA前體在細胞表面轉化成為激活的uPA,使纖溶酶原激活,uPA和纖溶酶還可以通過激活MMP或者通過直接蛋白水解作用,促進細胞外基質及基底膜中多種成分的降解參與炎性反應[1,2]。此外uPA和uPAR還參與了炎性細胞的分化增殖、遷移和黏附[3-5]。由此可見,uPA系統在炎性過程中發揮著重要的作用。有研究發現在肌肉損傷的模型中,uPA基因敲除小鼠肌肉損傷部位沒有巨噬細胞的聚集[6,7]。uPA參與了巨噬細胞的趨化性。此外在肌肉損傷模型中還發現內源性產生的uPA可以增加單核細胞產生TNF-α[8],這說明吞噬細胞來源的蛋白酶是導致炎性前(致炎信號)產生的機制,uPA可能在肌肉炎性反應中發揮了同樣的作用。本實驗發現uPA基因mRNA在EAM組肌肉中的表達水平高于正常組,提示uPA參與了EAM的發病。EAM肌肉組織uPA轉錄水平的高表達,可能與入侵肌肉局部的炎性細胞,以及內源性單核巨噬細胞的產生有關。一方面uPA通過直接或間接的ECM降解作用,破壞血管基底膜,促進T細胞侵入肌組織,同時進一步降解基底膜,使肌纖維完整性遭到破壞,出現肌纖維壞死和吞噬現象。另外,uPA可能通過參與肌肉炎性部位巨噬細胞的趨化、炎性前信號的產生、炎性細胞的激活分化和增殖促進了EAM的發生。
纖溶酶原激活物抑制劑(PAI)是纖溶系統的重要組成成分,纖溶酶原活化系統(PAs)的主要的特異性抑制物。關于PAI在EAM中的作用可能具有雙重性。一方面,PAI-1是uPA活性以及纖溶酶產生的主要調節劑,PAI-1與uPA以1∶1比例形成復合物滅活uPA的活性,從而對纖溶系統、及纖溶酶原激活劑參與的細胞外基質降解和信號傳導起到重要調節作用,通過調節血管外蛋白水解抑制炎性過程。研究發現PAI-1基因敲出小鼠,肌肉損傷部位的巨噬細胞聚集增加[9],進一步證實了這一點。另一方面,PAI-1可以與血漿和細胞外基質的玻璃體結合蛋白、纖溶酶原激活劑及/受體(Upa/Upar)復合物結合,參與炎性細胞的黏附和脫離,從而促進炎性的發生[10]。PAI-1還能與炎性及細胞因子如腫瘤壞死因子-α、轉化生長因子β、白細胞介素-1、白細胞介素-6等相互作用,使炎性因子滲出增加促進炎性的發生、發展[11]。本實驗發現在EAM組肌肉中PAI-1基因mRNA的表達高于正常組,有統計學差異,提示PAI-1參與了EAM的發病機制。PAI-1在轉錄水平上的高表達,一方面可能是炎性過程中uPA表達增加后的一個自身調節,從而保證uPA系統的穩定,保證細胞內外環境的穩定;但更重要的是它可能促進了炎性的發生。筆者對正常組和EAM組之間uPA與PAI-1基因mRNA表達的參數比值進行了統計分析,兩者沒有差異。這說明uPA、PAI-1基因mRNA表達的增加在EAM組沒有差異,這提示uPA/PAI-1系統的失衡并不是EAM發病的主要機制之一,如前所述,uPA/uPAR/PAI-1復合物的形成,參與炎性細胞的黏附和脫離,促進了炎性反應的發生,因此筆者推測在EAM發病機制中uPA/uPAR/PAI-1復合物的形成可能發揮了作用。
[1]Castellino F J,Ploplis V A.Structure and function of the plasminogen/plasmin system[J].Thromb Haemost,2005,93(4):647-654.
[2]張慶成,趙 杰,汪承煒,等.CD 40L、MMPs和 a-GMP-140在急性冠脈綜合征致病中的作用[J].武警醫學,2011,22(3):220-222.
[3]Luikart S M,Masri D,Wahl,et al.Urokinase is required for the formation of mactinin,an alpha-actinin fragment that promotes monocyte/macrophage maturation[J].Biochim Biophys Acta,2002,1591(1-3):99-107.
[4]Navaneetha K Rao,Guo Ping Shi,Harold A.Urokinase receptor is a multifunctional protein:influence of receptor occupancy on macrophage gene expression[J].J Clin Invest,1995,96(1):465-474.
[5]Paulis A,Montuori N,Prevete N,et al.Urokinase induces basophil chemotaxis through a urokinase receptor epitope that is an endogenous ligand for formyl peptide receptor-like 1 and-like 2[J].J Immunol,2004,173(9):5739-5748.
[6]Suelves M,Vidal B,Serrano A L,et al.uPA deficiency exacerbates muscular dystrophy in MDX mice[J].J Cell Biol,2007,178(6):1039-1051.
[7]Lluis F J,Roma M,Suelves,et al.Urokinase dependent plasminogen activation is required for efficient skeletal muscle regeneration in vivo[J].Blood,2001,97(6):1703-1711.
[8]Lòpez Alemany R,Suelve M,Mu?oz Cánoves P.Plasmin gener-ation dependent on α-enolase-type plasminogen receptor is required for myogenesis[J].Thromb Haemost,2003,90(4):724-733.
[9]Koh T J,Bryer S C,Pucci A M,et al.Mice deficient in plasminogen activator inhibitor-1 have improved skeletal muscle regeneration[J].Am J Physiol Cell Physiol,2005,289(1):217– 223.
[10]Czekay R P,Loskutoff D J.Plasminogen activator inhibitors regulate cell adhesion through a uPAR-dependent mechanism[J].J Cell Physiol,2009,220(3):655-663.
[11]Zorio E,Gilabert-Estellés J,Espa?a F,et al.Fibrinolysis:the key to new pathogenetic mechanisms[J].Curr Med Chem,2008,15(9):923-929.

