吸煙合并慢性牙周炎患者齦溝液NO含量檢測
高朋杰 王瑋 解用江 王洪霞 王麗杰
一氧化氮(NO)是機體內重要的信使分子和效應分子,參與細胞信息的傳遞、介導細胞免疫和炎癥毒性作用[1]。慢性牙周炎的病理改變是牙槽骨的破壞和吸收[2]。其發生機制主要是長期慢性炎癥導致的血管調節功能失控,使局部血流動力學發生改變,導致局部牙槽骨組織血流量下降,造成局部骨代謝的失調[3]。而NO在此過程中發揮重要作用。吸煙是牙周炎的高危因素,可通過多種途徑對牙周組織產生影響[4]。在此檢測吸煙合并慢性牙周炎患者基礎治療前后齦溝液內NO含量的改變,結合牙周炎臨床癥狀的改善來探討吸煙與牙周炎的關系。
1 材料與方法
1.1 主要試劑與材料 Whatman3#濾紙條(2mm 10mm,3 m);NO免疫熒光試劑盒(biovision,美國);BP211 d萬分之一電子天平(德國Sartorius公司);D-37520離心機(美國Thermo公司);時間分辨熒光讀數儀(Wallac Victor2,美國)。
1.2 實驗方法
1.2.1 病例選擇 在大慶油田總醫院口腔內科門診選取20位以《牙周病學》(3版人民出版社)標準確診患有廣泛性慢性牙周炎患者,全口牙中有附著喪失和骨吸收。所有患者均無其他全身代謝性疾病,近3個月內沒有服用過任何抗生素或激素類藥物,半年內未接受過牙周治療。婦女無妊娠。將20例患者隨機分為吸煙組和不吸煙組。吸煙標準為每天吸煙10支以上或吸煙時間三年以上。所有患者均知情同意。
1.2.2 基礎治療前后牙周臨床指標的檢測 使用牙周探針對各組牙周炎進行牙周檢查,每名患者選取雙側上下前后牙各一顆,記錄牙周探診深度(PD)、附著喪失(AL),探診出血(BOP)等。所有患者第一次就診先進行口腔衛生宣教后施以必要咬合調整、齦上潔治術,牙面進行拋光。一周后復診進行齦下刮治術、根面平整術。所有臨床檢查均由同一位醫生完成。治療過程中避免外源性高濃度亞硝酸鹽的給入。吸煙者始終保持吸煙習慣。牙周基礎治療后4周復診,再次檢查上述 PD、AL、BOP 等指標。
1.2.3 齦溝液樣本的采集 在基礎治療前每名患者仍選取上述雙側上下前后牙,清水漱口,吹干牙面,棉卷隔濕,用4條Whatman3#濾紙條分別插入取樣每牙的頰腭(舌側)、近中、遠中牙周袋內,留置60 s后取出。將每顆牙的4條濾紙條作為1個樣本,密封在液氮中保存待測試。牙周基礎治療后4周按同樣方法采集齦溝液樣品保存。
1.2.4 NO含量的檢測 將裝濾紙條的冷凍液從液氮中取出放入4℃冰箱中解凍,在每一個試管中加入300 μl三蒸水將4條濾紙條完全浸沒,3000r/min 10min離心后將濾紙條丟去,保留上清液于4℃冰箱。采用NO免疫熒光檢測試劑盒,按說明書進行操作,按所給公式換算出每個樣本中硝酸鹽和亞硝酸鹽濃度,得出NO的濃度。
1.3 統計學方法 采用SPSS 11.5統計軟件包進行統計分析,實驗組與對照組計量資料的差異采用單因素方差分析或兩獨立樣本t檢驗。基礎治療前后臨床指標的差異采用重復測量數據的方差分析,P<0.05表示差異有統計學意義。齦溝液NO含量計量資料差異采取兩樣本比較的t檢驗,檢驗標準a=0.01.
2 結果
2.1 治療前,吸煙組與不吸煙組的各項牙周臨床指標差異無統計學意義。治療后,不吸煙組的下降幅度明顯高于吸煙組。
表1 吸煙與不吸煙組基礎治療前后牙周指標比較()
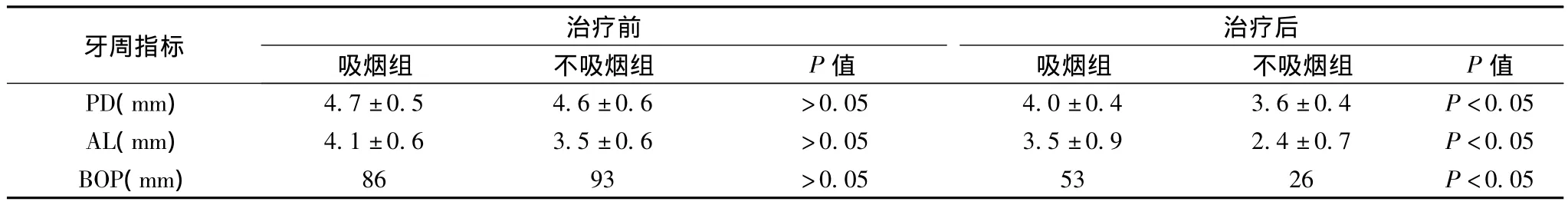
表1 吸煙與不吸煙組基礎治療前后牙周指標比較()
牙周指標治療后吸煙組 不吸煙組 P值 吸煙組 不吸煙組 P值治療前<0.05 AL(mm) 4.1±0.6 3.5±0.6 >0.05 3.5±0.9 2.4±0.7 P<0.05 BOP(mm) 86 93 >0.05 53 26 P<0.05 PD(mm) 4.7±0.5 4.6±0.6 >0.05 4.0±0.4 3.6±0.4 P
2.2 牙周基礎治療前后齦溝液NO含量比較。
表2 吸煙組和不吸煙組基礎治療前后NO含量比較(μmol/L,)

表2 吸煙組和不吸煙組基礎治療前后NO含量比較(μmol/L,)
測量時間NO吸煙組 不吸煙組治療前<0.017.21±2.13 5.33±1.28治療后 5.01±0.6 1.37±0.21 P值 P<0.01 P
3 討論
正常人口腔內產生的NO是由L-精氨酸在一氧化氮合酶的催化下生成L-瓜氨酸時釋放的。一些研究已證實NO對維持口腔內正常菌群的平衡以及抗微生物感染有直接影響。同時,適量的NO對牙周組織的健康及功能的正常發揮起著重要作用[5]。在牙周炎癥狀態下,血管內皮素的含量顯著增高,NO的水平相應增高來對抗血管內皮素所造成的牙周組織小血管及微血管的強烈收縮,在此防御反應過程中,過量產生的NO使擴血管因子與縮血管因子之間的關系失衡,通過活化多重級聯信號引發炎癥級聯瀑布反應,促進炎癥發展[6]。NO的大量生成也能導致巨噬細胞、中性粒細胞等的自身凋亡,間接造成牙周組織的損傷。以前的動物實驗研究也證實了牙周組織中的NO確實參與了牙周病的整個病理過程,在牙周炎的發生發展過程中起到重要作用[7]。大量流行病學調查資料顯示[8,9],吸煙可通過多種途徑對牙周產生影響:吸煙可以使牙周組織缺氧;可以引起骨質疏松;降低免疫系統功能;還可使口腔內處于缺氧狀態,牙周氧化還原電勢下降,有利于厭氧菌生長[10]。
齦溝液來自并通過牙周組織,疾病時其中成分的變化可較準確反應牙周組織的狀態。本研究利用特異性強、敏感性高、速度快的免疫熒光法檢測牙周炎基礎治療前后齦溝液NO的含量并進行比較,同時觀察牙周臨床指標的變化情況,得出結論:吸煙與不吸煙患者基礎治療后齦溝液NO含量均下降,但吸煙者下降幅度較小,臨床指標改善程度較差。提示基礎治療是牙周炎的常規治療,對于吸煙合并慢性牙周炎的患者單純采取基礎治療并不能根本解決炎癥問題,戒除吸煙對慢性牙周炎的治療有積極作用。同時提示我們直接取齦溝液樣本測定NO含量而不是采用收集靜脈血的方式測量其NO含量更容易被患者接受,對牙周炎活動期的診斷以及預防疾病的發展可能是一項簡單易行的措施。
[1]李波.NO與牙周病周期性發病關系的研究.現代生物醫學進展,2006,6(6):27-28.
[2]孟煥新.牙周病學.第3版.北京:人民衛生出版社,2008.
[3]陳世璋.牙周炎病人牙齦組織中ET和NO改變與局部骨吸收的研究.中國骨質疏松雜志,1999,5(#):40-43.
[4]孫曉強.吸煙對牙周炎病人牙齦組織中成纖維細胞及膠原纖維的影響.北京口腔醫學雜志,2006,14(1):27-29.
[5]龔斌.一氧化氮在牙周組織中的生物學作用.口腔材料器械雜志,2002,11(2):80-81.
[6]Bian K,Ke Y,Yoshinoti K,et al.Proteomic modification by nitric oxide.J Pharmacol Sci,2006,101(4):271-279.
[7]Lohinai Z,Stachlewitz R,Viragl,et al.Evidence for reactive nitrogen species formation in the gingivomucosal tissue.Journal Dental Research.2001,80(2):470-475.
[8]Kluft C,Maat MPM.Sensitive bakers of inflammation make it possible to study the chronic process:the rise of interest in low levels of C-reactive ptotein.Vasc Pharmacal,2002,39(3):99-104.
[9]Ghezzi F,Franchi M,Raia L,et al.Elevated amniatic fluid C-reactive protein at the time of genetic amniacentesis is a marker for pretem delivery.Am J Obstet Gynecal,2002,2:268-273.
[10]王敏.吸煙與非吸煙著慢性牙周炎齦下福賽類桿菌的檢驗.臨床口腔醫學雜志,2006,22(8):478-480.

