BUT-6010的抗腫瘤活性實驗研究
王燕萍 張 寧 沈曉燕 陳海波 胡云雁 譚芬來
浙江貝達藥業北京新藥研發中心,北京 100176
鉑類藥物是臨床治療腫瘤應用較多的抗癌藥物之一,20世紀60年代順鉑(Cisplatin)抗癌作用的發現拉開了鉑類抗腫瘤藥物研究的序幕。隨著人們對金屬配合物的結構和藥理作用認識的進一步深入,新的高效、低毒、具有抗癌活性的鉑類配合物不斷被研制出來[1-2],特別是順鉑和卡鉑(Carboplatin)是目前臨床上使用最廣的抗癌藥物之一,是治療許多腫瘤的首選藥物。但是目前臨床使用的鉑類抗癌藥對腫瘤細胞無特異選擇,導致用藥過程中出現副作用如神經毒性、腎毒性、耳毒性、惡心嘔吐等,且容易產生耐藥性,這些因素限制了它們在臨床上更廣泛的應用[2-5]。因此,尋找和設計合成出對腫瘤細胞有選擇殺傷作用、使用安全,而不易產生耐藥性的新一代鉑類抗癌藥已顯得十分迫切。BUT-6010是以順鉑、卡鉑的結構為基礎,按照經典的構效關系設計和合成的新鉑類配合物,旨在通過改變載體或離子基團來改善鉑類抗癌藥的藥代動力學特性,以提高療效或降低毒副作用。本文旨在研究BUT-6010的抗腫瘤活性。
1 材料與方法
1.1 細胞系和動物
HepG2、Hep3B、PLC/PRF/5、786-0、Caki-1、MDA-MB-231、HCT-116、NCI-H460、SK-OV-3 共 9 種人癌細胞株,購于中國醫學科學院干細胞醫學中心;健康ICR小鼠43只,由北京華阜康生物科技股份有限公司提供,許可證號:SCXK(京)2009-0004。
1.2 藥物
BUT-6010,由浙江貝達藥業提供,批號:20101227;順鉑,購于南京制藥廠有限公司,批號:20081202。
1.3 試劑和儀器
1.4 細胞培養
HepG2細胞和PLC/PRF/5細胞用DMEM培養基,Hep3B細胞用MEM培養基,786-0細胞株和NCI-H460細胞株用RPMI1640培養基,Caki-1細胞株、HCT-116細胞株和SKOV-3細胞株用McCoy's5A培養基,MDA-MB-231細胞株用L15培養基。細胞均在含10%FBS的培養液中37℃,5%CO2,95%濕度條件下培養。
1.5 試驗方法
1.5.1 體外對腫瘤細胞生長的抑制作用 腫瘤細胞株分為BUT-6010組、順鉑陽性對照組、細胞對照組、培養基空白對照組。BUT-6010和順鉑稀釋成系列濃度100.000 0、31.600 0、10.000 0、3.160 0、1.000 0、0.316 0、0.100 0、0.031 6 μmol/L。取對數生長期細胞,細胞計數器計數,臺盼藍拒染法測定活細胞大于 95%。96 孔板中加 90 μL 細胞懸液,5×103cells/well,各濃度設3個復孔。培養24 h后每孔加入10 μL相應藥物溶液。培養48 h后,每孔加20 μL MTS/PMS混合液,總反應體積 120 μL。 繼續 37°C、5%CO2培養 4 h,490 nm 處讀值[6]。
1.5.2 體內對S180瘤重的影響 選擇S180瘤源動物,脫頸處死,置于75%酒精中消毒2 min,剪開并剝去腹部皮膚,用空針吸取腹水10 mL,放入無菌離心管中離心(1 000 r/min),去上清液,加生理鹽水吹打細胞使之成為均勻溶液,二次離心,去上清液,再次洗滌,加生理鹽水吹打使之成為瘤細胞的均勻溶液,0℃保存。用生理鹽水稀釋細胞懸液至2×107個/mL,于右側腋窩皮下接種0.2 mL。接種后第5天小鼠按腫瘤體積分為5組:模型組、順鉑陽性對照組(2.5 mg/kg)、BUT-6010 30 mg/kg組、BUT-6010 20 mg/kg組、BUT-6010 10 mg/kg組。模型組腹腔注射生理鹽水,其余各組腹腔注射相對應藥物,給藥體積為10 mL/kg,隔天給藥1次,給藥10 d。末次給藥48 h后脫頸椎處死小鼠,取腫瘤及各臟器(胸腺、心、肝、脾、肺、腎)稱重并記錄,統計各組瘤重、臟器系數,計算抑瘤率[7]。
1.6 統計學方法
數據使用SPSS 13.0軟件分析,計量資料數據以均數±標準差()表示,采用LSD-t檢驗。計數資料以率表示,采用χ2檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1 體外對腫瘤細胞生長的抑制作用
實驗結果顯示,BUT-6010 對 HepG2、Hep3B、PLC/PRF/5、786-0、Caki-1、MDA-MB-231、HCT-116、NCI-H460、SKOV-3這9種人癌細胞株的IC50均小于順鉑,見表1。
2.2 體內對S180瘤重的影響
實驗結果顯示,BUT-6010(30 mg/kg)和順鉑(2.5 mg/kg)均有顯著的抑瘤作用,均對動物體重有影響,見圖1及表2。
3 討論
順鉑是目前臨床上使用最廣的抗癌藥物之一,其作用機制是與腫瘤細胞的DNA結合,阻止DNA的合成與復制,抑制細胞分裂,最終殺死腫瘤細胞[7-10]。順鉑因其嚴重的毒副作用、低溶解性和耐藥性,限制了臨床應用劑量和療效。經歷了幾十年的研究發展,一系列鉑類化合物如卡鉑、奧沙利鉑、奈達鉑、庚鉑、洛鉑等已用于臨床治療癌癥[11]。這些鉑類化合物擴大了抗癌譜,不同程度減輕了腎毒性、神經毒性、胃腸道反應、骨髓抑制等不良反應。抗腫瘤活性的廣譜性帶來的非特異性是造成毒副作用的主要原因,因此尋找在保留抗腫瘤活性基礎上具有低毒副作用的鉑類抗腫瘤藥物已成為當前的主要研究方向。本實驗改變順鉑或卡鉑配位體,設計了新型的順鉑或卡鉑類似物BUT-6010,旨在降低鉑類藥物耐藥性和毒性,改善治療效果。
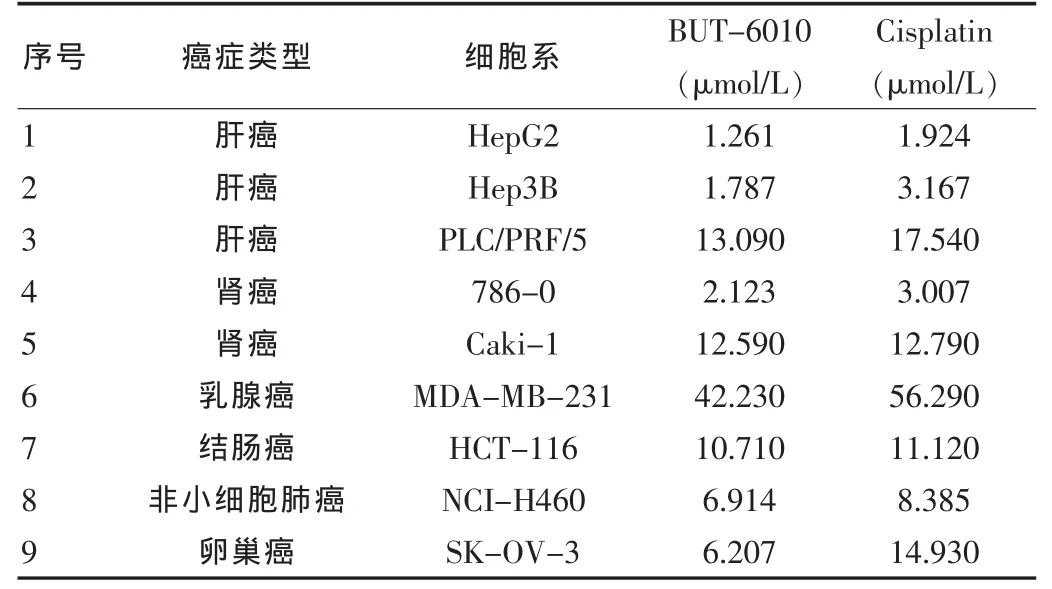
表1 MTS法測BUT-6010對9種人源腫瘤細胞系的IC50

體外 9種人源腫瘤細胞株 HepG2、Hep3B、PLC/PRF/5、786-0、Caki-1、MDA-MB-231、HCT-116、NCI-H460、SKOV-3篩選實驗中,BUT-6010的IC50均小于順鉑,表明BUT-6010對在體外有廣譜抗腫瘤活性,對腫瘤細胞生長的抑制作用強于順鉑。BUT-6010抑制腫瘤細胞增殖作用的強弱規律也基本類似于順鉑。S180荷瘤小鼠的體內實驗中,BUT-6010(30 mg/kg)和順鉑(2.5 mg/kg)均有顯著的抑瘤作用,抑瘤率分別為52.8%、51.8%,同時BUT-6010的不良反應導致的小鼠體重下降在高劑量時表現較明顯。試驗需進一步研究BUT-6010對其他類型動物和人腫瘤模型的抗腫瘤作用,全面評價藥物體內作用,逐步揭示抗其腫瘤活性機制,為臨床試驗研究的開展提供依據。
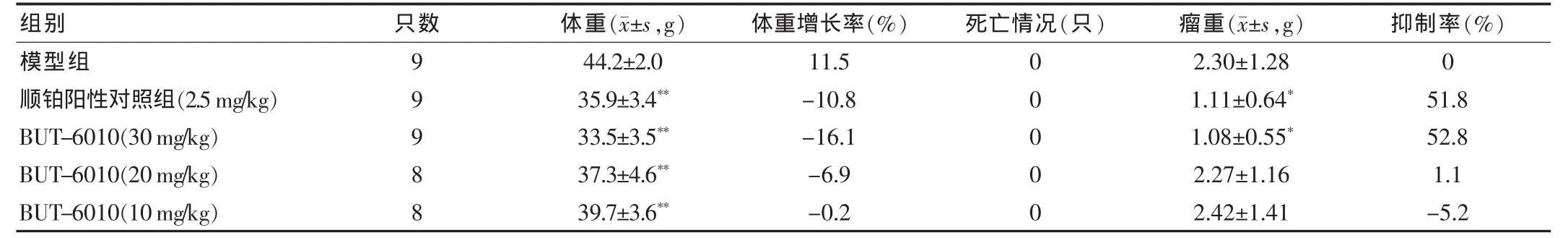
表2 BUT-6010體內對荷S180小鼠瘤重的影響
[1]Komeda S.Drug discovery research on in vivo antitumor-active azolatobridged dinuclear Pt(Ⅱ) complexes[J].Yakugaku Zasshi,2012,132(3):253-259.
[2] 金雪梅.鉑類藥物的毒性作用與預防措施[J].現代醫藥衛生,2010,26(21):3294-3295.
[3]Uehara T,Yamate J,Torii M,et al.Comparative Nephrotoxicity of Cisplatin and Nedaplatin:Mechanisms and Histopathological Characteristics[J].J Toxicol Pathol,2011,24(2):87-94.
[4]Amptoulach S,Tsavaris N.Neurotoxicity caused by the treatment with platinum analogues[J].Chemother Res Pract,2011,2011:843019.
[5]Kozubík A,Vaculová A,Soucek K,et al.Novel Anticancer Platinum(IV)Complexes with Adamantylamine:Their Efficiency and Innovative Chemotherapy Strategies Modifying Lipid Metabolism[J].Met Based Drugs,2008,2008:417897.
[6]王洪燕,全康,蔣燕靈,等.木犀草素抗腫瘤細胞增殖及增敏抗腫瘤藥物作用研究[J].浙江大學學報,2010,39(1):36-42.
[7]張佳麗,王增,莊蓓蓓,等.二氫青蒿素聯合環氧化酶2抑制劑抗S180肉瘤作用機制研究[J].中國藥理學通報,2009,25(3):308-312.
[8]宣麗君.吉西他濱聯合順鉑治療晚期乳腺癌的療效觀察[J].中國當代醫藥,2011,18(5):44-44.
[9]李喜茹.多西紫杉醇聯合順鉑同步放療不可手術胃癌的療效分析[J].中國當代醫藥,2011,18(36):66-67.
[10]李靜靜.順鉑聯合多西他賽或吉西他濱治療晚期非小細胞肺癌的臨床對照研究[J].中國當代醫藥,2011,18(11):54-55,58.
[11]林曉雯,張艷華.鉑類抗腫瘤藥的進展與臨床評價[J].中國醫院用藥評價與分析,2011,11(1):4-6.

