紅土鎳礦鎳和鐵的綜合回收試驗
曹占芳,鐘宏,劉廣義,王帥,劉斌
(1.中南大學 化學化工學院,湖南 長沙,410083;2.中南大學 有色資源化學教育部重點實驗室,湖南 長沙,4100833)
近年來,全球不銹鋼市場需求旺盛,我國更是增勢迅猛。國家發改委數據顯示,2010年我國不銹鋼消費量達8×106t以上,連續6年高居世界第1,這極大刺激了不銹鋼冶煉的基礎原料 —— 金屬鎳的市場需求,導致全球鎳價持續高漲,進而對我國不銹鋼產業發展形成制約之勢[1-2]。我國硫化鎳礦資源儲量只占全球鎳資源儲量的40%,卻提供全部鎳金屬產量的60%。隨著世界硫化鎳礦資源量的不斷消耗和鎳市場的強勁需求,紅土鎳礦的開發利用日趨重要。從紅土礦中生產金屬鎳已有100多年的歷史。由于紅土礦品位較低,且很難通過選礦獲得較高品位(6%以上)的鎳精礦,其開發投資比較大[3-5]。雖然很多學者曾經對紅土鎳礦的浸出技術進行研究,但大多是對高鎳低鐵類型的紅土礦進行處理,且浸出時一般采用還原焙燒—氨浸工藝以及高壓酸浸工藝條件要求比較苛刻[6-9]。為此,本文作者通過對紅土鎳礦常壓浸出工藝的研究,以期實現紅土鎳礦中鎳、鐵資源的高效利用,并為類似紅土鎳礦的技術開發提供新思路。
1 礦石性質
試驗紅土鎳礦來源于多米尼加某礦山。礦石呈風化強烈的褐黃色松散砂土狀。原礦的化學成分分析結果見表1,鐵和鎳的化學物相分析結果分別見表2和表3。
由表1~3可知:礦石中可供回收的鎳、鐵含量分別為1.27%和39.93%。礦石中主要脈石組分為SiO2,Al2O3和MgO,其余組分含量甚少。其中:鐵主要存在于赤(褐)鐵礦中,其質量分數占68.57%,其次鐵分布在假象赤鐵礦中,少量以磁鐵礦形式存在。在這些氧化鐵礦物中鐵的質量分數合計達94.67%。礦石中鎳則主要賦存在于以赤(褐)鐵礦為主的氧化鐵礦物中,其中鎳的質量分數為74.43%,其次是分布在硅酸鹽和氧化鎳中,該礦石屬強烈氧化的含鎳酸性鐵礦石。在顯微鏡下觀察發現:褐鐵礦集合體中多彌散分布泥質物,并嵌布赤鐵礦、假象赤鐵礦等鐵礦物和脈石礦物,且鎳的選別也沒有明顯的富集對象,屬分散分布,不可能通過選礦方法富集[9-12]。因此,本論文采用濕法工藝對礦石中的鎳和鐵進行綜合回收。
2 試驗方法
試驗過程中,每次取礦樣20 g,經粉碎后采用硫酸溶液為浸出劑進行浸出試驗,試驗流程如圖1所示。
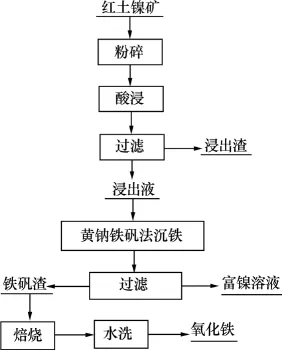
圖1 試驗流程圖Fig.1 Flowsheet of acid leaching of nickel laterite ore
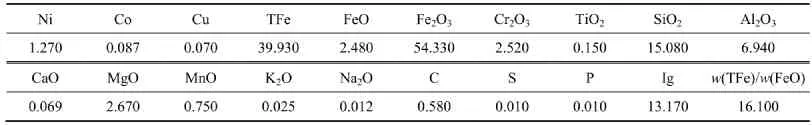
表1 礦石的化學成分(質量分數)Table1 Chemical composition of ores %

表2 鐵的化學物相分析結果(質量分數)Table2 Chemical phase analysis results of Fe %
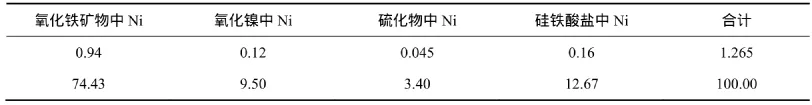
表3 鎳的化學物相分析結果(質量分數)Table3 Chemical phase analysis results of Ni %
3 結果與討論
3.1 粒度試驗
確定液固比5:1,H2SO4質量分數為16%,浸出溫度為80 ℃,攪拌速率為400 r/min,浸出時間為2 h,考察礦石粒度對浸出過程的影響。實驗結果見表4。從表4可見:該紅土鎳礦屬于較易磨的礦樣,當磨礦時間為3 min時,礦樣中小于0.074 mm顆粒質量分數已達到95.60%。未經磨礦的原礦樣的鎳浸出率為62.31%,隨著礦樣細度的增加,鎳的浸出率明顯增加,當礦樣細度達到小于0.074 mm顆粒質量分數為95.60%時,鎳的浸出率達到71.30%;繼續提高礦物細度,鎳的浸出率已無明顯增加。因此,確定浸出試驗所用樣品的粒度為小于0.074 mm顆粒質量分數為95.60%。
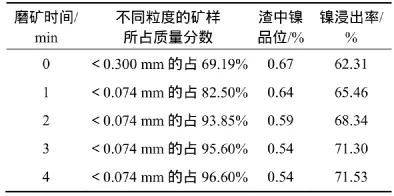
表4 礦樣粒度對浸出過程的影響Table4 Influence of particle size of ore samples on leaching process
3.2 浸出時間試驗
原礦磨至小于0.074 mm顆粒質量分數占95.60%,在液固比為5:1,溫度為80 ℃,攪拌速率為400 r/min,H2SO4質量分數為16%的條件下,考察浸出時間對鎳浸出的影響,結果見表5。由表5可知:隨著浸出時間的延長,鎳的浸出率增大,但浸出2 h以后,鎳的浸出率提高幅度不大。由于攪拌浸出需要一定的能耗,因此,浸出時間確定為2 h。
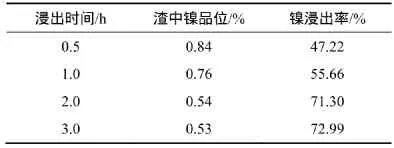
表5 浸出時間對鎳浸出的影響Table5 Influence of leaching time on leaching nickel
3.3 液固比試驗
在溫度為80 ℃,H2SO4質量分數為16%,攪拌速率為400 r/min,浸出時間為2 h的浸出條件下,考察液固比對鎳浸出的影響,結果見表6。由表6可知,液固比的提高有利于鎳的浸出,當液固比達到5:1時,鎳的浸出率達到71.30%;再增大液固比,對鎳浸出的貢獻已不明顯,且液固比太大將使過濾以及萃取等后續工藝操作成本增大。因此,確定浸出工藝的液固比為5:1。
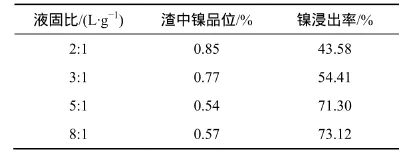
表6 液固比對鎳浸出的影響Table6 Influence of liquid-solid ratio on leaching nickel
3.4 硫酸用量試驗
原礦磨至小于0.074 mm顆粒質量分數占95.60%,在液固比為5:1,溫度為80 ℃,浸出時間為2 h的條件下,考察硫酸用量對鎳浸出的影響,結果見表7。由表7可知:隨著硫酸質量分數的增大,鎳浸出率迅速增大。當硫酸質量分數為16%時,鎳浸出率為71.30%;當硫酸質量分數達到30%時,鎳浸出率達到82.39%。
由表7還可知:該紅土鎳礦酸溶性物質含量較大,隨著硫酸濃度的增大,浸出渣的質量顯著減少,說明礦石中褐鐵礦具有一定的酸溶性。過高的酸度不僅使鎳浸出率提高,也會使礦樣中更多的鐵進入浸出液。綜合考慮各因素,適宜的硫酸質量分數為16%~20%。
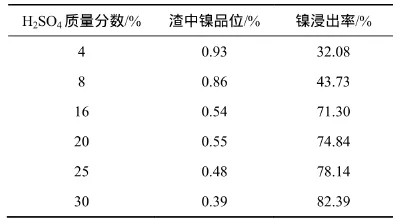
表7 硫酸濃度對鎳浸出的影響Table7 Influence of concentration of sulfuric acid on leaching nickel
3.5 浸出溫度試驗
原礦磨至小于0.074 mm顆粒質量分數占95.60%,在液固比為5:1,H2SO4濃度為16%,攪拌速率為400 r/min,浸出時間2h的條件下,考察浸出溫度對鎳浸出的影響,結果見表8。由表8可知:溫度對鎳的浸出影響很大,隨著浸出溫度的增大鎳浸出率提高顯著,80℃時,鎳浸出率達到71.30%;進一步提高溫度到95 ℃,鎳浸出率可以提高到77.89%。
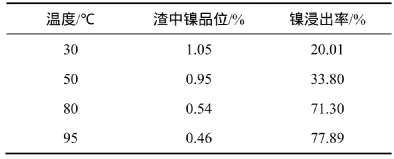
表8 浸出溫度對鎳浸出的影響Table8 Influence of leaching temperature on leaching nickel
3.6 二次浸出試驗
確定浸出條件為:溫度為95 ℃,酸度為20%,液固比為5:1、浸出時間為2 h。在一次浸出試驗的基礎上,對浸出渣再進行二次浸出,結果見表9。由表9可知:在優化的鎳浸出條件下,一次浸出鎳的浸出率可以達到83.52%,而經過二次浸出后鎳的浸出率將可以達到96.32%,取得較理想的浸出率。
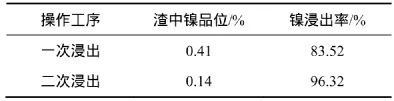
表9 二次浸出試驗結果Table9 Test results of secondary leaching under optimized conditions
3.7 浸出閉路循環試驗
由前述試驗可知:原礦樣經過2次浸出后,鎳浸出率可以達到96.32%,但也存在硫酸溶液消耗過大的問題。因此,采用濃度為20%的硫酸溶液,在溫度為95 ℃、液固比為5:1、浸出時間為2 h的條件下進行閉路循環試驗,工藝流程如圖2所示,試驗結果見表10。由表10可知:經過4~5次循環后,鎳浸出過程逐漸穩定;鎳、鐵浸出率則可以分別達到91.95%和67.96%(取最后2次的平均值)。對浸出液進行化學成分分析,結果見表11。
由表11可知:浸出液中鎳含量為2.15 g/L,而鐵質量濃度達到52.9 g/L;若直接進行萃取等后續操作,則必將對鎳萃取造成影響,且這部分鐵也具有很大的回收價值。因此,對鐵的回收進行探索性試驗。
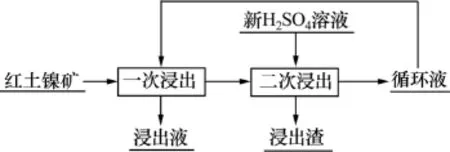
圖2 浸出閉路循環工藝流程圖Fig.2 Flowsheet of circuit leaching process
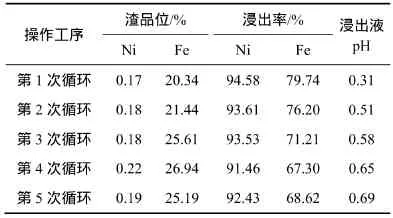
表10 閉路試驗結果Table10 Result of circuit leaching with 20% sulfuric acid

表11 浸出液主要元素質量濃度Table11 Mass concentrations of main elements of lixivium g/L
4 鐵的回收
對于紅土鎳礦浸出液中含有大量的鐵離子,一般采用針鐵礦沉淀法和黃鈉鐵礬法進行去除。但形成針鐵礦(FeOOH)晶體的主要條件是Fe3+質量濃度低。本試驗所得浸出液中鐵離子濃度相對較高,因此,考慮采用黃鈉鐵礬法去除并回收鐵離子。
4.1 黃鈉鐵礬法除鐵
按圖3所示工藝流程,取100 mL浸出液,加入2 mL次氯酸鈉溶液(質量分數10%),在80 ℃條件下反應30 min,從而將溶液中的Fe2+氧化成Fe3+。然后,升高溫度到90~95 ℃,用Na2CO3溶液調節pH到1.5~1.9,攪拌2 h,形成鐵礬,控制終點pH在1.75~2.53之間。實驗考察終點pH對沉鐵效果的影響,結果見表12。
由表12可知:隨著溶液終點pH逐漸升高,沉鐵率則由40.57%逐漸提高到99.27%,而黃鈉鐵礬中帶走的鎳量僅由0.24%增加到2.78%。考慮到繼續升高終點pH,將使鐵離子生成Fe(OH)3趨勢增強,造成鎳離子的吸附而損失,并造成過濾困難,因此,確定控制沉鐵終點pH在2.5左右為宜。沉鐵后溶液組成如表13所示,溶液中鐵質量濃度僅為1.99 mg/L,已經能夠滿足后續鎳萃取工藝要求。
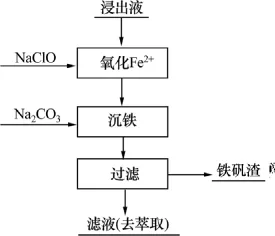
圖3 黃鈉鐵礬除鐵工藝流程圖Fig.3 Flowsheet of sodium jarosite process for removing iron
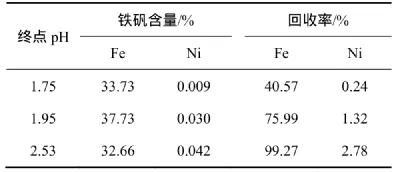
表12 終點pH對除鐵的影響Table12 Influence of pH for removing iron

表13 沉鐵后溶液主要元素質量濃度Table13 Mass concentrations of main elements of filtrate after precipitation g/L
4.2 黃鈉鐵礬渣的利用
酸浸過程中有一半以上的鐵被浸出進入液相,且鐵礬渣中Fe質量分數大于30%,這部分鐵具有較大的利用價值,因此,有必要將這些黃鈉鐵礬渣加以回收利用。
實驗考察采用焙燒工藝生產氧化鐵產品的可行性。在溫度為700 ℃的條件下將黃鈉鐵礬渣焙燒2 h后,用水洗去硫酸鹽及殘堿,烘干粉碎既得氧化鐵產品。所得產品的X線熒光光譜分析結果見表14,其X線衍射分析如圖4所示。由圖4可見:焙燒產品主要成分為Fe2O3。
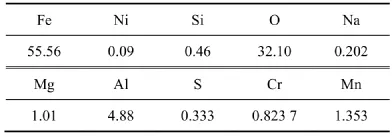
表14 黃鈉鐵礬渣焙燒所得產品X線熒光光譜分析(質量分數)Table14 X-ray fluorescence spectrum analytical results of roasting products from sodium jarosite residue(Mass fraction)%
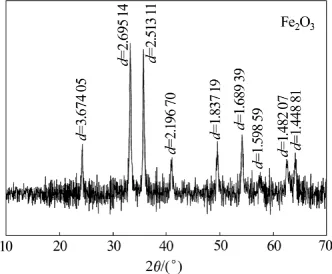
圖4 黃鈉鐵礬渣焙燒所得樣品X線衍射分析Fig.4 X-diffraction analytical result of roasting products from sodium jarosite residue
5 結論
(1)可供回收的主要元素為鎳和鐵。鐵主要以褐鐵礦形式存在,并且褐鐵礦集合體中多彌散分布泥質物;礦石中鎳主要賦存在于以赤(褐)鐵礦為主的氧化鐵礦物中,其中鎳的質量分數為74.43%,其次是分布在硅酸鹽和氧化鎳中,鎳的選別沒有明顯的富集對象,屬分散分布。因此,鐵和鎳很難通過選礦方法進行富集。
(2)常壓酸浸試驗表明,采用質量分數為20%的硫酸溶液,在樣品粒度小于0.074 mm顆粒質量分數為95.60%、溫度為95 ℃、液固比為5:1、浸出時間為2 h的條件下,鎳、鐵浸出率分別可以達到91.95%和67.96%。
(3)采用黃鈉鐵礬法在終點pH為2.5左右時,能夠去除99.27%的鐵。對黃鈉鐵礬渣進行焙燒后能夠得到鐵品位為55.56%的氧化鐵產品。全流程鎳和鐵的回收率分別達到89.39%和67.46%。該工藝實現了多米尼加紅土鎳礦中鎳和鐵的綜合回收,對紅土鎳礦資源的高效開發利用具有重要意義。
[1]蔣繼波, 王吉坤.紅土鎳礦濕法冶金工藝研究進展[J].濕法冶金, 2008, 28(1): 3-11.JIANG Ji-bo, WANG Ji-kun.Review on progresses for hydrometallurgy of laterite nickel ore[J].Hydrometallurgy of China, 2008, 28(1): 3-11.
[2]邱莎, 車小奎, 鄭其, 等.紅土鎳礦硫酸化焙燒-水浸試驗研究[J].稀有金屬, 2010, 34(3): 406-412.QIU Sha, CHE Xiao-kui, ZHENG Qi, et al.Experimental study on laterite-nickel ore with suifating roasting-water immersion methods[J].Chinese Journal of Rare Metals, 2010, 34(3):406-412.
[3]Agatzini-Leonardou S, Zafiratos I.G.Beneficiation of a Greek serpentinic nickeliferous ore Part Ⅱ.Sulphuric acid heap and agitation leaching[J].Hydrometallurgy, 2004, 74(3/4): 267-275.
[4]Baghalha M, Papangelakis G V.Pressure acid leaching of laterites at 250 ℃: A solution chemical model and its applications[J].Metallurgical and Materials Transactions B,1998, 29(5): 945-952.
[5]Canterford J H.Leaching of some Australian nickeliferous laterites with sulphuric acid at atmospheric pressure[J].Proceedings of the Australasian Institute of Mining and Metallurgy, 1978, 265(1): 19-26.
[6]Canterford J H.Acid leaching of chromite-bearing nickeliferous laterite from Rockhampton, Queensland[J].Proceedings of the Australasian Institute of Mining and Metallurgy, 1986, 291(3):51-56.
[7]Rice N M, Strong LW.The leaching of lateritic nickel ores in hydrochloric acid[J].Canadian Metallurgical Quarterly, 1974,13(2): 485-493.
[8]Liu K, Chen Q Y, Hu H P.Comparative leaching of minerals by sulphuric acid in a Chinese ferruginous nickel laterite ore[J].Hydrometallurgy, 2009, 98(3/4): 281-286.
[9]劉志宏, 馬小波, 朱德慶, 等.紅土鎳礦還原熔煉制備鎳鐵的試驗研究[J].中南大學學報: 自然科學版, 2011, 42(10):2905-2910.LIU Zhi-hong, MA Xiao-bo, ZHU De-qing, et al.Preparation of ferronickel from laterite ore in reduction smelting process[J].Journal of Central South University: Science and Technology,2011, 42(10): 2905-2910.
[10]Luo W, Feng Q M, Ou L M, et al.Fast dissolution of nickel from a lizardite-rich saprolitic laterite by sulphuric acid at atmospheric pressure[J].Hydrometallurgy, 2009, 96(1/2): 171-175.
[11]Stamboliadis E, Alevizos G, Zafiratos J.Leaching residue of nickeliferous laterites as a source of iron concentrate[J].Minerals Engineering, 2004, 17: 245-252.
[12]Whittington B I, Mcdonald R G, Johnson J A, et al.Pressure acid leaching of arid-region nickel laterite ore (Part Ⅰ): Effect of water quality[J].Hydrometallurgy, 2003, 70(1/2/3): 31-46.

