SO2-4濃度對304不銹鋼在NaCl溶液中點蝕行為影響的研究
杜 楠,田文明,趙 晴,孟保利
(1南昌航空大學輕合金加工科學與技術國防重點學科實驗室,南昌330063;2中航工業西安飛機工業(集團)有限責任公司,西安710089)
SO2-4濃度對304不銹鋼在NaCl溶液中點蝕行為影響的研究
杜 楠1,田文明1,趙 晴1,孟保利2
(1南昌航空大學輕合金加工科學與技術國防重點學科實驗室,南昌330063;2中航工業西安飛機工業(集團)有限責任公司,西安710089)
利用動電位極化、電化學阻抗譜(EIS)和激光電子散斑干涉(ESPI)研究了3.5%NaCl溶液中,濃度對304不銹鋼點蝕行為的影響。使用0.3V(vs SCE)極化條件下的計時電流法結合ESPI確定了點蝕誘導時間。結果表明:當濃度為0.5%時,不銹鋼的耐蝕性最差;當濃度低于1%時,不銹鋼的耐蝕性較不存在時的耐蝕性差;當濃度高于1%時,不銹鋼的耐蝕性較不存在時的耐蝕性好。在3.5%NaCl+0.5%Na2SO4溶液中,點蝕誘導時間是4s,在3.5%NaCl溶液中和3.5%NaCl+4%Na2SO4溶液中點蝕誘導時間分別是9s和94s。
304不銹鋼;點蝕;激光電子散斑干涉技術;硫酸根離子
304不銹鋼是應用最為廣泛的一種鉻-鎳不銹鋼,具有優良的不銹耐腐蝕性能和較好的抗晶間腐蝕性能,耐熱性、低溫強度和力學性能優良,同時具有良好的加工性和可焊性,廣泛應用于家庭用品、建材、化學、食品等工業。但在海水和其他含氯介質中則容易發生點蝕。點蝕[1,2]是不銹鋼失效的主要形式之一,嚴重時能導致設備穿孔,在實際生產中存在很大的隱患。研究表明,點蝕主要由侵蝕性陰離子Cl-引起,當溶液中還存在其他離子時,可能加速材料的腐蝕,也可能減緩材料的腐蝕。Sherbini等[3]發現陰離子抑制劑對Zn溶解和點蝕發生的抑制程度與離子種類和濃度有關;葛紅花等[4]研究了冷卻水中SO2-4對不銹鋼冷凝器的緩蝕作用,認為SO2-4在金屬氧化物表面上發生競爭性吸附,置換出表面的Cl-,從而使點蝕受到抑制;Lee等人[5]通過SO2-4與Cl-的協同效應對純Al點蝕電位影響的研究,發現SO2-4會阻礙點蝕的發生,但會加速點蝕的發展。SO2-4對鈍性金屬在含Cl-水溶液中點蝕行為的影響,存在加速點蝕和抑制點蝕兩種情況,并且加速或者抑制與SO2-4的濃度密切相關。
激光電子散斑干涉(Electronic Speckle Pattern Interferometry,ESPI)是20世紀70年代初發展起來的以激光、光電子技術及數字圖像處理為基礎的現代光學測量方法[6-8]。ESPI可以對材料表面形變進行原位、全場、高精度、動態連續的監測。王梅豐等人利用ESPI監測45#碳鋼在0.5mol/L Na HCO3+0.05mol/L NaCl體系中的局部腐蝕行為時發現,當電極表面發生點蝕時,ESPI圖像上會出現亮斑,亮斑由電極表面點蝕產物擴散引起,它與電極表面蝕點一一對應[9,10]。從ESPI視頻中可以確定電極材料表面發生點蝕的時刻和位置[11]。本工作采用動電位極化法、電化學阻抗技術(EIS)和ESPI研究了不同濃度的SO2-4對304不銹鋼在3.5%(質量分數,下同)NaCl溶液中點蝕行為的影響。
1 實驗方法
研究電極為304不銹鋼,化學成分由QSN750直讀光譜測出,如表1所示。用線切割技術將電極加工成?10mm的圓片。電極用酚醛樹脂鑲嵌,焊接導線,非工作面用環氧樹脂密封。實驗前工作面依次用150#,400#,600#,800#Al2O3水砂紙打磨平整,經去離子水洗并吹干后,依次用酒精、丙酮擦拭,然后放入干燥皿中備用。

表1 304不銹鋼的化學成分(質量分數/%)Table 1 Chemical composition of 304 stainless steel(mass fraction/%)
電化學測試采用三電極體系,輔助電極為鉑片,參比電極為飽和甘汞電極(SCE),通過鹽橋與工作電極連接。研究采用的設備為電化學工作站Autolab PGSTAT30,通過設備附帶軟件完成實驗控制。EIS測試在開路電位穩定后進行,激勵信號是幅值為5m V的正弦交流電,測量頻率范圍為105~10-2Hz。動電位極化測試在開路電位穩定后進行,先陰極極化,后陽極極化,掃描速率為20m V/min。
ESPI監測系統由邁克爾遜干涉光路、圖像采集卡和相應的數據處理軟件組成。其中邁克爾遜干涉光路由氦氖激光器,散斑測量光路系統和CCD攝像頭等部分組成[12]。所有光學器件及電解池裝置都固定在防震水平臺上。
采用分析純NaCl,Na2SO4和二次蒸餾水配置成含有不同濃度SO2-4的3.5%的NaCl溶液。EIS、動電位極化曲線和ESPI測試實驗溫度分別為35,30,28℃。實驗溶液未經除氧處理,溶液p H值用NaOH水溶液和稀鹽酸調整。
2 結果與討論
2.1 動電位極化曲線
圖1是304不銹鋼在Cl-濃度為3.5%,SO2-4濃度分別為0%,0.3%,0.5%,0.8%,1%,2%,3.5%,4%溶液中的動電位極化曲線。由曲線得到的點蝕破裂電位Eb與SO2-4濃度的關系見圖2。
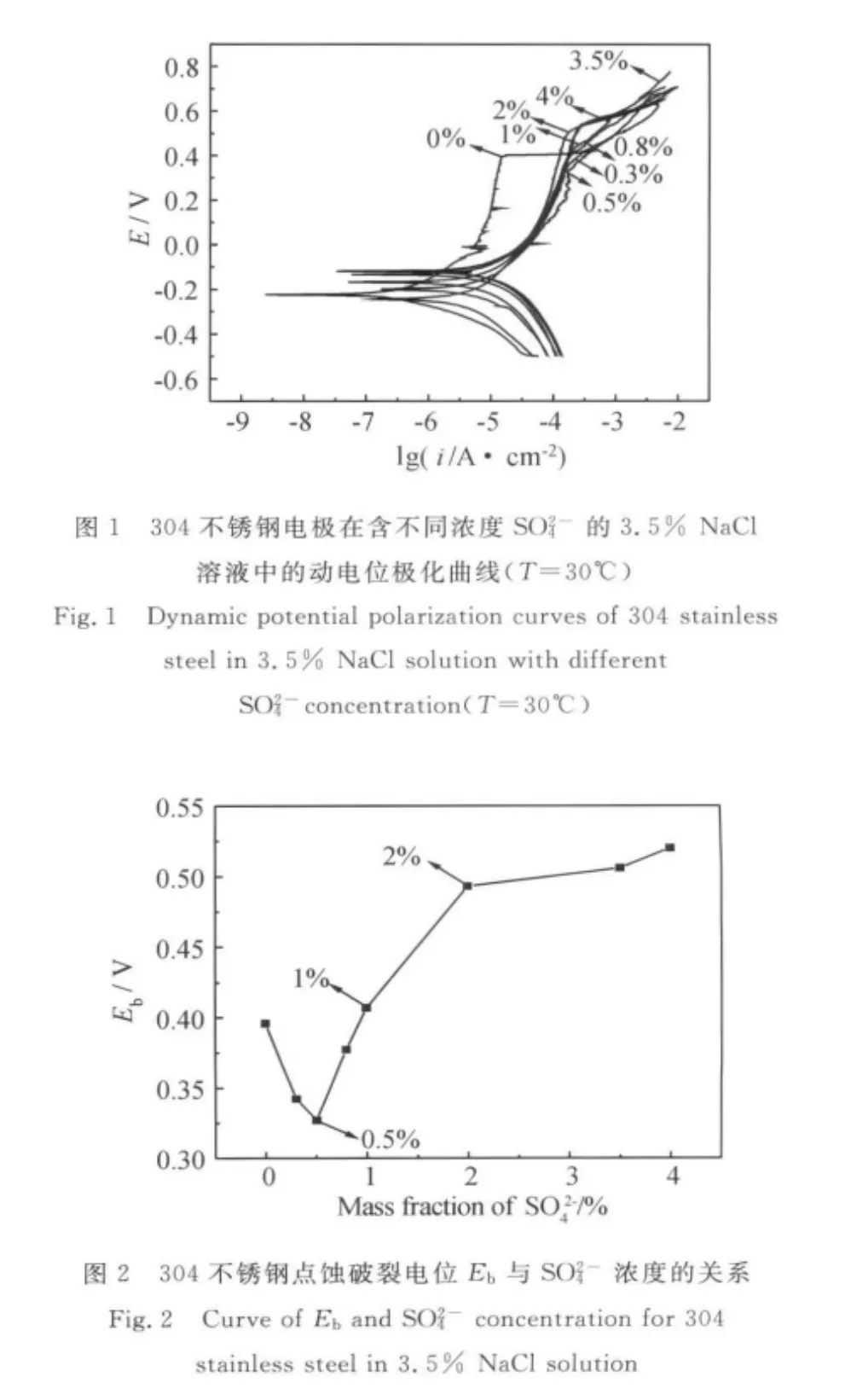
不銹鋼在含Cl-的介質中,電極電位朝正方向掃描到鈍化區的某一電位時,由于發生點蝕,會出現電流密度突增的現象,則該點電位稱為點蝕破裂電位E[13]b。其值越正,材料的耐點蝕性能越好。由圖1和圖2可知,在SO2-4濃度低于0.5%時,304不銹鋼的點蝕破裂電位Eb隨SO2-4濃度的增加而減小;當SO2-4濃度大于0.5%時,隨著SO2-4濃度的增加,304不銹鋼的Eb逐漸正移;Eb值在SO2-4濃度為0.5%時取得極小值。當SO2-4濃度小于1%時,不銹鋼的Eb低于不存在SO2-4時的Eb;當SO2-4濃度大于等于1%時,不銹鋼的Eb高于不存在SO2-4時的Eb。當SO2-4濃度大于2%時,隨著SO2-4濃度的繼續增加,Eb增大較為平緩。
一般認為,在含有Cl-的腐蝕體系中,點蝕的誘發動力學過程分為三步:Cl-的吸附,吸附的Cl-與鈍化膜中的金屬陽離子形成氯化物,該氯化物快速溶解。如果存在其他離子能夠影響上述過程,就能影響點蝕的發生。在不存在SO2-4的NaCl溶液中,Cl-均勻地吸附在不銹鋼表面,造成鈍化膜的加速溶解,個別薄弱處最先露出基體。在SO2-4和Cl-共存的水溶液中,SO2-4和Cl-在金屬表面發生競爭吸附[5,14],此吸附過程是一個動態平衡過程,存在離子吸附與脫附現象。當SO2-4濃度較低時(0%~1%),Cl-是主要的吸附離子,但吸附在不銹鋼表面的少量SO2-4由于在脫附與遷移過程中與Cl-碰撞會使Cl-分布隨機性增大,引起不銹鋼表面局部Cl-濃度遠大于Cl-平均濃度,使該區域鈍化膜破裂更加迅速,點蝕敏感性增加,即材料的Eb負移。實驗結果表明,SO2-4濃度為0.5%時,Cl-局部濃度增大的效果最明顯,即Eb最負。當SO2-4濃度較高時(1%~4%),SO2-4成為主要吸附離子,隨著SO2-4濃度的增加,吸附在不銹鋼表面的Cl-越來越少。在Cl-和SO2-4的競爭吸附過程中,雖然Cl-也在不銹鋼表面遷移,但是由于其有效濃度較低,不易引起Cl-在不銹鋼表面局部區域瞬時集中,此時不銹鋼的點蝕敏感性降低,即材料的Eb逐漸正移。由圖2亦可知,當SO2-4濃度在1%~2%之間時,點蝕破裂電位Eb迅速升高,表明不銹鋼表面局部區域Cl-濃度瞬間升高的可能性迅速降低;當SO2-4濃度大于2%時,Eb變化較為平緩,表明SO2-4與Cl-碰撞引起Cl-分布趨于平均。
2.2 不同濃度SO2-4對304不銹鋼電化學阻抗譜的影響
圖3是304不銹鋼在SO2-4濃度分別為0%,0.3%,0.5%,0.8%,1%,2%,3.5%,4%的NaCl溶液中浸泡不同時間的電化學阻抗譜復數平面圖。通過等效電路擬合得到的電極在這8種溶液中的電荷轉移電阻Rt隨浸泡時間的變化曲線見圖4。
由圖3可知,304不銹鋼電極在這8種溶液中的阻抗圖譜均表現為一單容抗弧,表明電極表面均處于穩定的鈍化狀態[15]。隨著浸泡時間的延長,304不銹鋼電極在這8種溶液中的單容抗弧半徑均逐漸減小,表明耐蝕性不斷降低。
Rt表示電極電化學反應過程中的電荷轉移電阻,其大小與不銹鋼腐蝕速率成反比,它能一定程度上反映不銹鋼的腐蝕速率。由圖4可知,在這8種溶液中,304不銹鋼的Rt均隨著浸泡時間的延長不斷降低,表明材料的腐蝕速率不斷增加。在相同的浸泡時間內,當溶液中SO2-4濃度為4%時,Rt最大,表明材料在該溶液中耐蝕性最好;當溶液中SO2-4濃度為0.5%時,其Rt最小,表明材料在該溶液中耐蝕性最差;當溶液中SO2-4濃度為1%,2%,3.5%時,其Rt均比不含SO2-4的NaCl溶液高,表明在這三種溶液中,材料的耐蝕性較不含SO2-4的NaCl溶液好;當SO2-4濃度為0.3%時,其Rt比不含SO2-4的NaCl溶液低,表明材料在該溶液中耐蝕性較不含SO2-4的NaCl溶液差。以上分析結果印證了動電位極化曲線的分析結果。
2.3 激光電子散斑干涉測試
圖5是304不銹鋼在3.5%NaCl,3.5%NaCl+0.5%Na2SO4,3.5%NaCl+4%Na2SO4溶液中,施加0.3V(vs SCE)恒電位極化時的計時電流曲線。三組曲線對應的ESPI圖像分別見圖6~8。
由圖5(a)可知,在3.5%NaCl溶液中,304不銹鋼在0.3V(vs SCE)恒電位極化下,極化電流先下降,然后產生小幅度上升。極化至6s左右時,極化電流呈鋸齒形緩慢波動,表明電極表面可能在經歷鈍化膜破裂與修復的交替過程。極化9s時,極化電流為0.3m A,ESPI圖(圖6(b))上出現兩個亮斑,表明電極表面在相應位置有點蝕產生。極化15s時,ESPI圖(圖6(c))上原有的兩個亮斑一個略有長大且更加清晰,另一個亮度相對變弱。極化29s時,ESPI圖(圖6(d))上原來亮度變弱的亮斑消失,無腐蝕產物擴散現象,這可能是由于電極表面相應位置的蝕孔發生了再鈍化。另一亮斑繼續長大并有向下擴散的趨勢,表明該處蝕孔不斷生長,腐蝕產物不斷積累并在重力作用下向下移動。極化50s時,ESPI圖(圖6(e))上亮斑擴散趨勢變大,蝕孔繼續生長,腐蝕產物不斷向外擴散。極化120s時,ESPI圖(圖6(f))上亮斑范圍繼續擴大,腐蝕產物擴散到了較大的范圍。
由圖5(b)可知,在3.5%NaCl+0.5%Na2SO4溶液中,304不銹鋼在0.3V(vs SCE)恒電位極化下,極化電流先下降,然后隨時間呈鋸齒形上升,表明電極表面可能在經歷鈍化膜破裂與修復的交替過程。
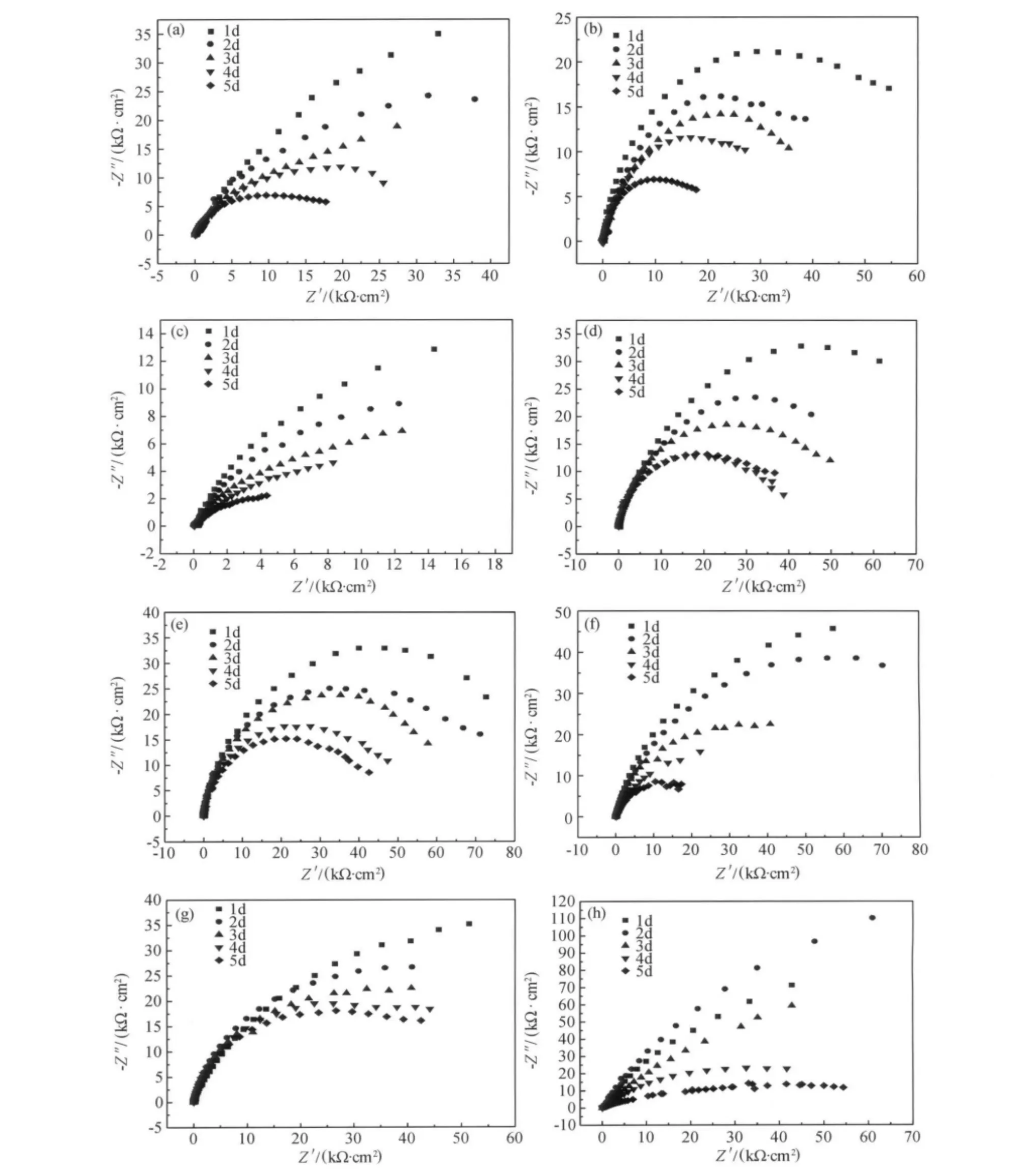
圖3 304不銹鋼電極在不同濃度的3.5%NaCl溶液中浸泡不同時間后的電化學阻抗譜復數平面圖(T=35℃)(a)0%;(b)0.3%;(c)0.5%;(d)0.8%;(e)1%;(f)2%;(g)3.5%;(h)4%Fig.3 Nyquist plots at different immersion time for 304 stainless steel in 3.5% NaCl solution with different concentration(T=35℃)(a)0%;(b)0.3%;(c)0.5%;(d)0.8%;(e)1%;(f)2%;(g)3.5%;(h)4%
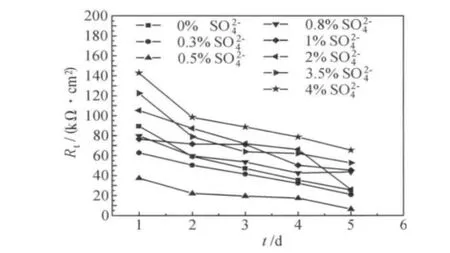
圖4 304不銹鋼電極在不同濃度的3.5%NaCl溶液中電荷轉移電阻Rt隨浸泡時間的變化曲線Fig.4 Curves of charge transfer resistance Rtand immersion time for 304 stainless steel in 3.5%NaClsolution with different concentration
304不銹鋼極化4s時,極化電流為0.2m A,ESPI圖(圖7(b))上出現了一個亮斑,表明電極表面在該位置處產生了一個蝕孔。極化17s時,ESPI圖(圖7(c))上的亮斑略有長大,變得更加清晰,表明該蝕孔在繼續生長,同時腐蝕產物在不斷向外擴散。極化67s時,ESPI圖(圖7(d))上在原有亮斑的左方又出現了一個亮斑,表明又有一個新的蝕孔在該處產生。極化91s時,ESPI圖(圖7(e))上兩個亮斑繼續增大,并有向下擴散的趨勢。極化120s時,激光散斑干涉圖(圖7(f))上兩個亮斑變得更大,表明隨著極化反應的進行,蝕孔內不斷向外釋放出腐蝕產物,腐蝕產物在重力的作用下不斷向下方擴散。
由圖5(c)可知,在3.5%NaCl+4%Na2SO4溶液中,304不銹鋼在0.3V(vs SCE)恒電位極化下,極化電流隨時間呈鋸齒形上升。極化94s時,極化電流為0.3m A,ESPI圖(圖8(b))上出現了一個亮斑,表明電極表面在相應位置產生了一個蝕孔。極化120s時,ESPI圖(圖8(c))上亮斑長大,變得更加清晰,表明該蝕點在繼續長大,同時腐蝕產物不斷地向外擴散。
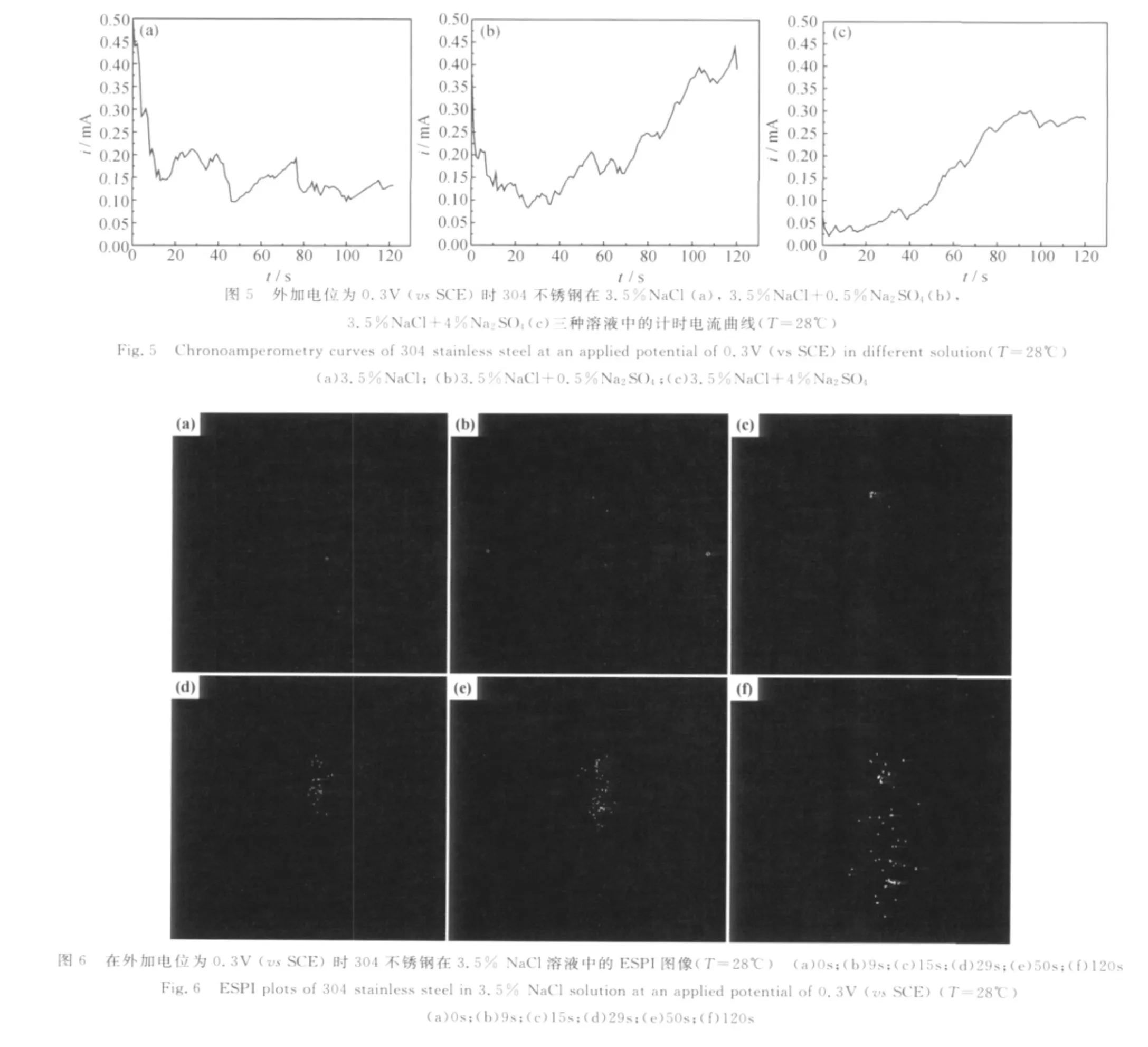

點蝕感應時間(τ)是指在恒電位極化條件下蝕孔開始形成所需要的時間。τ值的大小隨實驗所使用的溶液成分不同而不同,溶液的腐蝕性越強,孔蝕感應時間越短。由以上ESPI監測結果可知,在0.3V(vs SCE)恒電位極化下,304不銹鋼在3.5%NaCl+0.5% Na2SO4溶液中,點蝕感應時間τ為4s;在3.5%NaCl溶液中,τ為9s;在3.5%NaCl+4%Na2SO4溶液中,點蝕感應時間τ為94s;由此可以得出結論,在這三種溶液中,304不銹鋼的耐蝕性大小依次為(3.5%NaCl+4%Na2SO4)>(3.5%NaCl)>(3.5%NaCl+0.5% Na2SO4)。這一結果印證了動電位極化和EIS的分析結果。
3 結論
(1)不同濃度的SO2-4對304不銹鋼的點蝕破裂電位Eb有不同的作用效果。當SO2-4濃度為0.5%時,不銹鋼的Eb最負;當SO2-4濃度低于1%時,不銹鋼的Eb比不存在SO2-4離子時的Eb負;當SO2-4濃度高于1%時,不銹鋼的Eb比不存在SO2-4離子時的Eb正。
(2)304不銹鋼在8種溶液中的EIS復數平面圖均為一單容抗弧,電極表面處于穩定的鈍化狀態。電荷轉移電阻Rt都隨著浸泡時間的延長而降低。在相同的浸泡時間內,當濃度為0.5%時,Rt最小;當濃度為4%時,Rt最大。
(3)利用ESPI監測溶液中不銹鋼點蝕行為時,如果散斑圖上出現亮斑,表明材料表面對應位置發生了點蝕。由ESPI結果可知,304不銹鋼在3.5%NaCl+0.5%Na2SO4溶液中的點蝕感應時間τ為4s;在3.5%NaCl溶液中的τ為9s;在3.5%NaCl+4% Na2SO4溶液中的τ為94s。
[1] 周本省.工業冷卻水系統中金屬的腐蝕與防護[M].北京:化學工業出版社,1993.25.
[2] 劉道新.材料的腐蝕與防護[M].西安:西北工業大學出版社,2006.119-120.
[3] SHERBINI E E,REHIM S S.Pitting corrosion of zinc in Na2SO4solutions and the effect of some inorganic inhibitors[J].Corros Sci,2000,42(5):785-789.
[5] LEE W J,PYUN S I.The effect of prior Cl-ion incorporation into native oxide film on pure aluminium in neutral chloride solution on pit initiation[J].Corrosion Science,2001,43(2):353-363.
[6] PETZING J N,TYRER J R.Recent development and applictions in electronic speckle pattern interferometry[J].The Journal of Strain Analysis for Engineering Design,1998,33(2):153-169.
[7] HABIB K,MUHANA K.Holographic interferometry as electrochemical emission spectroscopy of a carban steel in 5-20 ppm TROS C-70 inhibited seawater[J].Optics and Lasers in Engineering,2002,38:577-588.
[8] HABIB K,BOURESLI K.Detection localizied corrosion of stainless steels by optical interferometry[J].Electrochemical Aata,1999,44(25):4635-4641.
[9] 王梅豐,杜楠,李曉剛,等.利用電子散斑干涉技術研究45碳鋼在Na HCO3+NaCl體系中的早期點蝕行為[J].中國腐蝕與防護學報,2009,29(3):210-214.
[10] WANG M F,LI X G,DU N,et al.Direct evidence of initial pitting corrosion[J].Electrochemistry Communications,2008,10(7):1000-1004.
[11] DU Nan,LIU Gang,ZHAO Qing.Monitoring initial pitting behaviors of 30Cr MnSi steel in Na HCO3-NaCl solution by ESPI and electrochemical noise[J].Material Science,2008,2(3):326-329.
[12] WANG M F.Study on initial pitting corrosion behaviors and mechanisms of metals using electronic speckle pattern interferometry[D].Beijing:University of Science and Technology Beijing,2008.
[13] 李狄.電化學原理[M].北京:北京航空航天大學出版社,2008.275-276.
[14] WU J W,LI X G,DU C W,et al.Effects of Cl-andions on corrosion behavior of X70 steel[J].Journal of Materials Science and Technology,2005,21(1):28-32.
[15] 胡麗華,杜楠,王梅豐,等.1Cr18Ni9Ti不銹鋼在酸性NaCl溶液中的點蝕電化學特征[J].失效分析與預防,2006,1(3):6-9.
Effect of SO2-4Concentration on 304 Stainless Steel Pitting Corrosion in NaCl Solution
DU Nan1,TIAN Wen-ming1,ZHAO Qing1,MENG Bao-li2
(1 National Defence Key Discipline Laboratory of Light Alloy Processing Science and Technology Institute,Nanchang Hangkong University,Nanchang 330063,China;2 AVIC Xi’an Aircraft Industry(Group)Company Ltd.,Xi’an 710089,China)
Effect of SO2-4concentration on 304 stainless steel pitting corrosion in 3.5%NaCl solution was investigated by means of dynamic potential polarization,electrochemical impedance spectroscopy(EIS)and electronic speckle pattern interferometer(ESPI).The pitting induction timeτunder 0.3V(vs SCE)polarization was detected by means of ESPI and chronoamperometry.The results showed that the stainless steel corrosion resistance was the worst when theconcentration was 0.5%.When theconcentration was below 1%,the corrosion resistance was worse than that having no.When theconcentration was beyond 1%,the corrosion resistance was better.The pitting induction timeτof the 304 stainless steel were 4s,9s and 94s in 0.5%NaCl+0.5%Na2SO4solution,3.5%NaCl solution and 3.5%NaCl+4%Na2SO4solution respectively.
304 stainless steel;pitting;ESPI;
TG174
A
1001-4381(2012)07-0064-07
國家自然科學基金項目(51071083)
2011-10-08;
2012-03-26
杜楠(1956—),男,教授,主要從事金屬腐蝕與防護方面的研究工作,聯系地址:南昌市豐和南大道696號南昌航空大學國防科技研究院318室(330063),E-mail:d_unan@ sina.com

