5-氟尿嘧啶節律性化療對晚期胃癌患者的臨床療效觀察
劉立新
寶應縣人民醫院消化內科,江蘇 揚州 225800
既往化療所用細胞毒性藥物均采用較高濃度,以腫瘤細胞為殺傷靶目標,然而,在化療間期,營養腫瘤的小血管內皮細胞得以死灰復燃,殘余腫瘤細胞得以迅速恢復并影響化療療效[1]。為從根本上抑制腫瘤細胞復制,需截斷其營養的供應,節律性化療為使用化療藥物定期、低劑量持續重復給藥,抑制血管內皮細胞的修復再生,從而逐步抑制營養供應血管,減少腫瘤細胞的增殖,達到控制臨床癥狀的目的[2]。再次化療過程中使用細胞毒性藥物劑量較低,對人體的毒副作用也較低。為提高患者的生活質量,改善患者預后,筆者采用氟尿嘧啶對晚期胃癌患者進行節律性化療,取得較為滿意療效,現將結果報道如下。
1 資料與方法
1.1 臨床資料 選擇2009年5月-2011年11月于我院住院治療的24例晚期胃癌患者,臨床分期均為Ⅳ期,其中有7例患者為首次就診發現,余17例為復診,所有患者均胃鏡下取活組織病檢證實。男16例,女8例,年齡59~75歲,平均年齡(67.6±12.5)歲。22例患者為腺癌,其中16例發生在賁門部,6例發生在胃體部;2例患者為鱗癌,均發生在胃體部。所有患者伴有淋巴結受累,3例患者累及胃部周圍臟器,11例伴有肺轉移,10例伴有肝轉移,所有患者1個月內未接受其他治療方案。
1.2 治療方案 化療前均告知患者治療方案,向其闡明優劣,并簽署知情同意書。使用5-氟尿嘧啶500 mg以恒定速率靜脈持續泵入12 h d1-21,4周為1個療程,所有患者化療3~9個療程。如果患者在治療期間出現食欲不振、惡心嘔吐、腹痛腹瀉等胃腸道反應,則給予患者胃復安靜脈注射;所有患者化療期間應1周抽血復查肝腎功能及電解質,密切觀察患者病情變化,一旦出現骨髓抑制現象如WBC<3.0×109/L或中性粒細胞計數<1.5×109/L,即皮下注射粒細胞集落刺激因子或給予口服藥物升白細胞。所有患者在化療前1周行CT,測量病灶大小并做記錄,化療3個療程后,再次行CT并測量記錄。
1.3 療效評價標準 化療的近期療效評價標準采用實體瘤療效評價[3];不良反應評價標準采用WHO抗腫瘤藥物毒性反應標準。化療3個療程后,如果病情好轉,實體瘤療效評價為疾病控制者則仍然按照原化療方案進行,如果患者出現副作用較大,不能耐受或CT顯示患者病情惡化則停止治療。所有患者每3個化療療程結束后進行復查并對其療效及不良反應進行評價。
1.4 隨訪方法 所有患者在開始節律性治療之日開始進行計算,末次隨訪時間為2011年11月15日。記錄其各項實驗室檢查結果,對其臨床療效及不良反應進行記錄并及時給予對癥處理。
1.5 統計學方法 所記錄的數據均采用SPSS 17.0軟件包進行處理,TTP采用COX回歸進行分析,P<0.05為差異有統計學意義。
2 結果
2.1 患者隨訪病情變化 24例患者隨訪8~24個月,平均(11.8±4.6)個月,其中有3例患者部分緩解(12.5%),9 例患者病情穩定(37.5%),無1 例患者完全緩解,12例患者疾病繼續進展(50.0%),疾病控制率為50.0%。治療有效患者的中位TTP為3.2個月(見圖1)。
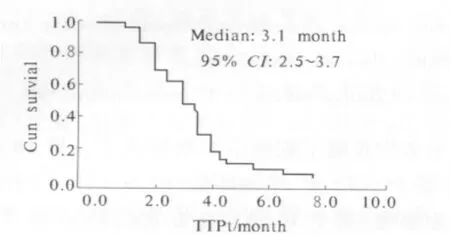
圖1 24例晚期胃癌患者的TTP曲線Fig 1 TTP curve of 24 patients with advanced gastric cancer
2.2 不良反應 使用5-氟尿嘧啶治療后的主要不良反應表現為骨髓抑制引起的白細胞及中性粒細胞減少、惡心嘔吐、腹瀉及口腔黏膜炎、潰瘍等(見表1)。
3 討論
本實驗結果發現,使用5-氟尿嘧啶節律性化療可以有效控制老年晚期胃癌患者的病情進展,不良反應少且輕。化療是胃癌的重要治療方法之一[4],根據治療的時機和目的將其分為3種:(1)新輔助化療:其目的是降低腫瘤分期,提高手術根治切除率;(2)輔助性化療:目的是減少亞臨床病灶,防止術后復發轉移;(3)姑息性化療:指晚期胃癌不能治愈的治療,以改善生活質量及延長生命為目的。胃癌化療至今仍無標準的化療方案,5-氟尿嘧啶是胃癌聯合化療的最基本藥物,單藥化療的有效率為10% ~20%,緩解期為3~5個月,對生存無明顯影響。5-氟尿嘧啶對新生腫瘤血管的抑制機制是在非細胞毒濃度下表現出的特殊能力,臨床上以緩慢滴注的方式對整個細胞周期都有作用,腫瘤血管床長時間暴露于藥物下,改變了血管生長的內環境,對血管內皮細胞的增殖及腫瘤誘導的血管因子的釋放產生影響,我們推測與其誘導細胞凋亡、抑制促血管生成因子的分泌有關[5]。
一個不同模型提示抗血管生成療法治療胃癌是有效的[6],因為前者的優先靶標為內皮細胞,而后者靶標為循環中的血管內皮前體細胞(circulating endothelial precursor,CEP),臨床上用最大耐受量(maximum tolerated dose,MTD)治療之后經常會有一個患者停止用藥節段,使患者從治療中受到的毒性及骨髓抑制作用中恢復過來,MTD化療通常會造成循環造血細胞數量顯著減少,包括中性粒細胞和其他的骨髓細胞,還有CEP,這些細胞的減少非常迅速,并且接下來通常會有一個快速的反彈時期,從骨髓中動用造血前體細胞進入循環,這種反應在小鼠和人里面都有發現。該反應的一個潛在的負面結果就是會造成CEP的增加,CEP會分化為成熟內皮細胞。骨髓來源的髓細胞額外聚集,會直接或間接地促進腫瘤血管生成。因此,MTD治療方案中的停藥節段會使腫瘤血管系統進行修復或擴增,從而削弱細胞毒性作用的有益之處,盡管CEP及其分化的子細胞的真正本質及功能仍然存在爭議,但是已經有證據表明促血管生成因子和其他的血管生成因子能夠刺激骨髓釋放CEP,因此節律性化療能抑制腫瘤募集CEP及其子細胞的能力。
停藥間歇期的減少對腫瘤血管生成有額外的抑制作用。2000年,當對小鼠的MTD治療改為用同一種藥物低劑量多間歇的方法時,能夠增強抑制腫瘤生長的效應。盡管腫瘤細胞本身對毒性藥物有抵抗性,腫瘤生長被同一種藥物抑制甚至逆轉,這些結果表明化療并不針對腫瘤細胞,也會抑制正常的細胞,如內皮細胞或CEP的募集。后續工作表明在小鼠中定期的、低劑量的節律性化療會誘導血管生成抑制因子TSP-1的表達,在這些模式中TSP-1的遺傳缺失會促進腫瘤的生長及血管的生成[7-8]。實際上,我們推測,在既沒有被轉化也沒有遺傳不穩定因素的正常內皮細胞會比腫瘤細胞對化療的毒性作用更加敏感。如果對患者持續低劑量用藥并避免MTD治療方案中的間歇期,就有可能利用足夠低劑量的細胞毒性藥物來抑制內皮細胞的增殖、存活及功能,同時沒有嚴重的骨髓抑制效果。節律性治療的研究還在起始階段,但是已經有令人信服的臨床案例,非小細胞肺癌、轉移性乳腺癌或卵巢癌患者對每周低劑量的DNA損傷藥或抑制微管的治療有反應。同時,節律性化療使用藥物的劑量較低,也會減少它們的毒副作用如脫發、惡心等,從而改善患者的生活質量。
本實驗未能使5-氟尿嘧啶與其他抗腫瘤細胞的化療藥物一同使用,未能觀察到其最好的療效,以后的臨床試驗可設計將抗血管生成療法和其他療法聯合使用,以得到更好的治療效果,改善患者預后,提高生活質量和生存率。
[1]Tao JL,Zhuang ZX,Shen LQ.Elderly patients with advanced gastric cancer patients with fluorouracil rhythm observation of clinical efficacy of chemotherapy[J].Guide of China Medicine,2011,9(31):128-129.陶家龍,莊志祥,沈麗琴.老年晚期胃癌患者氟尿嘧啶節律化療臨

