左卡尼汀對(duì)異丙腎上腺素誘導(dǎo)大鼠心肌肥厚的保護(hù)作用及機(jī)制研究
姚秀云,楊育紅,宋 瑩,王洪新,張 晶,李洪秀
(1.遼寧醫(yī)學(xué)院藥理學(xué)教研室,遼寧 錦州 121000;2.遼寧省盤錦市第二醫(yī)院,遼寧 盤 錦 124000)
心肌肥厚(myocardial hypertrophy,MH)是心血管疾病患者發(fā)病率和死亡率增加的一個(gè)重要原因,心肌肥厚最終發(fā)展成心衰。左卡尼汀(L-carnitine)又稱左旋肉堿,是哺乳動(dòng)物能量代謝必需的體內(nèi)天然物質(zhì),對(duì)細(xì)胞中能量的產(chǎn)生和轉(zhuǎn)運(yùn)起重要作用。L-carnitine能促進(jìn)脂肪酸經(jīng)β-氧化進(jìn)人三羧酸循環(huán),產(chǎn)生能量,與機(jī)體的器官、組織代謝密切相關(guān)[1]。L-carnitine的缺乏會(huì)導(dǎo)致能量供應(yīng)障礙及脂肪酸代謝的各種中間產(chǎn)物累積酸中毒,出現(xiàn)心肌病變、心律失常、機(jī)體疲勞等癥狀[2]。一般認(rèn)為在缺血、缺氧時(shí),心肌細(xì)胞內(nèi)脂肪酸β-氧化障礙,脂肪酸堆積,葡萄糖酵解增強(qiáng),腺嘌呤核苷三磷酸(ATP)水平下降,線粒體膜結(jié)構(gòu)改變,線粒體膜相崩解而導(dǎo)致細(xì)胞死亡。另有研究表明L-carnitine通過線粒體外膜上的卡尼丁脂酰轉(zhuǎn)移酶I和內(nèi)膜內(nèi)側(cè)的卡尼丁脂酰轉(zhuǎn)移酶Ⅱ作用,促使脂肪酸進(jìn)一步分解。L-carnitine能調(diào)節(jié)乙酰輔酶A/脂酰輔酶A的比值,從而激活丙酮酸脫氫酶復(fù)合體的活性,促進(jìn)葡萄糖的代謝[3]。臨床應(yīng)用L-carnitine輔助治療冠心病、心絞痛、心肌梗死合并心源性休克均具有一定療效,但是應(yīng)用L-carnitine在心肌肥厚及能量代謝方面的研究尚未見報(bào)道。因此本實(shí)驗(yàn)采用異丙腎上腺素(Isoproterenol,Iso)誘導(dǎo)的大鼠心肌肥厚模型,觀察L-carnitine對(duì)心肌肥厚及反映線粒體功能的線粒體膜電位的影響,初步探討L-carnitine改善心肌肥厚后在能量代謝方面的相關(guān)機(jī)制。
1 材料與方法
1.1 藥物、主要儀器與試劑 L-carnitine:沈陽東宇精細(xì)化工廠,批號(hào):101101,純度98%。乳酸LAC測(cè)定試劑盒、游離脂肪酸FFA測(cè)定試劑盒、總蛋白測(cè)定試劑盒(考馬斯亮藍(lán)法)、羥脯氨酸測(cè)定試劑盒:南京建成生物工程研究所。線粒體膜電位Jc-1試劑盒:江蘇碧云天生物技術(shù)研究所。激光掃描共聚焦顯微鏡(Leica sp5,德國Leica)
1.2 實(shí)驗(yàn)動(dòng)物、模型制備及分組 清潔級(jí),SD大鼠,♀♂各半40只,體質(zhì)量180~200 g,由遼寧醫(yī)學(xué)院實(shí)驗(yàn)動(dòng)物中心提供,動(dòng)物合格證號(hào):SCXK(遼)2003-0007。
大鼠隨機(jī)分為4組,每組♀♂各5只。① Iso組:按Rona等[4]方法略作修改,皮下注射(sc)Iso,以20、10 和 5 mg·kg-1·d-1劑量遞減 3 d,再以 3 mg·kg-1·d-1連續(xù) 7 d,每天腹腔注射蒸餾水 2 ml·kg-1;②空白組:以等量生理鹽水代替Iso處理,并以等量蒸餾水腹腔注射;③ L-carnitine組:sc Iso同時(shí)給予 L-carnitine,按 100 mg·kg-1劑量腹腔注射每天1次;④ Propranolol組:sc Iso同時(shí)給Propranolol,按50 mg·kg-1劑量腹腔注射每天1次。各組均持續(xù)8周,標(biāo)準(zhǔn)飲食飲水。術(shù)后正常飲食,定期觀察生長狀態(tài)。
1.3 測(cè)定心肌肥厚的指數(shù) 麻醉開胸,取心臟,稱全心濕重(heart wet weight,HW)及左心室濕重(left ventricle wet weight,LVW),計(jì)算心臟質(zhì)量指數(shù)(heart mass index,HMI=HW/BW,mg·kg-1)和左室質(zhì)量指數(shù)(left ventricular mass index,LVMI=LWH/BW,mg·g-1)。
1.4 測(cè)定心臟血流動(dòng)力學(xué)指標(biāo) 4組大鼠于停藥24 h后稱體重(body weight,BW),腹腔注射20%烏拉坦(5 ml·kg-1·d-1)麻醉。于頸部偏右側(cè)開縱行切口,分離右頸總動(dòng)脈,經(jīng)右頸總動(dòng)脈插入聚乙烯導(dǎo)管,用Pclab生物信號(hào)采集處理系統(tǒng),導(dǎo)管插入3~3.5 cm即可進(jìn)入左心室,穩(wěn)定5 min后測(cè)定大鼠心室收縮壓(left ventricular systolic pressure,LVSP)、心室舒張末壓(left ventricular end-diastolic pressure,LVEDP)及左室壓力變化最大速率(±dp/dtmax)。
1.5 Masson染色檢查心肌組織改變 取心尖組織迅速固定于10%甲醛中,常規(guī)石蠟包埋,制備石蠟切片,石蠟橫斷面連續(xù)切片5~6片,厚度約5 μm。切片常規(guī)脫蠟脫水,行Masson染色,光鏡下做常規(guī)觀察。
1.6 測(cè)定心肌生化指標(biāo) 取心尖組織100 mg,置入含0.9%生理鹽水0.9 ml的試管中,用勻漿器勻漿,得到組織勻漿。按試劑盒方法考馬斯亮藍(lán)法測(cè)定心肌總蛋白,測(cè)定心肌羥脯氨酸(hydroxyproline,Hpy)游離脂肪酸(free fatty acids,F(xiàn)FA)、乳酸(lactic acid,LAC)含量。
1.7 心肌細(xì)胞線粒體膜電位(mitochondrial membrane potential,MMP)的測(cè)定 按照文獻(xiàn)[5-6]的方法制備肥厚心肌的單個(gè)心室肌細(xì)胞,取(1~6)×105細(xì)胞,重懸于 0.5 ml KB 液(mmol·L-1:L-谷氨酸70,牛磺酸 20,KCl 40,EGTA 0.5,KH2PO420,MgCl23,D-glucose 10,HEPES 10,KOH 70)中保存。加入JC-1染色工作液,細(xì)胞培養(yǎng)箱中37℃孵育20 min。用JC-1染色緩沖液洗滌2次,再用適量JC-1染色緩沖液重懸。在線粒體膜電位較高時(shí),JC-1聚集在線粒體的基質(zhì)中,形成聚合物(J-aggregates),可以產(chǎn)生紅色熒光;在線粒體膜電位較低時(shí),JC-1不能聚集在線粒體的基質(zhì)中,此時(shí)JC-1為單體,可以產(chǎn)生綠色熒光。激光共聚焦顯微鏡檢測(cè)JC-1單體時(shí)把激發(fā)光設(shè)置為490 nm,發(fā)射光設(shè)置為530 nm得到紅色熒光圖像;檢測(cè)JC-1聚合物時(shí),把激發(fā)光設(shè)置為525 nm,發(fā)射光設(shè)置為590 nm觀察得到綠色熒光圖像,此兩通道重疊得到橘色圖像,并測(cè)得熒光強(qiáng)度。隨機(jī)選擇20個(gè)視野,每個(gè)視野約測(cè)4個(gè)細(xì)胞。通過對(duì)紅色和綠色熒光強(qiáng)度的比值計(jì)算出MMP的相對(duì)數(shù)值。
2 結(jié)果
2.1 L-carnitine對(duì)心肌肥厚大鼠心臟指數(shù)的影響
Iso連續(xù)注射10 d可引起大鼠HMI和LVMI兩指數(shù)增加50.2%和63.1%;L-carnitine和普萘洛爾能降低注射Iso后大鼠的HMI和LVMI,P<0.01,而與空白組比較,差異無顯著性(見Fig 1)。
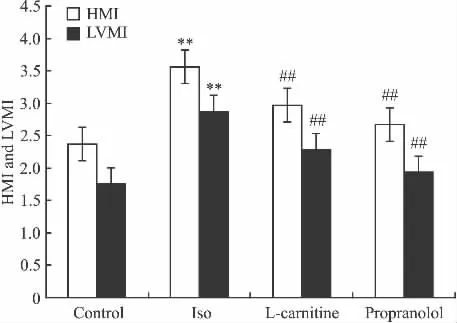
Fig 1 Effect of L-carnitine on heart mass index(HMI)and left ventricular mass index(LVMI)in myocardial hypertrophy induced by Isoproterenol(Iso)in rats(±s,n=8)
2.2 L-carnitine對(duì)心肌肥厚大鼠血流動(dòng)力學(xué)的影響 Iso連續(xù)注射10 d可引起大鼠-dp/dtmax和LVEDP高于空白組36%和50%,+dp/dtmax和LVSP也有所增加;L-carnitine和Propranolol能改善注射Iso后大鼠工作心臟的-dp/dtmax和LVEDP,分別降低了33.8%和21.4%(P<0.01)(Tab 1)。
2.3 L-carnitine處理后心肌組織病理學(xué)觀察 大體觀察見Iso組大鼠心臟體積較空白組明顯增大,L-carnitine組和propranolol組大鼠心臟增大不明顯。光鏡下,空白組(A)心肌細(xì)胞未見明顯肥大及壞死,無膠原纖維增生;Iso組(B)見心肌細(xì)胞變大,有灶性壞死,大量膠原纖維增生呈大斑片狀,病理改變多位于心尖部心內(nèi)膜下層;L-carnitine組(C)和prop-ranolol組(D)可見心肌細(xì)胞肥大程度較Iso組減輕,心肌纖維排列整齊,偶有點(diǎn)片狀壞死,膠原纖維增生較少(Fig 2)。
Tab 1 Effects of L-carnitine on hemodynamic parameters in myocardial hypertrophy induced by Isoproterenol(Iso)in rats(±s,n=8)
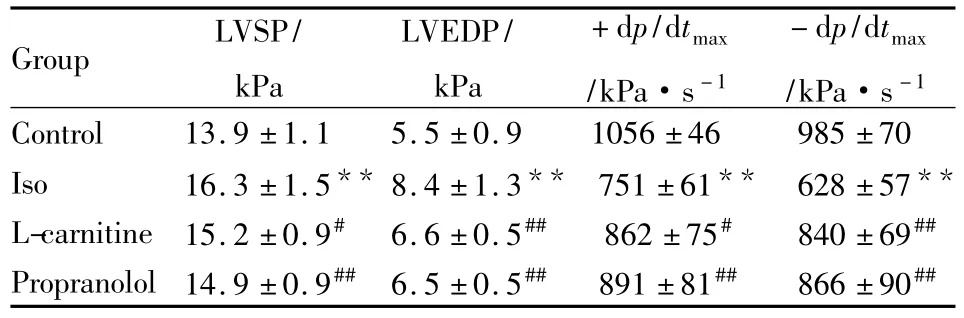
Tab 1 Effects of L-carnitine on hemodynamic parameters in myocardial hypertrophy induced by Isoproterenol(Iso)in rats(±s,n=8)
**P<0.01 vs control group;#P<0.05,##P<0.01 vs Iso group
Group LVSP/kPa LVEDP/kPa+dp/dtmax/kPa·s-1-dp/dtmax/kPa·s -1 Control 13.9 ±1.1 5.5 ±0.9 1056 ±46 985 ±70 Iso 16.3±1.5** 8.4±1.3** 751±61** 628±57**L-carnitine 15.2 ±0.9# 6.6 ±0.5## 862 ±75# 840 ±69##Propranolol14.9 ±0.9## 6.5 ±0.5## 891 ±81## 866 ±90##

Fig 2 Effect of L-carnitine on myocardial tissue pathogenic changes of myocardial hypertrophy induced by Isoproterenol(Iso)in rats
2.4 L-carnitine對(duì)大鼠左心室肌組織LD和FFA含量和Hpy的影響 Iso組HPY、LAC和FFA含量高于空白組53.7%、23.1%和30.2%,L-carnitine和Propranolol能降低注射Iso后大鼠的這3項(xiàng)指標(biāo),各自降低了15.8%、14.5%和16.9%,但 L-carnitine組在Hpy上與空白組還是有差異,propranolol組在FFA上與空白組有差異。表明L-carnitine可以降低心肌的Hpy含量,防止膠原沉積;降低心肌FFA和LAC含量,防止其在細(xì)胞中的堆積(Tab 2)。
2.5 L-carnitine對(duì)心肌細(xì)胞線粒體膜電位影響通過對(duì)紅色和綠色熒光強(qiáng)度的比值計(jì)算出線粒體膜電位的相對(duì)數(shù)值。與空白組比較,Iso組MMP降低了37.3%,差異具有統(tǒng)計(jì)學(xué)意義(P<0.01)。L-carnitine和propranolol組與Iso組相比MMP增高,差異有顯著性。表明L-carnitine可以在一定程度上起到保護(hù)心肌線粒體的作用(Fig 3,4)。
Tab 2 Effects of L-carnitine on contents of hydroxyproline(Hpy),lactic acid(LAC)and free fatty acids(FFA)in myocardial hypertrophy induced by Isoproterenol(Iso)in rats(±s,n=8)

Tab 2 Effects of L-carnitine on contents of hydroxyproline(Hpy),lactic acid(LAC)and free fatty acids(FFA)in myocardial hypertrophy induced by Isoproterenol(Iso)in rats(±s,n=8)
**P<0.01 vs control group;##P<0.01 vs Iso group
Group Hpy/μg·g-1Pro LAC/mmol·g-1Pro FFA/μmol·g-1Pro Control 0.41 ±0.039 0.39 ±0.036 195.87 ±24.71 Iso 0.63 ±0.028** 0.48 ±0.084** 254.26 ±25.11**L-carnitine 0.53 ±0.031## 0.41 ±0.035## 211.53 ±22.65##Propranolol 0.48 ±0.021** 0.46 ±0.015** 244.16 ±40.90**
3 討論
目前,MH已被公認(rèn)為是猝死、心力衰竭等心血管事件強(qiáng)有力的獨(dú)立危險(xiǎn)因素,因此,探索用于防治該病的藥物對(duì)與臨床用藥有重要的指導(dǎo)意義。Iso是一種人工合成的兒茶酚胺,連續(xù)皮下注射Iso可以起MH,操作簡單易于掌握,這一模型已被廣泛使用[7]。本次試驗(yàn)在此模型基礎(chǔ)上用L-carnitine干預(yù)治療,普萘洛爾為對(duì)照,目的在于觀察L-carnitine對(duì)Iso所致大鼠MH的保護(hù)作用。結(jié)果顯示:L-carnitine有改善心功能、降低重量指數(shù)、抗心肌細(xì)胞肥大的作用。Iso組在心臟重量指數(shù)、羥脯氨酸含量指標(biāo)中都較空白組有明顯增加,說明連續(xù)注射Iso確實(shí)可引起大鼠MH并伴有纖維化,對(duì)心肌組織切片的鏡下觀察也可以充分證實(shí)這一點(diǎn)。而MH伴纖維化也正是該組大鼠心臟舒張功能下降的直接原因。L-carnitine能改善Iso所引起的心臟重量指數(shù)增加和Hpy含量的增高,外部表現(xiàn)即為心功能的恢復(fù)。
有人認(rèn)為L-carnitine心肌保護(hù)作用的可能機(jī)制是減少心肌對(duì) ATP儲(chǔ)備的消耗,拮抗脂質(zhì)過氧化[8],從而在能量代謝、細(xì)胞保護(hù)、血管新生等多環(huán)節(jié)發(fā)揮作用。臨床觀察應(yīng)用L-carnitine輔助治療患者冠心病、心絞痛、心肌梗死合并心源性休克的療效觀察,均發(fā)現(xiàn)L-carnitine組心功能明顯改善,治療組療效明顯優(yōu)于對(duì)照組[9]。L-carnitine在大鼠缺血/再灌注中具有抗心律失常的作用且該作用可被肉堿脂酰轉(zhuǎn)移酶I(CPTI)抑制劑依托莫司(etomoxir)拮抗。提示我們L-carnitine的作用可能與促進(jìn)線粒體對(duì)脂肪酸的氧化有關(guān)[10]。本次試驗(yàn)的結(jié)果就 L-carnitine對(duì)Iso引起MH大鼠心肌組織中的FFA和LAC增多都有很好的調(diào)節(jié)作用,使FFA和LAC減少。這些變化心肌肥厚的能量代謝機(jī)制直接相關(guān),同時(shí)也不能排除其對(duì)線粒體保護(hù)所產(chǎn)生的作用。線粒體膜電位(MMP)是反映線粒體功能的重要生物能量學(xué)參數(shù)[11-12],控制線粒體呼吸率、ATP和ROS`生成,其電位值大小可以直接反映線粒體功能的變化。Iso組的線粒體膜電位明顯降低,L-carnitine明顯提高線粒體膜電位,對(duì)線粒體的具有保護(hù)作用,又在心肌肥厚能量代謝的另一方面起到了調(diào)節(jié)作用。
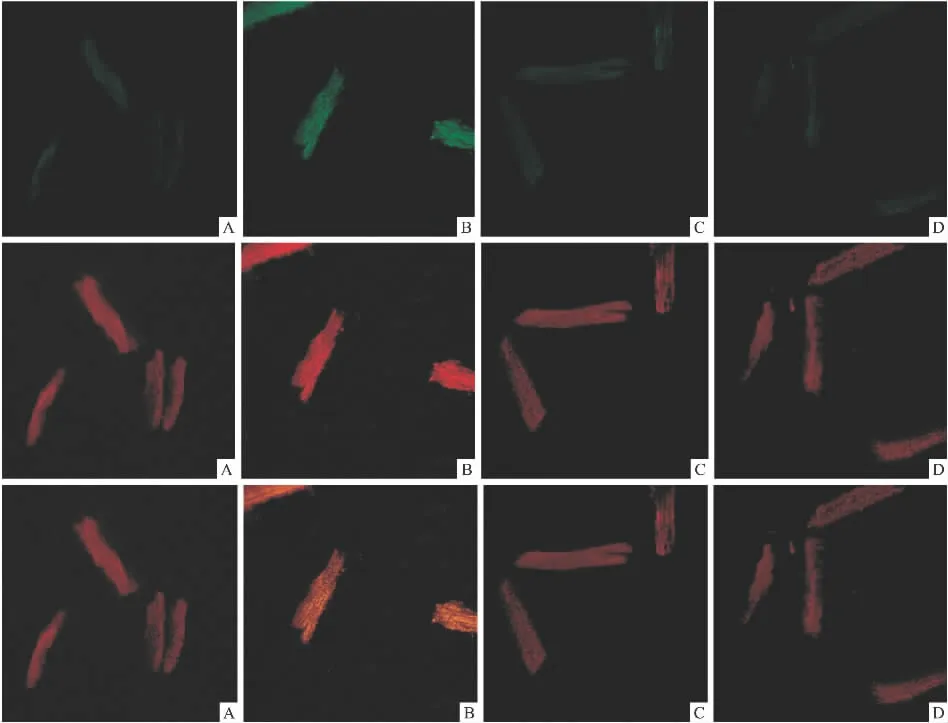
Fig 3 Effects of L-carnitine on mitochondrial membrane potential(MMP)of hypertrophic cardiomyocytes induced by Iso in rats
綜上所述,L-carnitine可以通過對(duì)肥厚心肌細(xì)胞能量代謝的調(diào)節(jié),起到改善Iso致大鼠心肌肥厚的作用,為臨床防治心肌肥厚提供新的思路。然而L-carnitine是如何作用達(dá)到保護(hù)線粒體的,其具體機(jī)制有待進(jìn)一步實(shí)驗(yàn)探討。

Fig 4 Quantitative results of JC-1 fluorescence as a marker for membrane potential changes(±s,n=5)
[1]Tang J M,Xie Q Y,Pan G D,et al.Mesenchymal stemcells participatein angiogenesis and improveheart function in ratmodel of myocardial ischemiawith reperfusion[J].Eur J Cardiothorac Surg,2006,30(2):353-61.
[2]時(shí)慧琦,殷仁富,張治宇,等.左卡尼汀對(duì)高血壓并發(fā)糖尿病大鼠心肌代謝和心功能的影響[J].心臟雜志,2009,21(2):165-9.
[2]Shi H Q,Yin R F,Zhang Z Y,et al.Influence of L-carnitine on myocardial metabolism and function in rats suffering from hypertension complicated by diabetes[J].China Heart J,2009,21(2):165-9.
[3]黃 潔,嚴(yán)文華.左卡尼汀對(duì)大鼠阿霉素心肌病的干預(yù)作用[J].蘇州大學(xué)學(xué)報(bào)(醫(yī)學(xué)版),2009,29(2):259-61.
[3]Huang J,Yan W H.Effect of L-carnitine on adriamycin-induced dilated cardiomyopathy in rats[J].Suzhou Univ J Med Sci,2009,29(2):259-61.
[4]Rona G,Chappel C I,Balazs T,et al.An infact-like myocardial lesion and other toxic manifestations produced by isoproterenol in the rat[J].Arch Pathol Lab Med,1959,67:443.
[5]Katoh H,Nishigaki N,Hayashi H.Diazoxide opens the mitochondrial permeabilitytransition pore and alters Ca2+transients in rat ventricular myocytes[J].Circulation,2002,105(22):2666-71.
[6]Saotome M,Katoh H,Satoh H,et al.Mitochondrial membrane potential modulates regulation of mitochondrial Ca2+in rat ventricular myocytes[J].Am J Physiol Heart Circ Physiol,2005,288(4):H1820-8.
[7]Kitagawa Y,Yamashita D,Ito H,Takaki M.Reversible effects of isoproterenol-induced hypertrophy on in situ left ventricular function in rat hearts[J].Am J Physiol Heart Circ Physiol,2004,287(1):H277-85.
[8]向到康,孫宗全,夏家紅,等.左-卡尼汀心停搏液對(duì)犬體外循環(huán)心肌的保護(hù)作用[J].中國藥理學(xué)通報(bào),2007,23(7):945-8.
[8]Xiang D K,Sun Z Q,Xia J H,et al.Myocardial protective effect of L-carnitine cardioplegia solution in canine undergoing cardiopulmonary bypass[J].Chin Pharmacol Bull,2007,23(7):945-8.
[9]陳冬梅,沈 濤,李玉潔,等.左卡尼汀治療老年冠心病心衰的療效觀察[J].中國現(xiàn)代醫(yī)藥雜志,2010,12(1):51-7.
[9]Chen D M,Shen T,Li Y J.Effect of L-carnitine on heart failure in the elderly patients with coronary heart disease[J].Mod Med J China,2010,12(1):51-7.
[10]Najafi M,Garjani A,Maleki N.Antiarrhythmic and arrhythmogenic effects of L-carnitine in ischemia and reperfusion[J].Bull Exp Biol Med,2008,146(2):210-3.
[11]Liedtke A J.The origins of myocardial substrate utilization from an evolutionary perspective:The enduring role of glucose in energy metabolism[J].J Mole Cell Cardiol,1997,29:1073-86.
[12]Marcil M,Ascah A,Matas J,et al.Compensated volume overload increases the vulnerability of heart mitochondria without affecting their functions in the absence of stress[J].J Mol Cell Cardiol,2006,41(6):998-1009.

