鈦基錫銻中間層上二氧化鉛電沉積過程的研究
姚穎悟, 王 超
(河北工業大學化工學院電化學表面技術研究室,天津 300130)
鈦基錫銻中間層上二氧化鉛電沉積過程的研究
姚穎悟, 王 超
(河北工業大學化工學院電化學表面技術研究室,天津 300130)
運用電化學手段研究了鈦基錫銻中間層上二氧化鉛的陽極電沉積過程。循環伏安曲線表明,二氧化鉛的電沉積經歷了晶核形成過程,通過恒電位階躍暫態曲線可知,二氧化鉛在Ti/SnO2-Sb2O5電極上的電沉積初始過程遵循擴散控制的瞬時成核和三維長大方式,且隨著過電位的增加,電極表面上晶核數增多。
二氧化鉛;電沉積;鈦基錫銻中間層
引 言
二氧化鉛電極由于具有較高的電化學活性、低廉的價格及良好的穩定性等特點而被廣泛地應用于電有機合成[1]和污水處理[2]等方面。為了改進電極性能,人們使用抗腐蝕能力強、熱膨脹性能與二氧化鉛接近的金屬鈦作為基體,將鈦基體進行表面粗化處理、再通過熱分解法制備錫銻氧化物(SnO2-Sb2O5)中間層[3],以防止在基體上形成不導電的鈍化層,進一步提高二氧化鉛涂層和基體的結合力、減少界面電阻和內應力。人們對在錫銻氧化物上制備二氧化鉛電極進行了大量研究,但是主要集中在電極制備與性能表征方面,對二氧化鉛在錫銻氧化物中間層上的電沉積過程尚不清楚。本文將運用電化學測試手段研究二氧化鉛在鈦基錫銻氧化物上的陽極電沉積過程。
1 實驗部分
1.1 鈦基錫銻中間層的制備
首先將2 cm×5 cm×0.1 cm的Ti基體用10%的NaOH溶液脫油、水洗后,用20%的草酸水溶液在80℃下蝕刻2 h,用去離子水沖洗干凈備用。將n(SnCl2·2H2O)和n(SbCl3)按9∶1溶于正丁醇中,加入幾滴濃鹽酸防止水解,刷涂在處理好的鈦基體上,100℃下烘干15 min,反復操作,直至將涂液全部涂完為止,然后在氧氣氣氛中500℃熱氧化2 h。
1.2 電化學測試
二氧化鉛電鍍溶液組成:0.2 mol/L Pb(NO3)2,0.6 g/L NaF,pH為2。以飽和甘汞電極(SCE)作為參比電極;以銅板作為輔助電極,以鈦基錫銻中間層作為電鍍基體(陽極),控制幾何面積為1 cm×1 cm。用CHI604D電化學工作站做循環伏安、恒電位階躍暫態和阻抗-電位測試,進行恒電位階躍暫態測定時,起始電位設定為開路電位,將電極脈沖到一個較高的過電位,記錄電流的變化。
2 結果與討論
2.1 循環伏安曲線
圖1是鈦基錫銻中間層在二氧化鉛電鍍溶液中的循環伏安曲線,電位掃描速度為10 mV/s,θ為25℃。
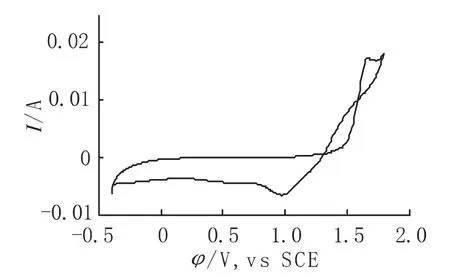
圖1 循環伏安曲線
由圖1中可以看出,正向掃描陽極分支電位大于1.5 V時,二氧化鉛開始在鈦基錫銻中間層上沉積,電極上有陽極電流流過,隨著電位的不斷正移,電流逐漸增大,并于1.67 V出現氧化電流峰,電位掃描至1.8 V后,反向回掃至1.6 V處,陰極電流曲線與陽極電流曲線發生相交,說明二氧化鉛的電沉積經歷了晶核形成過程。根據電結晶原理,金屬離子在基體上放電并形成金屬原子之后,必須聚集為尺寸大于臨界值的晶核才能繼續生長,而新相的形成需要一定的過電位。由于在陽極掃描期間成熟的晶核已經產生,當電位掃描由陽極方向變為陰極方向時,無需經歷成核過程便可繼續生長,因而表現為在同一電位下陰極掃描時的沉積電流大于陽極掃描時的沉積電流。隨著電位的負移,晶核變得不穩定,陽極電流終于被陰極電流所代替,并于0.9~1.2 V之間出現一個還原峰,該峰發生如下反應[4]:
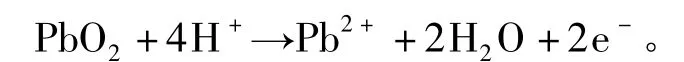
2.2 二氧化鉛在鈦基錫銻中間層上的成核機理
圖2為二氧化鉛在鈦基錫銻中間層上的恒電位階躍暫態曲線,從圖2可知,溶液中二氧化鉛電結晶經歷成核過程,曲線的特征,電結晶初期由于晶核的形成和新相的生長,電流逐漸上升,在電流達到最大值后出現電流衰減,此時可能發生生長中心的消失和新生長中心的再生。
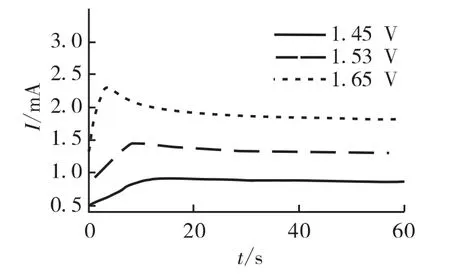
圖2 鈦基錫銻中間層上的恒電位階躍曲線
電結晶三維成核過程的瞬時成核和連續成核機理的無因次方程分別為[5]:
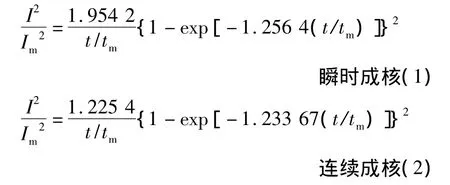
式中:I與Im分別表示電流密度與最大電流密度,A/dm2;t為時間,s;tm表示達到Im的時間,s。
對應于圖2,取圖2中數據利用式(1)和(2)繪制無因次曲線I2/Im2~t/tm,如圖3所示。
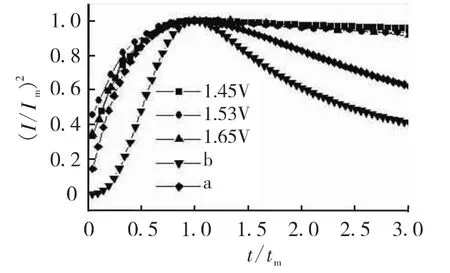
圖3 I2/Im2~t/tm無因次曲線
圖3曲線a表示式(1)所對應的瞬時成核理論曲線,曲線b表示式(2)所對應的連續成核理論曲線,由圖3可以看出,在不同的過電位下,二氧化鉛電沉積的無因次I2/Im2~t/tm實驗曲線更靠近瞬時成核的無因次曲線。表明二氧化鉛在鈦基錫銻中間層上的電沉積初始過程遵循擴散控制的瞬時成核和三維長大方式。
電沉積瞬時成核初期,電流與時間遵循下式:

其中,K=(8πCM/ρ)1/2;J 為電流密度,A/dm2;F為法拉第常數;n為電荷轉移數;D為擴散系數,cm2/s;N為晶核數密度,個/cm-2;M為分子的摩爾質量,g/mol;ρ為相對密度,g/cm3;c為摩爾濃度,mol/dm3;t為時間,s。取圖2曲線上升部分的數據,對應于圖2做I-t1/2的關系曲線,如圖4所示。從圖4表明,圖4中各曲線的線性較好。從式(3)可知,如果假定擴散系數D對電位的變化不顯著,則晶核數密度N與I-t1/2直線的斜率成正比,斜率越大表明成核數目越多。由圖4可知,隨著沉積電位的負移,曲線斜率不斷的增大,表明隨著電位的增加,電極表面上晶核數密度N增大。
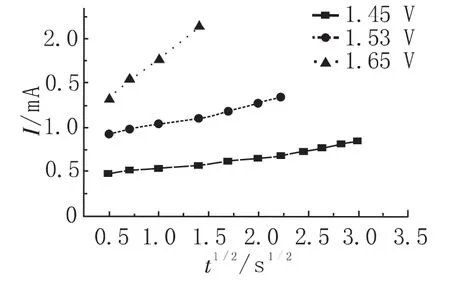
圖4 I-t1/2曲線
2.3 阻抗-電位曲線
用阻抗-電位曲線研究了二氧化鉛在鈦基錫銻中間層上的電沉積,圖5為鈦基錫銻中間層上二氧化鉛的阻抗-電位曲線圖,f為1 000 Hz,振幅5 mV。由圖5可以看出,當二氧化鉛未發生沉積時,阻抗和電流基本上不隨電位而變,電位正掃至1.5 V時,二氧化鉛開始沉積,阻抗顯著降低,但過了2.2 V之后,又隨電位的負移阻抗值略為增大。阻抗達到最小后又緩慢增大的原因可能與陽極過程控制步驟有關。在電位掃描的過程中,阻抗達到最小值之前,濃差極化還不顯著,主要是以電化學極化為主,此時電位越正電化學反應阻抗越小,隨著陽極過電位的增加,擴散極化逐漸上升為主導地位,最終成為控制步驟,此時阻抗便再隨過電位的增加而增大[6]。
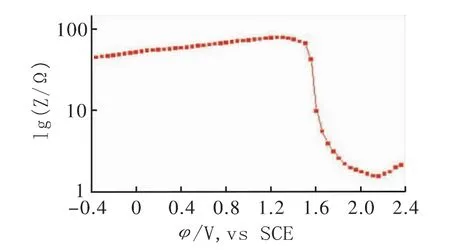
圖5 鈦基錫銻中間層上二氧化鉛的阻抗-電位關系
3 結論
1)二氧化鉛在鈦基錫銻中間層表面電沉積時,循環伏安曲線的陽極電流曲線與陰極電流曲線發生相交,說明二氧化鉛的電沉積過程經歷了晶核形成過程。2)由恒電位階躍暫態曲線可知,二氧化鉛在鈦基錫銻中間層上的電沉積初始過程遵循擴散控制的瞬時成核和三維長大方式。3)阻抗-電位曲線表明在二氧化鉛達到沉積電位時,阻抗迅速降低,但是隨著電位的繼續正移,阻抗略有增大,這與電極過程控制步驟有關。
[1]Serdar Abacia,Ugur Tamer,Kadir Pekmez,et al.Electrosynthesis of benzoquinone from phenol on α and β surfaces of PbO2[J].Electrochimica Acta,2005,50(18):3655-3659.
[2]Jose'M Aquino,Romeu C Rocha-Filho,Nerilso Bocchi,et al.Electrochemical degradation of the Acid Blue 62 dye on a β-PbO2anode assessed by the response surface methodology[J].J Appl Electrochem,2010,40(10):1751-1757.
[3]任秀斌,陸海彥,劉亞男,等.鈦基二氧化鉛電極電沉積制備過程中的立體生長機理[J].化學學報,2009,67(9):888-892.
[4]Velichenko A B,Amadelli R,Rnysh V A,et al.Kinetics of lead dioxide electrodeposition from nitrate solutions containing colloidal TiO2[J].Journal of Electroanalytical Chemistry,2009,632(1-2):192-196.
[5]Benjamin Scharifker,Graham Hills.Theoretical and experimental studies of multiple nucleation[J].Electrochimica Acta,1983,28(7):879-889.
[6]李俊華,費錫明,徐芳.2種有機添加劑對錫電沉積的影響[J].應用化學,2006,23(9):1042-1046.
Study of Lead Dioxide Electrodeposition Process on Ti/SnO2-Sb2O5Electrode
YAO Ying-wu,WANG Chao
(Electrochemical Surface Technology Research Laboratory,School of Chemical Engineering and Technology,Hebei University of Technology,Tianjin 300130,China)
Electrodepositon processes of lead dioxide on Ti/SnO2-Sb2O5intermediate layer was studied by electrochemical methods.Cyclic voltammetry curves indicated the presence of nucleation process in lead dioxide electrodeposition.According to i-t curves of potential step,it was revealed that the initial process of lead dioxide electrodeposition on Ti/SnO2-Sb2O5electrode would follow the mechanism of instantaneous nucleation and three dimensional growth with diffusion controll,and the amount of crystal nucleus on electrode surface would increase along with the increasement of overpotential.
lead dioxide;electrodeposion;Ti/SnO2-Sb2O5intermediate layer
TQ153.19
A
1001-3849(2012)02-0006-03
2011-01-27
2011-09-04
河北工業大學優秀青年科技創新基金項目(2011010);河北省高等學校科學技術研究優秀青年基金(Y2011104)

