超聲指導下心臟再同步化治療慢性心力衰竭的臨床研究
張悅 管小娟 凌鋒 楊繼東 厲朝喜
超聲指導下心臟再同步化治療慢性心力衰竭的臨床研究
張悅 管小娟 凌鋒 楊繼東 厲朝喜
目的 觀察超聲指導下心臟再同步化治療(CRT)對慢性心力衰竭(CHF)患者的臨床療效。方法 選擇2008年9月至2012年1月接受CRT的CHF患者35例,于術后1周、3個月、9個月對房室(AV)和室室(VV)間期進行優化,觀察術前及術后3、9個月的心功能分級、6min步行距離、QRS時間、左心室射血分數(LVEF)、左心室舒張末期內徑(LVEDd)及QRS波群起點距左心室12節段收縮速度峰值的時間標準差(Ts-12SD)、主動脈射血前期時間和肺動脈射血前期時間之差(IVMD)等指標的變化。結果與術前比較,35例患者平均術后心功能分級提高,6min步行距離增加,超聲指標如LVEF、LVEDd及Ts-12SD、IVMD等指標明顯改善(P<0.01),隨訪時間延長,獲益更顯著(P<0.01)。結論 在超聲指導下對AV、VV間期進行優化后行CRT可改善雙心室的同步性和心臟功能。
心臟再同步化治療 慢性心力衰竭 超聲心動圖 心功能
【 Abstract】 Objective To evaluate the echo-guided cardiac resynchronization therapy (CRT)for chronic heart failure (CHF)patients. Methods Thirty five CHF patients received CRT,the AVand VVintervals were optimized by echocardiography at 1 week,3 and 9 months after pacemaker implantation.The echocardiography,heart function classification,distance of 6 min walk test,QRS interval of all patients were evaluated during follow-up. Results The levels of NYHA functional class,6-min walk distance of 35 patients were improved during follow-up;the left ventricular ejection fraction(LVEF),left ventricular end-diastolic dimension(LVEDd),the standard deviation of regional time intervals in 12 left ventricular(Ts-12SD)and interventricular mechanical delay (IVMD)on echocardiography were significantly improved (P<0.01)after device implantation.The improvement of these parameters was more markedly in later than earlier time after implantation(P<0.01). Conclusion CRT can improve the biventricular mechanical synchrony and cardiac function with AV/VVdelay optimization guided by echocardiography.
【 Key words】 Cardiac resynchronization therapy Chronic heart failure Echocardiography Heart function
慢性心力衰竭(CHF)是多種器質性心臟病的終末階段,目前臨床上規范的抗心力衰竭藥物的應用已使CHF患者的生活質量和生存期得到較大改善,但心功能NYHA分級Ⅲ和(或)Ⅳ級的患者預后仍很差,1年病死率高達50%以上。心臟再同步化治療(CRT)作為慢性心力衰竭的一種非藥物治療策略,可以逆轉心室重構,提高LVEF,改善患者生活質量,并且能降低因心力衰竭所導致的住院率。本研究旨在分析CHF患者在超聲心動圖指導下進行房室、室間起搏間期優化,對CRT臨床療效的影響。
1 資料和方法
1.1 一般資料 選擇2008年9月至2012年1月在我院因CHF行CRT的患者35例,其中男30例,女5例,年齡42~78(58.21±11.52)歲。擴張型心肌病18例,缺血性心肌病17例。納入標準:(1)CHF患者,充分、合理的藥物治療效果不佳;(2)心功能NYHA分級Ⅱ~Ⅳ級;(3)QRS時間≥120ms;(4) 左心室舒張末期內徑(LVEDd)≥55mm;(5)左心室射血分數(LVEF)≤35%。CRT有反應者被定義為:(1)無心臟性猝死;(2)無因心力衰竭失代償住院;(3)心功能改善至少1級或以上。
1.2 方法
1.2.1 超聲心動圖檢查 于CRT術前及術后行超聲心動圖及組織多普勒檢測心臟同步性指標。所有超聲心動圖檢查由同一位有經驗的超聲醫生采圖和分析,采用美國GE公司VIVID7超聲診斷儀和M3S探頭,至少采集連續3個心動周期進行脫機分析。使用二維超聲心動圖,在胸骨旁長軸切面測量左心室舒張末期內徑(LVEDd)、左心室收縮末期內徑(LVESd)和左心房內徑(LAD),采集心尖四腔心切面,用Simpson法測量左心室舒張末期容積(LVEDV)、左心室收縮末期容積(LVESV),計算LVEF。左心室內機械不同步指標的測定:使用M型超聲采集心尖四腔、三腔和兩腔心切面彩色多普勒組織速度圖像,測量QRS波群起點距左心室12節段收縮速度峰值的時間(Ts),并計算其標準差(Ts-12SD);左右心室間機械不同步的指標測定:應用脈沖頻譜多普勒在心尖五腔心切面主動脈瓣口采集脈沖多普勒頻譜,測量QRS起始點距脈沖多普勒頻譜起始的時間即主動脈射血前時間(APEI),在大血管短軸切面肺動脈瓣口采集脈沖多普勒頻譜,測量肺動脈射血前時間(PPEI),兩者之差為心室間機械延遲(IVMD)。
1.2.2 心電圖檢查 于術前及術后運用常規體表心電圖,在Ⅱ、V1及V6選擇最寬QRS波群進行測量。測量3個QRS時間后取其平均值為最終測值(術后QRS時間定義為起搏信號至QRS波群終點的寬度)。
1.2.3 手術方法 CRT植入均采用左鎖骨下靜脈穿刺法,采用冠狀靜脈竇(CS)逆行法造影,了解冠狀靜脈及其分支的情況,結合術前組織多普勒結果,確定左心室電極導線的靶靜脈。右心房和右心室的電極導線常規放置于右心耳及右心室心尖部。
1.2.4 術后房室(AV)、室室(VV)間期優化 起搏器植入術后1周、3個月和9個月在超聲指導下進行AV間期和VV間期優化。優化時根據心電圖確保雙心室起搏后,進行AV間期優化,AV間期從80ms開始,每次遞增10ms,直至180ms,并確保雙心室起搏,每調整一次參數須等待5min再采集二尖瓣血流頻譜圖像,使二尖瓣血流頻譜的E峰和A峰波形完整,既不發生融合,也不發生“切尾”現象,以達到左心室最大舒張期充盈和二尖瓣反流面積(MRA)最小為標準。VV間期優化從-60~+60ms,每次調整5~10ms,同樣在調整參數5min后再采集圖像,采集左心室流出道血流頻譜,計算其速度時間積分(VTI),能將左心室同步性和心排量最大化的VV間期為最佳VV間期值。
1.3 隨訪 35例CHF患者分別于CRT植入前,植入后1周,植入后3、9個月評估心功能分級,測定QRS時間,6min步行距離,超聲測量LAD、LVEDd、LVESd、LVEF及Ts-12SD、IVMD等同步性指標。術后均進行規范的藥物治療。
1.4 統計學處理 應用SPSS 16.0統計軟件,計量資料以 表示,治療前后各指標比較采用配對t檢驗。
2 結果
2.1 治療結果 35例CHF患者均完成CRT起搏器植入,完成9個月或9個月以上的隨訪34例。29例術后較術前心功能至少改善1級或以上,患者自覺胸悶、氣促癥狀明顯好轉;6例患者CRT治療后無或低反應(17.1%),其中3例患者上述指標改善不明顯,2例患者因心力衰竭失代償再次住院,1例陳舊性心肌梗死合并腎功能不全患者于術后第4個月死亡。
2.2 超聲心動圖、心電圖及臨床指標的變化 見表1。
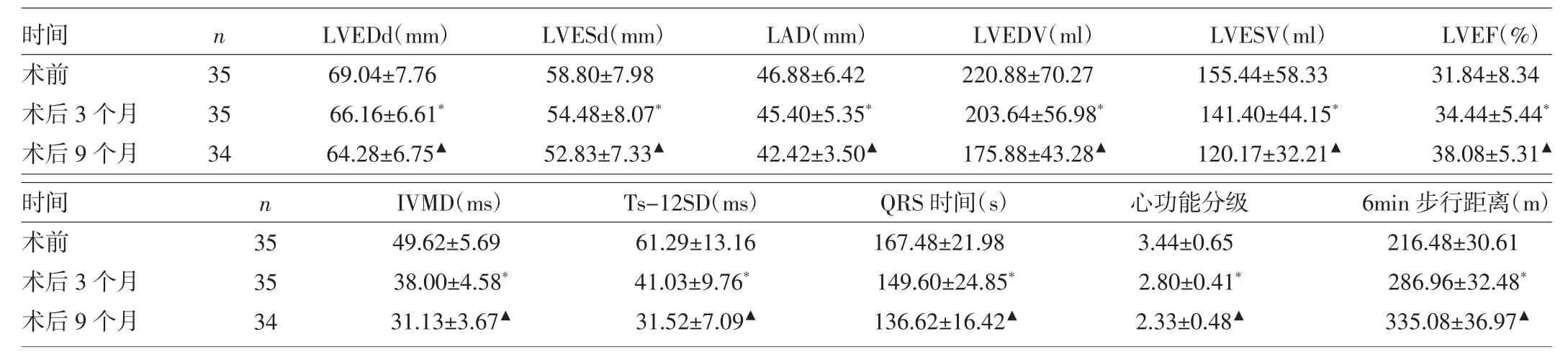
表1 CRT前后超聲心動圖、心電圖和臨床指標的比較
由表1可見,患者術后超聲心動圖、心電圖指標及心功能分級、6min步行距離與術前比較,差異均有統計學意義(均P<0.01);CRT后9個月各指標與3個月比較差異均有統計學意義(均P<0.01)。
3 討論
CRT治療CHF已逐漸被人們接受,雙心室同步起搏可以有效降低心力衰竭患者的病死率,與藥物治療相比,CRT可以降低全因病死率[1]。但臨床仍有20%~30%的CHF患者對CRT治療無反應[1-2]。目前認為,影響CRT療效的主要因素有:術前患者的心室機械不同步化程度、術中左心室電極放置的位置、術后起搏參數的設置及術后規范的抗心力衰竭治療等[3-4]。目前心力衰竭治療指南仍以心電圖QRS波群增寬作為不同步的主要指標之一,但QRS波群有時并不能準確地反應心臟機械不同步的程度。有研究表明QRS時間只能作為CRT入選的一個參考因素,對CRT療效的預測性并不高,心肌電活動的改善并不代表心室機械收縮不同步的改善,糾正心室機械運動的不同步較改善心臟電活動的不同步更為重要[5]。
超聲心動圖如M型超聲、頻譜多普勒及組織多普勒顯像是目前評估心臟機械同步性最常用的方法,也是最常用于預測CRT療效的手段之一。Ts-12SD是反應左心室內收縮不同步的指標之一,它被證實是左心室重構逆轉的獨立預測因子,Ts-12SD≥32.6ms預測CRT反應的敏感性和特異性可達94%和83%[6-7]。在無超聲心動圖定量評價延遲最明顯節段的情況下,盲目放置起搏器電極,尤其是左心室電極,往往不能達到預期的效果,這可能是部分患者術后無反應的重要原因。我們根據該結果,指導術中靶靜脈的選擇和左心室電極的放置,將左心室電極植入靠近收縮最慢的Tsmax節段,此法有效改善了左心室內的不同步,使得左心室能夠更有效地射血,使得CRT改善心功能的療效更顯著。
CRT術后采用AV、VV間期優化也是本研究中患者取得良好療效的重要原因。有研究表明術后心臟超聲優化能夠減少CRT無反應者數量,且可以補償左心室導線植入部位不佳帶來的影響,特別是對心房顫動患者可增加其對CRT的反應[8]。AV優化使舒張期左心室充分充盈且充盈后即出現左心室收縮,在左心室完全充盈的情況下盡量縮短AV間期,從而減少舒張期功能性反流保證最大每搏量;VV優化通過左右心室電激動順序進一步增加收縮同步性,使室間隔與左心室各節段運動不協調性進一步改善,主動脈前向血流時間積分也獲得最大。
我們的研究結果顯示,CHF患者經超聲指導下優化CRT后,心功能分級均有不同程度的改善,在隨訪過程中,可見LVEDd、LVESd、LAD、LVEDV、LVESV減小,LVEF增高,左右心室間不同步指標IVMD及左心室內不同步指標Ts-12SD差值減小,6min步行距離延長,QRS時間明顯變窄,且隨訪時間延長,獲益更明顯。入選的患者中有10例心房顫動患者,其中6例為持續性心房顫動,4例為陣發性心房顫動,這部分患者選用雙心室VVI起搏,同樣也取得了良好的治療效果,且有3例陣發性心房顫動患者在隨訪過程中未再發生心房顫動。2008年的一項多中心研究,入選了126例心力衰竭合并持續性心房顫動的患者,研究發現心房顫動患者CRT術后臨床癥狀及左心室逆重構指標均有明顯改善,且與竇性心律組相比差異無統計學意義[9]。同樣發表于2008年的一項有關心房顫動患者CRT的薈萃分析表明,心房顫動患者可以從CRT中得到與竇性心律患者相似的益處[10]。另有1例缺血性心肌病、糖尿病腎病、腎功能不全的患者在3個月時因腎功能衰竭,并再次發生心肌梗死死亡。目前還沒有大型的臨床研究說明腎功能不全對CRT療效的影響,術前血肌酐水平達到多少會影響CRT的應答尚沒有明確的定論,但現有的研究提示,術前血肌酐水平>1.4mg/dl,CRT術后的病死率高,聯合終點風險增加[11]。慢性腎功能不全可能會影響CRT的應答,是否入選CRT治療需慎重考慮。
目前,CRT治療已成為CHF的一種有效治療方法,植入術前應按照指南和建議選擇適應證,規范做好植入手術,術后根據患者具體情況做好參數優化及隨訪管理,這對提高CRT的療效有重要影響。本研究在超聲指導下評估心室間及心室內的同步性,完成CRT術后參數優化,提高了CRT的療效。
[1]Cleland J G,Daubert J C,Erdmann E,et al.The effect of cardiac resynchronization on morbidity and mortality in heart failure[J].N Engl J Med,2005,352(15):1539-1549.
[2]Dtaz-Infante E,Mont L,Leal J,et al.Predictors of lack of response to resynchronization therapy[J].Am J Cardiol,2005,95 (12):1436-1440.
[3]Birnie D H,Tang A S.The problem of non-response to cardiac resynchronization therapy[J].CurrOpin Cardio,2006,21(1):20-26.
[4]駱志玲,郭濤,顧云,等.超聲心動圖在心臟再同步化治療優化中的應用研究[J].臨床心血管病雜志,2008,24(12):889-893.
[5]Brandt R R,Reiner C,Arnold R,et al.Contractile response and mitral regurgitation after temporary interruption of long-term cardiac resynchronization therapy[J].Eur Heart J,2006,27(2):187-192.
[6]Yu C M,Zhang Q,Fung J W,et al.A novel tool to assess systolic asynchrony and identify responders of cardiac resynchronization therapy by tissue synchronization imaging[J].J Am Coll Cardiol, 2005,45(5):677-684.
[7]Yu C M,Fung J W,Chan C K,et al.Comparison of efficacy of reverse remodeling and clinical improvement for relatively narrow and wide QRS complexes after cardiac resynchronization therapy for heart failure[J].J Cardiovase Electrophysiol,2004,15(9):1058-1065.
[8]StockburgerM,Fateh-MoghadamS.Optimizationofcardiac resynchronization guided by Doppler echocardiography:haemodynamic improvement and intraindividual variability with different pacing configurations and atrioventricular delays[J].Europace, 2006,8(10):881-886.
[9]Tolosana J M,Hernandez Madrid A,Brugada J,et al.Comparison of benefits and mortality in cardiac resynchronization therapy in patients with atrial fibrillation versus patients in sinus rhythm (Results of the Spanish Atrial Fibrillation and Resynchronization [SPARE]Study)[J].Am J Cardiol,2008,102(4):444-449.
[10]Upadhyay G A,Choudhry N K,Auricchio A,et al.Cardiac resynchronization in patients with atrial fibrillation:a meta-analysis of prospective cohort studies[J].J Am Coll Cardiol,2008, 52(15):1239-1246.
[11]Shalaby A,El-Saed A,Voigt A,et al.Elevated serum creatinine at baseline predicts poor outcome in patients receiving cardiac resynchronization therapy[J].Pacing Clin Electrophysiol,2008, 31(5):575-579.
Echo-guided cardiac resynchronization in treatment of chronic heart failure patients
ZHANG Yue,GUAN Xiaojuan,LING Feng,et al.
Department of Cardiology,Zhejiang Hospital,Hangzhou 310013,China
2012-11-20)
(本文編輯:馬雯娜)
310013 杭州,浙江醫院心內科
厲朝喜,E-mail:liyangguai@sohu.com

