原發性肝細胞癌伴PVTT患者肝切除術的預后及影響因素
周云鵬,吳力群
(青島大學醫學院,山東青島266003)
原發性肝細胞癌(HCC)是最常見的惡性腫瘤之一,因其發生最早和最常見的轉移是肝內血行播散,癌組織經常可以侵入門靜脈而形成門靜脈癌栓(PVTT)[1]。本文回顧性分析了60例HCC伴PVTT者肝切除術的預后情況,并對其影響因素進行了分析。現報告如下。
1 資料與方法
1.1 臨床資料 1997年1月~2009年12月在我院連續實施的HCC肝切除術患者共681例,除失訪47例、術后30 d內死亡10例、合并肝靜脈癌栓10例(R0切除9例,非R0切除1例)外余614例患者均進入回顧性分析,男515例(83.9%)、女99例(16.1%),男女比例 5.2∶1;年齡 14~82歲,平均54.1歲;并PVTT者60例(PVTT組,腫瘤位于左葉29例、位于右葉26例、左右葉均有5例),無PVTT者554例(無PVTT組)。PVTT診斷標準:術前影像學檢查結合術中所見有門靜脈及其分支癌栓,其發生部位達門靜脈主干(A型)9例(15.0%)、僅侵達門靜脈左干或右干(B型)35例(58.3%)、位于肝葉或段門靜脈內(C型)16例(26.7%)。
1.2 手術方法、隨訪及復發后治療 兩組均行根治性肝切除術,其中PVTT組RO者53例、非RO者7例,無PVTT組RO者539例、非RO者15例。術后3個月內每月復查1次肝臟超聲和血清甲胎蛋白(AFP),對于手術切緣<1cm,伴有衛星灶和血管侵犯者于術后3~4周內施行經導管肝動脈化療栓塞術(TACE);以后每3個月復查1次,懷疑復發時行上腹部CT、肺部CT和(或)肝動脈碘油造影確診。隨訪日期截止至2011年12月31日或死亡時間,中位隨訪時間35.8(1.3~168.7)個月。
1.3 統計學方法 采用SPSS13.0統計軟件。臨床、手術和病理單因素分析用χ2檢驗和t檢驗。采用Kapian-Meier法和Log-rank檢驗分析生存情況,采用Cox風險回歸模型行預后多因素分析。P≤0.05為差異有統計學意義。
2 結果
2.1 預后 614例患者中,無PVTT組術后1、2和5年總生存率(OS)分別為87.7%、76.0%和47.3%,PVTT組分別為50.0%、26.7%和11.6%,組間比較有顯著差異(P=0.000);無PVTT組無病生存率(DFS)分別為75.9%、59.2%和36.6%,PVTT組分別為31.9%、17.9%和9.6%,組間比較有顯著差異(P=0.000),見圖1。PVTT組A型患者術后1、2和5年生存率分別為11.1%、0和0,B型患者分別為48.6%、22.9%、5.7%,C型患者分別為68.8%、43.8%和13.7%,各型間比較均有顯著差異(P均=0.000),見圖2。R0切除和非R0切除者的術后1、2和5年生存率分別為52.8%、30.2%、13.2%及28.6%、0、0(P=0.007),見圖3。
2.2 PVTT患者1年生存率的影響因素 在PVTT組,非R0切除、大肝癌和手術切緣<0.5cm者的OS顯著降低(Log-rank檢驗,P<0.05);Cox回歸風險模型分析結果表明,非R0切除是影響PVTT組患者生存的獨立危險因素,危險比(HR)為2.799、95%CI為1.220~6.424(P<0.05)。見表1。

圖1 兩組患者肝切除術后生存曲線

圖2 PVTT組三型患者的術后生存曲線
3 討論
PVTT的形成是進展期肝癌最常見的病理特征之一。日本肝癌研究組的研究證實,HCC患者尸檢中PVTT的發生率為62%,而術中PVTT發生率僅為14%[2]。本組病例PVTT的發生率為9.8%,且PVTT是肝癌術后復發和預后較差的主要原因。根據第7版肝癌美國腫瘤聯合會(AJCC)分期,單個或多發腫瘤,無論大小,侵及門靜脈的主要屬支或肝靜脈定為T3b期。Inoue等[3]研究顯示,患者一旦出現PVTT,特別是門靜脈主干及左、右干的癌栓,會在短期內導致門靜脈壓力增高,引起大量腹水甚至上消化道出血等嚴重并發癥,嚴重影響患者的預后和生存質量。伴PVTT的HCC患者肝切除術后的預后極差。周儉等[4]研究顯示,381例伴 PVTT的HCC患者肝切除術后總的1年生存率為47%。本研究結果顯示,PVTT組肝切除術后的OS及DFS均顯著低于無PVTT組,且A型患者術后1、2和5年生存率顯著低于B型及C型患者。表明癌栓位于門靜脈主干的HCC患者其預后最差,應視為肝切除的相對禁忌證;而癌栓侵達門靜脈左、右干的HCC患者作為肝切除手術指征時應當慎重,需要結合患者全身情況綜合考慮。林新居等[5]研究表明,腫瘤和癌栓一并切除者的術后生存率明顯高于從肝斷面門靜脈取癌栓者,亦高于門靜脈切開取栓者(P=0.004)。提示對伴有PVTT,但癌栓未侵及門靜脈主干或左、右干的患者應盡可能行解剖性肝切除術,以提高患者術后生存期。
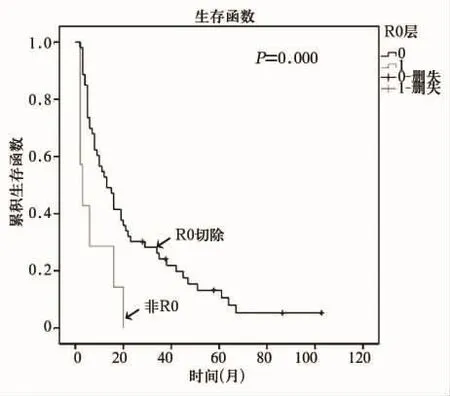
圖3 R0切除及非R0切除術后患者的生存曲線
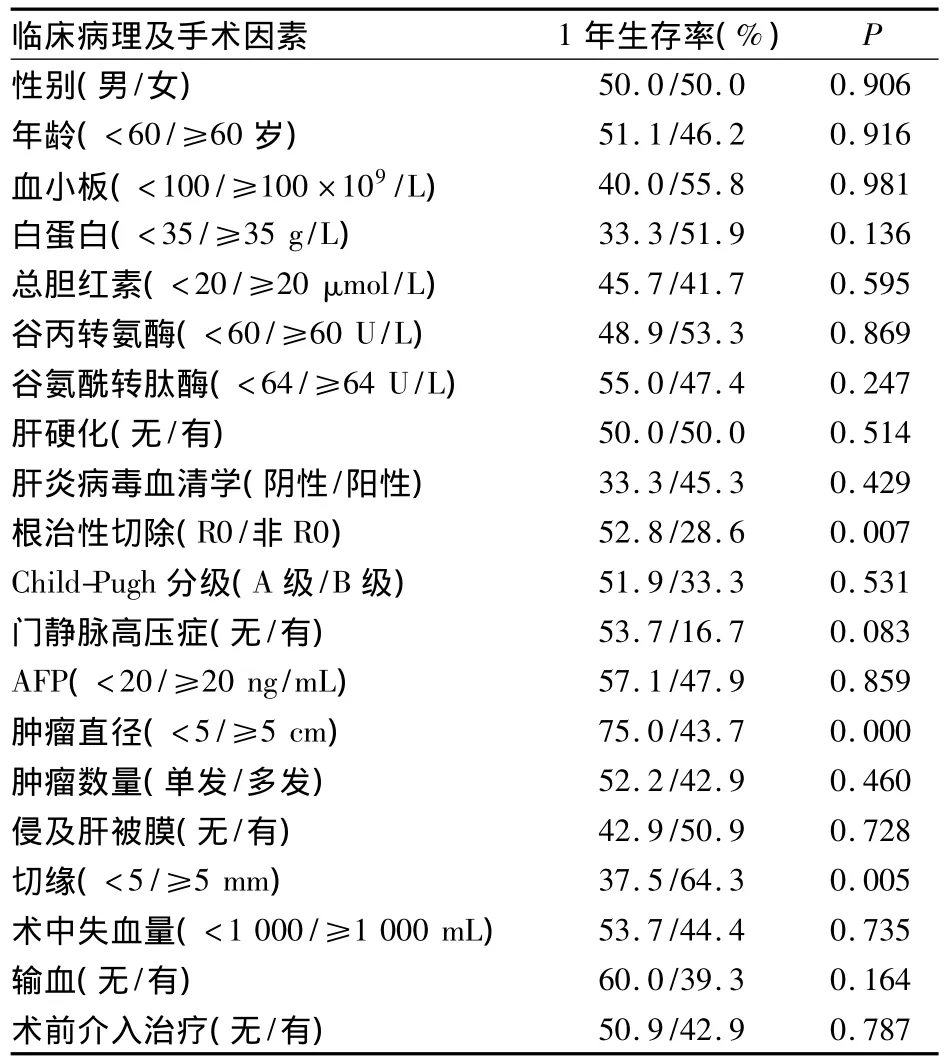
表1 影響PVTT患者1年生存率的臨床病理及手術因素
早在1978年AJCC即首次引入殘留腫瘤分級(R 分級)概念,1994年Hermanek等[6]詳細闡述了R分級的定義及與預后的關系。R0切除是治愈實體惡性腫瘤的標志性手術,指腫瘤切除后切緣肉眼無瘤、顯微鏡下亦無瘤。原發性HCC的生物學具有特殊性,早期侵犯肝內血管、導致PVTT形成是其獨特的生物學特性之一,對其行R0切除的正確認識是必要的。我們以往研究結果證明,手術切緣病理陽性和姑息切除是HCC患者非R0切除的重要因素之一[7]。
筆者體會,對于 HCC(特別是伴有 PVTT的HCC)患者,滿足以下條件方應視為R0切除:手術切緣病理陰性、腫瘤完整切除、無肉眼可見肝內血管癌栓、區域淋巴結無轉移、無肝外轉移、術后血清AFP值降至正常和術后1~2個月行TACE檢查陰性[7]。本研究結果顯示,PVTT組 R0切除者生存率顯著高于非R0切除者,非R0切除是影響伴PVTT的HCC患者生存的獨立危險因素。提示對伴PVTT的原發性HCC患者行R0切除可使其獲得長期生存,而非R0切除的預后未必優于其他姑息性治療;對于不可獲得R0切除的病例,應采用非手術療法,減少不必要的創傷。
綜上所述,伴PVTT(尤其A型)的HCC患者的預后差,非R0切除是影響其術后生存的獨立危險因素。
[1]劉宇斌,簡志祥,區金銳,等.原發性肝癌合并門靜脈癌栓的外科治療方式選擇[J].中華外科雜志,2005,43(7):436-438.
[2]Liver Cancer Study Group of Japan.Primary liver cancer in Japan:clinicopathologic features and results of surgical treatment[J].Ann Surg,1990,211(3):277-287.
[3]Inoue Y,Hasegawa K,Ishizawa T,et al.Is there any difference in survival according to the portal tumor thrombectomy method in patients with hepatocellular carcinoma[J].Surgery,2009,145(1):9-19.
[4]周儉,樊嘉,湯釗猷,等.肝細胞癌合并門靜脈癌栓術后時間依賴性的預后因素分析[J].中華醫學雜志,2006,(42):3005-3008.
[5]林新居,湯陽陽,彭民浩,等.原發性肝癌合并門靜脈癌栓的手術療效分析[J].中國普外基礎與臨床雜志,2012,19(4):382-386.
[6]Hermanek P,Wittekind C.Residual tumor(R)classification and prognosis[J].Semi Surg Oncol,1994,10(1):12-20.
[7]吳力群,邱法波,張順,等.原發性肝細胞癌R0切除標準的探討[J].中國實用外科雜志,2011,31(11):1027-1030.

