汽油替代燃料燃燒過程中多環芳烴生成的化學動力學模型
鄭 東 張云鵬 鐘北京,*
(1清華大學航天航空學院,北京100084;2國家節能中心,北京100045)
1 引言
PAHs是指含有兩個及兩個以上苯環的碳氫化合物.這類化合物不僅有很強的三致(致癌、致畸、致突變)作用,而且還是生成劇毒物質二惡英1和碳煙顆粒2的前驅物.內燃機污染物排放是PAHs的重要來源之一,尤其是缸內直噴式(GDI)汽油機.駱路勝等3的實驗研究表明,GDI汽油機的PAHs排放總量遠高于進氣道噴射汽油機.要控制汽油機PAHs的排放,必須深入理解汽油燃燒過程中PAHs的生成機制.因此,發展汽油替代燃料燃燒及其PAHs生成的化學動力學模型顯得尤為重要.
雖然關于PAHs生成的詳細機理至今還不太明確,但是相關的研究還是取得了一定的進展.Wang等4-7用脫氫加乙炔(HACA)反應發展了PAHs的HACA生成機理,并在C2(乙烯、乙炔)預混火焰中進行了驗證.鐘北京等8提出簡化的HACA機理,并與正庚烷燃燒機理結合,用于研究層流預混正庚烷火焰的PAHs生成.然而,HACA機理并不完善,在某些工況下HACA機理對于芘(A4)濃度的預測過小.9Marinov等10認為,共振穩定自由基的復合反應是PAHs生成的重要反應路徑,并在HACA機理基礎上發展了新的PAHs機理.該PAHs模型較好地預測了甲烷、乙烷、正丁烷等10,11預混火焰的實驗結果.但是,該模型只適用于三個苯環及以下的PAHs生長.D?Anna等12,13的研究也表明共振穩定自由基復合反應是PAHs生成的主要路徑,并進一步擴展了這類反應,發展了適用于乙烯和甲烷擴散火焰的PAHs生成機理.Slavinskaya等14,15綜合分析了上述所有的PAHs生成路徑,并進一步補充了更多反應路徑,提出了應用于甲烷、乙烯層流火焰和乙烷、乙炔擴散火焰的詳細的PAHs生成機理.該機理中PAHs達到了五個苯環.
上述PAHs生成機理都是基于小碳氫燃料提出來的.對于大鏈烷烴燃料的PAHs生成機理普遍認為,大鏈烷烴首先斷鍵生成小的不飽和碳氫化合物(C2H4、C2H2、C3H3等),然后這些不飽和小碳氫化合物通過上述小碳氫燃料的PAHs生成機理生成PAHs.描述大碳氫燃料PAHs生成的機理也有少量研究,如Marchal等16提出了正癸烷、異辛烷、正庚烷三組分碳氫燃料PAHs機理(154組分、850反應),以及Raj等17發展了包含正癸烷、異辛烷、正庚烷和甲苯四組分汽油替代燃料燃燒及其PAHs生成的機理(231組分、1350反應).由于Marchal機理包含的組分不能夠很好地反映汽油的燃燒特性,而Raj機理的規模較大不太適用于多維內燃機燃燒的數值模擬.因此,本文在考慮汽油燃燒以及PAHs生成的基礎上,提出規模相對較小的異辛烷/正庚烷/乙醇/甲苯/二異丁烯多組分汽油替代燃料PAHs的化學動力學機理模型.
2 PAHs子機理
在之前的研究工作中,我們提出了異辛烷/正庚烷/乙醇三組分燃料著火機理,18進而發展了三組分燃料氧化機理.19該模型能夠再現單組分或多組分汽油替代燃料的著火和燃燒特性.本文在此基礎上構建一個多組分汽油替代燃料燃燒及其PAHs生成的化學動力學機理模型.在這個模型中除著火和燃燒機理外,還要考慮以下幾個涉及PAHs生成的機理.
2.1 小碳氫組分機理
不飽和的小碳氫分子(C2-C4)是PAHs生成的核心組分,能否正確預測這些組分直接影響到PAHs的生成.因此,首先需要進一步修正和補充多組分機理中的小碳氫組分反應.
考慮到C2H2在HACA機理中的重要性,以及多組分汽油替代燃料機理對于乙炔(C2H2)預測的不準確性,我們對多組分機理中的C2H2組分進行了靈敏度分析,得到了對C2H2消耗和生成影響最大的兩個反應R1和R2.其中R1對C2H2消耗很重要,而R2對C2H2生成很重要.因此,為了增加C2H2產率,我們對反應R1和R2的動力學參數A(指前因子)分別減小和增加了一倍.與此同時,還補充了乙烯(C2H4)脫氫生成C2H2的重要中間反應R3.

Slavinsksya等15提出的詳細乙烯、乙炔擴散火焰PAHs生成機理中,不飽和C2-C4組分的反應機理較為全面.因此通過對其機理中的不飽和C2-C4組分做產率分析和靈敏度分析,找出了對這些組分生成和消耗起關鍵作用的反應(見Supporting Information中的R4-R12).其中丙炔基(C3H3)和n-C4H3自由基是形成第一個苯環的重要組分,下面就分析第一個苯環形成的反應.
2.2 單環組分——苯機理
對于第一個苯環的形成,本文考慮四種生成路徑.前兩種反應路徑是Wang和Frenklach7提出的HACA機理,即n-C4H3或者通過與C2H2的反應R13生成苯環結構的c-C6H4,然后進一步通過反應R14生成苯基(A1―),或者直接通過R15脫氫加C2H2生成A1―.
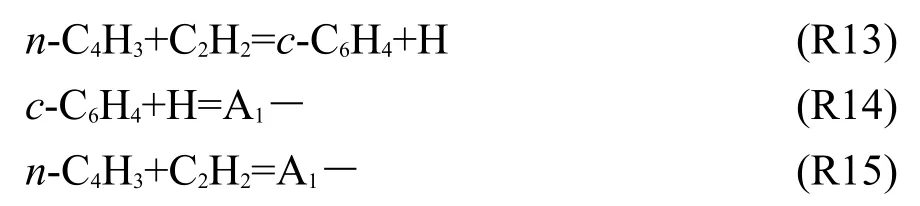
Miller20的研究表明,兩個C3H3的復合反應R16是生成苯(A1)的重要反應路徑,這個反應幾乎采用了所有的PAHs機理模型,因此,本文把該反應作為生成苯環的第三種路徑.

本文考慮的苯環生成的第四種路徑是環戊二烯基(C5H5)和甲基(CH3)的反應R17.

Lindstedt和Rizos21對這一反應做了詳細的討論.Slavinskaya等15的PAHs機理中就采用這一反應,取其動力學參數為k=1.00×1018exp(-30000/T).為了更準確地預測A1,本文將其動力學參數修正為k=1.00×1017exp(-30000/T).C5H5不僅是上述A1生成的重要組分,也是下面會討論的萘(A2)生成的關鍵物質.因此,需要引入生成C5H5的以下兩個重要反應R18和R19.

在Slavinskaya等提出的甲烷、乙烯層流火焰PAHs機理14和乙烷、乙炔擴散火焰PAHs機理15中均采用了這兩反應.在五組燃料的甲苯子機理中已經包含詳細的A1氧化和熱解反應.所以,這里只用引入A1和A1―相互轉化的反應R20(M代表第三體).

2.3 雙環組分——萘機理
上述反應生成A1和A1―后,會通過HACA機理不斷長大.通過對Wang和Frenklach7的HACA機理進行A1到A2的反應路徑分析,提取了主要組分和關鍵反應(見Supporting Information中的R21-R35).圖1給出了A1―通過HACA機理至A2的生長過程.
與此同時,A1―也可以通過與乙烯基乙炔(C4H4)反應,然后異構化生成A2,這一過程如圖2所示.其總包反應為:

除了這兩種生成A2的路徑外,Marinov等10提出了一個由C5H5生成A2的反應路徑R37.

對于這個反應Murakami等22和Kislov和Mebel23分別通過實驗和理論計算進行了研究.與此同時,在Slavinsksya等15的PAHs機理中也采用了類似的反應R38,并給出了其反應動力參數.

本文也采用這兩反應R37和R38,其動力學參數參考Slavinskaya的PAHs機理,且把指前因子A降低了1.5倍,使其能夠更準確地預測A2的生成量.進一步還需要補充A2消耗的重要反應R39-R42,其中R39-R41是A2和萘基(A2―)相互轉化的主要反應,而反應R42是A2斷開其中一個苯環,生成單環組分的反應,而且是不可逆反應.
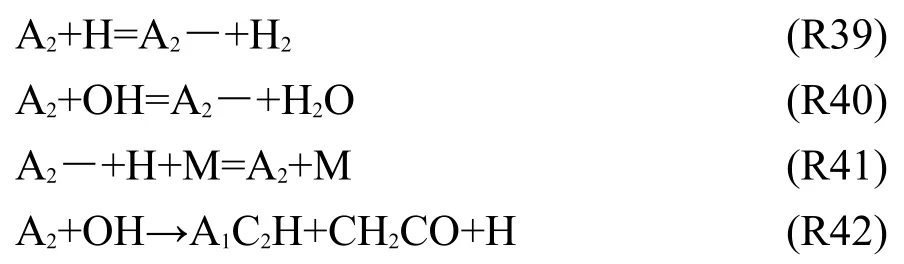
這些反應均來源于Wang和Frenklach7的PAHs機理.
2.4 三環組分——菲機理
關于菲(A3)和菲基(A3―)的生成的路徑可分為三類.第一類是上述生成的A2和A2―組分通過HACA機理長大,生成A3.這一類型反應在Wang和Frenklach7的PAHs機理中有較為詳細的描述.通過靈敏度和路徑分析,提取出A2通過HACA機理生成A3的關鍵組分和反應(見Supporting Information中的R43-R50),這一過程與圖1類似.
第二類是A2或A2―與C4組分直接生成三環物質(A3、A3―)的反應R51和R52.



圖1 通過HACA機理由A1―生成A2Fig.1 FormationA2fromA1―through HACAmechanism
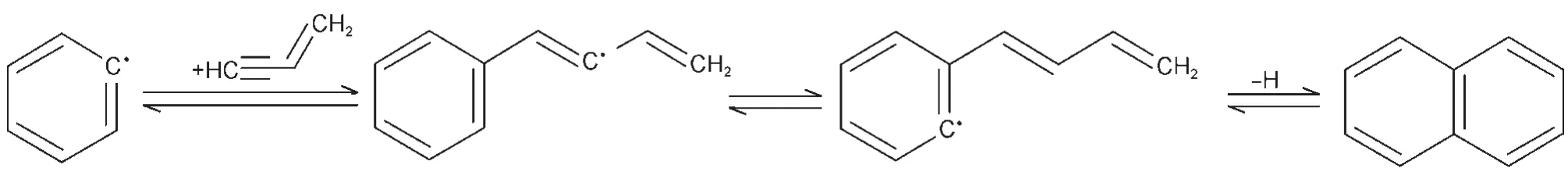
圖2 通過A1―加成C4H4生成A2Fig.2 FormationA2through C4H4addition toA1―
Appel等9的C2層流預混火焰碳煙生成的動力學模型中就采用了R51,其靈敏度分析也表明反應R51對于A3生成有一定的貢獻.Slavinskaya等15的分析表明,反應R52在整個溫度范圍內都是生成A3―的重要反應路徑.
第三類是兩個單環組分反應生成A3.

Appel等9的研究表明,反應R53對于A3靈敏度系數最大.Slavinskaya等14,15的PAHs模型也都采用了這類反應.同樣,還需要引入A3消耗的如下反應:
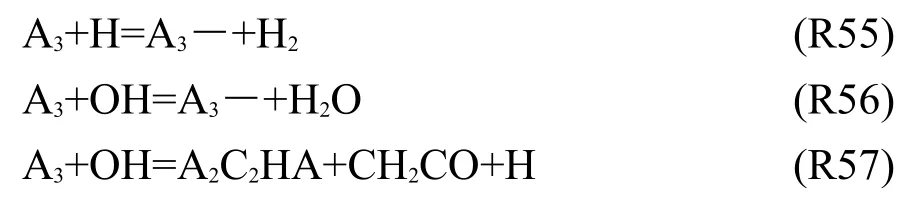
R55和R56是A3和A3―之間的反應,R57是A3開環,生成兩環組分和小分子組分的反應.
2.5 四環組分——芘機理
和以上分析一致,芘(A4)的反應主要包括生成和消耗兩部分.對于A4的生成,Wang和Frenklach7以及Appel等9的PAHs機理都只采用了如下HACA生成反應:

然而這兩機理對A4的預測都過低.因此,本文在采用這一反應時,對其反應動力學參數A擴大了三倍.同時還增加了在Slavinskaya等15的PAHs機理中所采用的另一種生成A4的反應R59和R60.

A4的消耗反應也包括兩類.一類是A4和A4―之間的反應R61-R63:
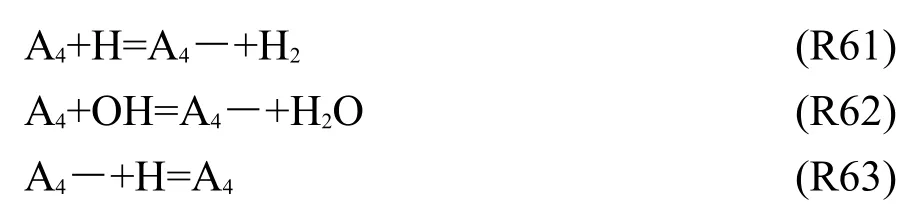
另一類是A4斷開其中一環生成A3―和小分子組分的反應R64和R65:
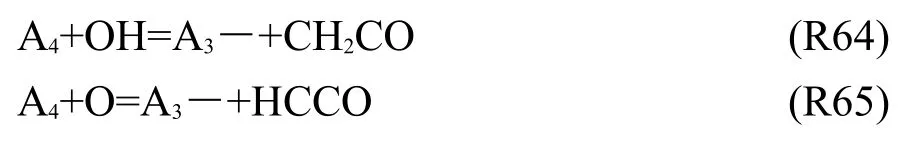
這些反應均來自于Wang和Frenklach7的PAHs機理.由于目前A4以上的PAHs鮮有實驗研究,可用于機理驗證的實驗結果很少,同時考慮到控制機理的規模,因此本文的PAHs機理就只到A4.至此,本文就構建了包含小碳氫分子和涉及PAHs反應的PAHs子機理(見Supporting Information).將其與異辛烷/正庚烷/乙醇/甲苯/二異丁烯多組分汽油替代燃料燃燒機理整合,最后得到了多組分汽油替代燃料PAHs的化學動力學機理模型,其PAHs組分的熱力學參數及其輸運參數均來自于文獻14.該模型包含103組分和395個基元反應,其合理性需要通過下一節的驗證.
3 機理的驗證
在本文作者之前的有關多組分汽油替代燃料機理的文中19已經詳細地驗證了燃料的燃燒特性,所以這里我們重點討論PAHs子機理的合理性.本文使用所建立的反應機理分別計算了乙烯、甲苯、正庚烷預混火焰和正庚烷部分預混對沖火焰中PAHs,及其前驅物的分布,并與實驗結果進行了比較.計算是在化學反應動力學程序CHEMKIN24上完成的.
3.1 乙烯預混火焰
Castaldi等25利用氣相色譜/質譜(GC/MS)技術對乙烯預混火焰中PAHs生成進行了詳細的實驗研究.在壓力0.1 MPa,入口流量0.0084 g·cm-2·s-1,入口物質摩爾分數分別為21.3%C2H4、20.9%O2、0.578%Ar(化學計量比為3.06)的條件下測得重要組分的分布.圖3給出了本文機理計算的乙烯預混火焰中重要PAHs及其前驅物組分的分布,并與實驗結果進行了對比.由圖3可見,本文機理預測的PAHs前驅物C2H2的摩爾分數分布與實驗值一致,而C4H4低于實驗值.PAHs(A1、A2、A3)組分的預測值基本上與實驗值一致,而A4高于實驗值.與主要反應物和生成物不同,PAHs含量很低,實驗技術可能導致其濃度測量存在較大的不確定性和誤差.因此這些組分濃度預測值也很難與實驗結果完全相符.圖3表明,本文機理總體上能夠較好地預測乙烯火焰中PAHs的生成.
3.2 甲苯預混火焰
Yang等26利用SVUV-PIMS方法詳細研究了低壓預混甲苯火焰結構.在壓力4 kPa,入口速度35 cm·s-1,入口物質摩爾分數分別為8.14%C6H5CH3、41.86%O2、50%Ar(化學計量比為 1.75),初始溫度410 K的條件下測量了重要組分的濃度分布.圖4給出了本文機理計算的甲苯富燃料預混火焰中PAHs及其前驅物組分的分布與實驗結果的對比.由圖可以看出,本文機理計算的C5H5的濃度分布與實驗結果較為一致.對于PAHs前驅物C2H2和C3H3,雖然計算的摩爾分數分布與實驗值有一定的偏差,但在趨勢上和實驗結果是一致的.同樣,本文機理預測的PAHs(A1、A2、A3)分布也基本上與實驗結果一致,表明該機理能夠基本上描述甲苯富燃料預混火焰中PAHs的變化趨勢.
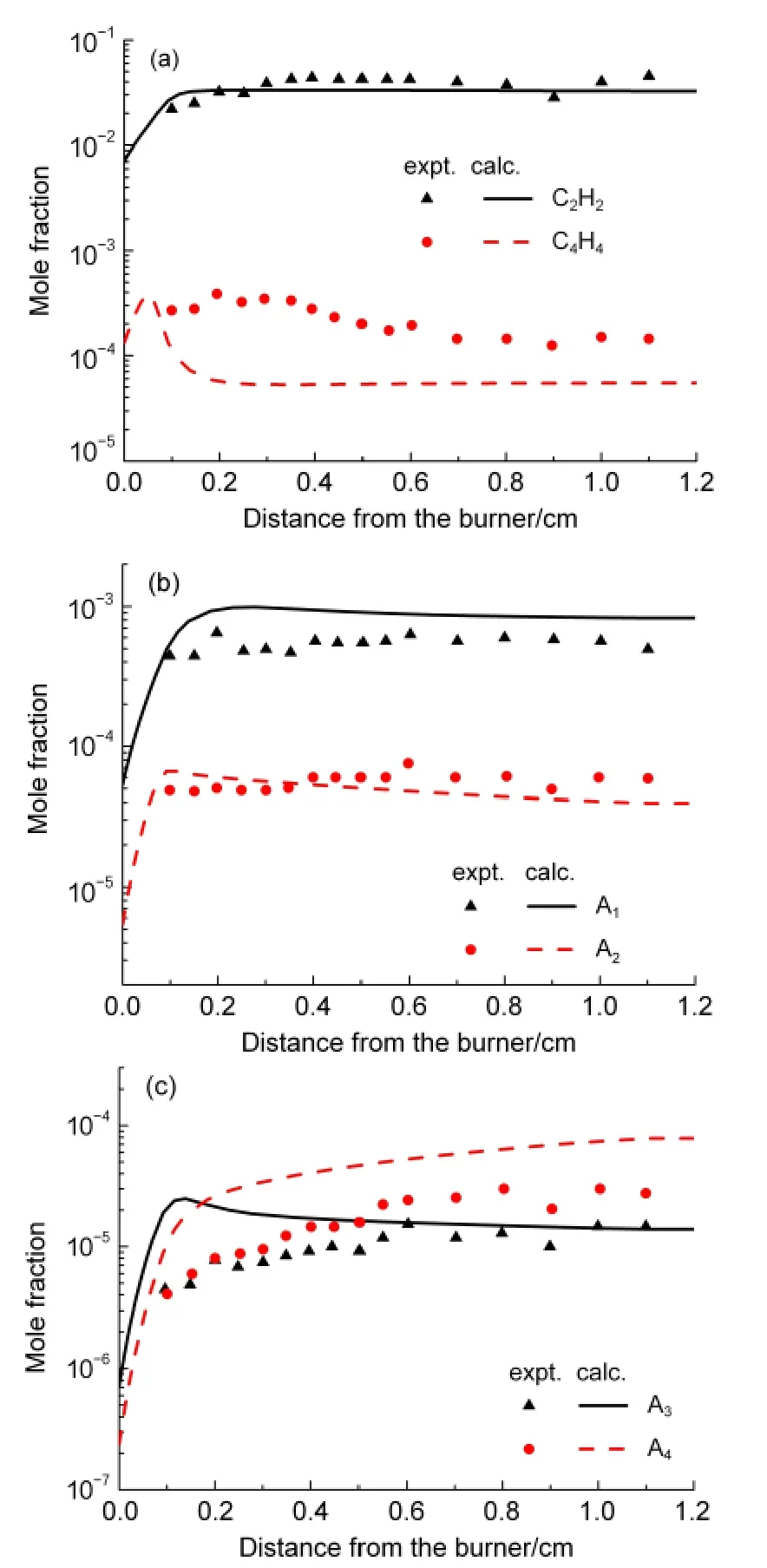
圖3 計算的乙烯預混火焰中PAHs及其前驅物摩爾分數分布與實驗結果25比較Fig.3 Comparison of mole fractions profiles of experimental25and calculated PAHs and precursors in premixed ethylene flame
3.3 正庚烷部分預混對沖火焰

圖4 計算的甲苯預混火焰中PAHs及其前驅物摩爾分數分布與實驗結果26比較Fig.4 Comparison of mole fractions profiles of experimental26and calculated PAHs and precursors in premixed toluene flame
Berta等27在不同化學計量比下,對正庚烷部分預混對沖火焰污染物的排放進行了詳細的實驗研究和數值模擬,并測得了重要組分的濃度分布.圖5為壓力0.1013 MPa,燃料入口溫度400 K,速度12.5 cm·s-1,10.43%nC7H16、18.81%O2、70.76%N2(化學計量比為6.1),氧化劑(空氣)入口溫度300 K,速度11 cm·s-1的條件下,本文機理和Marchal機理16計算的正庚烷部分預混對沖火焰中重要組分的濃度分布與實驗結果的對比.由圖可見,本文機理和Marchal機理預測的PAHs生長組分C2H2在趨勢上都與實驗值一致.而且,本文機理能更好地預測CH4組分的濃度分布.對于A1的預測,本文機理的計算值略高于實驗值,而Marchal機理的計算值低于實驗值.從圖給出的結果綜合來看,本文機理在預測正庚烷部分預混對沖火焰中C2H2、CH4、A1組分的濃度分布要略好于Marchal機理.
3.4 正庚烷預混火焰
Inal和Senkan28實驗研究了不同化學計量下正庚烷預混火焰的結構,給出了比較詳細的PAHs組分濃度分布.圖6為壓力0.1013 MPa,入口物質摩爾分數分別為 5.50%nC7H16、28.79%O2、65.71%N2(化學計量比為2.1),初始溫度700 K,速度5.17 cm·s-1的條件下,本文機理、Marchal機理16以及Raj機理17預測的正庚烷預混火焰中PAHs組分的濃度分布與實驗結果的對比.由圖可以看出,本文機理很好地預測了A1的實驗結果,較好地預測了A2、A3和A4的濃度分布;Raj機理較好地預測了A1、A2和A3,但對A4的預測值比實驗值小了一個數量級;Marchal機理高估了A1的濃度,低估了A2和A3,遠遠低估了A4的濃度,比Raj機理的預測值還小.

圖5 計算的正庚烷對沖火焰中PAHs及其前驅物摩爾分數分布與實驗結果27比較Fig.5 Comparison of mole fractions profiles of experimental27and calculated PAHs and precursors in opposed n-heptane flame
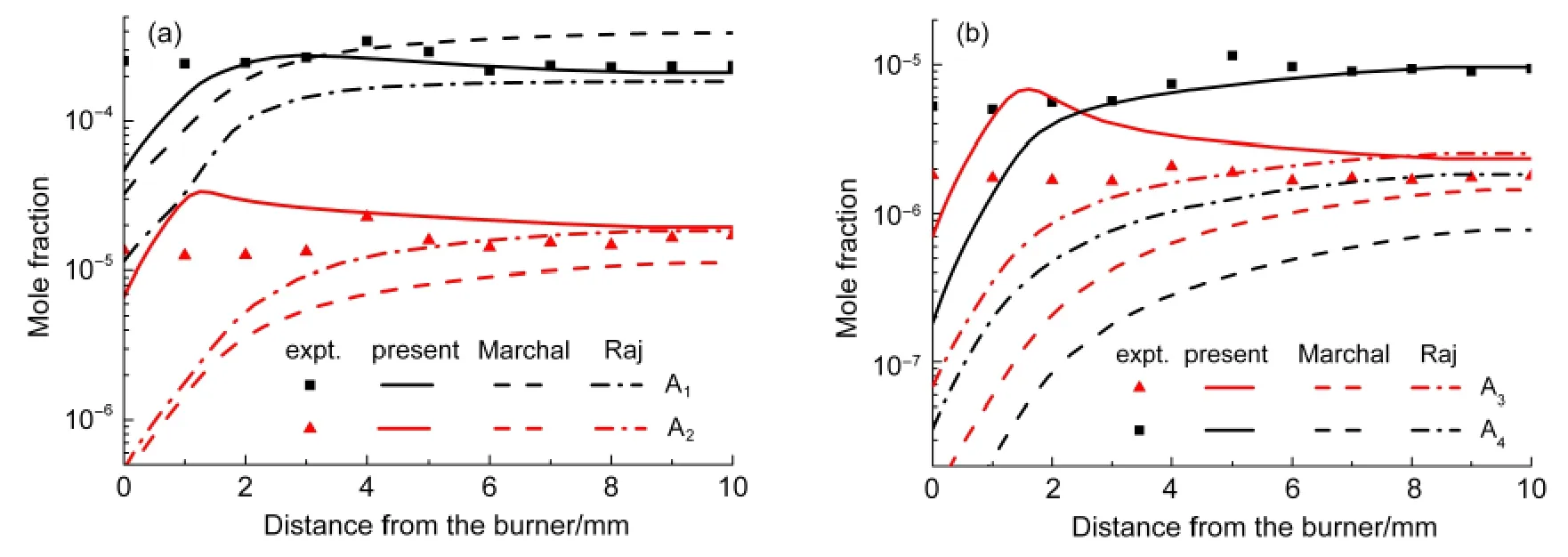
圖6 計算的正庚烷預混火焰中PAHs、及其前驅物摩爾分數分布與實驗結果28比較Fig.6 Comparison of mole fractions profiles of experimental28and calculated PAHs and precursors in premixed n-heptane flame
4 結論
構建了一個能夠描述并預測多組分汽油替代燃料PAHs生成過程的化學動力學機理模型,該機理包含103組分和395個基元反應.使用該機理模型分別計算了乙烯、甲苯、正庚烷預混火焰和正庚烷部分預混對沖火焰中PAHs及其前驅物組分的濃度分布,并與實驗結果進行了對比.結果表明該機理能夠較好地預測汽油替代燃料PAHs的生成過程和濃度分布特性.
雖然本文機理目前還無法直接應用于汽油機燃燒過程的PAHs多維數值模擬,但與現有的汽油替代燃料PAHs機理相比,本文提出的汽油替代燃料燃燒過程中PAHs生成機理包含較少的組分數與基元反應數,距離實際應用的目標更近.
Supporting Information:Sub-mechanisms of PAHs have been included.This information is available free of chargeviathe internet at http://www.whxb.pku.edu.cn.
(1) Iino,F.;Imagawa,T.;Takeuchi,M.;Sadakata,M.;Weber,R.Chemosphere1999,39(15),2749.doi:10.1016/S0045-6535(99)00209-X
(2) Richter,H.;Howard,J.B.Prog.Energ.Combust.2000,26(4-6),565.
(3) Luo,L.S.;Gao,J.H.;Zhang,Z.R.Automative Engineering2009,No.10,947.[駱路勝,高俊華,張仲榮.汽車工程,2009,No.10,947.]
(4) Frenklach,M.;Wang,H.Symposium(International)on Combustion1991,23(1),1559.doi:10.1016/S0082-0784(06)80426-1
(5) Frenklach,M.;Wang,H.Springer Series in Chemical Physics1994,No.59,165.
(6)Kazakov,A.;Wang,H.;Frenklach,M.Combust.Flame1995,100(1-2),111.
(7)Wang,H.;Frenklach,M.Combust.Flame1997,110(1-2),173.
(8) Zhong,B.J.;Hou,L.Y.Journal of Engineering Thermophysics2006,No.6,1048.[鐘北京,侯凌云.工程熱物理學報,2006,No.6,1048.]
(9)Appel,J.;Bockhorn,H.;Frenklach,M.Combust.Flame2000,121(1-2),122.
(10) Marinov,N.M.;Pitz,W.J.;Westbrook,C.K.;Castaldi,M.J.;Senkan,S.M.Combust.Sci.Technol.1996,116-117(1-6),211.
(11)Marinov,N.M.;Pitz,W.J.;Westbrook,C.K.;Vincitore,A.M.;Castaldi,M.J.;Senkan,S.M.;Melius,C.F.Combust.Flame1998,114(1-2),192.
(12)D?Anna,A.;D?Alessio,A.;Kent,J.Combust.Flame2001,125(3),1196.doi:10.1016/S0010-2180(01)00238-3
(13)D?Anna,A.;Kent,J.H.Combust.Flame2003,132(4),715.doi:10.1016/S0010-2180(02)00522-9
(14) Slavinskaya,N.A.;Frank,P.Combust.Flame2009,156(9),1705.doi:10.1016/j.combustflame.2009.04.013
(15) Slavinskaya,N.A.;Riedel,U.;Dworkin,S.B.;Thomson,M.J.Combust.Flame2012,159(3),979.doi:10.1016/j.combustflame.2011.10.005
(16) Marchal,C.;Delfau,J.L.;Vovelle,C.;Moréac,G.;Mounaim-Rousselle,C.;Mauss,F.Proc.Combust.Inst.2009,32(1),753.doi:10.1016/j.proci.2008.06.115
(17)Raj,A.;Prada,I.D.C.;Amer,A.A.;Chung,S.H.Combust.Flame2012,159(2),500.doi:10.1016/j.combustflame.2011.08.011
(18) Zheng,D.;Zhong,B.J.Acta Phys.-Chim.Sin.2012,28(9),2029.[鄭 東,鐘北京.物理化學學報,2012,28(9),2029.]doi:10.3866/PKU.WHXB201207042
(19) Zhong,B.J.;Zheng,D.Combust.Sci.Technol.2012,185(4),627.doi:10.1080/00102202.2012.739223
(20) Miller,J.A.Symposium(International)on Combustion1996,26(1),461.doi:10.1016/S0082-0784(96)80249-9
(21) Lindstedt,R.P.;Rizos,K.A.Proc.Combust.Inst.2002,29(2),2291.doi:10.1016/S1540-7489(02)80279-6
(22)Murakami,Y.;Saejung,T.;Ohashi,C.;Fujii,N.Chem.Letts2003,32(12),1112.doi:10.1246/cl.2003.1112
(23) Kislov,V.V.;Mebel,A.M.J.Phys.Chem.A2007,111(38),9532.doi:10.1021/jp0732099
(24) Kee,R.J.;Rupley,F.M.;Miller,J.A.CHEMKINRelease 4.1;Reaction Design:San Diego,CA,2006.
(25) Castaldi,M.J.;Marinov,N.M.;Melius,C.F.;Huang,J.;Senkan,S.M.;Pit,W.J.;Westbrook,C.K.Symposium(International)on Combustion1996,26(1),693.doi:10.1016/S0082-0784(96)80277-3
(26)Yang,B.;Li,Y.;Wei,L.;Huang,C.;Wang,J.;Tian,Z.;Yang,R.;Sheng,L.;Zhang,Y.;Qi,F.Proc.Combust.Inst.2007,31(1),555.doi:10.1016/j.proci.2006.07.171
(27) Berta,P.;Aggarwal,S.K.;Puri,I.K.Combust.Flame2006,145(4),740.doi:10.1016/j.combustflame.2006.02.003
(28) Inal,F.;Senkan,S.M.Combust.Flame2002,131(1-2),16.

