CdTe量子點作探針共振瑞利散射法測定鮭精蛋白
劉 丹,楊 莉,張 萍,羅飛華
(四川文理學院 化學與化學工程系,四川 達州 635000)
1 引言
量子點(quantum dots,QDs)又稱半導體納米晶(semiconductor nanocrystal),通常是由IIB-VIA族或IIIB-VA族原子構成的,粒徑尺寸在1~10nm之間的納米顆粒,具有獨特的物理和化學性質。最近幾年以來,量子點被用作生物探針的研究備受國內外科研工作人員的廣泛關注,目前研究較多的是CdX(X=S、Se、Te)QDs,最有前途的應用領域是在生物體系測定中作為熒光探針。相比于有機熒光分子,用QDs標記細胞、蛋白質和核酸等具有更好的熒光特性,它的相關應用研究,將促進超靈敏度、高穩定性以及長發光壽命的生物檢測技術的發展[1]。
鮭精蛋白(Salmine,Sal)是鮭魚精子中發現的一種魚精蛋白,它是一種天然存在于鮭魚成熟精細胞組織中、與DNA緊密結合在一起的一種32個氨基酸殘基的陽離子肽,顯強堿性,等電點為12.1,其中精氨酸成分極高,近年來,Sal在醫療衛生和食品行業具有廣闊的應用前景[2],目前用CdTe QDs作探針共振瑞利散射法研究Sal的方法還未見報道[3]。
2 材料與方法
2.1 儀器與試劑
儀器:Hitachi F-2500型熒光分光光度計(日本島津),測定參數:狹縫寬度5nm;pHS-3C型精密酸度計(中國上海精密科學儀器有限公司)。
試劑:單質碲(Te,國藥集團化學試劑有限公司),氯化鎘(CdC12·2.5H2O,上海試劑二廠),硼氫化鈉(NaBH4,天津市環威精細化工有限公司),巰基乙酸(C2H4O2S簡寫TGA,國藥集團化學試劑有限公司,AR),氫氧化鈉(NaOH,1mol·L-1),硫酸(H2SO4,0.5mol·L-1)Britton-Robinson(BR)緩沖溶液。BR緩沖溶液:用0.2NNaOH 溶液和0.04NH3PO4,H3BO3和HAc溶液按一定的比例混合后,配成不同pH值的緩沖溶液,并用酸度計校正其pH值。其余試劑均為分析純,實驗用水均為二次蒸餾水。
2.2 TGA-CdTe QDs的合成
選用50mL三頸燒瓶,通入N2作為保護氣,攪拌,將0.0194g Te粉溶于10mL蒸餾水中,加入適量NaBH4,一段時間后,黑色Te粉消失,瓶內溶液變得無色澄清透明,制得NaHTe溶液,備用[4]。
在250mL三頸瓶中加入0.0687g CdCl2·2.5H2O溶液,N2做保護氣,攪拌,加入0.05mL的巰基乙酸,用1mol·L-1的 NaOH溶液調節pH值為11.5,然后向制得的NaHTe溶液中在適當攪拌速度下緩慢注入一定量的0.5mol·L-1的 H2SO4,并將生成的H2Te氣體用N2載入到CdCl2溶液中,直至顏色穩定不變。升溫至95℃ ,反應回流6h后得到橙黃色液體,即得TGA-CdTe QDs溶液(2×10-3mol/L)。
2.3 測定方法
選用10.0mL的比色管,依次加入2×10-3mol·L-1CdTe QDs1.5mL、pH 值為8.0BR緩沖液1.0mL和適量Sal樣品溶液,用水稀釋至10.0mL,搖勻,靜置,室溫下反應10min,在熒光分光光度計上選擇以λex=λem,在220~800nm范圍內進行同步掃描,狹縫寬度為5nm,獲得RRS光譜,在最大共振瑞利散射峰(λmax)處測定體系的RRS強度IRRS和試劑空白的RRS強度I0,且ΔIRRS=IRRS-I0。
3 結果與討論
3.1 CdTe QDs-Sal體系的RRS光譜
圖1為CdTe QDs與Sal相互作用的共振散射光譜,當CdTe QDs或Sal單獨存在時,它們各自的散射強度(RRS)都很弱;當兩者同時存在時,二者結合形成新的結合物,RRS光譜顯著增強,如圖2中的CdTe QDs-Sal體系的RRS光譜所示,其最大散射峰位于312nm。
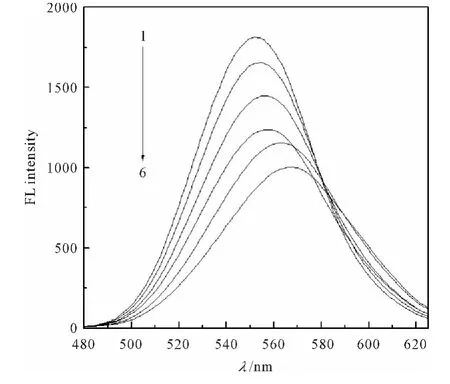
圖2 CdTe QDs-Sal體系的熒光光譜
圖1為CdTe QDs-Sal體系的散射光譜,由圖1可知,當TGA-CdTe QDs與Sal結合時,散射明顯增強,且散射強度在一定范圍內隨Sal濃度的增大而成線性增強,可以用于Sal的定量檢測。
3.2 CdTe QDs-Sal體系的熒光光譜
從圖2可以看出,QDs與Sal相互作用后,Sal能夠猝滅QDs的熒光,并且QDs的熒光強度隨著鮭精蛋白濃度的增大而逐漸減弱,同時伴隨著熒光發射峰位有規律地紅移。
3.3 體系適宜的反應條件
3.3.1 酸度的影響
通過實驗測定了CdTe QDs-Sal體系的最佳反應條件,實驗結果顯示,選擇BR緩沖溶液做介質時,實驗效果最佳,最佳的pH值范圍為7.5~8.5,用量為0.6~1.2mL,實驗選用1.0mL的pH值為8.0的BR緩沖溶液來調節體系酸度。
3.3.2 TGA-CdTe QDs濃度的影響
實驗研究了CdTe QDs用量對體系RRS強度的影響,結果表明:CdTe QDs溶液適宜用量為1.2~1.6 mL,CdTe QDs的用量過量或不足都將會影響實驗效果,實驗確定CdTe QDs的最佳用量為1.5mL(CdTe QDs濃度為2×10-3mol·L-1)。
3.3.3 反應時間的影響
實驗測定了在不同的反應時間,體系的RRS強度。在室溫下,按實驗方法將各試劑加完混勻后,該體系的ΔIRRS從反應開始逐漸增強,在10min后反應完全,2h之內散射強度基本保持穩定,故實驗選在反應完畢放置10min后立即進行測量。
3.4 標準曲線
在最佳反應條件下,以不同濃度的鮭精蛋白與CdTe QDs反應,10min后在最大波長處測量CdTe QDs-Sal體系的 RRS強度(IRRS),求出散射強度(ΔIRRS)后,以ΔIRRS對鮭精蛋白濃度作圖繪制標準曲線,線性范圍為:0.016~2.4μg/mL,線性方程:ΔI =233.25+947.54C,相關系數為0.9969,檢出限為5.00 ng/mL。
3.5 共存物質的影響
在鮭精蛋白濃度為2.5μg·mL-1時,相對誤差為10%范圍內,實驗考察了一些常見干擾物質對鮭精蛋白的影響,結果如表1所示。其中糖類對體系的影響較小,允許濃度較大;部分無機離子對體系的影響也較小,允許濃度較大;由于實驗是在堿性環境中進行的,某些金屬離子允許濃度較小,實驗中應使用掩蔽劑,減小其對體系的影響。
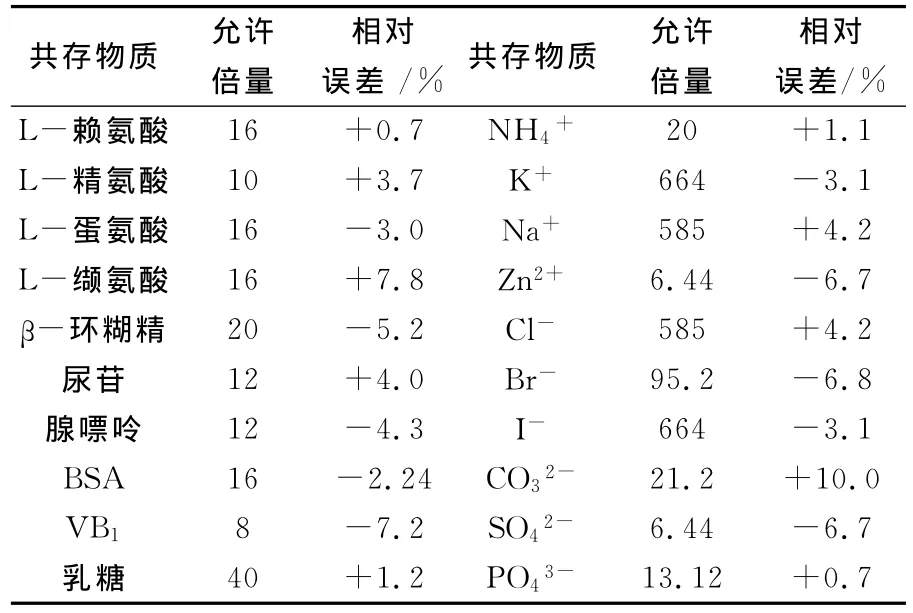
表1 CdTe QDs-Sal體系共存物質的影響(CSal=2.5μg·mL-1)
3.6 RRS增強的原因
3.6.1 分子體積增大
眾所周知分子體積的增大直接影響到散射強度的提高[5]。在弱堿性的緩沖溶液中帶正電的sal和帶負電的巰基乙酸修飾的量子點通過靜電引力和氫鍵結合在一起。隨著聚集到量子點表面的sal的量增多而使量子點的表面帶正電,這樣量子點又結合另一個帶有正電的量子點而最終導致量子點的聚集,導致分子體積的增大,RRS顯著增強。
3.6.2 CdTe QDs與鮭精蛋白共振增強散射效應
當Rayleigh散射的波長位于分子的吸收帶的附近時,散射強度將急劇增大,這種現象即為共振瑞利散射。由實驗知,產生增強的瑞利散射效應。
3.6.3 疏水性增強
反應前,帶負電荷的CdTe QDs和帶正電荷的鮭精蛋白均有較好的親水性,它們在水溶液中易形成水合物,因而RRS均很微弱。而當CdTe QDs與鮭精蛋白結合后,形成的聚合物成電中性,導致疏水性增加,從而可能形成一種疏水的液—固界面與水形成一種固—液界面,這種界面的形成有利于RRS光譜增強[6]。
3.7 熒光猝滅的原因
在弱堿性條件下,帶負電的CdTe QDs與帶正電的鮭精蛋白通過靜電引力及疏水作用力相互作用,導致QDs的熒光猝滅[7]。由CdTe QDs與鮭精蛋白相互作用的熒光光譜和RRS光譜得知,向CdTe QDs溶液中加入一定量的鮭精蛋白后,兩者結合形成大的結合物,這種結合物使得QDs的熒光猝滅,同時伴隨著發射峰位的紅移。從紫外光譜圖4也可以看出,鮭精蛋白與QDs之間存在著強烈的相互作用,結合后有新的吸收峰形成。由此可以說明,在pH值為8的弱堿性條件下,帶正電的鮭精蛋白與帶負電的CdTe QDs通過靜電引力及疏水作用力結合,形成不發光的結合物,導致QDs的熒光猝滅,其猝滅方式屬于靜態猝滅。
4 結論
本文用巰基乙酸作為穩定劑,合成了水溶性TGA-CdTe QDs。在弱堿環境中,用巰基乙酸做穩定劑修飾的帶負電的CdTe QDs與帶正電的鮭精蛋白通過靜電引力及疏水作用力結合,形成粒徑較大的結合物,引起RRS光譜的顯著增強和熒光的猝滅。在一定的條件下,RRS光譜的強度與鮭精蛋白的濃度呈現良好的線性關系。本文研究了鮭精蛋白和CdTe QDs相互作用的RRS光譜、適宜的反應條件和影響因素,通過RRS光譜、熒光光譜、紫外吸收光譜,研究了CdTe QDs與鮭精蛋白的相互作用機理,由此建立一種以CdTe QDs作探針共振瑞利散射法快速靈敏檢測鮭精蛋白的新方法。
[1]Liu Z W,Liu S P,Wang L,et al.Resonance Rayleigh scattering and resonance non-linear scattering method for the determination of aminoglycoside antibiotics with water solubility CdS quantum dots as probe[J].Spectrochim Acta A,2009,74(1):36~41.
[2]魯健章,王春曉,劉承初,等.鮭精蛋白基因工程菌高效表達條件的優化[J].中國食物與營養,2007,12,28~31.
[3]高 陽,畢紹丹.蛋白質與玫瑰桃紅R共振瑞利散射的研究及應用[J].廣東微量元素科學,2009,7(16):21~24.
[4]Deng D W,Yu J S,Pan Y.Water-soluble CdSe and CdSe/CdS nanocrystals:A greenersynthetic route[J].J Colloid Interface Sci,2006,299:225~232.
[5]Liu S P,Luo H Q,Li N B,et al.Resonance rayleigh scattering study of the Interaction of Heparin with some basic diphenyl naphthylmethane dyes [J].Anal Chem,2001,73(16):3907~3914.
[6]劉紹璞,蔣治良,孔 玲,等.[HgX]納米微粒的吸收光譜、Rayleigh散射和共振Rayleigh散射光譜[J].中國科學(B輯),2002,32(6):554~560.
[7]張 毅.單質碘對水溶性CdTe量子點的熒光猝滅研究[J].光譜實驗室,2009,4(26):974~978.

