成纖維生長因子受體在非小細胞肺癌中的研究進展
蒲丹 侯梅
肺癌是最常見的惡性腫瘤之一,在2008年全球約137萬人死于肺癌。肺癌患者中約85%為非小細胞肺癌(non-small cell lung cancer, NSCLC),研究人員在肺腺癌中發現表皮生長因子受體(epidermal growth factor receptor,EGFR)基因突變,ALK融合基因等,將其作為靶點進行分子靶向治療,取得了令人矚目的成果,使部分肺腺癌患者的生存質量和總生存期得到了明顯的改善。然而,EGFR基因突變及ALK融合基因在肺鱗癌中少見,以其為靶點的治療措施在肺鱗癌患者中難以奏效。2012年美國癌癥基因圖譜協作網(The Cancer Genome Atlas Research Network)通過對178例肺鱗癌組織的分析,描繪出了肺鱗癌大致的基因及表觀遺傳學改變,發現EGFR及K-ras突變在鱗癌中十分少見,而更為常見的是成纖維生長因子受體(fibroblast growth factor receptor, FGFR)激酶家族的異常,其中包括成纖維生長因子受體1基因擴增[1]。FGF信號通路介導NSCLC的生長和血管生成,同時被認為與抗血管內皮生長因子(vascular endothelial growth factor,VEGF)及抗EGFR治療耐藥相關。FGFR1作為FGF家族的酪氨酸激酶受體,其基因擴增被認為可作為非小細胞肺癌治療的分子靶點。
1 FGF信號通路
FGF與FGFR普遍存在于正常細胞中,共同構成FGF信號通路,在細胞生長、分化、遷移、血管生成以及組織創傷修復中起重要作用,近年研究表明,該通路在腫瘤的發生、發展過程中也扮演重要角色。FGF信號通路至少由22種FGFs和4種FGFR構成。FGFs是一類多肽生長因子,除了FGF19、FGF21、FGF23可通過類似激素的內分泌途徑入血,大部分FGFs通過自分泌或旁分泌途徑起生理作用。FGFs在細胞膜上主要存在兩類受體,一類是低親和力受體,即肝素硫酸蛋白多糖(heparin sulfate proteoglycan, HSPG),細胞外的FGFs通過與HSPG結合協助FGFRs發生二聚化、自磷酸化以及細胞內途徑的激活,同時使FGFs免于降解。另一類是高親和力受體,即FGFR,屬于跨膜酪氨酸激酶受體家族(transmembrane receptor tyrosine kinase, RTK),由FGFR1、FGFR2、FGFR3、FGFR4基因編碼,由胞外區,跨膜區及具有酪氨酸激酶活性的胞內區構成。胞外區包括配體結合位點、酸盒及2個或3個免疫球蛋白樣結構域(Ig I, Ig II, Ig III),如圖1。Ig I被認為與受體抑制相關[2],而不參與配體的特異性結合,缺乏Ig I并不影響FGFRs與FGFs的親和性,Ig III與Ig II是FGFRs與配體結合的部位,并決定結合的特異性。由于mRNA剪切形式的差異,Ig III存在IIIb和IIIc兩種異構體,不同的FGFs其優勢結合位點不同[3],如表1,FGF7和FGF1傾向于結合FGFR IIIb,其余的則對FGFR IIIc具有更好的親和性。在組織中,FGFR的類型間具有一定的分布特征,IIIc異構體常見于間質組織中,而IIIb異構體最多見于上皮細胞中,間質組織需要的配體常常通過鄰近上皮組織分泌,而上皮組織需要的配體常常通過鄰近間質組織分泌,這可能是維持細胞微環境穩定的一種方式,其異常可能是導致腫瘤發生以及腫瘤細胞上皮間質轉化的一個原因。當FGFR與相應配體結合后發生構型改變,使得胞內段酪氨酸激酶殘基磷酸化,活化的酪氨酸激酶殘基作為與下游信號通路的接駁點,可激活多條下游信號通路產生生物學效應(圖1),例如,FGFR近膜部的酪氨酸激酶磷酸化位點與接連蛋白FRS2結合后,使得FRS2的多個酪氨酸殘基磷酸化,招募SOS、GRB2、GAB1蛋白形成復合物激活Ras-Raf-MapK、PI3K信號通路;FGFR的-COOH端的酪氨酸激酶磷酸化位點與SH2結合,導致PLCγ磷酸化,促進細胞內鈣離子釋放,激活PKC。另外,根據細胞微環境的差異,FGFR還可激活包括Shb、Src、Crk、RSK在內的其他途徑,但目前研究表明,Ras-Raf-MapK、PI3K-Akt、Stats和PLCγ是FGFR的四個主要的下游信號通路。
2 NSCLC中FGFR的表達
FGFR的高表達在包括前列腺、乳腺、胃、口腔等多種腫瘤中均有發現[4-7]。1999年,Berger[8]等在NSCLC中發現FGF2、FGFR的表達升高后,陸續多個研究證實非小細胞肺癌中存在FGFR基因異常[9-11],包括染色體異位、基因擴增、點突變、修復和剪切異常等[12],常用的檢測手段為免疫組化、熒光原位雜交以及RT-PCR。
FGFR1基因位于8號染色體短臂,Zhang等[13]報道,中國人中FGFR1基因擴增率在肺鱗癌中為12.5%(6/48),肺腺癌中為7%(5/76),Heist等[10]通過分析226例美國患者后顯示肺鱗癌中FGFR1擴增率為16%,在德國的一項研究中10.5%的肺鱗癌以及4.7%的肺腺癌患者中存在FGFR基因擴增[11]。結合目前中外研究顯示,肺鱗癌中FGFR1擴增率為10%-20%,明顯高于肺腺癌,且亞歐人群中并不存在明顯的種族差異。Heist的研究[10]同時也指出FGFR基因擴增與年齡、性別、腫瘤分期以及吸煙史無相關性,FGFR基因狀態不同的人群間總生存期無統計學差異,這與Weiss之前的研究結論不一致,Weiss等[14]等通過分析232例NSCLC患者,其結果顯示,FGFR1基因擴增主要見于吸煙者,且FGFR1基因擴增的患者傾向于不良的生存預后。Tran等[15]的研究中從未吸煙的患者雖然例數較少,但全部為FGFR1陰性,支持Weiss的研究結論,不同的是,該研究的多因素分析中FGFR1基因拷貝數高的患者傾向于更長的總生存期(overall survival,OS),研究者認為FGFR1基因拷貝數升高是NSCLC有益的預后預測因子。既往研究結論不一致,有可能是受樣本量及分層因素的影響,包括病理類型、是否手術以及EGFR基因狀態等,例如,Kohler等[11]一個樣本量非常小的分析提示FGFR1擴增的肺腺癌傾向于有生存獲益,假如這種現象并非偶然,那么如果將腺癌與鱗癌共同納入分析就有可能得出NSCLC中FGFR1擴增傾向于生存獲益的結論;另外EGFR基因突變的患者在后續治療中使用酪氨酸激酶抑制劑(tyrosine kinase inhibitor, TKI)類藥物可能導致OS無差別。近期韓國研究者Kim等[16]的研究納入262例肺鱗癌根治術后患者,研究同時檢測了EGFR及KRAS基因突變,結果顯示FGFR1基因高度擴增的患者較FGFR基因無擴增或低度擴增的患者,其無疾病生存期(disease-free survival, DFS)及總生存期OS明顯較短(DFS:26.9個月 vs 94.6個月,P<0.001;OS:51.2個月 vs 115.0個月,P<0.002),吸煙患者的FGFR1擴增率明顯高于已戒煙者和從不吸煙的患者(28.9% vs 2.5% vs 0),與以往研究一致,FGFR1基因狀態與性別、腫瘤分期、脈管浸潤、胸膜受侵等無明顯相關性,表明FGFR1基因擴增預示鱗癌術后患者的預后不良,且不存在明顯的“優勢人群”,在選擇FGFR抑制劑時需要對患者進行FGFR基因檢測。
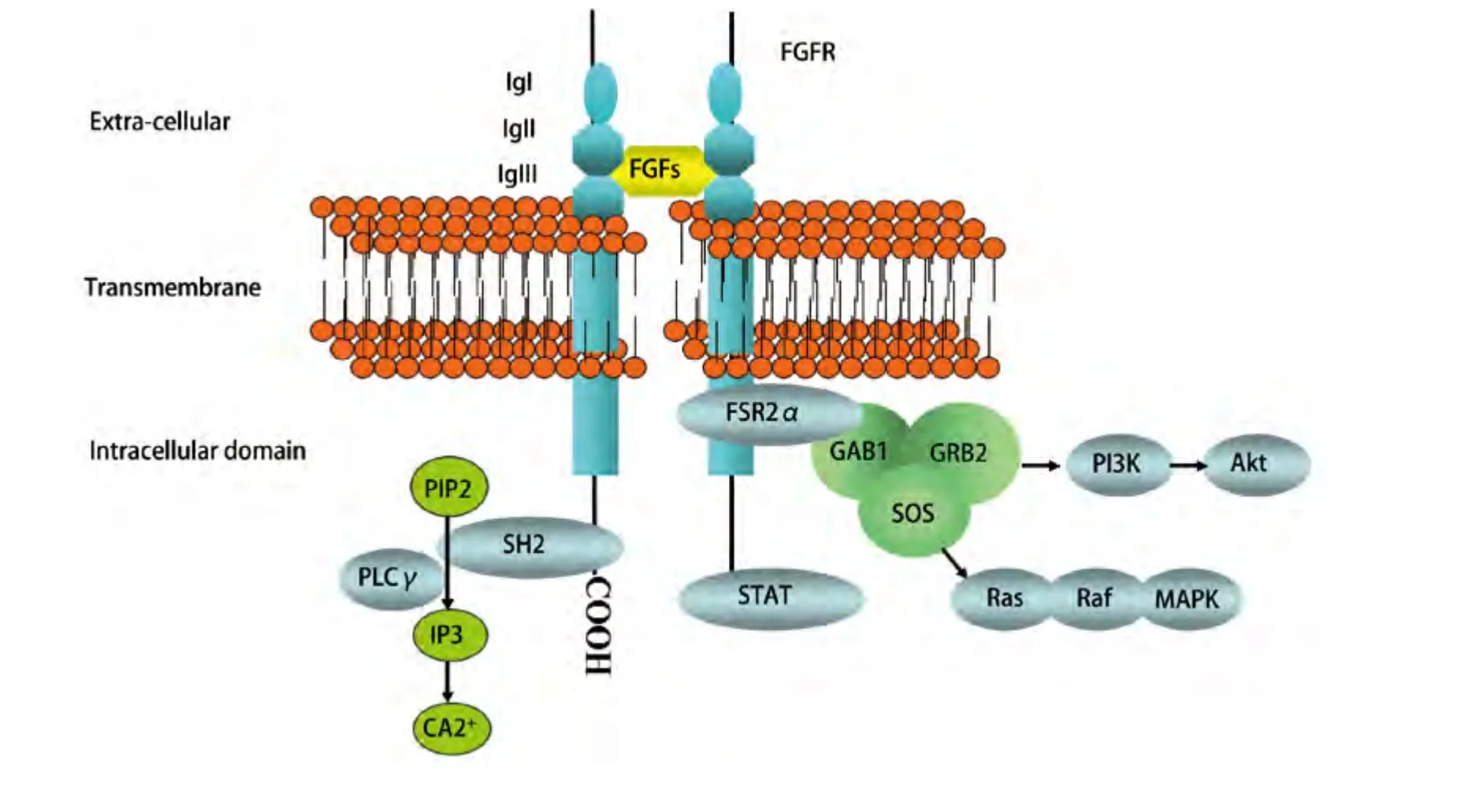
圖 1 成纖維生長因子受體的結構及其下游信號通路Fig 1 The structure and downstream signaling pathways of fibroblast growth factor receptor. PIP2: phosphatidylinosital-4,5-biphosphate;PLCγ: phospholipase Cγ; IP3: inositol triphosphate; FSR2α: FGFR substrate 2α; GRB2: growth factor receptor bound 2; GAB1: Grb2-associated binder; SOS: son of sevenless; MAPK: mitogen-activated protein kinases; STAT: signal transducers and activators of transcription; PI3K:phosphatidylinositol 3-hydroxy kinase; Akt: serine-threonine protein kinase.

表 1 22種FGFs的7個亞型及其特異性受體Tab 1 The subfamilies of FGFs and their specific receptors
FGFR2與FGFR1結構相似,其在膀胱癌中的表達降低,而增加FGFR2表達可阻斷膀胱癌細胞株的生長[17],因此一些研究者認為FGFR2對腫瘤有抑制作用。在乳腺癌移植瘤模型中[18],阻斷FGFR1腫瘤生長明顯放緩,然而阻斷FGFR2可使FGFR1表達上調,導致腫瘤長大以及腫瘤血管生成,研究者認為FGFR1密切參與腫瘤形成,而FGFR2并不直接參與腫瘤增殖,反而可能存在抑制作用。但FGFR2遠不能被籠統的看作是抑癌基因,因為除了在部分生殖泌尿系統腫瘤中發現FGFR2表達降低之外,在胃癌、胰腺癌、乳腺癌、肺癌中都發現FGFR2的上調,其表達及作用在不同腫瘤中產生差異的原因尚不清楚,可能與腫瘤微環境相關。另外,Sasaki等[19]在日本肺癌人群,以及Matakidou等[20]在歐洲肺癌人群中沒有發現FGFR4的突變,但FGFR4 Gly388Arg存在基因多態性,目前研究顯示其基因型與吸煙狀態、病理分型、分期以及OS沒有相關性。雖然Sasaki的研究顯示Gly388Arg的基因多態性與術后淋巴結陽性患者的不良OS相關,但尚不足以證明FGFR4 Gly388Arg的基因多態性可作為肺癌預后的預測因子。
FGF信號通路被認為可作為肺鱗癌靶向治療的潛在靶點,FGFR1基因擴增見于約20%的肺鱗癌患者中,在體內及體外試驗中,FGFR抑制劑可使存在FGFR1基因擴增的腫瘤體積明顯縮小,這些似乎都預示著FGFR1在肺鱗癌中的靶向治療前景,目前關于FGFR在肺癌中的研究也主要集中在FGFR1。
3 FGFR與NSCLC的治療
3.1 FGFR與抗血管生成治療 腫瘤新生血管是腫瘤生長的營養支持以及遠處轉移的重要途徑,目前抗血管生成的靶向治療藥物主要作用于VEGF通路,但Bevacizumab(VEGF單克隆抗體)與化療聯用并不能使患者OS得到明顯的延長[21],原因是大部分患者的獲益是短暫的,還有部分患者不能從加用Bevacizumab的治療中獲益。抗血管生成藥物的作用靶點在血管內皮細胞,這類細胞并不像腫瘤細胞一樣具有無限增殖的能力,因此對Bevacizumab的耐藥并不傾向于VEGF信號通路中某些位點的基因突變,而更可能來源于腫瘤微環境或者其它替代途徑的改變。FGFs是最先被發現的血管生長因子之一,它們在內皮細胞增殖、遷移、細胞黏附等血管形成過程中的作用已被廣泛研究。體外實驗中,FGFR1、FGFR2與配體FGFs1、FGFs2、FGFs4、FGFs8結合后通過MAPK、PKC信號傳導通路促進上皮細胞增殖,與配體FGFs1、FGFs2、FGFs8、FGFs10結合后可通過刺激上皮細胞的趨化性,促進上皮細胞的遷移,同時,FGF1、FGFs2、FGFs4還可上調纖溶酶原激活物和基質金屬蛋白酶促進細胞外基質的改變[22],為新生血管的形成提供適宜的條件,FGF2、FGFs8可誘導上皮細胞形成毛細血管樣結構,在血管的構型和成熟方面起重要作用[23]。有足夠的證據表明FGFs與VEGF通路在促進血管生成中具有協同作用,FGF2可上調內皮細胞中VEGFR和VEGF的表達,VEGF也可促進FGF2表達[24.25],阻斷VEGF后FGF2表達減少,反過來,阻斷FGFR1、FGFR2的表達同樣可降低VEGF水平[26]。同時,FGF介導的血管生成并不完全依賴于VEGF,在VEGF高表達的情況下,FGF-2過度表達仍能大大增加新生血管形成。Ogawa等[27]在多個肺癌細胞株中發現,阻斷FGFR1能有效抑制抗VEGF耐藥的腫瘤血管生成,增加細胞凋亡,并且同時阻斷FGFR1和VEGFR對腫瘤的抑制作用較單用其中一種更加明顯。這表明FGF信號通路與VEGF信號通路在促進腫瘤血管生成中相互促進而又互不依賴,FGF通路可能是腫瘤逃避抗VEGF治療的一種途徑,預示著使用多靶點的抗血管生成治療藥物可能將是一個行之有效的方法。
3.2 FGFR與EGFR-TKI耐藥 EGFR TKI在EGFR基因突變的NSCLC患者中的有效率高達70%,但部分患者存在原發耐藥,另外幾乎所有初始使用有效的患者隨著用藥時間的延長將會產生繼發耐藥。約50%的EGFR TKI耐藥與EGFR T790M突變相關,5%-15%與Met擴增相關。另外仍有約30%原因不明,推測與酪氨酸激酶旁路途徑的建立與激活相關,可能部分來自于FGFR基因改變。Terai等在吉非替尼耐藥的NSCLC細胞株(PC9 GR)中發現腫瘤細胞的擴增通過依賴bFGF-FGFR1的途徑,并且在PD173074(FGFR抑制劑)處理后可恢復對吉非替尼的敏感性。Ware等[28]的研究支持了Terai[29]的結論,他們在研究中培育了吉非替尼繼發耐藥的肺癌細胞株HCC4006,發現b-FGF和FGFR1的mRNA分別增加了2.5倍和9倍,聯用AZD4547(FGFR抑制劑)可抑制耐藥株的生長,他們同時發現耐藥株中上皮型E-鈣粘蛋白、交聯蛋白表達降低,波形蛋白、N-鈣粘蛋白、ZEB1、ZEB2等間質組織標記物升高,并且這種情況并不是偶然,在實驗誘導的其他耐藥株中也發現了近似的現象。目前在許多腫瘤類型中的研究顯示,FGF信號通路可誘導細胞上皮間質轉化(epithelial-mesenchymal transition, EMT),異常的FGFR1促進腫瘤細胞發生EMT的主要作用點在于激活Snail家族,MAPK信號通路可上調snail mRNA水平,PI3K/Akt信號通路可阻斷抑制蛋白GSK-3β使Snail穩定表達,促進上皮間質轉化,而具有間質表型的NSCLC對EGFR TKI的敏感性降低[30]。多數研究者認為吉非替尼的獲得性耐藥與FGF旁路信號通路的建立及其伴隨的上皮間質轉化相關,推測可能存在這樣的一個模式:上皮表型為主的腫瘤細胞耐藥與IGF1活化、Met擴增、EGFR T790M突變關系更為密切,而間質表型為主的腫瘤細胞耐藥與PDGFR、FGFR信號通路相關。目前臨床上,尚無條件分析患者使用EGFR TKI類藥物前后腫瘤細胞表型及FGFR狀態的改變,但在體外和動物實驗中,FGF信號通路作為EGFR TKI治療耐藥的旁路途徑已得到證實。目前一項厄洛替尼聯合dovitinib(FGFR及VEGFR抑制劑)應用于晚期NSCLC患者的I期臨床試驗(NCT01515969)正在進行,研究者期望聯用FGFR抑制劑可對抗或延緩EGFR TKI耐藥。
4 FGFR抑制劑在NSCLC中的應用
近年,多項FGFR酪氨酸激酶抑制劑已進入臨床研究。Cediranib是一種多靶點口服酪氨酸激酶抑制劑,其靶點包括VEGFR、血小板衍生生長因子受體(plateletderived growth factor receptor, PDGFR)、c-kit以及FGFR1,Cediranib聯合PC方案(紫杉醇加卡鉑)用于NSCLC患者的一項II期-III期臨床研究顯示,cediranib組的有效率提高(38% vs 16%, P<0.001)[31],雖然由于嚴重的毒副反應使得研究提前終止,但該研究展示出多靶點藥物的應用前景,目前正在探索更低劑量的cediranib聯合化療的耐受性(NCT00795340)。BGJ398是選擇性的FGFR酪氨酸激酶抑制劑,正在進行I期臨床試驗(NCT01004224),試驗針對包括肺癌在內的實體腫瘤,要求入組的患者必須存在FGFR1或FGFR2基因擴增,或是FGFR3突變。FGFR抑制劑的出現以及進一步研究,為肺癌尤其是肺鱗狀細胞癌的治療提供了新的選擇。雖然目前開展臨床試驗(Brivanib, Pazopanib, XL999, E-3810, AZD4547, PD173074)的多種FGFR酪氨酸激酶抑制劑,同時也是VEGFR抑制劑,它們對腫瘤的抑制作用有可能首先來源于抑制新生血管形成,但有研究顯示FGFR抑制劑本身還存在除抑制腫瘤血管生成之外的直接的抗腫瘤效應,該效應可能與凋亡因子caspase3活化相關,且FGF通路參與VEGFR抑制劑耐藥,因此多靶點的酪氨酸激酶抑制劑仍有可能提高療效或延長疾病進展時間。
FGF信號通路與腫瘤的發生及腫瘤血管形成密切相關,新近研究表明,它參與抗VEGF以及抗EGFR靶向治療耐藥。FGFR1基因擴增在肺鱗癌以及肺腺癌中均有發生,但在鱗癌中明顯高于腺癌,在具有FGFR1基因擴增的腫瘤中使用FGFR抑制劑可增加腫瘤細胞凋亡,使腫瘤明顯縮小,同時FGFR可解救抗VEGF和抗EGFR治療耐藥,發揮抗腫瘤效應。在NSCLC中,研究針對FGFR的靶向治療藥物具有重要的應用前景。

