復合光催化材料Ag-AgCl/石墨烯的制備及性能
褚亮亮,董 斌,周建偉,王儲備
(1. 新鄉學院 能源與燃料研究所,河南 新鄉 453003;2. 新鄉學院 生命科學與技術學院,河南 新鄉 453003)
光催化降解以其經濟、環保等獨到優點[1],在處理廢水、廢氣中有機污染物方面受到人們廣泛關注。用光催化法降解污染物的關鍵問題是找到高效的光催化劑[2-3]。貴金屬納米粒子因具有表面等離子共振效應而成為近年的研究熱點,尤其以Ag及Ag與鹵化銀復合納米粒子為等離子體光催化劑的研究較多。Wang等[4]以AgMoO4和HCl為原料,合成了Ag-AgCl等離子體光催化劑。Ag-AgCl以金屬為殼、電介質為核,是一種基于納米金屬表面等離子體共振效應和半導體光催化效應的新型可見光催化材料[5]。
由于Ag-AgCl為納米顆粒,在實際應用中容易流失,難以回收重復利用,目前多將Ag-AgCl負載在不同載體上制成復合催化劑。周建偉等[6-7]采用化學沉積-光還原法,將Ag-AgCl負載在介孔材料MCM-41及Al2O3上,分別制備了Ag-AgCl/MCM-41和Ag-AgCl/Al2O3復合光催化材料。載體的引入使催化劑比表面積、分散性、吸附性能、可見光催化活性和重復使用性提高。Yu等[8]在TiO2納米管陣列上負載Ag-AgCl,使AgCl的光響應范圍擴大到可見光區。2004年Geim等[9]首次制備出石墨烯。石墨烯是目前世界上最薄的二維材料,石墨烯以其獨特的結構和優異的性能,有望成為理想的載體材料。
本工作采用原位化學沉淀—光還原法以自制的石墨烯為載體,將Ag-AgCl納米粒子高度分散于石墨烯表面,制備了負載型Ag-AgCl/石墨烯光催化劑,并以羅丹明B為目標降解物,研究了Ag-AgCl/石墨烯的可見光催化性能及其反應機理。
1 實驗部分
1.1 試劑和儀器
AgNO3、NaCl、檸檬酸鈉、羅丹明B:分析純;實驗用水為去離子水。
80-2型離心機:江蘇榮華儀器制造有限公司;SartoriusBT型電子天平:德國賽多利斯公司;752型紫外-可見分光光度計:上海第三分析儀器廠;D8-FOCUS X型XRD儀:德國布魯克公司;cary-5000 型UV-Vis漫反射光譜儀:美國瓦里安公司;FTS-40型FTIR儀:KBr壓片,波數范圍400~4 000 cm-1, 美國伯樂公司;高壓汞燈:250 W,λ<400 nm,北京天脈恒輝光源電器有限公司;氙燈:500 W ,濟南宏遠電氣有限公司。
1.2 催化劑的制備
石墨烯的制備方法見文獻[10-11]。
Ag-AgCl/石墨烯催化劑的制備:取一定量石墨烯浸泡在去離子水中,超聲30 min使其充分浸漬。在磁力攪拌下加入5 mL濃度為 0.02 mol/L的AgNO3溶液,并依次滴加5 mL濃度為 0.01 mol/L 的NaCl溶液和1 mL濃度為0.034 mol/L的檸檬酸鈉溶液,繼續攪拌0.5 h后,將混合液用高壓汞燈照射0.5 h,經過濾、洗滌和干燥,最終得到黑色粉末狀Ag-AgCl/石墨烯復合材料,其中Ag和AgCl的負載量(w)分別為5.04%和5.46%。Ag-AgCl的制備方法除了不需要加入石墨烯,其余步驟與制備復合Ag-AgCl/石墨烯的方法相同。
1.3 光催化降解實驗
光催化降解實驗在自制光催化降解反應裝置中進行。在30 mL一定質量濃度的羅丹明B模擬廢水中加入30 mg光催化劑,在磁力攪拌下暗反應0.5 h使體系達到吸附平衡。然后將廢水置于500 W氙燈照射下進行光降解反應,保持光源至液面距離為20 cm,鼓入空氣攪拌,間隔10 min取樣7~8 mL,離心除去固體催化劑后,取上清液于比色皿中,用分光光度計在吸收波長554 nm處測定吸光度,計算羅丹明B的降解率。
2 結果與討論
2.1 催化劑的表征
2.1.1 XRD分析
Ag-AgCl的XRD譜圖見圖1。由圖1可見:Ag-AgCl的XRD譜圖中出現了Ag及AgCl的特征峰(對照JCPDS65-2871和JCPDS31-1238),在2θ為27.88°,32.18°,46.20°,54.85°,57.56°,67.35°,74.37°,76.61°處的衍射峰分別對應于AgCl的(111),(200),(220),(311),(222),(400),(331),(420)晶面;在2θ為38.1°處有較弱的Ag衍射峰出現,說明材料中存在少量的Ag納米顆粒,由于其粒徑太小或無定形導致其衍射峰較弱。
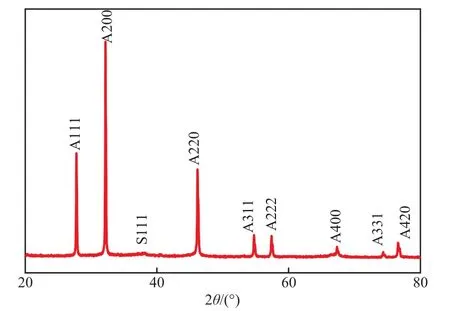
圖1 Ag-AgCl的XRD譜圖
2.1.2 UV-Vis分析
Ag-AgCl的UV-Vis吸收光譜譜圖見圖2。
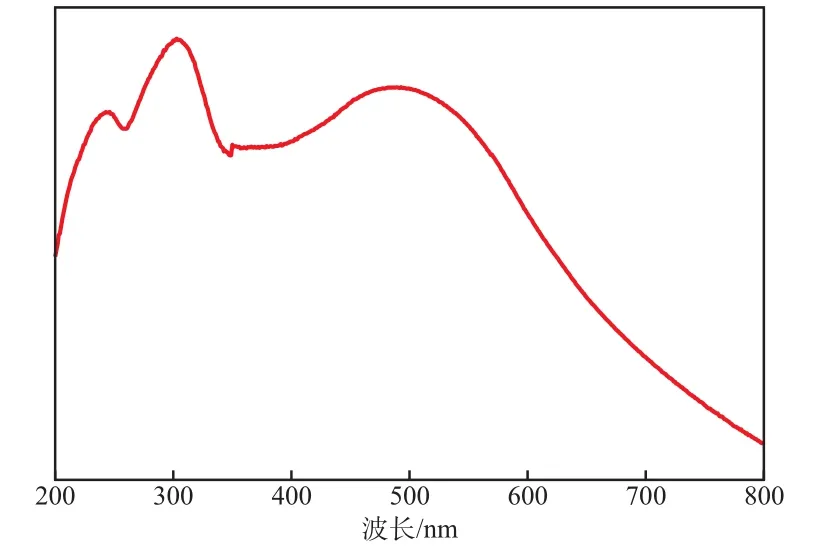
圖2 Ag-AgCl的UV-Vis吸收光譜譜圖
由圖2可見:Ag-AgCl在紫外和可見光區都有吸收峰,在波長小于400 nm的紫外光區有強吸收峰,在400~600 nm波長區域有較強吸收峰。AgCl間接能帶隙為3.25 eV左右,只對紫外光有響應,在其表面負載貴金屬Ag納米粒子后,由于Ag納米粒子具有等離子體共振效應而存在很強的紫外-可見吸收,從而使Ag-AgCl的光響應范圍擴大到可見光區,提高了其在可見光下的光催化活性。
2.1.3 FTIR分析
氧化石墨(a)和石墨烯(b)的FTIR譜圖見圖3。由圖3可見:氧化石墨中含有大量極性基團,其中3 000~3 700 cm-1處的寬吸收峰是氧化石墨中羥基及其吸收的水分子中羥基的伸縮振動峰,1 726 cm-1處是羧基上的伸縮振動峰,1 647 cm-1處為水分子的變形振動峰,1 248 cm-1處的吸收峰歸屬為環氧基的對稱伸縮振動峰,1 089 cm-1處歸屬為C—O—C振動吸收峰;氧化石墨被還原為石墨烯后表面官能團引起的吸收峰基本消失,在3 200~3 700 cm-1附近弱小吸收峰可能是未被還原的羥基及吸收的水分子中羥基的振動峰,在1 045 cm-1附近的吸收峰在還原后還存在,可能是納米粒子表面吸附羥基所致。
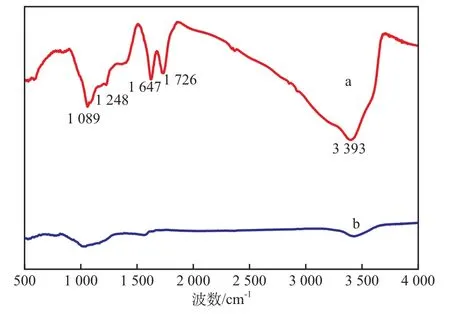
圖3 氧化石墨(a)和石墨烯(b)的FTIR譜圖
2.2 Ag-AgCl/石墨烯復合光催化劑的催化性能
2.2.1 可見光照射下的羅丹明B降解率
當初始羅丹明B質量濃度為5 mg/L時,Ag-AgCl和Ag-AgCl/石墨烯在可見光照射下的羅丹明B降解率見圖4。由圖4可見:當光照時間為10 min時,Ag-AgCl/石墨烯及Ag-AgCl對羅丹明B的降解率分別為72%和21%;當光照時間為60 min時,二者對羅丹明B的降解率分別為99%和73%,Ag-AgCl/石墨烯基本可將羅丹明B完全降解;與Ag-AgCl相比,Ag-AgCl/石墨烯對羅丹明B的降解速率更高,催化性能更強。
2.2.2 初始羅丹明B質量濃度對羅丹明B降解率的影響
初始羅丹明B質量濃度對羅丹明B降解率的影響見圖5。由圖5可見:當光照時間一定時,隨初始羅丹明B質量濃度的增加,羅丹明B降解率減小。這可能是因為當目標降解物初始質量濃度增加時,廢水中大量染料分子的存在影響催化劑對光能的吸收,催化劑的表面被染料占據,使得光生空穴在催化劑表面的活性位子數減少,從而降低了催化反應的效率。而隨著目標降解物質量濃度的降低,光生空穴在催化劑表面的活性位子數增加,染料分子與光生空穴之間反應的可能性增加,使羅丹明B降解率增大。
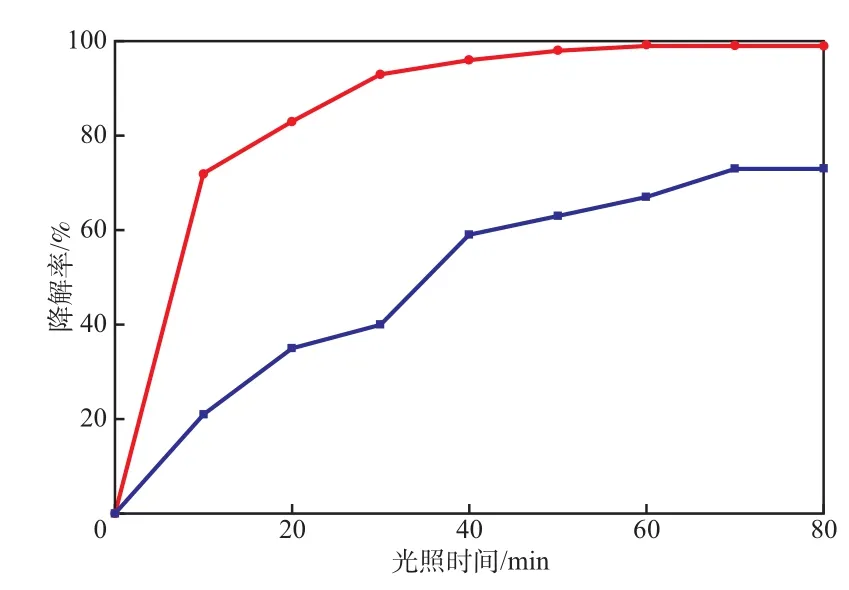
圖4 可見光照射下羅丹明B降解率
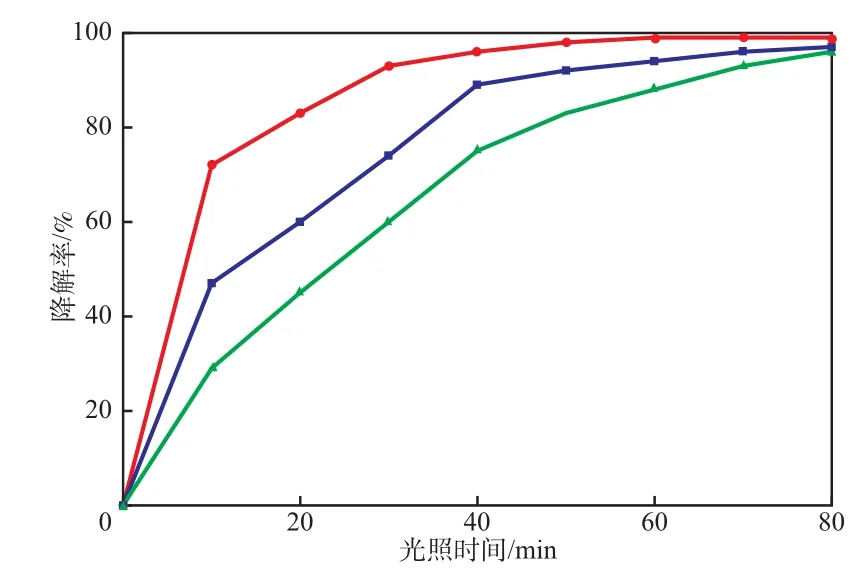
圖5 初始羅丹明B質量濃度對羅丹明B降解率的影響
2.2.3 Ag-AgCl/石墨烯的穩定性
為了了解Ag-AgCl/石墨烯的穩定性,做了重復使用實驗。實驗結果表明:復合光催化劑連續使用3次羅丹明B降解率均為99%;第5次使用時,羅丹明B降解率為98%。Ag-AgCl/石墨烯經多次使用后,羅丹明B降解率降低很小,說明Ag-AgCl/石墨烯復合光催化劑有良好的穩定性。
2.3 Ag-AgCl/石墨烯光催化反應機理
銀粒子的表面等離子體共振效應及電子-空穴對的產生使Ag-AgCl和Ag-AgCl/石墨烯在可見光照射下具有催化活性[7-8]。AgCl表面的負電性使與其接觸的銀粒子中的自由電子被極化,在AgCl的極場作用下,等離子體誘導電子向銀粒子表面遷移聚集,而空穴則移向AgCl表面對污染物分子進行氧化降解[4]。石墨烯優良的電子遷移能力能夠增加電荷轉移速率實現高效的電荷分離[12]。污染物分子向催化劑表面的傳遞會影響催化性能。由于羅丹明B和石墨烯之間大π鍵的存在[12],使污染物能夠被石墨烯快速吸附并在催化劑表面聚集。在光照下,催化劑表面富集的污染物分子加速與光生活性物種反應,因此提高了催化劑對羅丹明B的光催化降解速率。
3 結論
a)以石墨烯為載體, 采用原位化學沉淀—光還原法制備了Ag-AgCl/石墨烯復合光催化劑。將制備的催化劑用于光催化降解羅丹明B模擬廢水,用30 mg催化劑降解30 mL質量濃度為5 mg/L的羅丹明B模擬廢水,光照60 min后羅丹明B的降解率可達99%,羅丹明B的降解率隨其初始質量濃度的增加而降低。
b)Ag-AgCl/石墨烯復合光催化劑重復使用5次后降解率為98%,所制備的復合光催化劑具有良好的穩定性。
[1] 陳旭,王緒緒. 光催化技術[J]. 福建環境,2003,20(1):60-61.
[2] 范少華,崔玉民. 光催化技術在污水處理方面的應用[J]. 化工進展,2002,21(5):345-347.
[3] 韓金霞,崔玉民. 無機光催化技術研究進展[J]. 化學試劑,2004,26(2):76-80.
[4] Wang Peng,Huang Baibiao,Lou Zaizhu,et al. Synthesis of highly efficient Ag-AgCl plasmonic photocatalysts with various structures[J]. Chem Eur J,2010,16(2):538-544.
[5] An Changhua,Peng Sheng,Sun Yugang.Facile synthesis of sunlight-driven AgCl:Ag plasmonic nanophotocatalyst[J]. Adv Mater,2010,22(23):2570-2574.
[6] 周建偉,程玉良,黃艷芹,等. Ag@AgCl/MCM-41納米材料的制備及光催化性能研究[J]. 材料導報,2009,23(11):177-180.
[7] 周建偉,張引沁,姜雪鋒,等. Ag-AgCl/Al2O3復合光催化材料的制備與光催化性能研究[J].人工晶體學報,2011,40(6):1563-1568.
[8] Yu Jiaguo,Dai Gaopeng,Huang Baibiao. Fabrication and characterization of visible-light-driven plasmonic photocatalyst Ag/AgCl/TiO2nanotube arrays[J]. Phys Chem C,2009,113(37):16394-16401.
[9] Geim A K,Novoselov K S. The rise of graphene[J].Nature Mater,2007,6(3):183-191.
[10] Hummers W S,Offeman R E. Preparation of graphitic oxide[J]. J Am Chem Soc,1958,80(6):1339.
[11] Wang Guoxiu,Yang Juan,Park J,et al. Facile synthesis and characterization of graphene nanosheets[J].Phys Chem C,2008,112(22):8192-8195.
[12] Zhang Hui,Fan Xinfei,Quan Xie,et al. Graphene sheets grafted Ag@AgCl hybrid with enhanced plasmonic photocatalytic activity under visible light[J].Environ Sci Technol,2011,45(13):5731-5736.

