Pd和甲醛對Ag/C催化四氯化碳原位液相加氫脫氯性能的影響
周秀蓮,魯墨弘,朱 劼,李明時,單玉華,朱建軍
(常州大學 石油化工學院,江蘇 常州213164)
四氯化碳對臭氧層具有很強的破壞性。根據(jù)《關于消耗臭氧層物質的蒙特利爾議定書》,四氯化碳的生產(chǎn)和工業(yè)應用已經(jīng)被禁止。而工業(yè)上所有甲烷氯化物(如一氯甲烷、二氯甲烷和氯仿)生產(chǎn)工藝均會副產(chǎn)四氯化碳。因此,如何有效處理和利用四氯化碳已成為該領域可持續(xù)發(fā)展必須解決的難題。目前,對四氯化碳的處理最有效的方法是通過催化加氫使之轉化為有用的化合物。一般該轉化是在貴金屬Pt、Pd或者兩者組合的催化劑上與H2反應來實現(xiàn)[1-4]。Weiss等[5]最先發(fā) 現(xiàn) Pt/Al2O3催化劑 可 以對四氯化碳進行催化轉化。Lu等[6]研究了溶劑對四氯化碳液相催化轉化反應的影響,發(fā)現(xiàn)甲醇為溶劑時最利于提高Pd/C催化劑活性。孫建芝等[7]研究了四氯化碳液相加氫制氯仿的催化劑,發(fā)現(xiàn)在Pd/C中加入助劑Ag有效抑制了甲烷的生成,提高了氯仿的選擇性。盡管催化加氫法是綠色生產(chǎn)工藝,但H2來源不易,給企業(yè)生產(chǎn)帶來了困難[8]。Pena等[9]研究了甲醇催化分解制氫,發(fā)現(xiàn)合成甲醇的催化劑可以用于甲醇催化分解制氫的反應中,其中以Cu基催化劑為主。因此,無需外加氫源的催化加氫反應技術引起了人們的關注,這類新的液相催化加氫反應體系具有良好的應用前景[10]。
在本研究中,筆者考察了助劑對四氯化碳原位液相催化轉化反應的影響,重點考察了雙金屬催化劑中Pd/Ag摩爾比和助劑甲醛用量對Ag/C催化劑性能的影響,并探討了助劑的作用機制。
1 實驗部分
1.1 催化劑制備
采用等體積浸漬法制備Ag/C催化劑。采用共浸漬法制備雙金屬Pd-Ag催化劑,將配制好的相應濃度的硝酸銀和氯化鈀溶液浸漬在20~40目的活性炭顆粒上,浸漬24h后,將樣品于120℃干燥12h,然后置于立式固定床中,在25mL/min H2流下,400℃還原3h。還原結束后停止加熱,冷卻至室溫,取出密封備用。制備的所有催化劑中,Ag的質量分數(shù)均為8%。含Pd和Ag的催化劑記為Pd-Ag(x)/C,其中,x為Pd和Ag的摩爾比(x=0.01、0.03和0.05)。
1.2 催化劑活性評價
采用100mL有聚四氟內襯的高壓反應釜評價催化劑的催化活性。將5mL CCl4和25mL甲醇及0.3g催化劑加入反應釜后,擰緊釜蓋和取樣閥,用N2置換反應釜中的空氣至少3次,然后通入所需壓力的N21MPa,并開啟磁力攪拌器和控溫儀。待溫度升到130℃、壓力至2MPa,開始反應。反應結束后,將反應釜用冷水迅速冷卻至室溫,然后緩慢打開排氣閥釋放反應器內的壓力,尾氣經(jīng)堿液吸收后放空,通過抽濾回收催化劑和反應液。反應過程中,每隔一段時間收集液體產(chǎn)物,采用美國VARIAN CP-3800氣相色譜儀分析產(chǎn)物組成。色譜條件:30m×0.53mm SE-30彈性石英毛細管柱,F(xiàn)ID檢測,柱溫40~80℃,檢測室、氣化室溫度均為250℃,液相進樣量0.2μL。主要液相產(chǎn)物為CH2Cl2和CHCl3,反應過程中幾乎不產(chǎn)生CH4氣體,可采用歸一化法定量。
1.3 甲醇/甲醛分解反應
甲醇或甲醛的分解反應在高壓反應釜中進行。將物料及0.3g Ag/C催化劑加入反應釜后,先用N2置換反應釜中的空氣至少3次,再用Ar置換反應釜中的N2至少3次,然后通入所需壓力的Ar 1MPa,并開啟磁力攪拌器和控溫儀。待升到溫度130℃、壓力2MPa,開始反應。反應結束后,將反應釜與質譜儀連接,先開啟質譜儀走基線,載氣為Ar。待基線穩(wěn)定后,關閉Ar,打開釜的排氣閥,使釜內氣體進入質譜儀進行檢測。待氣體檢測完畢后,關閉排氣閥,打開載氣Ar。
1.4 催化劑的表征
采用日本理學D/max 2500PC粉末X-射線衍射儀分析樣品的晶相。Cu靶/石墨單色器,步進掃描,Ni濾波,管電壓40kV,管電流80mV。
采用英國Thmu公司Multilab2000型X射線光電子能譜儀測定催化劑的表面組成和元素的化合態(tài)。光源為Mg-Kα,通過能20eV,以C1s(284.6eV)峰來校準其他元素的XPS峰。
2 結果與討論
2.1 甲醇分解反應產(chǎn)物
考察了甲醇在Ag/C催化劑作用下的分解反應,通過質譜檢測CO2、CO、和H2。反應9h后釜內產(chǎn)物的質譜檢測結果示于圖1。
從圖1可以看出,在釜內氣體進入質譜儀0.01min后開始檢測到釜內氣體信號,Ar濃度沒有反應前走基線時的濃度高,因此Ar響應值略微下降。而H2響應值較基線顯著上升了2個數(shù)量級,說明反應生成了大量的H2,同時也檢測到了CO2和CO。因此,可以證明在Ag/C催化劑和所給反應條件下,甲醇可以發(fā)生自身分解反應,產(chǎn)生H2,從而可作為加氫反應的氫源。甲醇的分解反應如式(1)所示。
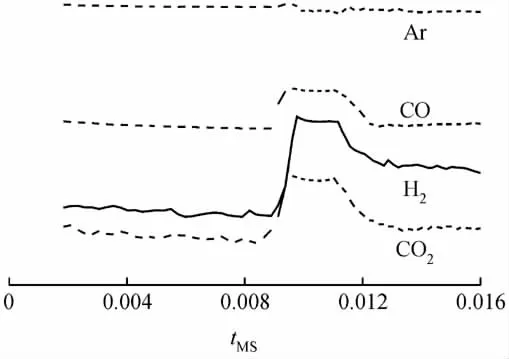
圖1 質譜檢測的甲醇分解反應結果Fig.1 The result of decomposition reaction of methanol detected by MS
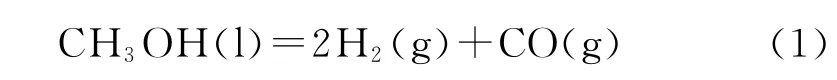
2.2 助催化劑Pd對Ag/C催化劑性能的影響
在Ag/C催化劑中加入不同量的Pd制備成Pd-Ag(x)/C催化劑(x=n(Pd)/n(Ag)),考察其在CCl4原位液相催化轉化反應中的催化活性。CCl4轉化率及各產(chǎn)物選擇性隨反應時間的變化示于圖2。
從圖2可以看出,在空白實驗中,即不加催化劑、其余條件保持不變的情況下,9h后CCl4轉化率為36.6%。這可能是因為在該反應條件下,CCl4與甲醇反應生成HCl,反應釜雖然使用了四氟內襯,不能保證完全與釜內壁隔絕,HCl蒸氣會對反應釜產(chǎn)生一定的腐蝕,形成的Fe2+溶解在反應液中,F(xiàn)e2+和Fe可能為還原劑[11],將CCl4還原脫氯生成CH2Cl2和 CHCl3。Deng等[12]通過加入能與 Fe2+形成絡合物的試劑證實,參與還原反應的Fe2+的數(shù)量有限。此外,如果沒有有效的催化劑,很難產(chǎn)生活性氫,且與空白實驗相比,使用催化劑后CCl4轉化率大幅提高,因此,可以忽略Fe對反應的影響。故以下內容中無特別要求,省略與空白實驗的對比,且每組CCl4的轉化率中均包含F(xiàn)e對于CCl4的轉化率的貢獻。

圖2 Pd-Ag(x)/C催化CCl4液相轉化反應的轉化率(X)和產(chǎn)物選擇性(s)隨反應時間的變化Fig.2 Conversion(X)and product selectivity(s)vs reaction time of CCl4liquid phase conversion reaction over Pd-Ag(x)/C catalyst
從圖2還可見,微量Pd的加入明顯提高了Ag/C催化劑的活性。隨著x的增加,即Pd-Ag(x)/C催化劑中Pd含量的增加,催化活性逐漸增加;但當x增加為0.05時,催化活性反而下降。反應2h時,采用Ag/C催化劑的CCl4轉化率為44.1%;采用Pd-Ag(0.01)/C、Pd-Ag(0.03)/C和 Pd-Ag(0.05)催 化 劑 時, 轉 化 率 分 別 為 64.3%、82.4% 和77.0%。Pd的加入對產(chǎn)物選擇性沒有影響,CH2Cl2和CHCl3選擇性之比值保持在6/4左右。這是因為甲醇在Pd-Ag(x)/C催化劑的作用下發(fā)生分解,催化劑表面形成活性物Ag-H,同時也形成了活性物[Pd0-H];隨著Pd含量的增加,活性物[Pd0-H]在催化劑表面富集得越來越多,使得催化劑的活性增強。但是當Pd負載量過大,分布在載體上的金屬粒子變大,甚至發(fā)生團聚,從而降低金屬活性中心的利用率,同時也影響了Ag的活性,使得產(chǎn)生的活性氫減少。因此Pd-Ag(0.03)/C為該反應的最適宜催化劑。
2.3 液體助劑對CCl4原位液相加氫脫氯反應的影響
2.3.1 甲醛溶液加入量的影響
由于甲醛為強還原劑,選擇甲醛溶液(質量分數(shù)37%~40%)為助劑,控制加入反應體系的液體的總體積為30mL,考察了甲醛溶液加入量對Ag/C催化CCl4液相轉化反應轉化率和產(chǎn)物選擇性的影響,結果如圖3所示。
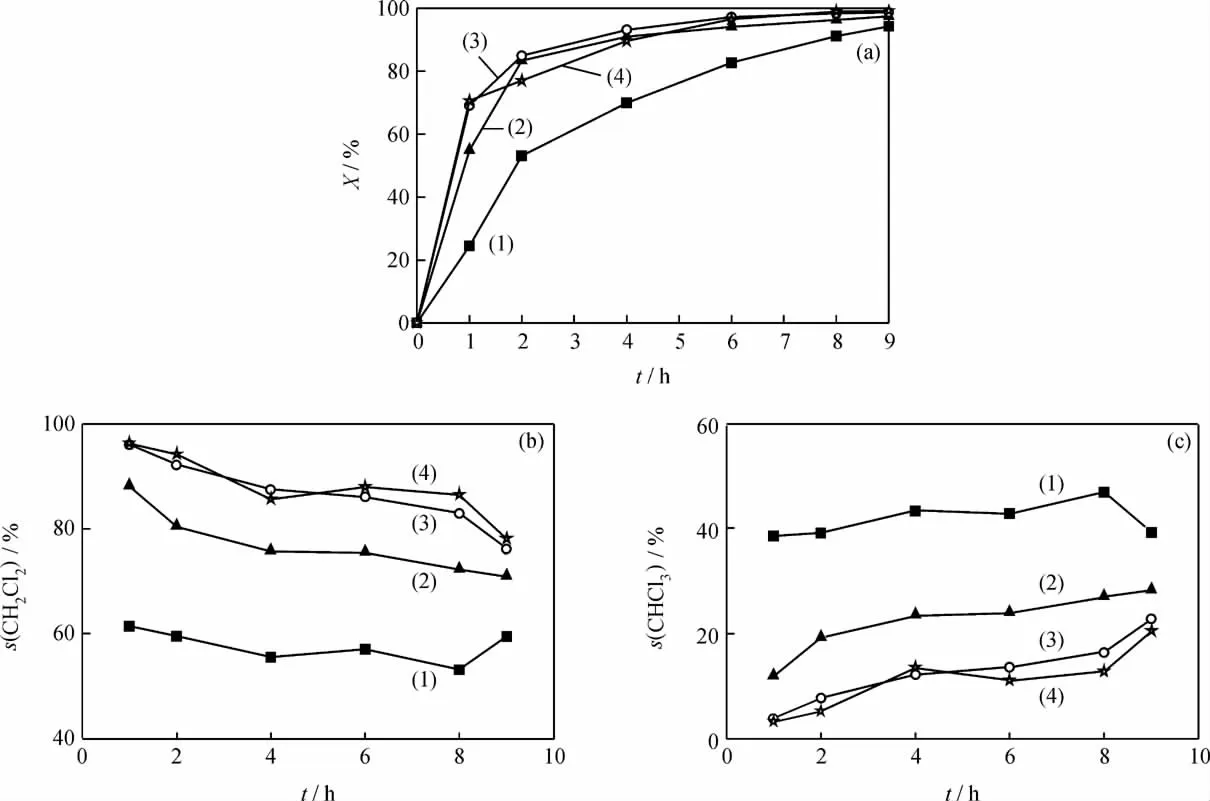
圖3 甲醛溶液加入量對Ag/C催化CCl4液相轉化反應轉化率(x)和產(chǎn)物選擇性(s)的影響Fig.3 Effect of formaldehyde solution addition on conversion and product selectivity(s)of CCl4liquid phase catalytic conversion(x)reaction over Ag/C catalyst
由圖3可以看出,在反應體系中加入甲醛溶液,CCl4轉化率明顯增加。隨著甲醛溶液加入量的增加,CCl4轉化率呈現(xiàn)先增加后降低的趨勢。反應2h時,不加甲醛溶液,CCl4轉化率為44.1%;加入2、5和10mL甲醛溶液后,轉化率分別達到83.4%、84.9%和77.0%。由此可見,當加入2mL甲醛溶液,CCl4轉化率就增加了近1倍;隨著反應時間的延長,甲醛溶液的加入量為5mL時,CCl4轉化率較2mL時略高。當甲醛溶液加入量為10mL時,CCl4轉化率反而有所下降,這是因為甲醛溶液過多時,水量就多,導致體系分層,從而抑制了反應的進行。張?zhí)煊赖龋?3]曾利用甲醛還原法代替催化加氫法,將硝基還原為胺基。向反應體系中加入甲醛溶液作為助劑,一方面甲醛在催化劑作用下,可發(fā)生分解產(chǎn)生H2;另一方面因其具有較強的還原性[14-15],可加快催化劑表面形成的Ag-Cl物種還原為Ag的進程,使得催化劑表面的Ag-H物種增多。
由圖3還可以看出,甲醛溶液的加入使產(chǎn)物的選擇性有明顯的改變。不加甲醛時,CH2Cl2和CHCl3同時生成,且其選擇性隨反應時間的延長基本保持穩(wěn)定,分別在60%和40%左右。加入甲醛后,CH2Cl2和CHCl3也是同時生成,但隨著甲醛量的增加,CH2Cl2選擇性明顯增加,而CHCl3選擇性顯現(xiàn)下降的趨勢;隨著反應進行,CH2Cl2選擇性緩慢下降,CHCl3選擇性緩慢上升。甲醛溶液加入量為5mL和10mL時,CH2Cl2和CHCl3選擇性變化不大。
盡管甲醛溶液的加入量為5mL時,CCl4轉化率較加入量2mL時略高,但CH2Cl2選擇性明顯提高。因此,選擇甲醛溶液量為5mL進行下一步研究。
2.3.2 驗證實驗
石小玉[16]研究發(fā)現(xiàn),少量的水對CCl4的轉化反應有促進作用。由于甲醛溶液中含有大量的水,為了驗證甲醛對反應的促進作用,筆者選用三聚甲醛(質量分數(shù)≥98%)作為助劑。本反應體系為酸性體系,而三聚甲醛在酸的作用下,可重新分解成甲醛,它是甲醛的一種特殊商品形式。經(jīng)計算,5mL上述甲醛溶液中水的體積為2.7mL,甲醛的摩爾量與2.1g三聚甲醛中甲醛的摩爾量相當。考察了2.7 mL水和2.1g三聚甲醛單獨存在下對CCl4催化轉化反應轉化率和產(chǎn)物選擇性的影響,結果如圖4所示。
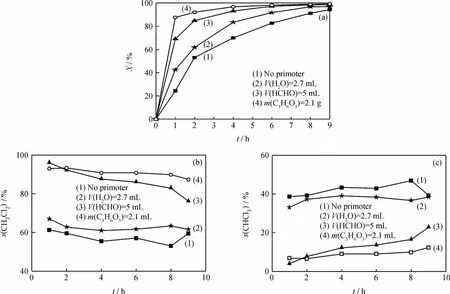
圖4 甲醛和水對CCl4催化轉化反應轉化率和產(chǎn)物選擇性的影響Fig.4 Effect of formaldehyde and H2O on conversion and product selectivity of CCl4liquid phase catalytic conversion reaction
由圖4可以看出,甲醛加入對CCl4轉化率的影響較大。反應1h時,不加任何助劑,CCl4轉化率為24.4%;加入助劑H2O、甲醛溶液和三聚甲醛,對應 的 CCl4轉 化 率 分 別 為 42.6%、69.1% 和87.6%。單獨加入2.7mL H2O后,CCl4轉化率上升,與石小玉[16]的研究結果相吻合。與H2O相比,加入甲醛溶液后,CCl4轉化率明顯上升,說明甲醛溶液中甲醛對該反應的促進作用比H2O明顯。而加入三聚甲醛比加入甲醛溶液時的CCl4轉化率更高,這可能因為三聚甲醛加入反應體系后就被分解為甲醛,其甲醛量與甲醛溶液中的甲醛量相等,但甲醛溶液會帶入過量的水,對反應不利。這一驗證結果更加證實了甲醛對CCl4催化轉化反應的促進作用。
由圖4還可以看出,與不加任何助劑相比,2.7mL H2O的加入對產(chǎn)物的選擇性沒有明顯影響,CH2Cl2選擇性保持在60%左右,CHCl3選擇性保持在40%左右。當向體系中加入甲醛溶液后,CH2Cl2選擇性明顯提高,CHCl3選擇性明顯下降;隨著反應的進行,CH2Cl2選擇性呈現(xiàn)下降的趨勢,由96.1%下降到76.3%;CHCl3選擇性呈現(xiàn)上升的趨勢,由3.9%上升至22.8%。向體系中加入三聚甲醛,CH2Cl2選擇性最高,保持在90%左右,CHCl3選擇性保持在10%左右。說明甲醛的加入明顯改變了CCl4液相催化轉化反應的產(chǎn)物分布。
2.4 CCl4液相催化轉化反應中甲醛作用機制的初步探討
2.4.1 反應前后Ag/C催化劑的晶相結構和Ag價態(tài)的變化
對加有甲醛溶液的CCl4液相催化轉化反應前后的Ag/C催化劑進行了XRD表征,結果如圖5所示。
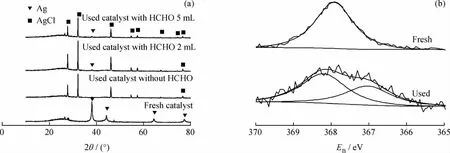
圖5 加有甲醛溶液的CCl4液相催化轉化反應前后Ag/C催化劑的XRD和XPS譜Fig.5 XRD and XPS patterns of Ag/C catalyst after CCl4liquid phase catalytic conversion reaction with formaldehyde solution added
由圖5可以看出,反應前Ag/C催化劑在2θ為38.1°、44.3°、64.5°和 77.8°處出現(xiàn)了比較明顯的Ag的特征衍射峰。不加甲醛溶液反應9h后的Ag/C催化劑的XRD譜中出現(xiàn)AgCl的特征衍射峰[17]。經(jīng)計算,0.3g Ag/C催化劑中含0.22mmol的Ag,5μL CCl4含0.21mmol的Cl。也就是說5μL CCl4幾乎可以將0.3g Ag/C催化劑的Ag全部轉化為AgCl;當將CCl4的量放大到1000倍,即5mL時,反應9h,CCl4轉化率仍在90%左右(見圖2),說明該催化反應還是能進行下去。筆者直接制備了與Ag/C催化劑中Ag的摩爾量相等的AgCl/C的催化劑,其反應活性與Ag/C相當。筆者猜想在無甲醛的反應體系中,Ag/C催化劑表面經(jīng)歷了由活性組分Ag轉變?yōu)锳gCl,然后又被還原為Ag的循環(huán)往復的過程,從而保證了催化劑的活性。
反應體系中加入甲醛溶液反應后的Ag/C催化劑均具有AgCl的特征衍射峰,同時在2θ為38.1°處出現(xiàn)Ag(111)晶面的衍射峰,且隨著甲醛溶液量的增加,該衍射峰逐漸增強。這說明在反應體系中,甲醛的加入可能加速了催化劑表面Ag-Cl物種還原為Ag的循環(huán)過程,從而保證了催化劑的活性。
反應前后Ag/C催化劑的XPS譜見圖5。由于XPS對Ag不敏感,因此不能精確地從化學位移來判斷Ag的價態(tài)。從圖5可見,反應前的Ag/C催化劑只有1種價態(tài)的Ag,根據(jù)其結合能并結合圖5 XRD表征結果可以認為,是0價態(tài)的金屬Ag。反應后的Ag/C催化劑明顯存在2種不同價態(tài)的Ag,結合圖5XRD表征結果可以認為,它們是Ag0和Ag+1。由此筆者推測,在反應過程中,Ag0總是存在,由它催化甲醇的分解,產(chǎn)生反應所需的活性氫(Ag-H)。
2.4.2 甲醛分解反應
考察了甲醛溶液在Ag/C催化劑作用下的自身分解反應,通過質譜檢測H2,結果示于圖6。
圖6為Ar氛圍中,甲醛在Ag/C催化劑作用下發(fā)生分解反應,反應9h后釜內產(chǎn)物經(jīng)質譜檢測的結果。從圖6可以看出,甲醛分解反應產(chǎn)生的氣體極少,因此Ar響應值幾乎不變;H2(實線表示)響應值上升了0.5個數(shù)量級,與空氣中H2(虛線表示)的響應值相當。與甲醇分解反應檢測的氣體信號相比(見圖1),可以認為在催化劑和所給反應條件下,甲醛分解反應中幾乎不產(chǎn)生H2。
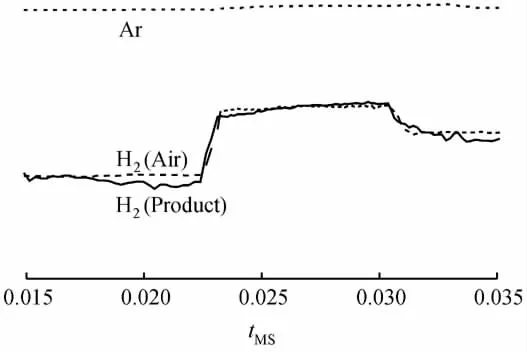
圖6 質譜檢測的甲醛自身分解反應結果Fig.6 The result of decomposition reaction of formaldehyde detected by MS
綜上可知,反應體系的活化氫主要由甲醇提供,甲醛主要起加速催化劑表面Ag-Cl物種還原為活性物種Ag的作用。
3 結 論
(1)采用Pd摻雜的Ag/C催化劑,不改變CCl4轉化反應的產(chǎn)物分布,但明顯提高了Ag催化劑的活性,以n(Pd)/n(Ag)為0.03的Pd-Ag/C催化劑的活性最高。
(2)助劑甲醛溶液的加入明顯提高了Ag/C催化劑催化CCl4轉化反應轉化率和CH2Cl2的選擇性,以甲醛溶液為5mL時轉化率和CH2Cl2的選擇性最高,同時證實甲醛溶液中的甲醛對反應的促進作用明顯大于水的促進作用。
(3)助劑三聚甲醛的加入明顯提高了Ag/C催化劑催化CCl4轉化反應轉化率和CH2Cl2的選擇性。三聚甲醛在酸的作用下,可分解成甲醛,起到甲醛的作用。甲醛在該體系中主要起加速催化劑表面Ag-Cl物種還原為Ag的作用。
[1]WEISS A H, GAMBHIR B S,LEON R B.Hydrodechlorination of carbon tetrachloride[J].Journal of Catalysis,1971,22(2):240-245.
[2]CHOI H C,CHOI S H,LEE J S,et al.Effects of Pt precursors on hydrodechlorination of carbon tetrachloride over Pt/A12O3[J].Journal of Catalysis,1997,166(2):284-293.
[3]LUISA M A,GOMEZ S L,SEOANE A A.Hydrodechlorination of carbon tetrachloride in the liquid phase on a Pd/carbon catalyst:Kinetic and mechanistic studies[J].Applied Catalysis B:Environmental,2004,53(2):101-110.
[4]蔣曉原,毛建新,陸維敏,等.四氯化碳加氫制氯仿Pt-Pd/C催化劑的制備與研究[J].石油化工,2000,29 (7):484-485.(JIANG Xiaoyuan,MAO Jianxin,LU Weimin,et al.Studies of Pt-Pd/C catalyst for hydrogenation of CCl4to CHCl3[J].Petrochemical Technology,2000,29(7):484-485.)
[5]WEISS A H, VALINSKI S,ANTOSHIN G V.Hydrodechlorination and oligomerization of carbon tetrachloride over nickel Y zeolites[J].Journal of Catalysis,1982,74(1):136-139.
[6]LU Mohong,SUN Jianzhi,LI Mingshi,et al.High selective hydrodechlorination of CCl4into CHCl3on Ag-Pd/carbon catalysts[J].React Kinet Mech Catal,2010,100(1):99-103.
[7]孫建芝,張東寶,魯墨弘,等.Ag-Pd/C催化四氯化碳液相加氫反應的研究[J].高校化學工程學報,2010,24 (5):795-800.(SUN Jianzhi,ZHANG Dongbao,LU Mohong,et al. Hydrogenation of carbon tetrachloride over Ag-Pd/C catalysts in liquid phase[J].Journal of Chemical Engineering of Chinese Universities,2010,24(5):795-800.)
[8]沈穎旎,羅智偉,嚴新煥.原位液相催化加氫法合成N-乙基苯胺和N,N-二乙基苯胺[J].催化學報,2008,29(7):612-616.(SHEN Yingni,LUO Zhiwei,YAN Xinhuan.In situ liquid-phase catalytic hydrogenation for the synthesis ofN-ethylaniline andN,N-diethylaniline[J].Chinese Journal of Catalysis,2008,29(7):612-616.)
[9]PENA M A,GOMEZ J P,F(xiàn)IERRO J L G.New catalytic routes for syngas and hydrogen production[J].Applied Catalysis A:General,1996,144(1):7-57.
[10]ZHOU L,YAN X H.A novel transfer hydrogenation with high hydrogen utilization for the hydrogenation of halogenated nitrobenzene without hydrodehalogenation[J].Catalysis Letters,2009,132(1-2):16-21.
[11]MATHESON L J,TRATNYEK P G. Reductive dehalogenation of chlorinated methanes by iron metal[J].Environmental Science and Technology,1994,28(12):2045-2051.
[12]DENG B,BURRIS D R,CAMPBELL T J.Reduction of vinyl chloride in metallic iron-water system [J].Environmental Science and Technology,1999,33(15):2651-2658.
[13]張?zhí)煊溃瑥堄烟m,刑文康.甲醛還原法制備2,2’-二氯氫化偶氮苯[J].應用化學,2004,21 (5):521-523.(ZHANG Tianyong,ZHANG Youlan,XING Wenkang.Preparation of 2,2’-dichlorohydrazobenzene by formaldehyde reduction[J].Chinese Journal of Applied Chemistry,2004,21(5):521-523.)
[14]CHOU K S,REN C Y.Synthesis of nanosized silver particles by chemical reduction method[J].Materials Chemistry and Physics,2000,64(3):241-246.
[15]KHANNA P K,SINGH N,CHARAN S,et al.Synthesis and characterization of Ag/PVA nanocomposite by chemical reduction method[J].Materials Chemistry and Physics,2005,93(1):117-121.
[16]石小玉.四氯化碳催化加氫研究[D].常州:常州大學,2010.
[17]張燕,王源升,宋玉蘇.納米AgCl粉末制備高穩(wěn)全固態(tài)Ag/AgCl電極[J].武漢理工大學學報,2008,30(9):32-35.(ZHANG Yan, WANG Yuansheng,SONG Yusu.Preparation of steady solid Ag/AgCl electrode by AgCl nano-powders[J].Journal of Wuhan University of Technology,2008,30(9):32-35.)

