射頻消融聯合骨成形術治療髂骨巨細胞瘤一例
宋紅梅,吳春根,田慶華,程永德
患者女,45歲。主因“右側骶髂部酸痛伴下腹部墜脹感2個月”入院。患者2個月前右側骶髂部無明顯誘因下出現酸痛伴下腹部墜脹感,行走時右下肢無力。2012年4月CT提示:右髂骨骨質破壞灶,建議進一步檢查。PET-CT示:右髂骨病灶,考慮嗜酸性肉芽腫可能,轉移瘤不除外。2012年5月2日門診以“右髂骨腫瘤,良惡性待定”收入院。一般檢查無特殊。患者甲狀腺功能亢進病史半年余,現服藥控制,病情穩定。否認腫瘤病史,否認家族遺傳病史。經患者與家屬知情同意,于2012年5月3日在DSA監控下行右髂骨活檢、射頻消融聯合骨成形術(POP)。
手術經過:患者取俯臥位,手術區域常規消毒鋪巾,在C型臂X線機引導下定位,局部逐級麻醉穿刺通道,透視下將骨穿針(13 G,COOK公司,美國)穿入右髂骨病灶內,注入少量對比劑后,顯示病灶輪廓,經正側位確認,用活檢槍取出部分組織送病理,然后插入射頻針,加熱至80℃,持續約10 min,調和骨水泥,待黏稠后用高壓注射器緩慢注入(COOK公司,美國)右髂骨病灶內,注入量4 ml左右,術畢壓迫止血,包扎傷口(圖1)。術后CT示:骨水泥填充完全,無外滲(圖2)。術后活檢結果提示:富于巨細胞性腫瘤,間質細胞增生活躍,有少量可疑瘤骨形成,良惡性待定,建議定期隨訪。
術后患者出于對“骨腫瘤”的恐懼心理,在與骨科醫師充分溝通后,仍強烈要求進行腫瘤切除術,遂于2012年5月22日再次行右髂骨切開活檢并刮除植骨內固定術,術中沿右髂骨翼做弧形切口,逐層切開皮膚及皮下組織,暴露髂骨翼外側,透視確定病灶位置,開骨窗2 cm×2 cm,內見棕黃色液體,周圍有肉芽樣囊壁組織,徹底刮除囊壁,用石炭酸和乙醇處理骨腔,并植入同種異體骨。術后病理提示:右髂骨腫瘤微創手術治療后腫塊擴大切除,髂骨內見大片凝固性壞死,未見明顯活躍的腫瘤細胞,髓腔纖維組織、反應性骨質增生,伴慢性炎細胞浸潤,請注意隨訪(圖3)。
討論
骨巨細胞瘤是臨床上常見的進行性、骨質破壞性病變,起源于骨髓結締組織的間充質細胞,因含有巨細胞而得名。好發于20~40歲成年人,女性略多。多見于股骨下端及脛骨上端,偶爾見于骶骨或者骨盆。骨巨細胞瘤具有潛在惡性,其多數典型CT表現為膨脹性骨質破壞,有包殼包繞,邊界清楚,有時可見病變內骨性分隔或假分隔形成,一般無骨膜反應,多數無鈣化。但不少病例發生部位少見,影像缺乏特征性,需要與骨肉瘤、嗜酸性肉芽腫甚至轉移瘤相鑒別。因此,對其判定應臨床、病理、影像諸方面結合。我們認為對特殊部位的膨脹性骨質破壞,皮質變薄,破壞區內有細小骨嵴者應考慮本病的可能性。
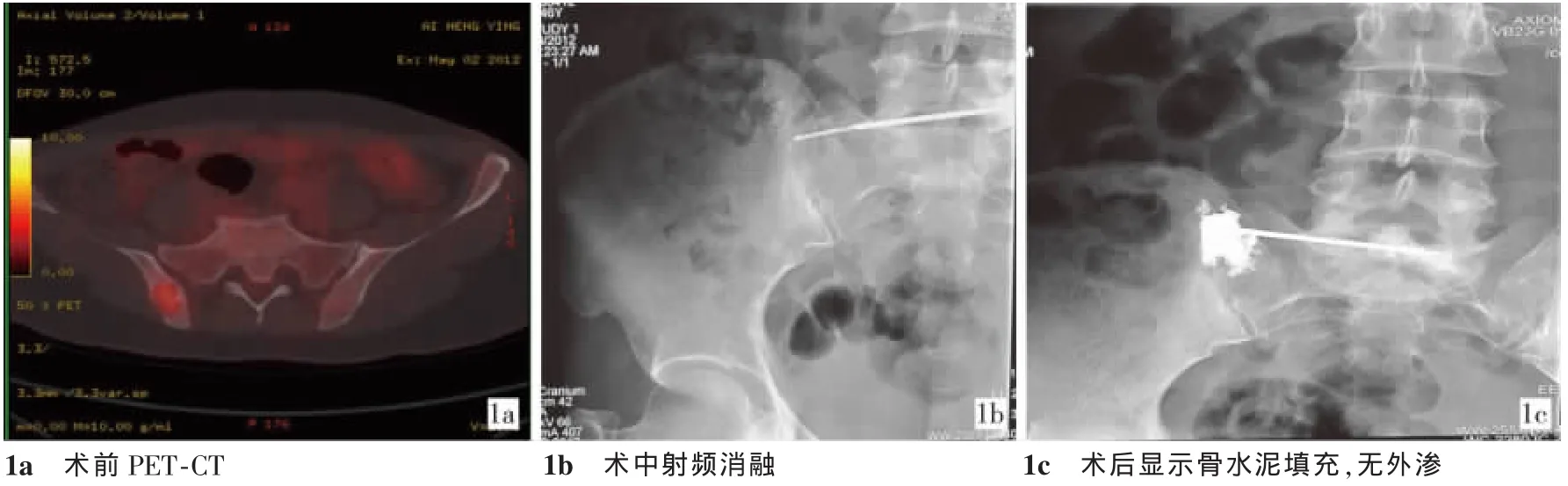
圖1 髂骨巨細胞瘤治療過程
骨巨細胞瘤因具有多變的生物學行為,且極易復發,治療目標主要是去除腫瘤病灶,控制腫瘤復發和修復骨缺損,維護骨骼功能[1]。該患者入院時診斷不明確,骨腫瘤(良惡性待定)、嗜酸性肉芽腫[2]均在考慮,在與患者及家屬充分溝通后,采用了活檢、射頻消融聯合POP治療。射頻消融一方面通過高溫殺滅腫瘤細胞,同時起到緩解疼痛的作用;另一方面,腫瘤組織壞死會形成一個反應性水腫帶,切斷腫瘤血供,對防止腫瘤轉移亦起到一定的屏障作用。骨水泥則在凝聚過程中釋放大量熱量及一定的毒性作用,也可殺滅殘留的腫瘤細胞。Schaefer等[3]認為采用射頻消融聯合POP治療效果可以疊加,具有協同作用,射頻消融在殺滅腫瘤細胞的同時,所產生的熱量可促使骨水泥彌散分布更均勻,使得骨水泥的沉積更符合骨的力學結構;骨水泥成形術也可通過加固消融部位以增強射頻消融減輕疼痛的效果。

圖2 術后CT橫斷面+冠狀位
該患者手術順利,骨水泥填充完全,無外滲。術前患者的VAS評分為7分,術后3 d為4分,術后2周為3分,療效確切。射頻消融時,能量隨傳播距離的增大而迅速下降,其程度與傳播距離的平方成反比。為保證腫瘤細胞的徹底滅活,腫瘤的消融范圍至少應包括周圍1 cm以上的正常組織。單個消融電極使組織壞死區域最多為1.5 cm[4],對于大的直徑超過5 cm,以及鄰近重要血管和神經的病灶,單純的消融很難達到理想的治療效果,目前認為射頻消融治療的腫瘤范圍以不超過6 cm為宜。該患者病灶較局限,范圍較小,為1.8 cm×3.3 cm,從術后病理可以看出本例消融較徹底,患者臨床癥狀也明顯改善。
因此,射頻消融技術聯合POP在治療骨巨細胞瘤方面的應用很有價值,但對其遠期療效評估仍需大量臨床應用以及長期隨訪。

圖3 術前、術后病理圖像
[1]丁羅賓,呂 智.骨巨細胞瘤診斷與治療現狀[J].國際骨科學雜志,2011,32:40-42.
[2]何 煜,吳春根,顧一峰,等.兒童脊柱嗜酸性肉芽腫介入干預臨床價值初探[J].介入放射學雜志,2011,20:729-732.
[3]Schaefer O,Lohrmann C,Markmiller M,et al.Combined treatmentofa spinalmetastaseswith radiofrequency heat ablation and vertebroplast [J].Am J Roentqenol,2003,180:1075-1077.
[4]Moser T,Buy X,Goyault G,et al.Image-guided ablation of bone tumors: review of current technjques [J].J Radiol,2008,89:461-471.

