糖痹康湯治療2型糖尿病周圍神經病變氣陰兩虛兼血瘀證60例*
蘆少敏,張定華,張雅嫻
(1.甘肅省中醫院內分泌科,甘肅 蘭州 730050; 2.甘肅中醫學院2011級碩士研究生,甘肅 蘭州 730000)
糖尿病周圍神經病變(diabetic peripheral neuropathy,DPN)是糖尿病病變過程中最常見的神經病變,與糖尿病視網膜病變以及糖尿病腎病并稱為糖尿病3大并發癥,多表現為四肢遠端感覺、運動障礙,肢體麻木、攣急疼痛,肌肉無力和萎縮,腱反射減弱或消失等,具有起病緩慢、隱匿性強、癥狀逐漸加重、不易逆轉的特點。其發生機制尚未完全明了,但普遍認為與高血糖引起的代謝異常、神經營養因子缺乏、微血管病變、自由基損傷及基因表達異常等因素有關[1];而血流動力學異常和血管病變也是引起神經缺血的重要因素之一[2]。有報道認為:DPN的發生與C-肽的含量呈負相關[3-4]。筆者也做了相應的臨床觀察[5],認為西醫治療僅能對DPN的特定環節起作用,并不能有效阻止本病的發生和發展。2011年1月—2013年4月,筆者采用糖痹康湯治療2型糖尿病周圍神經病變氣陰兩虛兼血瘀證60例,總結報道如下。
1 一般資料
選取本院住院或門診符合中西醫診斷標準2型糖尿病周圍神經病變氣陰兩虛兼血瘀證患者120例。采用隨機數字表法隨機分為治療組和對照組。治療組60例,男31例,女29例;年齡40~75歲,平均(55.23±4.71)歲;糖尿病病程5~26 a,平均(12±2.37) a;周圍神經病病程0.6~7 a,平均(3.18±1.05) a;使用胰島素治療者33例,使用口服降糖藥治療者13例,胰島素聯合口服降糖藥治療者14例。對照組60例,男33例,女27例;年齡43~75歲,平均(58.68±3.22)歲;糖尿病病程4~28 a,平均(11.18±2.98) a;周圍神經病病程0.6~8 a,平均(3.41±1.14) a;使用胰島素治療者32例,使用口服降糖藥治療者11例,胰島素聯合口服降糖藥治療者17例。兩組患者一般資料對比,差別無統計學意義(P>0.05),具有可比性。
2 病例選擇標準
2.1 中醫診斷標準
按照《中藥新藥臨床研究指導原則》[6]消渴病分期辨證標準,選擇證屬氣陰兩虛兼血瘀證者。主要表現為肢體麻木不仁,肢涼疼痛或有燒灼感,以下肢為甚,入夜加劇,神疲乏力,腰膝酸軟,舌暗或有瘀斑,脈沉細或澀。
2.2 西醫診斷標準
按照《糖尿病周圍神經病變診療規范》[7]及《實用神經病學》[8]標準。1)有明確的糖尿病病史。2)在診斷糖尿病時或之后出現的神經病變。3)電生理檢查提示神經傳導速度減慢,臨床癥狀和體征符合糖尿病周圍神經病變的表現,常伴有四肢末梢感覺異常或感覺障礙,其疼痛性質多樣,如針刺樣、燒灼樣或刀割樣疼痛,可伴或不伴肌萎縮、肌無力(主要影響下肢)。4)以下5項檢查中如果有2項或2項以上異常者診斷為DPN:①溫度覺異常;②尼龍絲檢查足部感覺減退或消失;③振動覺異常;④踝反射消失;⑤神經傳導速度(NCV)有2項或2項以上減慢。5)排除其他病變,如頸腰椎病變、腦梗死等。
3 試驗病例標準
3.1 納入病例標準
①符合DPN西醫診斷標準;②符合中醫診斷標準;③40~75歲之間;④簽署知情同意書,志愿受試者,可納入試驗病例。
3.2 排除病例標準
①合并有肝、腎功能不全及造血系統等嚴重原發性疾病;②妊娠或哺乳期婦女;③年齡>75歲<40歲;④惡性高血壓、臨床期糖尿病腎病(Ⅳ~Ⅴ期)、心肌梗死、腦血管意外等重癥病史;⑤有急性感染、糖尿病足壞疽、糖尿病酮癥酸中毒。凡具備上述任意1條的患者均予以排除。
4 治療方法
兩組均給予控制飲食、運動、降血糖、降血壓等基礎治療,對照組給予維生素B1100 mg/次、維生素B6100 mg/次,3次/d,口服;甲鈷胺0.5 mg/次,2次/d,口服。治療組在對照組用藥基礎上加服糖痹康湯,藥物組成:黃芪30 g,山茱萸15 g,當歸10 g,雞血藤30 g,桂枝10 g,赤芍20 g,牛膝15 g,地龍15 g,威靈仙30 g,丹參20 g。1 d 1劑,水煎,分早晚2次口服。
兩組均以12周為1個療程,共治療1個療程。
5 觀測指標及方法
兩組治療前后肢體麻木、疼痛、肌無力等癥狀變化及膝、跟腱反射等體征變化。兩組治療前后FPG、2 h PG、HbA1c及C-肽變化。兩組治療前后血脂指標(包括TC、TG、HDL-C、LDL-C);血流動力學指標(包括全血高切黏度、全血低切黏度、血漿黏度、紅細胞比容及紅細胞聚集指數)。采用廣州產WOND2000C肌電誘發電位儀,測定治療前后正中神經、尺神經、腓總神經及腓腸神經的運動神經傳導速度(MNCV)和感覺神經傳導速度(SNCV)。
6 療效判定標準
參照參考文獻[9]制訂。顯效:自覺癥狀、體征消失,腱反射基本正常,神經傳導速度增加>5 m/s或恢復正常。有效:自覺癥狀和體征明顯減輕,出現頻度和持續時間明顯減少,腱反射未完全恢復正常,神經傳導速度增加<5 m/s。無效:自覺癥狀無好轉,鍵反射無改善,神經傳導速度無變化。
7 統計學方法
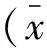
8 結 果
8.1 兩組療效對比
見表1。兩組對比,經Ridit分析,u=2.06,P<0.05,差別有統計學意義。

表1 兩組療效對比
8.2 兩組治療前后血脂變化對比
見表2。

表2 兩組治療前后血脂變化對比
8.3 兩組治療前后FPG、2 h PG、HbA1c變化對比
見表3。

表3 兩組治療前后FPG、2 h PG、HbA1c變化對比
8.4 兩組治療前后血流動力學指標變化對比
見表4。
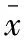
表4 兩組治療前后血流動力學指標變化對比 ±s
8.5 兩組治療前后MNCV、SNCV變化對比
見表5。

表5 兩組治療前后MNCV、SNCV變化對比
8.6 兩組治療前后C-肽含量對比
見表6。

表6 兩組治療前后C-肽含量對比
9 討 論
慢性高血糖是糖尿病周圍神經病變發生的主要原因。高血糖可引起一系列代謝異常,亦可通過其他間接因素作用于神經組織導致導致神經病變,而糖尿病神經病變的另一個重要因素是微血管病變所致的神經缺血缺氧。血管閉塞所致循環障礙,尤其是微循環障礙引起的血供不足,最終導致組織缺血缺氧。本病屬中醫學“痹證”“血痹”范疇。仲景謂:“血痹者,曰尊榮人骨弱,肌膚盛重,因疲勞汗出,臥不時動搖,加被畏風,遂得之。”大抵此證原于質虛勞倦之故,蓋尊榮者,素安閑,故骨弱;素膏粱,故肌膚盛,符合現代醫學肥胖及缺少運動誘發2型糖尿病的發病機制。消渴日久,久病必虛,耗傷正氣,引起氣血不足,脈絡痹阻,使氣血不能濡養四肢,陽氣不能布達四末,產生肌膚不仁、麻木、疼痛等癥狀。正如《靈樞·五變》云:“五藏皆柔弱者, 善病消癉。”《類證治裁》曰:“諸氣血凝滯, 久而成痹。”糖痹康湯就是遵循這一理論選方,方中黃芪、山茱萸滋陰益氣;當歸、赤芍、牛膝、丹參活血化瘀,理氣止痛;威靈仙、雞血藤、桂枝、地龍舒筋活絡,養血通脈。
現代藥理實驗表明:當歸、赤芍能夠擴張血管,改善微循環,并對血管內皮起到直接保護作用[10];黃芪具有改善蛋白質、脂肪及糖類代謝,調節免疫功能,改善血液動力學異常變化,抗血栓等作用[11];丹參中的有效成份丹參酮ⅡA 磺酸鈉、丹參素等能夠抑制體外血栓的形成,并通過抑制ADP誘導血小板聚集,使血小板黏性降低,通過抑制磷酸二酯酶的活力,增加血小板中C-AMP,從而抑制血小板的聚集[12];山茱萸有胰島素樣保護作用,同時具有增強小鼠體力、抗疲勞、耐缺氧和增強記憶力的作用[13];芍藥苷是赤芍的主藥效成分之一,芍藥苷可通過活化腺苷A1 受體來抑制神經細胞營養不良,改善6-羥基多巴胺誘導的神經損傷[14];威靈仙煎劑對熱刺激引起的疼痛反應能明顯提高小鼠的痛闡值,并且酒炙品的鎮痛作用較強且持久[15];地龍善入絡搜剔,滌痰逐瘀力專,有鎮痛作用;雞血藤有鎮痛、擴血管、抗凝血、抑制血小板凝聚、抗炎等作用[16];牛膝中含有的植物甾酮類成分,有調節糖代謝、抗脂質過氧化、保護內皮細胞等作用[17]。諸藥合用,共奏益氣養陰、活血化瘀、通絡止痛之效。糖痹康湯采用純中藥制劑,不僅減輕了西藥的副作用,改善臨床癥狀,同時起到輔助降血糖、降低血黏度、降血脂作用,保護血管內皮,調節蛋白質、脂肪及糖等物質代謝,調節機體免疫功能,改善異常的血流動力學變化,并減輕氧自由基損傷等作用,且具有改善C-肽功能的作用。
本臨床觀察表明:采用益氣養陰、活血化瘀、通絡止痛之糖痹康湯治療DPN,可明顯緩解或解除臨床癥狀,并改善神經傳導速度,通過早期治療,可達到有效延緩神經病變的作用。
[1]衡先培.糖尿病性神經病變診斷與治療[M].北京:人民衛生出版社,2002:12-23.
[2]劉磊,邵政一.糖尿病周圍神經病變發病機制研究進展[J].南通醫學院學報,2004,24(1):115-117.
[3]Sima AA.New insights into the metabolic and molecular basis for diabetic neuropathy[J].Cell Mol Life Sci,2003,60(11):2445-2464.
[4]金興權,王麗萍,張斌,等.C-肽變化與糖尿病周圍神經病變的關系[J].山東醫藥,2009,49(37):16-18.
[5]蘆少敏.糖尿病周圍神經病變與C-肽關系的臨床觀察[J].西部中醫藥,2011,24(10):65-66.
[6]胡仁明,樊東升.糖尿病周圍神經病變診療規范(征求意見稿)[J].中國糖尿病雜志,2009,17(8):638-640.
[7]史玉泉.實用神經病學[M].2版.上海:上海科學技術出版社,1995:986-989.
[8]鄭筱萸.中藥新藥臨床研究指導原則[M]. 北京:中國醫藥科技出版社,2002:233-235.
[9]蔡少雄,向海燕,蘭國斌,等.舒血寧注射液與甲鈷胺聯合治療糖尿病周圍神經病變的研究[J].中華中醫藥雜志,2008,23(1):77-78.
[10]王娟.常用活血化瘀中藥的現代研究[J].時珍國醫國藥,2006,17(10):2082-2083.
[11]黃飛華,夏翔,柳玉瑾,等.復方黃芪飲治療老年期癡呆60例臨床研究[J].中國臨床醫生,2002,30(9):51.
[12]徐麗君,黃光英.丹參的化學成分及其藥理作用研究概述[J].中西醫結合研究,2009,1(1):45-48.
[13]楚晉,山萸肉化學成分及其藥理活性的研究[J].中國自然醫學雜志,1999 ,1(1):46-48.
[14]冀蘭鑫,黃浩,李長志,等.赤芍藥理作用的研究進展[J].藥物評價研究,2010,33(3):233-236.
[15]徐小云.威靈仙化學成分和藥理作用研究進展[J].現代中醫藥,2003(4):67-69.
[16]陳曉軍.雞血藤的藥理作用研究綜述[J].中國民族民間醫藥,2009,18(13):3-4.
[17]鄭義哲,劉本.牛膝中植物甾酮類成分的研究進展[J].2008,24(6):821-825.

