再說說精密度
馮仁豐
(上海市臨床檢驗中心,上海200126)
美國于1988年發布了臨床實驗室修正法規(CLIA’88)。該法規明確規定了描述一個檢測系統分析性能的指標包括7個方面:(1)精密度;(2)正確度;(3)患者結果可報告范圍;(4)分析靈敏度;(5)分析特異性;(6)參考區間;(7)其它必須的性能[1]。
為什么要將精密度放在檢測系統分析性能的第1位?關鍵原因是臨床實驗室在檢測患者樣品時,對樣品中的任何分析物或項目都只做一次檢測就發出報告!這是全球臨床實驗室的特殊之處!因此,確保檢測結果可靠性的第一前提是檢測結果的精密度要好,也就是同一份樣品再次檢測的結果與第1次是相同的!否則臨床和患者均不會對檢測結果感到滿意。當臨床和患者對臨床實驗室的結果有懷疑時就會要求臨床實驗室重做一次檢測。如果重復檢測的結果與上次報告的結果一致,臨床與患者均會認為臨床實驗室報告的結果是“準確”的!兩次檢測結果一樣還不準確嗎?其實這并不是準確度好,而是精密度好!由此可見,在任何時候,確保精密度是臨床實驗室的首要任務。
一、精密度的定義
《2012年國際計量學詞匯——基礎與通用》[2]的概念和相關術語(VIM)中,第 2.15 節定義測量精密度(measurement precision)[簡稱精密度(precision)]為在規定條件下對同一或類似被測對象重復測量所得示值或被測量的量值間的一致程度。注意:(1)測量精密度通常用不精密度表示,其值以數字形式表示,如在規定測量條件下的標準差(s)、方差或變異系數(CV);(2)規定條件可以是測量的重復性條件、測量的綜合(intermediate)精密度條件或測量的再現性(reproducibility)條件;(3)測量精密度用于定義測量的重復性、綜合的測量精密度或測量再現性;(4)術語“測量精密度”有時用于指“測量準確度”,這是錯誤的。美國臨床實驗室標準化協會(Clinical and Laboratory Standards Institute,CLSI)EP5-A2文件中對這些規定條件都做了說明[3]。
二、近期困擾我的疑惑
最近,某公司準備將 CLSI EP15文件[4]寫成便于臨床實驗室使用的應用軟件。我認為在形成軟件之前必須充分理解CLSI EP15文件的統計含義,絕不能依樣畫葫蘆。否則,當今后有客戶遇到不理解的問題進行咨詢時,公司只會回答:這是美國CLSI EP15-A文件規定的!但是,該公司的想法促使我再次認真閱讀該文件與EP5文件。
CLSI EP15文件的重點是讓臨床實驗室在使用某個新引入的檢測系統時必須對廠商聲明的精密度和正確度分析性能進行驗證。當我再次閱讀EP5文件時,發現在EP5文件中已對如何驗證廠商聲明的精密度提出了實驗方案。EP5和EP15文件驗證廠商精密度性能的統計做法是一樣的。臨床實驗室使用與某個廠商聲明中相似分析物濃度的樣品進行精密度實驗,得到該分析物項目的不精密度指標(s或CV)。如該指標低于廠商聲明中提供的不精密度指標(s或CV),則臨床實驗室的精密度性能驗證通過;若該指標高于廠商聲明,則臨床實驗室該分析物項目的精密度性能驗證未通過,需要進行統計學檢驗。經統計學檢驗后,如果臨床實驗室的不精密度指標與廠商聲明無明顯差異,即可認為臨床實驗室的精密度性能通過驗證,反之則為不符合要求。
我反復閱讀這兩個文件,突然注意到它們在進行精密度(CV或s)比較時沒有使用方差檢驗(F-test),卻使用了卡方(χ2)檢驗!這令我感到非常突然。我查閱我的統計學書籍[5-6],書中均無答案。這些書籍提供的信息與我了解的一樣,從來沒有介紹使用卡方檢驗去判斷不精密度(s或CV)的大小。于是我只能向CLSI專家請教,他們很快就給了回答。經過幾次的交流,編寫CLSI EP15文件的主席Dr.Neill Carey給出了很好的回答,還怕我不理解,一定要我提出看法。我在EP5文件中看到了相關參考文獻,但未找到相關的資料。因此我很希望他能夠提供使用卡方檢驗進行精密度評價的原始文件,但他們回答我說沒有參考文獻!最后,Dr.Neill Carey給了我一個非常詳細的討論精密度問題的多媒體文件。這給了我很大的啟發,讓我知道了一個小小的不精密度指標還有許許多多的學問。
我應該是國內最早了解CLSI的人員之一。早在1988年澳大利亞進修期間,看到導師有許多CLSI文件我幸喜若狂。在征得導師的許可后,我復制了幾個認為最要緊的標準文件,其中之一即為EP5文件(定量檢測方法精密度的評價)[7]。回國后,我反復多遍閱讀這個文件,而且還看過該文件的每一個修改版本。自認為熟悉和了解EP5文件的我恰恰只著重閱讀該文件的前半部分,忽略了后面驗證部分,導致不知道以卡方檢驗比較s的大小已經有了30余年!
為了彌補我過去的疏忽,近期我重新認真閱讀EP5-A2文件。閱讀后更感到許多早已經在20年前講到的問題我卻一直沒有去理解!盡管EP5-A3及EP15-A2文件將在今年6月發布,但要讀到新的文件還需要一段時間。因此,溫故知新已不能再等待。
三、臨床實驗室檢測系統精密度性能的重要性
1.方法學比較中精密度性能的影響 為什么在方法學比較中,在評估檢測系統的正確度時EP9文件[8]強調對每份比對樣品進行雙份檢測?主要原因是當兩個比較方法對每個樣品僅做單次檢測時會受到方法不精密度很大的影響,使最后正確度性能的評估產生偏移。因此,在進行方法學比較了解系統誤差時,如果兩個比較方法僅對每個樣品只做一次比對,肯定會嚴重受檢測不精密度的影響,導致比對誤差過大。
2.不精密度對線性實驗的影響 EP6文件[9]是定量檢測線性評價的文件。線性評價需對系列已知濃度或稀釋關系的樣品進行檢測。最早的EP6-P文件要求對每份樣品進行4次重復檢測。只有這樣才能了解在實驗中每組樣品的檢測結果是否產生了離群點,也可真實了解是否確實具有線性。這就是精密度性能對線性評價實驗的影響。檢測范圍(measuring range)[可報告范圍(repotable range)]定義為測量誤差限定在一個特定范圍內的分析物測量的一系列值。注意:EP6-P文件的值的范圍[分析物(被測量)相應計量單位]在整個范圍內符合方法的可接受指標,即非線性、不精密度或其他來源的誤差應在確定的限值之內。由此可見,在分析線性的定義中已提及了不精密度對整個檢測結果的影響。
3.不精密度對基質效應評估的影響 EP14文件是評價基質效應的文件[10]。為了確認不同類型的樣品是否具有基質偏移,EP14文件要求對每個樣品至少進行3次重復檢測。醫學事業的發展促使臨床對更多疾病有了深入了解,同時也對臨床實驗室提出了更高的要求。面臨眾多分析物、“被測量”和各類疾病的患者,臨床實驗室必須較以往更重視臨床檢驗基質效應以及不同批號試劑盒間檢測結果的差異!
4.不精密度對分析靈敏度的影響 EP17文件是確定檢出限值和定量限值的重要文件[11]。對某個檢測系統可報告的最低分析物濃度的確定依賴于該檢測系統(方法學)的不精密度水平。如果廠商或臨床實驗室不認真進行精密度實驗,將由錯誤的過小的s估計出“檢出靈敏度”作為自己產品或某個檢測系統的最佳檢出限值,那么就會對臨床診斷造成危害!
四、臨床實驗室精密度的問題
(一)精密度實驗的重復性問題
在所有的分析性能中,精密度性能只要進行重復檢測,計算均值()和s即可。這種做法涉及到多個問題。
1.分析物濃度 不同分析物濃度會影響不精密度中s大小,所以應選擇適當的分析物濃度進行重復性實驗。
2.基質差異 絕大多數實驗室直接使用質控品進行重復性實驗,沒有意識到質控品與患者天然樣品的基質差異。隨著臨床對實驗室的需求不斷增加,實驗室可以開展的分析物或項目的不斷增多,臨床實驗室需要隨時注意在檢測某些特殊分析物時真實樣品與質控品的顯著差異。此時就需使用患者真實樣品或其混合物(混合血清)進行分析性能評估及開展質量控制。
3.精密度估計的重要性 目前,臨床實驗室無論在評估某檢測系統精密度性能還是開展質量控制時均忽略了精密度估計的重要性。更有甚者,直接使用每天質量控制的重復數據計算不精密度。該數據既是該檢測系統的精密度,又是開展質量控制的基礎資料。但是,我們是否注意到,采用某個檢測系統或方法對樣品連做20次重復檢測,計算和s,得出該檢測系統或方法的精密度;若再次進行這樣的批內重復檢測,可以發現兩次精密度結果不一致!多年前,某雜志上的一篇有關精密度的文章引起了討論。經詢問,作者為了突出自己報道的檢測方法的性能,在多組重復檢測數據中找出s最小的一組數據作為該檢測方法的性能資料。而讀者僅做幾次這樣的重復檢測實驗,計算得出的s總是比該篇文章的大,因此認為該篇文章的數據是捏造的。在設計一個評價實驗時,必須事先就決定如何很好地確定檢測設備的實際精密度。每運行一次精心設計的精密度方案,就會得到檢測設備精密度的一個估計值。盡管檢測設備的實際精密度是相同的。但當相同實驗室相同檢測設備再次運行相同方案時將得到一個不同的精密度估計值。這些精密度的估計值預期會環繞分布于一個“真值”的周圍。觀察得到的估計值越多,“真實”精密度的周圍也就更緊密。一般來說,觀察數越大,一個估計值的可信性就越大;估計值的可信性越大,對檢出性能的“統計功效”也就越大。所以,臨床實驗室一定要認真重視自己的實驗工作,記錄每天開展的質量控制使用的和s,將每月的質量控制數據累積計算,求出真實的和s,這樣才如實地反映實驗室的狀態。
4.EP5文件[3]精密度實驗方案的主要做法 EP5文件中提出的“批內不精密度”、“批間不精密度”的實驗方案是較客觀地反映真實不精密度的估計。可惜,國內大多實驗室并沒有這樣去做。期望大家能花點精力,認真學習EP5文件中的實驗方案。EP5文件的做法可以概括成幾句話:每天做2批、每批做2份、連做20 d;每批2個結果間的差異就是該樣品該批檢測不精密度的具體表現。每天上、下午各做一批,最后的數據為20 d、40對、80個。將40對結果間的不精密度差異合在一起就會得到較客觀的“批內不精密度”的估計。每批做雙份,每天做2批,將每批結果求,它代表了這批檢測的平均水平。1 d內兩批結果間的差異表明了每天檢測“批間”的不精密度差異。將20 d的“批間”差異合在一起統計,得到了20 d內批間不精密度的估計。由于這一估計必然包含了批內不精密度的影響,那么通過方差估計的計算就可以得到批間不精密度的估計。每批做雙份、每天做2批,則2批4個結果的(也可以是各批結果的)代表當天對該樣品檢測的平均水平。一共檢測了20 d,有20個每天的檢測。將這些求一個總(也可以用80個結果計算)。所有每天對總的離散程度就是實驗室“天間”的不精密度估計。將批內不精密度的s、批間不精密度的s和天間不精密度的s以方差的形式疊加,得到這20 d在同一檢驗人員操作下,同一檢測系統對同一實驗樣品的精密度估計。多年前將這樣的估計稱為“總不精密度”估計,現在認為這個名稱不妥當,改稱為“實驗室內精密度(within-laboratory precision)”。
(二)EP5文件能否反映真實不精密度水平
EP5文件這樣認真的實驗方案是否能很完美地反映臨床實驗室中檢測系統對分析物的真實不精密度水平?30年前,起草EP5文件的專家們就已經想的很多、很遠。他們是臨床實驗室專家、質量管理專家、統計學專家、臨床專家和行政管理官員等的完整組合。
1.EP5文件的目的 起草EP5文件的專家們首先考慮的是該文件的目的。EP5文件是為體外診斷(IVD)設備廠商和臨床實驗室方法的開發者們建立他們方法的精密度能力,也為這些方法的用戶們確認性能聲明的驗證,或度量他們自己的精密度。自動檢測程序的用戶僅使用最簡單的方案驗證廠商精密度聲明應按照EP15-A2文件(用戶展示精密度和準確度性能)進行。該導則對以上情況是完全通用的,因為它包括了考慮精密度估計可靠性的目標。EP5文件也適用于對近期方法做了顯著修改的實驗室。當使用修改的某個IVD設備或方法時,用戶需要確認設備的基本性能特性沒有改變,但與原有聲明精密度性能進行比較可能不是有效的。典型修改的示例是使用的試劑、樣品來源、校準或質控物質或操作程序等不同于廠商使用說明中規定的。
2.在精密度性能確認和驗證上的要求有區別 針對我國大多實驗室均為“已經修改了原廠商檢測系統組成”的情況,所以不能簡單地去驗證性能,應該是去確認性能(即建立實驗室自行組合的檢測系統的性能)或是建立新組合的檢測系統的分析性能。因此,應使用EP5文件的方案確認精密度性能。
3.實驗時間長短對精密度性能的影響 EP5文件的實驗設計著重考慮了實驗時間長短對精密度性能的影響。由于已經考慮到許多因素會影響精密度的結果,所以EP5文件設計方案中已經規定了在一臺儀器上,一個批號的試劑、一個批號的校準品、一個操作人員的條件下得到的不精密度水平。在這樣的條件下,實驗時間成為最重要的因素,用以區分不同的精密度結果。用來敘述與實驗時間有關的精密度詞語有重復性(repeatability)、批間精密度(between-run precision)、天間精密度(between-day precision)、實驗室內精密度(within-laboratory precision)。在這些精密度中,重復性和實驗室內精密度一般是最受重視的。EP5文件的實驗設計沒有合并或特別單獨估計其它可能的重要變異來源,如校準品或試劑批號的差異、或技師/操作人員的差異;但是廠商應包括這樣的因素以及在不同場地的設備間的變異。影響精密度的其它因素如樣品準備、檢測材料穩定性、交叉污染和漂移等被包括在本方案中作為實驗室內部精密度的來源,但沒有分別估計。在EP5文件完整的方案中會使用一個批號的試劑和校準品,但結果的解釋(在合適時明確標記)必須包括這個事實,因為這樣的結果會低估長期實驗室內(或設備內)精密度。引入多批試劑和校準品將增加觀察的變異,盡管實驗方案中沒有允許分別估計這些因素的影響,但會較好地反映檢測系統在實際使用中的真實的精密度性能。
4.我的理解 上述內容明確告訴我們,在估計某個檢測系統的精密度性能時,越與日常檢驗工作接軌就越真實。因此,在估計精密度時不僅需要如EP5文件要求的20 d、40批、80個結果的做法;而且還應考慮多個操作人員輪班操作、換用不同批號的試劑和/或校準品、重新校準等因素,將這些日常的變異因素加入到精密度估計的影響因素中,得到真實的精密度水平。但決不可加入隨意更換試劑廠商、隨意調整計算因子等不規范行為造成的影響因素!
五、驗證實驗室精密度性能
1.驗證精密度的問題 當前的實驗室管理要求中規定實驗室在使用檢測系統檢測患者樣品、發出檢測報告前必須驗證檢測系統的分析性能,確認其分析性能符合廠商說明書中的聲明(claim)。因此,檢測系統廠商建立的分析性能必須要比臨床實驗室的常規檢測更加嚴格。CLSI EP5文件中對廠商建立分析性能也提出了相應的建議。國內外有那么多試劑、儀器組成的各種不同的檢測系統均被我國CFDA批準準許銷售。但是各家廠商在建立分析性能的嚴密性上各不相同。按照美國政府的認識,無論FDA對IVD產品的管理還是CLIA對臨床實驗室的管理均代表政府行為。因此,臨床實驗室使用的IVD產品必須得到FDA的批準;臨床實驗室在使用前必須按照CLIA要求對分析性能進行驗證(驗收)。驗證的指標就是廠商的分析性能聲明!所以,廠商的分析性能指標就成為國家要求實驗室“遵守”的要求!那么在驗證中,臨床實驗室得到的精密度性能如何與廠商聲明的精密度性能進行比較呢?現在的做法很簡單:在與廠商精密度指標采用的分析物濃度幾近一致的條件下,只要臨床實驗室得到的s低于廠商的指標,該分析物項目的精密度性能即被驗證!但實驗室管理部門從來沒有考慮過:廠商說明書中的精密度指標是否符合要求?實驗室的實驗方案是否符合要求?廠商在建立分析性能時大多會選擇簡便的方法。而且為了說明產品質量的優秀,相關數據也會選擇偏小的進行報告。因此,臨床實驗室越是認真的進行相關實驗,得到的精密度數據就越客觀,但精密度性能通過驗證的機率也越小!所以沒有臨床實驗室愿意嚴格按照CLSI EP5文件的要求進行相關實驗。這種做法是當今臨床實驗室的嚴重弊病!也正因為如此,當臨床實驗室的精密度指標與廠商的精密度指標進行比較時,兩個精密度均不確切,很難說明究竟哪個精密度更真實!
2.專家的認識 編制CLSI EP5文件的專家很早就認識到:僅僅將2個s放在一起比較數值是不可靠的。值得注意的是,這些比較是一個濃度下的點的比較!在廠商沒有說明得到s的實際實驗方案,但產品又獲得政府批準的情況下,只能假設廠商s的自由度為無窮大!臨床實驗室的驗證實驗也做的很簡單,最終導致得到的精密度只能是“真實s”的一個很粗糙的抽樣,不可靠的因素很多。因此,在臨床實驗室的精密度指標與廠商比較時,必須調整檢測的自由度(degree of freedom),使兩者標準差的比較在相應估計的自由度下進行。
3.我的膚淺認識 Westgard 等[12]提到,在方法評價研究中,F檢驗有時候用于比較檢測方法和比較方法的方差。方差簡單地說就是s的平方。簡言之,t檢驗用于系統誤差或準確度;F檢驗用于隨機誤差或精密度。為了進行F檢驗,取實驗方法和比較方法s的平方值,將較大的方差作為分子,較小的方差作為分母,求F值。公式為,式中 s為較大的 s,s為較小的 s。12將計算得出的F值與統計表中臨界F值比較。檢驗的無效假設是兩個比較的方差間沒有差異。自由度一般為檢測重復次數(n)減1,即“n-1”。按照兩個s的自由度分別從F臨界值表中尋找相應F臨界值。當觀察(計算)的F值>臨界F值,無效假設不成立,即方差或隨機誤差間的差異有統計學意義。若計算得出的F值<臨界F值,則無效假設成立,在統計學上兩個s無差異。我的統計學起步就是從這里開始的。所以,我一直認為:要比較s的大小就做F檢驗。
4.CLSI專家的啟示 在比較臨床實驗室按CLSI EP5文件和EP15文件得出的精密度結果與廠商聲明的一致性上,CLSI導則使用了卡方檢驗,而不是使用F檢驗,這是基于以下的考慮:在廠商說明書的精密度表中,“聲明”代表了有關行政機構批準的標記(labeled)s。我對這段話的理解是廠商的s經FDA批準后已經成為實驗室必須要實現的目標。但是,廠商沒有明確說明他們的精密度具體是怎樣得到的,因此不可能按F檢驗的要求確定與廠商估計有關的自由度。同時廠商也沒有明確說明在重復性實驗中是否進行多個試劑批號、多個儀器的實驗。所以臨床實驗室在處理廠商說明書中的值時沒有方法可供選擇,但又處于必須去評估估計自由度的境地。再者,正如前所述,臨床實驗室實驗得出的s也有很多不足的地方。那么,如何來比較臨床實驗室和廠商聲明中的精密度?一個做法是調整比較時的自由度。一般來說,自由度越小(即重復檢測次數越少),得到的抽樣s值的可信性就越差,即s的可信區間很大。F檢驗的自由度由兩個進行比較的實驗各自的重復次數決定,無法進行調整。所以在統計功效上的能力較差。相比之下,卡方檢驗在比較s的差異上具有較好的統計功效。這也是我以往不懂的地方,至今對此概念依然非常模糊。請教工業上的有關專家,他們告知在統計學上確實有使用卡方檢驗比較s的方法[13]。
5.與廠商聲明的比較 臨床實驗室通過上述實驗得到的精密度估計應與廠商聲明的精密度進行比較。可以采用以下敘述的卡方檢驗進行統計。為使用這個方法,廠商的性能聲明中被表示為一個點的估計(即一個s)。重復性和綜合精密度的估計應分別進行比較。性能聲明標準差(σr)須注明。卡方檢驗使用了臨床實驗室和廠商重復性估計的平方,必須知道臨床實驗室估計的批內方差與自由度的關系。在本方案敘述的實驗中將具有用來計算批內s的數據成對(即批內重復檢測)那樣大的自由度,這樣就等于實驗中的批數(以R表示)。卡方檢驗涉及的計算如下式中為臨床實驗室估計的重復性變異方差為廠商重復性變異聲明的方差、R為批的總數(為的自由度)。實驗室內(設備內)的精密度與廠商聲明進行比較應使用上述一樣的卡方檢驗。計算實驗室內標準差(sT)實際自由度涉及了復雜的計算,不像重復性估計那樣簡便。因為在該實驗的設計和統計檢驗的做法上,不是以所有實驗測定值相互獨立為前提,因此不可以像以往的做法那樣將實驗觀察數-1就成為了自由度的估計,需要采用較特殊的方法進行實驗數據自由度的估計。例如以下公式中ST的自由度就是考慮了實驗數據相互非獨立的情況。公式式中為用戶估計的實驗室內(設備內)s的平方值為廠商聲明的設備s的平方或醫學上要求的s的平方、T為sT的自由度(即實驗室內精密度比較的自由度)。T的計算較復雜,公式為設:ME為批內均方差或重復性方差);MR=2A2(所有批的均方差);MD=4B2(所有天的均方差);I為實驗天數;A和B將在“附錄”中介紹。將計算的“自由度”(T)代入前述的公式,計算出實驗室內s與廠商聲明s比較的卡方值。在相應自由度下與臨界卡方值比較。計算得出的卡方值<臨界卡方值,表示實驗室內s與廠商聲明差異無統計學意義;反之,則為差異有統計學意義。
六、總結
1.精密度性能是醫學檢驗的基礎 由于醫學檢驗的特殊性,全球臨床實驗室在對每份患者標本進行分析物檢測時,如無特殊情況,均對每個分析物只做單次檢測就發出檢驗報告。臨床和患者對檢測結果是否滿意取決于實驗室再做一次檢測的結果與前次結果是否一致。因此重復性是臨床實驗室檢測最重要的方面,千萬不可忽視。
2.認真學習EP5文件 30余年前,美國臨床實驗室標準化委員會(NCCLS)已經考慮到多方需求和影響精密度的各個因素,編寫了EP5文件。完成一個重復性實驗的方式有多種。為了患者樣品檢測結果的可靠性,必須充分考慮眾多影響因素,以適當的方式得到可靠的精密度估計。我已在臨床實驗室領域內工作和學習50年了,但是還有許多方面需要我繼續努力學習的。我將精密度視為臨床實驗室的關鍵所在。幾乎所有的臨床檢驗問題均由此產生。因此關注和重視精密度性能是解決臨床檢驗問題的基礎和起點。我愿意與臨床實驗室的同道們一起,為提高臨床實驗室的地位而努力。臨床實驗室的地位只能靠自己去爭取,依靠自身的提升,得到臨床和患者的認可。在與CLSI專家的交流中,Dr.Neill Carey告訴我:“EP15-A2文件中的方法比較實驗將在EP15-A3中刪除;在EP15-A3文件中,我們不再比較兩個方法的精密度估計。我們做了實驗,評估EP15(A2和A3)文件中一個方法的精密度。我們比較了觀察(計算)得到的s與廠商聲明的s。為了了解觀察到的s是否真的超過廠商聲明的s,我們計算了廠商聲明中s的確認限值,將觀察到的s與確認限值做比較。如果觀察到的s超出確認限值,即觀察到的 s確實高于廠商聲明的 s,僅有5%的可能性是因為隨機所致。”這兩個文件將于今年6月正式發布。由于上述的實驗結果,專家們在新的文件中不再要求臨床實驗室對驗證中實驗精密度超過廠商聲明進行統計檢驗。這無疑是簡化了驗證程序。
附錄:EP5文件實驗室內精密度估計
實驗方案:對穩定的實驗樣品每天做2批實驗,批間相隔的時間不少于2 h;每批實驗均對樣品做雙份檢測;共做20 d。一共有40對、80個結果。每對結果間的差是每批的批內差。20 d內共做了40批,這些差值的歸納客觀反映了較長時間周期內的批內不精密度。對每批實驗的雙份結果以表示平均水平,每天做2批,2批之間的差表示這一天的批間差;20 d有20個批間差,對這些差值進行統計后,減去其中批內差,即為真正的批間不精密度。每天做2批,有2個批,再求每天的,表示每天4個結果的平均水平,20 d有20個天,這些之間的差即為天間差,扣除內含的批間差因素就是真正的天間不精密度。將批內、批間和天間的不精密度以方差形式相加,可得到樣品下的實驗室內s,它可客觀地反映真正的實驗室內不精密度。
下述統計公式基于上述雙份檢測得出的s。
1.批內不精密度的標準差(s批內)
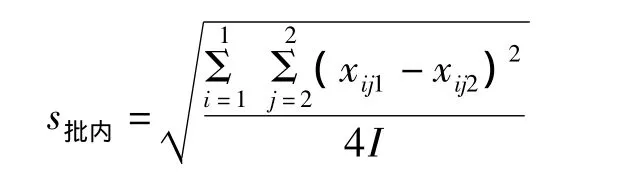
式中:I為實驗總天數;i=1為總和從第1天開始計;2表示1 d內實驗的批數,j表示批數的序號(只能是1和2,因為每天做2批;j=1表示總和要從每天的第1批開始計);4I表示組成總和的實驗數據的個數(如果做了20 d,則I為20、4I為80)。
2.批間變異的估計值(A)
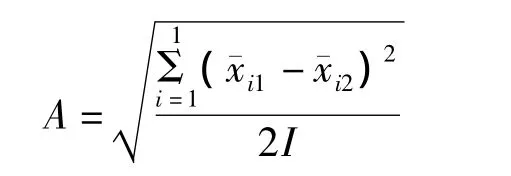
3.天間變異估計值(B)

4.天間標準差(s天間)由B值可求s天間,公式為。s天間的方差是從B2中減去1/2批間方差估計值,扣除了天間方差中批間方差的因素,成為真正的天間s。在具體計算時,會出現B2<1/2 A2,使差值為負數。這說明天間變異幾乎都是由批間變異形成的,所以就直接令s天間為0。
5.實驗室內標準差(s總) 最后,可以按照方差和的方式將批內s、批間s和天間s結合起來求出s總。公式為。
[1]§493.1253 Standard:establishment and verification of performance specifications[EB/OL].(2003-08-22)[2014-06-05]http://www.gpo.gov/fdsys/pkg/CFR-2003-title42-vol3/xml/CFR-2003-title42-vol3-part493.xml#seqnum493.1253.
[2]Joint Committee for Guides in M etrology.International vocabulary of metrology-Basic and general concepts and associated terms(VIM)[S].3rd edition.JCGM 200:2012(E/F),JCGM,2012.
[3]National Committee for Clinical Laboratory Standards.Evaluation of precision performance of quantitative measurement methods[S].EP05-A2,NCCLS,2004.
[4]Clinical and Laboratory Standard Institute.User verification of performance for precision and trueness[S].EP15-A2,CLSI,2005.
[5]金丕煥,陳 峰.醫用統計方法[M].第3版.上海:復旦大學出版社,2009:1-761.
[6]Netrella MG.實驗統計學[M].毛鎮道,蔣子剛,譯.上海:上海翻譯出版公司,1990:351-356.
[7]National Committee for Clinical Laboratory Standards.Proposed guideline for user evaluation of performance of clinical chemistry devices[S].EP05-P,NCCLS,1982.
[8]National Committee for Clinical Laboratory Standards.Method comparison and bias estimation using patient samples[S].EP9-A2,NCCLS,2002.
[9]National Committee for Clinical Laboratory Standards.Evaluation of the linearity of quantitative measurement procedures;a statistical approach[S].EP6-A,NCCLS,2003.
[10]Clinical and Laboratory Standard Institute.Evaluation of matrix effects[S].EP14-A2,CLSI,2005.
[11]National Committee for Clinical Laboratory Standards.Protocols for determination of limits of detection and limits of quantitative[S].EP17-A,NCCLS,2004.
[12]Westgard JO,de Vos DJ,Hunt MR,et al.Concepts and practices in the evaluation of clinical chemistry methods.Ⅲ:statistics[J].Am J Med Technol,1978,44(6):552-571.
[13]Sheskin DJ.Handbook of parametric and nonparametric statistical procedures[M].3rd Edition.New York:Chapman& Hall/CRC,2003:1-1193.

