老年冠心病患者下肢動脈硬化危險因素分析
張小波 于俊民 王慧冬 姜 文 李大鶴 胡 爽 陳洪葉
哈爾濱醫科大學附屬第四醫院老年病一病房,黑龍江哈爾濱 150001
伴隨著人口老齡化的加速,冠心病的發病率隨增齡而逐年增高。動脈粥樣硬化是一系統性進展的病理過程,常可累及冠狀動脈、頸動脈及下肢動脈,其具有相同的發病機制及一致的病理衍變過程[1]。 下肢動脈硬化閉塞癥 (lower extremity atherosclerosis disease,LEASD)是由于下肢動脈發生粥樣硬化進而累及下肢動脈狹窄甚至閉塞,出現不同程度的缺血性疾病[2],主要累及下肢大中動脈,引起下肢缺血癥狀,缺血性潰瘍,甚至干性壞疽,導致行走困難,重者截肢[3]。LEASD病變廣泛,呈漸進性發展,是多種因素共同作用的結果。 LEASD 患者的早期發現并積極干預防治,對于改善患者生存質量顯得尤為重要。 本研究通過對70 歲以上老年冠心病LEASD 患者伴發疾病等因素進行分析, 旨在探討影響LEASD 發生、 發展的相關危險因素,為有效預防老年冠心病下肢動脈硬化性病變提供新的思路。
1 資料與方法
1.1 一般資料
選擇2014 年1~3 月哈爾濱醫科大學附屬第四醫院住院冠心病穩定型心絞痛患者114 例為研究對象,其中男87 例,女27 例,平均年齡(81.22±5.94)歲,其中LEASD 患者74 例,診斷標準參照老年人四肢動脈粥樣硬化性疾病診治中國專家建議(2012)臨床診斷標準[4]。入選患者排除惡性腫瘤、代謝綜合征、腦卒中、肺感染及其他炎癥患者。根據彩色多普勒超聲將下肢動脈硬化者依血管狹窄程度分為狹窄率≥70%組(n=21)和狹窄率<70%組(n=53)。
1.2 觀察指標
觀察各組患者年齡及相關伴發因素,包括高血壓、糖尿病、腔隙性腦梗死、高密度脂蛋白-膽固醇(HDL-C)降低(<1.2 mmol/L)、載脂蛋白A(apoA)降低(<1 g/L)、高同型半胱氨酸血癥(HHCY)[同型半胱氨酸(HCY)>15 μmol/L]、超敏C 反應蛋白(hs-CRP)增高(>3 mg/L),并對狹窄率≥70%下肢動脈硬化患者上述伴發因素進行分析。
1.3 統計學方法
采用SPSS 17.0 統計學軟件進行數據分析, 計量資料數據用均數±標準差(±s)表示,兩組間比較采用t 檢驗;計數資料用率表示,組間比較采用χ2檢驗;相關因素分析采用二元Logistic 回歸分析, 以P < 0.05為差異有統計學意義。
2 結果
2.1 兩組一般資料比較
實驗入選老年冠心病患者114 例,檢出下肢動脈硬化者74 例,均伴發腔隙性腦梗死,占64.9%;下肢動脈硬化者平均年齡為(82.24±5.43)歲、非下肢動脈硬化者為(79.33±6.43)歲,二者年齡差異有統計學意義(P <0.05);下肢動脈硬化狹窄率≥70%組患者21例,狹窄率<70%組53 例,分別占18.4%、46.5%。
2.2 年齡與下肢動脈硬化血管狹窄程度相關性
狹窄率≥70%組≥90 歲的患者所占比例明顯高于狹窄率<70%組,差異有高度統計學意義(P <0.01)。見表1。

表1 兩組不同年齡患者下肢動脈硬化病變發生情況[n(%)]
2.3 各組患者伴發疾病因素分析
下肢動脈硬化狹窄率≥70%組患者伴發高血壓、糖尿病、HDL-C 降低、HHCY、hs-CRP 增高者多于狹窄率<70%組,差異有統計學意義(P <0.05),而兩組患者伴發apoA 降低情況比較,差異無統計學意義(P >0.05)。 見表2。
2.4 狹窄率≥70%相關因素分析
以狹窄率≥70%事件為因變量,高血壓、糖尿病、HDL-C 降低、HHCY、hs-CRP 增高及年齡為自變量,行二元Logistic 回歸分析,結果發現高齡(>90 歲)、高血壓、糖尿病、HDL-C 降低、HHCY、hs-CRP 增高是預測老年下肢動脈硬化患者狹窄率≥70%的獨立危險因素。 見表3。

表2 各組患者伴發疾病及因素[n(%)]
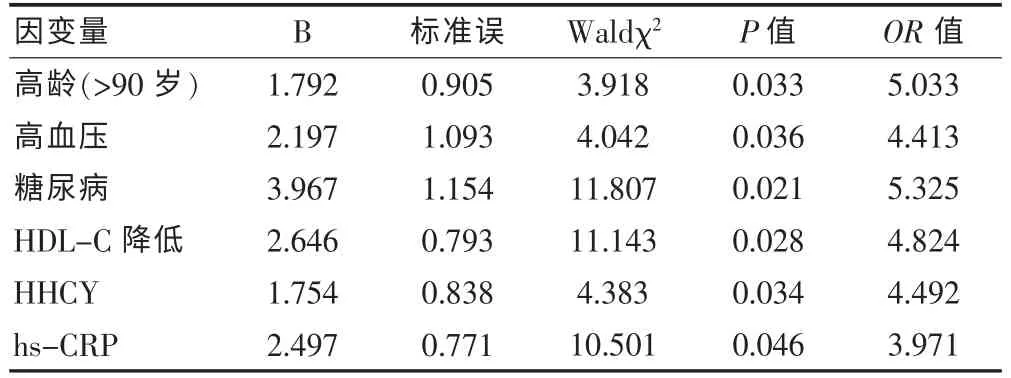
表3 下肢動脈硬化狹窄率≥70%危險因素分析
3 討論
動脈粥樣硬化是中老年人的常見疾病,近年來該病在我國逐年增多[5],病變多發于大、中型動脈,動脈增厚、變硬,伴有粥樣斑塊及鈣化斑,可繼發血栓形成。 LEASD 是常見的肢體動脈閉塞性疾病,以動脈粥樣硬化和微血管病變為主要機制的病理學改變,臨床上表現為以組織缺血為特征的一種慢性病癥[6],近年來其發病率、致殘率和致死率日趨增高,嚴重影響老年人群的身心健康[7]。 LEASD 下肢缺血癥狀僅為全身動脈硬化的外周血管表現,患者往往合并心腦血管疾病。 有文獻報道40 歲以后,LEASD 每10 年的發病率增高2~3 倍[8],70 歲以上人群中LEASD 的發病率高達20%[9]。 本研究入選老年冠心病患者114 例,64.9%發生不同程度下肢動脈硬化,所有下肢動脈硬化患者同時患有腔隙性腦梗死,18.4%下肢動脈硬化狹窄率≥70%,下肢動脈硬化者平均年齡為(82.24±5.43)歲,隨著年齡的增長,LEASD 的發生呈明顯增長趨勢,與上述報道相符。
目前,LEASD 流行病學資料研究較少,仍缺乏大樣本研究[10],既往發現其危險因素比較復雜,例如:吸煙、高血脂、糖尿病等,但這些因素尚不能完全解釋LEASD 的發生和發展, 臨床資料亦顯示并不是所有患者都存在這些危險因素。 已證實氧化應激、慢性炎癥和內皮損傷是LEASD 的核心環節[11]。 近年來國內外多項實驗證實體內HCY 對血管內皮細胞有毒性作用,造成血管內皮細胞骨架結構發生變化,易于促進血管內壁增厚,刺激血管平滑肌細胞增殖,增加血液中血小板的黏附性,甚至形成閉塞[12]。 HCY 是蛋氨酸代謝產生的中間產物, 生理情況下HCY 的代謝處于動態平衡狀態,維持體內含硫氨基酸的平衡。 血HCY水平升高可損傷動脈內皮,導致動脈管腔狹窄甚至閉塞[13],而氧化應激貫穿高HCY 引起動脈粥樣硬化發生和發展的全過程。動脈粥樣硬化同時是一種慢性炎癥性疾病,研究表明hs-CRP 是獨立的動脈粥樣硬化發展預測指標[14]。CRP 作為一種全身炎癥的血清標志物,反映炎癥的范圍和活動力,其改變早于臨床癥狀,同時反映粥樣斑塊的活動度,它的升高可能在動脈硬化發生發展中起促進作用。 在多重因素作用下,下肢動脈粥樣硬化病變進展、加重,促使易損斑塊破裂、出血,甚至引發血栓、栓塞。
本次研究入選冠心病LEASD 患者中發現下肢動脈硬化狹窄率≥70%組伴發高血壓、 糖尿病、HDL-C降低、HHCY、hs-CRP 增高者明顯多于狹窄率<70%組,并且通過二元Logistic 回歸分析,結果表明高齡(>90 歲)、高血壓、糖尿病、HDL-C 降低、HHCY、hs-CRP增高是預測老年下肢動脈硬化患者狹窄率≥70%的獨立危險因素, 由此可見上述各伴發因素在LEASD的發生、發展過程中發揮重要作用。因此在LEASD 患者的治療過程中, 不僅應注重下肢血管的病變情況,更要進行全身性伴發因素的干預,使患者血壓、血糖、血脂達到目標值,同時血HCY、hs-CRP 增高者,積極補充葉酸、維生素B12,有效控制hs-CRP 水平,可能是一個潛在的預防或延緩LEASD 發生、 發展的治療策略。 HDL 在動脈粥樣硬化中的有益作用與其主要結構性蛋白apoA1 密切相關,apoA1 是HDL 的主要成分,含有243 個氨基酸序列,由規則重復的雙性螺旋組成[15]。 研究證apoA1 模擬肽在動物模型和人體內具有抗炎抗氧化、抗血小板聚集、抗排斥反應等特性,進而在抗動脈粥樣硬化、抗心臟移植排斥反應以及肥胖的相關治療領域發揮積極的作用[16-17]。 有學者證實apoA1 降低為2 型糖尿病合并LEASD 的相關危險因素[18],但在本研究入選114 例患者中,下肢動脈硬化者apoA 降低與LEASD 無明顯相關性,分析原因可能與apoA 含AⅠ、AⅡ、AⅣ等成分,且與apoAⅡ、apoAⅣ在LEASD 發生、發展中是否存在相互作用有關。因此針對apoA 及其各相關亞型在LEASD 進展中的作用尚有待進一步探討。
LEASD 的治療已從最初的內膜剝脫術、人工血管或自體大隱靜脈旁路開放式手術,轉化為血管腔內修復。目前,國內LEASD 的腔內治療正處于探索實踐階段,尚未得出可靠的循證醫學結論[19]。 因此,早期識別積極地控制血壓、血糖,調脂,降低血HCY、hs-CRP水平,改善生活方式,可減少或延緩老年冠狀動脈及下肢動脈粥樣硬化的發生、發展,對降低老年冠心病下肢動脈硬化患者的發病率、致殘率及致死率具有極為重要的意義。
[1] 寇璐,馮津萍,秦勤.老年人下肢動脈硬化與冠心病關系的研究[J].中國慢性病預防與控制,2010,18(4):423-424.
[2] 洪泓,關麗卿,陳慕潔.下肢動脈硬化閉塞癥治療趨勢與思考[J].中國醫學創新,2013,10(24):162-164.
[3] 葉弘,臧曉鷺.中藥熏洗輔助治療以靜息痛為主訴的老年下肢動脈硬化閉塞癥30 例[J].中國老年學雜志,2013,33(16):4041-4042.
[4] 老年人四肢動脈粥樣硬化性疾病診治中國專家建議寫作組.老年人四肢動脈粥樣硬化性疾病診治中國專家建議(2012)[J].中華老年醫學雜志,2013,32(2):121-131.
[5] 崔明勇,王珊,黃榮,等.頸動脈彩色多普勒超聲在中老年腦梗死患者檢查中的臨床價值[J].中國醫藥導報,2013,10(3):100-102.
[6] 史均寶,孫慶華,聶建東,等.糖尿病腹膜透析患者下肢動脈硬化閉塞癥的臨床狀況分析[J].北京大學學報:醫學版,2013,45(1):109-113.
[7] 劉永升,魏梅,劉會英,等.西洛他唑對老年下肢動脈硬化閉塞癥患者超敏C 反應蛋白、血脂及基質金屬蛋白酶-9 的影響[J].實用老年醫學,2012,26(4):285-287.
[8] Hiatt WR. Pharm acologic therapy for peripheral arterial disease and clandication[J].J Vasc Surg,2002,36(6):1283-1291.
[9] 趙曉寧.下肢動脈硬化閉塞癥的診斷方法[J].現代生物醫學進展,2007,7(4):629-631.
[10] 王利會,邊忠平,高海濤,等.老年患者下肢動脈硬化閉塞癥綜合治療體會[J].中華老年心腦血管病雜志,2012,14(1):86.
[11] 范利,朱冰坡,曹劍.普羅布考對老年下肢動脈硬化癥患者血管內皮活性因子及炎性因子的影響[J].微循環血雜志,2006,16(3):55-57.
[12] 尤忠孝,時東彥,張靜,等.血清同型半胱氨酸和載脂蛋白a 水平與腦梗死相關性研究[J].腦與神經疾病雜志,2013,21(4):211-212.
[13] 張小波,于俊民,王慧冬,等.阿托伐他汀聯合福辛普利對老年穩定型心絞痛血同型半胱氨酸的影響[J].齊齊哈爾醫學院學報,2010,31(5):688-689.
[14] Juhan-Vague I,Pyke DM,Alessi MC,et al. Fibrinolytic factors and the risk of myocardial infarction or sudden death in patients with angina pectoris[J].Circulation,1996,94(9):2057-2063.
[15] 郭玉松,曹劍,范利.載脂蛋白A1 模擬肽研究進展[J].中華老年醫學雜志,2013,32(12):1368-1371.
[16] 杜林,張振剛.載脂蛋白A-1 模擬肽[J].國際心血管病雜志,2012,39(1):25-27.
[17] 葉穎劍,胡乃中.肝硬化并發腎上腺皮質功能不全患者的臨床特點分析[J].臨床肝膽病雜志,2012,28(5):364-367.
[18] 殷祿昌,隋萍,林松娟.2 型糖尿病合并下肢動脈硬化閉塞癥的危險因素探討[J].濰坊醫學院學報,2011,33(6):474-476.
[19] 吳慶華,楊培.下肢動脈硬化閉塞癥治療現狀與努力方向[J].心肺血管病雜志,2013,32(1):1-2.

