依達拉奉注射劑質量標準和穩定性研究
陳楠 蓋春燕 陳剛 付宏征
依達拉奉注射劑質量標準和穩定性研究
陳楠 蓋春燕 陳剛 付宏征
目的建立依達拉奉注射液的質量標準,并考察其穩定性。方法依達拉奉的含量測定應用HPLC法,檢測波長242 nm,理論塔板數以依達拉奉色譜峰計不低于2 000,保留時間為12~15 min;通過pH值、重金屬含量、細菌內毒素、無菌檢查等對其質量進行控制;通過影響因素試驗,加速試驗和室溫留樣觀察試驗考察注射液的穩定性。結果依達拉奉在1.5~7.5 μg/μl范圍內濃度與吸光度成良好線性關系(r=0.9994),平均回收率為100.02%,RSD=0.96%。3批依達拉奉注射液中依達拉奉的含量分別為標示量的100.73%、98.37%、100.64%。3批依達拉奉注射液的pH值分別為2.8、2.9、2.8。重金屬含量、細菌內毒素、無菌檢查等符合藥典規定。結論該試驗方法簡單,穩定性高,系統可重復性強,可有效控制依達拉奉注射液的質量并保證其穩定性。
依達拉奉注射液;質量標準;穩定性
依達拉奉是一種新型的治療腦梗死的腦保護劑,它療效確切,能抑制自由基引起的脂質過氧化和細胞壞死,有明確的抗腦缺血和腦保護作用,對于治療腦梗塞病是一個優良的藥物。依達拉奉注射液作為一種新型自由基清除劑于2001年4月4日在日本獲得以“改善腦梗死急性期伴發的神經癥候、日常生活動作障礙、機能障礙”為適應證的臨床用藥資格,并與2001年6月1日在日本正式上市,用于急性腦梗死的治療。現在的腦梗死急性期用藥主要為除水腫的高漲輸液,CDP-膽堿氯酯等腦代謝復活藥,或者戊巴比妥等中樞抑制藥。還沒有直接作用于腦缺血后損傷因素、相關受體等腦保護藥,依達拉奉抑制自由基引起的脂質過氧化和細胞壞死,有明確的腦缺血保護作用,成為保護腦免受脂質過氧化損傷的新藥,在我國依達拉奉廣泛應用于腦出血、腦梗死、腦卒中、顱腦外傷等的治療,因此,通過有效的質量標準控制其質量和穩定性對于臨床安全用藥具有重要的意義。
1 儀器與試藥
1.1 儀器 Waters e2695 Separations Module HPLC(美國Waters公司),Waters 2998 PAD紫外檢測器(美國Waters公司,含真空脫氣、高壓二元梯度泵、恒溫自動進樣器、柱溫箱),Empower 2色譜管理系統;旋轉蒸發器(鞏義市英峪高科儀器廠);DZTW型調溫電熱套(北京市永光明醫療儀器廠);分析天平(Sartorius CPA225D);超聲清洗器(昆山市超聲儀器有限公司);InoLab pH720試驗室臺式酸度計(德國WTW公司)。
1.2 試藥 依達拉奉注射液自制(批號:20010425、20010428、20010430 規格:20 ml∶30 mg);乙腈(色譜純);甲醇(色譜級);雙蒸水;其余試劑為分析純。
2 方法與結果
2.1 依達拉奉注射液中依達拉奉的含量測定
2.1.1 色譜條件和系統適性試驗:色譜柱:C18-鍵合硅膠柱(5 μm)250 mm × 4.6 mm;流動相:乙腈:磷酸鹽緩沖液(15∶85),1.0 ml/min;檢測波長:242 nm;進樣量:15 μl;保留時間為12~15 min。柱效:按依達拉奉色譜峰計,理論塔板數應不低于2 000[1,2]。含量測定結果見表1。

表1 依達拉奉含量測定結果
2.1.2 線性關系:取依達拉奉對照品約30.0 mg,精密稱量,置10 ml容量瓶,甲醇稀釋至刻度,精密量取1 ml,以甲醇稀釋至 100 ml,再精密量取 1 ml,以甲醇稀釋至100 ml,搖勻。精密吸取對照品溶液,50 μl,100 μl,150 μl,200 μl,250 μl用甲醇稀釋至 10 ml,分別精密吸取20 μl注入高效液相色譜儀進行分析,測量依達拉奉的峰面積[2,3]。結果表明,以依達拉奉的峰面積(A)對其濃度(C)進行線性回歸,在進樣量1.5~7.5 μg/ml范圍內,依達拉奉峰面積與濃度成良好的線性關系。見表2。
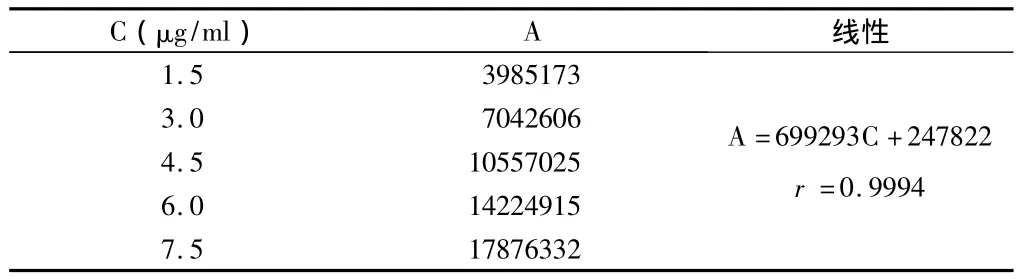
表2 依達拉奉HPLC法測定線性關系試驗結果
2.1.3 精密度試驗:取 3.0 μg/ml供試液分別連續測定5次,其相對標準偏差為1.27%,結果表明在此濃度下,HPLC 測定的 RSD%小于 2.0%[2,3]。見表 3。

表3 依達拉奉精密度試驗結果
2.1.4 加樣回收率試驗:精密吸取已知含量的同批供試品液0.5 ml共 3份,各加入依達拉奉 3.10 mg,6.20 mg,9.20 mg,依法測定各份樣品中依達拉奉的含量并計算回收率,結果平均回收率100.02%,RSD=0.96%[2,3]。見表 4。
2.2 依達拉奉注射液質量標準研究
2.2.1 pH值:參照pH值檢查法(《中華人民共和國藥典》2010年版二部附錄Ⅵ H)。見表5。

表5 依達拉奉注射液的pH值
2.2.2 顏色:參照《中華人民共和國藥典》2010版二部附錄ⅨE。見表6。

表6 依達拉奉注射液的顏色
2.2.3 重金屬測定:依據《中華人民共和國藥典》2010版二部附錄ⅧH第一法。見表7。
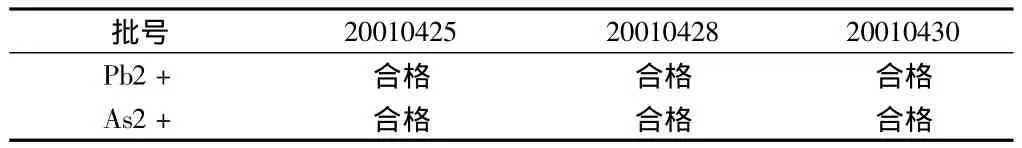
表7 依達拉奉注射液的重金屬檢查
依達拉奉原料藥的重金屬的含量極低,在注射液制備和生產過程中,并未引入重金屬,故此項不列入質量標準。
2.2.4 細菌內毒素檢查:依據《中華人民共和國藥典》2010版二部附錄ⅪE。見表8。

表8 依達拉奉注射液的細菌內毒素檢查
2.2.5 無菌檢查:依照《中華人民共和國藥典》2010版二部附錄ⅪH。見表9。

表9 依達拉奉注射液的無菌檢查
2.3 依達拉奉注射液的穩定性研究
2.3.1 影響因素試驗:強光照射試驗:將樣品在光強度為3 500 Lx的日光燈下放置10 d,分別于1、5、10 d各取樣1次,按考察項目檢查。取本品20010425,分別于40℃、60℃的恒溫水浴中放置10 d,于1、5、10 d取樣,按考察項目檢查[4,5]。依達拉奉注射在各考察條件下均較穩定。見表10。

表10 影響因素試驗結果
2.3.2 加速試驗:取本品置40℃,放置6個月,于1、2、3、6 個月時間取樣測定[4,5],試驗結果表明,40℃ 條件下放置6個月,樣品與0月相比無明顯變化。見表11。
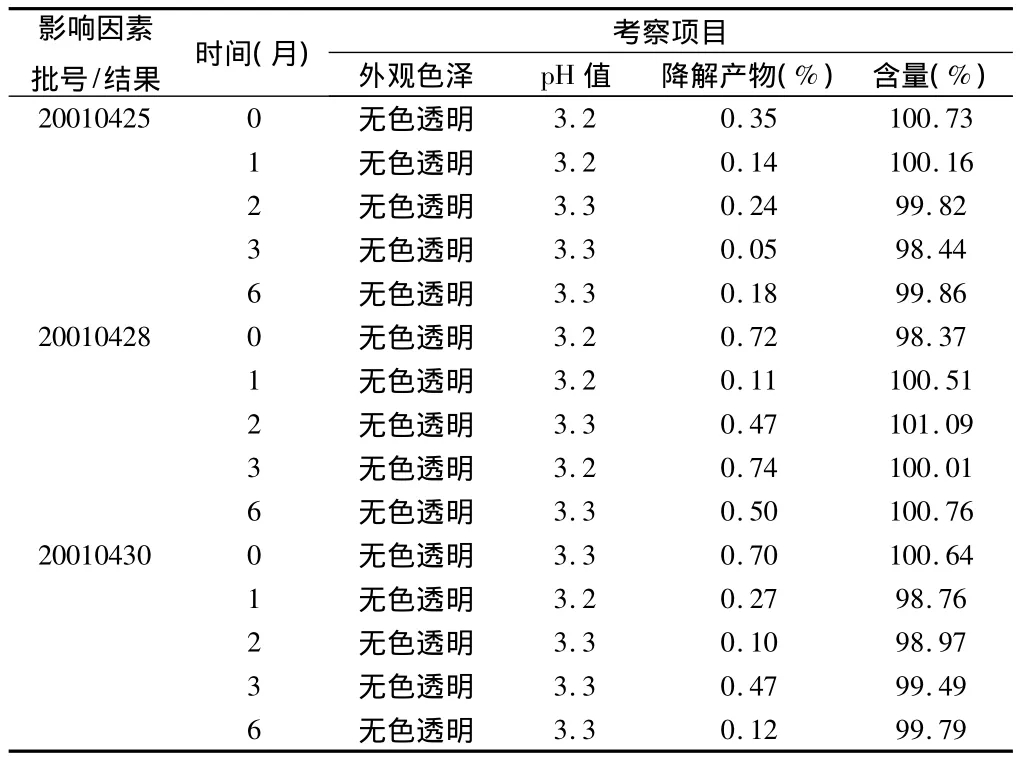
表11 加速試驗結果
2.3.3 室溫留樣觀察試驗:將樣品置自然室溫條件下,并于 1、3、6 個月時抽樣測定[4,5],結果表明:本品在室溫留樣的半年間質量穩定,考核各項均符合標準規定。見表12。

表12 室溫留樣觀察試驗
3 討論
3.1 色譜條件和系統適性 精密配制10 μg/ml的依達拉奉對照品溶液,通過紫外-可見分光光度法進行掃描,依達拉奉在242 nm的波長處有最大吸收,因而選擇242 nm作為依達拉奉的檢測波長。乙腈和磷酸鹽緩沖液比例15∶85作為流動相,得到的峰形較好、保留時間適宜。精密度實驗和加樣回收實驗證實該方法專屬性強、靈敏度高、選擇性好、簡便、準確,可有效地應用于依達拉奉注射液的質量控制。
3.2 質量標準通過pH值、顏色、重金屬含量、細菌和內毒素等標準控制注射液質量,依達拉奉原料藥重金屬的含量極低,在注射液工藝制備和生產過程中并未引入重金屬等相關物質,故此項不列入質量標準。本文所采用的三批樣品均符合質量標準草案的要求。
3.3 穩定性影響因素試驗,加速試驗和室溫留樣觀察試驗結果表明:本品在各考察條件下,各項指標均無明顯變化,說明本品在室溫下有效期可定為2年。
1 國家藥典委員會主編.中國藥典.第1部.北京:化學工業出版社,2010.
2 付桂英,溫明鈴,賈立華,等.高效液相色譜法測定依達拉奉注射液的含量及有關物質.解放軍藥學學報,2006,22:458-460.
3 董繼勝,黃利鵬,馬歆茹.依達拉奉注射液質量研究.黑龍江醫藥,2010,23:340-3342.
4 弋金龍,黃翔,何春曉,等.丹紅注射液的質量標準及其穩定性研究.中國中醫急癥,2013,22:864-865.
5 呂應年,龔先玲.半邊旗5F注射液的質量標準研究.中藥雜志,2008,33:2343-2346.
Study on the quality standard and stability of edaravone injection
CHEN Nan*,GAI Chunyan,CHEN Gang et al.*The First Hospital Affiliated to Beijing University,Beijing 100034,China
ObjectiveTo establish the quality standard of edaravone injection and to investigate its stability.MethodsThe quantitative detection of edaravone injection was performed by HPLC,detection wavelength was 242nm,theoretical plate number based on the chromatogram of edaravone was more than 2000,retention time was12 ~ 15 min.The quality was controlled by pH,contents of heavy metals,bacterial endotoxin and sterility tests.The stability of edaravone injection was evaluated by influence factors test,acceleration test and room temperature storage observation test.ResultsFrom 1.5 to 7.5μg/μl,the concentration and absorbance of edaravone injection had a good linear relationship(r=0.9994),the average recovery rate was100.02%,and RSD was 0.96%.The pH of three batches injections was 2.8,2.9,2.8,respectively,moreover,the contents of heavy metals,bacterial endotoxin and sterility tests were consistent with pharmacopoeias regulation.ConclusionThe method is simple,accurate,stable and repeatable,which can effectively control the quality of edaravone injection and can assure its stability.
edaravoneInjection;quality standard;stability
R 927.11
A
1002-7386(2014)14-2098-03
10.3969/j.issn.1002 -7386.2014.14.006
100034 北京市,北京大學第一醫院(陳楠);北京大學天然藥物及仿生藥物國家重點實驗室(蓋春燕、陳剛、付宏征)
付宏征,100034 北京大學天然藥物及仿生藥物國家重點實驗室;Email:drhzfu@sina.com
2014-01-11)

