正交設計優化尼美舒利NLC處方組成與制備工藝
杜廣盛,李德馨,魏振平
(1.天津大學化工學院,天津300072;2.天津天士力集團化學藥物研究所,天津300410)
納米結構脂質載體(nanostructured lipid nanoparticles,NLC)是在固體脂質納米粒 (solid lipid nanoparticles,SLN)基礎上逐漸發展起來的第二代脂質納米粒給藥系統,它是以一定比例的液態油或混合脂質代替SLN中的固體脂質而制備出的新型固體脂質納米粒[1-3]。
液態油脂能夠明顯的提高難溶藥物在脂質中的溶解度,因此NLC可以有效的克服SLN中存在的固體脂質材料結晶度高、載藥量低、貯存期間藥物容易泄漏、水分散體系含水量過大等缺點[4]。NLC制備方法主要包括高壓均質法、溶劑擴散法和微乳法等,其中高壓均質法可以有效的避免使用有機溶劑,可處理脂質濃度較高,并且易于擴大生產規模[5]。
尼美舒利作為傳統的消炎鎮痛藥,親脂性強,適合作為制備脂質納米粒的模型藥物。本研究采用高壓均質法,以粒徑和包封率為指標,采用單因素設計考察了處方組成和工藝條件對納米粒質量的影響。以包封率為指標,采用L9(34)正交設計表優化處方組成與制備工藝,確定了最適宜制備方案,并對所制備尼美舒利NLC制劑學性質進行了考察。
1 實驗部分
1.1 實驗儀器與材料
AB204-N萬分之一電子天平(瑞士梅特勒-托利多集團);XW-80A微型旋渦混合儀(上海滬西分析儀器廠);EMS-30超級恒溫水浴攪拌器(天津市歐諾儀器儀表有限公司);D-3L高壓均質機(美國PhD科技有限公司);Anke TGL-20B離心機(上海安亭科學儀器廠);KQ3200B超聲波清洗器(昆山市超聲儀器有限公司);Agilent 1260液相色譜儀(安捷倫科技有限公司);S-4800 SEM掃描電鏡(日本日立公司)。
尼美舒利(天津藥物研究院);單硬脂酸甘油酯(glycerin monostearate,GMS,天津市光復精細化工研究所);油酸(湖南爾康制藥有限公司);TPGS(陜西瑞源制藥有限公司);透析袋(截留相對分子質量12 000~16 000,天津市聯星生物技術有限公司);甲醇(分析純,利安隆博華天津醫藥化學有限公司);乙腈(色譜純,德國默克公司);磷酸(分析純,天津市化學試劑三廠);氨水(分析純,天津市化學試劑三廠)。
1.2 NLC制備
稱量處方量 TPGS,置于錐形瓶中,加蒸餾水40 m L攪拌使其完全溶解,置于75℃恒溫水浴磁力攪拌器中。在300 r/m in下磁力攪拌得到水相。
稱取處方量尼美舒利、油酸和單硬脂酸甘油酯(GMS)置于錐形瓶中,置于75℃恒溫水浴磁力攪拌器中,300 r/m in磁力攪拌得到油相。
在恒溫水浴75℃,300 r/m in磁力攪拌下,將水相緩慢滴加到油相中。待水相完全加入后,保持恒溫恒速攪拌15 min,得初乳。
將所得初乳在80 MPa壓力下,通過高壓均質機循環4次,得到納米液。冷至室溫,即得尼美舒利NLC水分散液。
1.3 單因素考察
1.3.1 油酸與GM S投料比的考察
固定脂質質量分數3%(輔料與水的質量比,下同),TPGS 1.2 g,藥脂比1∶40,水40 m L。 按照1.2項下制備工藝,分別考察油酸與 GMS投料比為1∶10、2∶10、3∶10、4∶10 時 NLC的粒徑和包封率。
1.3.2 脂質用量的考察
將油酸與 GMS投料比定為3∶10,其它處方條件同1.3.1項下。分別考察脂質用量為1%、2%、3%、6%、8%和10%時NLC的粒徑及包封率。
1.3.3 乳化劑用量的考察
固定脂質用量為3%,其它條件同1.3.2項下,分別考察 TPGS用量為 0.4、0.8、1.2和 1.6 g時NLC粒徑及藥物包封率。
1.3.4 藥脂比的考察
固定TPGS用量為1.2 g,其它處方與工藝條件同 1.3.3 項下,分別考察藥脂比為 1∶120、1∶80、1∶40和1∶30時NLC粒徑和包封率。
1.3.5 高壓均質壓力的選擇
固定脂質用量3%,油酸與 GMS投料比為3∶10,藥脂比為 1∶40,TPGS 用量為 1.2 g,高壓均質機循環4次,分別考察均質壓力為 40、60、80、100 MPa時NLC的粒徑和包封率。
1.3.6 循環次數的考察
循環次數的考察:均質壓力設為80 MPa,其它處方與工藝條件同1.3.5項下,分別考察循環次數為1、2、4和6時NLC的粒徑和包封率。
1.4 正交設計優化處方與制備工藝
在單因素考察基礎上,選擇油酸與GMS投料比(A)、藥脂比(B)、乳化劑用量(C)、高壓均質壓力(D)4個因素,每個因素選擇3水平,按L9(34)正交試驗設計表設計9組實驗,以包封率為評價指標,篩選最適宜處方組成和制備工藝。
1.5 NLC理化性質考察
1.5.1 粒徑與Zeta電位測定
采用馬爾文納米粒度儀測定納米粒粒徑與Zeta電位,測定溫度設為25℃,檢測角度設為90°。樣品測前用蒸餾水適當稀釋避免黏結,放入樣品池中檢測。每個樣品測定3次取平均值。
1.5.2 NLC形態觀察
采用掃描電鏡觀察尼美舒利NLC形態。測定前,用pH值為7.0 PBS適當稀釋后放在銅片上自然晾干,對樣品進行1 m in噴金處理,用掃描電鏡進行觀察。
1.5.3 包封率測定
采用離心法測定藥物包封率。將制得的新鮮NLC在7 000 r/m in下離心15 m in后從上清液精密移取1 m L至10 m L容量瓶中,甲醇定容后超聲10 min破乳。所得乳液在3 000 r/min下離心10 min。取上清液過濾后進樣HPLC測定尼美舒利濃度。包封率(EE)計算公式為:
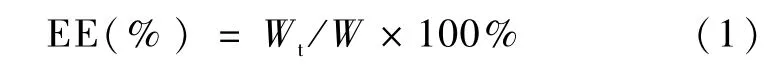
其中,Wt為上清液中藥物量,W為藥物投入量。
1.5.4 尼美舒利NLC體外釋放
按照1.4項下確定的最適宜方案制備尼美舒利NLC,采用動態膜透析法測定 NLC的體外釋放特性。精密移取1 m L尼美舒利NLC混懸液,置于透析袋中,將透析袋置于50 m L釋放介質中(10%乙醇的pH 7.4 PBS)中。溫度為37℃,轉速為200 r/min,分別于 1、2、4、6、8、10、12、24、36、48 和 72 h 取出2 m L透析介質,用0.45μm微孔濾膜過濾后進液相檢測濃度。同時補加同等體積的同溫釋放介質。另精密稱取18.5 mg尼美舒利原料藥,置于25 m L容量瓶中,用甲醇定容。采用同等方法測定體外釋放情況作為對照。第n個點的累積釋放率為:
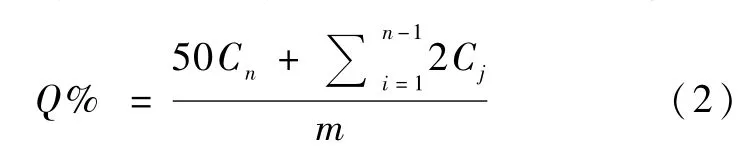
其中m為所加樣品中藥物質量,Cn為第n個點的藥物濃度。
1.6 HPLC檢測尼美舒利含量
尼美舒利含量采用反相液相色譜法進行測定。采用的色譜柱為Capcell PAK C18柱(250 mm×4.6 mm,5μm),柱溫設為25℃;進樣量為 20μL;流動相為0.1%H3PO4(氨水調節pH值為7.0)∶乙腈=60∶40,流速為 1.0 m L/min,檢測波長設為230 nm。
2 結果與討論
2.1 單因素考察
2.1.1 油酸與GM S投料比的選擇
固液態脂質投料比對納米粒質量的影響見表1。
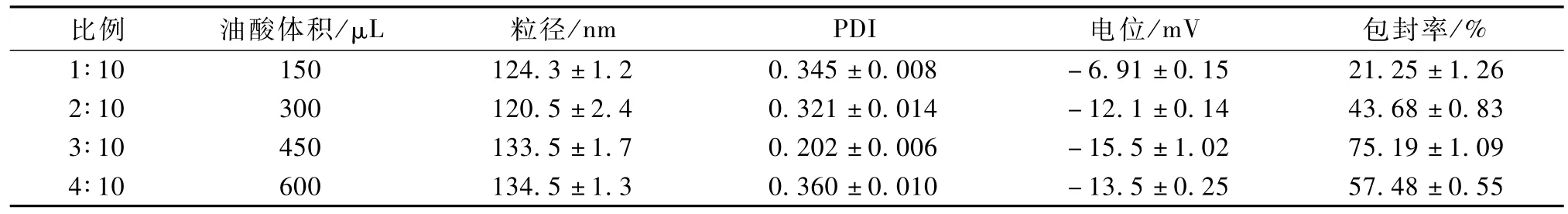
表1 油酸與GM S投料比的考察(n=3)Table 1 Study of feed ratio of oleic acid to GM S(n=3)
隨著油酸用量的增加,尼美舒利NLC粒徑沒有明顯的變化。這是因為在處方確定的情況下,NLC的粒徑主要受熔融脂質的黏度影響。而油酸用量的變化對熔融脂質黏度影響不大,因此粒徑變化較小[6]。
包封率隨著油酸用量增大先升高后降低。這是因為油酸用量增大時提高了藥物在混合脂質中的溶解度,使包封率提高。當油酸用量過大時,可能導致油酸較多的分散在納米粒表層,使藥物分散到水相的速度加快,導致包封率降低[7]。
2.1.2 脂質用量的考察
脂質用量對納米粒質量的影響見表2。

表2 脂質用量的考察(n=3)Table 2 Study of am ount of lipid(n=3)
隨著脂質用量的增加,粒徑有增加的趨勢,這與文獻報道一致[8]。隨著脂質用量增加,脂質對藥物的溶解能力增強,使包封率升高。當脂質用量過大時,樣品黏度增大,高壓均質機處理效果下降。從而使得藥物無法充分包裹進入脂質中,使包封率降低。
2.1.3 乳化劑用量的考察
TPGS用量對NLC粒徑和包封率的影響見表3。
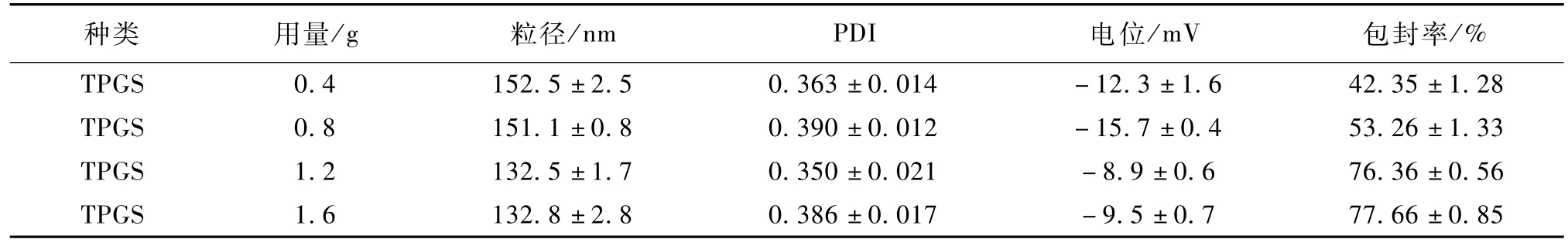
表3 TPGS用量對納米粒粒徑和包封率的影響(n=3)Table 3 In fluence of am ount of TPGS on par ticle size and entrapm en t efficiency of nanoparticles(n=3)
隨著TPGS用量的增加,尼美舒利NLC粒徑由152.5±2.5 nm降到 132.5±1.7 nm,包封率由42.35±1.28%升高到77.66±0.85%。TPGS覆蓋到新產生的納米粒子表面,可以降低表面張力,利于粒子的分離。因此TPGS用量增大時可以降低納米粒粒徑。但是用量過大時可能會在水相中形成膠束,增加尼美舒利的溶解度,導致包封率降低[9]。
2.1.4 藥脂比的考察
藥脂比對NLC粒徑和包封率的影響見表4。
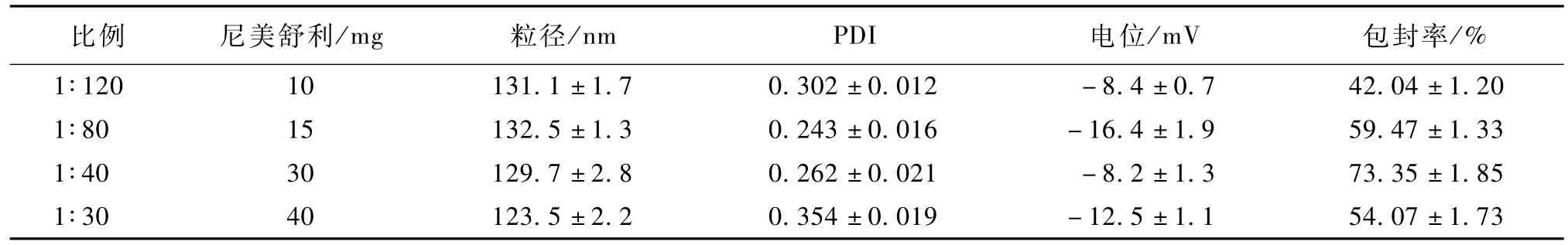
表4 藥脂比考察(n=3)Table 4 Study of ratio of drug to lip id(n=3)
由表4可知,藥物用量變化并沒有對NLC粒徑造成明顯的影響。包封率隨著藥物用量的增加先升高后降低。這是因為藥物用量較低時,溶解在水相中的藥物所占比例較大,導致藥物包封率較低。而當藥物用量較高時,藥物量超過了混合脂質的容納能力,導致包封率較低。
載藥量是評價一種劑型的重要指標。傳統SLN受限于藥物在固態脂質的溶解度較低而導致載藥量較低。本研究中制備的新型NLC由于油酸對藥物溶解度較高,能比較好的改善納米粒的載藥量。
2.1.5 高壓均質壓力的考察
均質壓力對NLC粒徑及包封率的影響見表5。
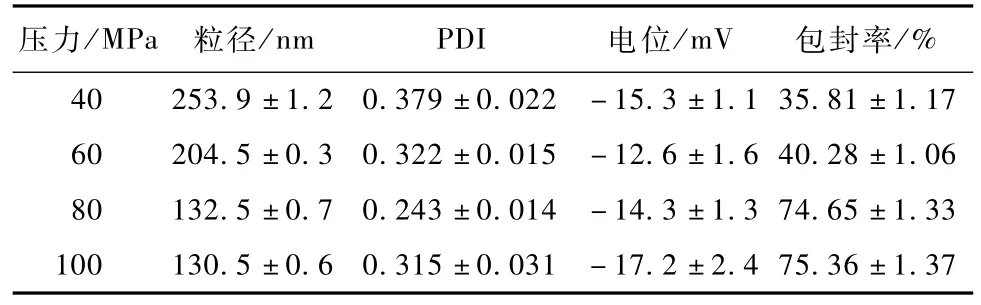
表5 均質壓力對NLC粒徑及包封率的影響(n=3)Table 5 In fluence of hom ogenization p ressure on particle size and en trapm ent efficiency of NLC(n=3)
隨著壓力的增大,粒徑顯著的降低,而包封率顯著的升高。但是過高的均質壓力并不能繼續改善粒徑與包封率。這可能是因為壓力過高時,粒子動能過大,容易發生聚集而使粒徑增大包封率降低[10]。另外,在實驗中發現,均質壓力超過 120 MPa時,會超出高壓均質機的安全工作范圍,產生漏液。因此,高壓均質機的壓力選擇是綜合考慮制備效果、安全性和經濟性的綜合結果。
2.1.6 循環次數的考察
均質循環次數對納米粒粒徑和包封率的影響見表6。
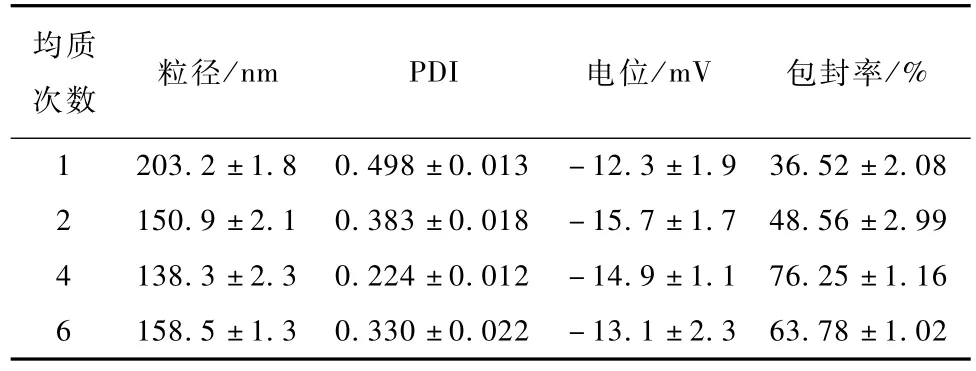
表6 高壓均質次數對NLC粒徑以及包封率的影響(n=3)Table 6 In fluence of cycle tim es on par ticle size and entrapm ent efficiency of NLC(n=3)
過高或過低的均質次數都會增加NLC的粒徑或者降低包封率。這是因為均質次數過少時,樣品沒有得到充分的處理,并且包含微米級顆粒,導致粒徑與包封率結果較差,粒徑分布較寬。當增加均質次數時,樣品被充分處理,粒徑分布較窄。這與以前的文獻報道相一致[11]。但是當均質次數過多時,與壓力過高類似會導致納米粒子動能較高,發生聚集,從而使粒徑增大且包封率降低。
2.2 正交設計考察結果
2.2.1 因素水平的確定
在以上單因素考察的基礎上,選定油酸和GSM投料比(A)、藥脂比(B)、TPGS用量(C)和均質壓力(D)為正交設計考察的因素。因素水平表見表7。
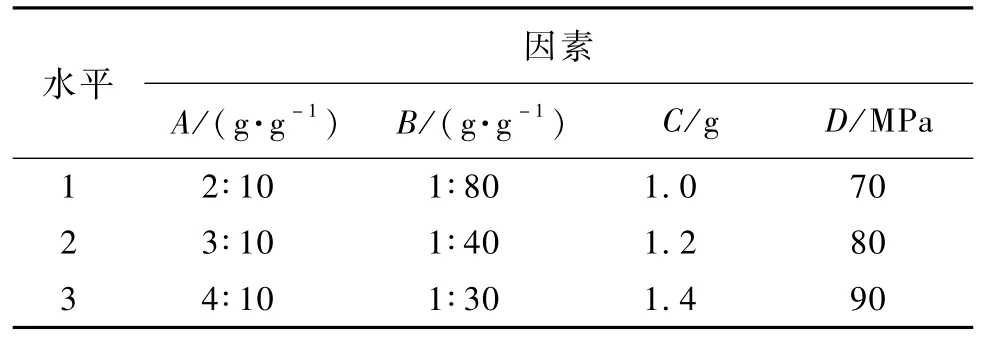
表7 因素水平表Table 7 Factors and levels
2.2.2 正交試驗設計結果
采用L9(34)正交設計表安排9組實驗,以包封率為評價指標,考察各因素對指標的影響,確定最優處方。其它處方與工藝條件為脂質用量為3%,水用量為40 mL,制備初乳溫度為75℃,均質次數為4。實驗結果見表8。
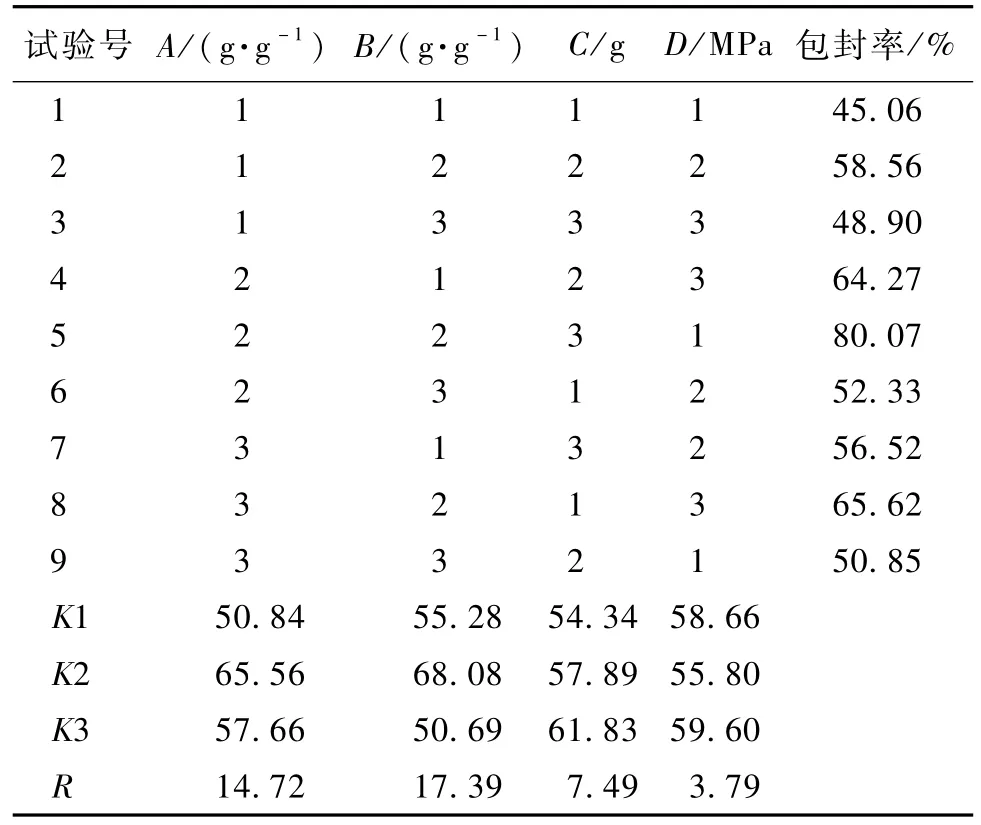
表8 正交設計實驗結果Table 8 Resu lts of or thogonal design
在表8中,R表示極差,R越大表明各因素的影響越大。由R的結果可知各因素對納米粒包封率的影響程度相對大小為B>A>C>D。另外,最優的因素水平組合為A2-B2-C3-D3,即油酸和 GSM投料比為 3∶10,藥脂比為 1∶40,TPGS 用量為 1.4 g,均質壓力為90 MPa。
2.2.3 實驗驗證
因為最適宜組合不在正交設計里的9組實驗中,故需要做實驗予以驗證。即以A2-B2-C3-D3處方條件安排實驗,測定NLC粒徑和包封率。所得結果為粒徑132.6±1.4 nm,包封率為82.35±1.23%。
2.3 Zeta電位測定
Zeta電位與納米粒體系的穩定性密切相關。Zeta電位絕對值越大,表明體系穩定性越好。按照最適宜制備方案制備3批尼美舒利NLC,測得Zeta電位為-14.5±1.2 mV,表明所制備粒子表面荷負電,體系比較穩定。
2.4 形態學觀察
按照最適宜處方制備尼美舒利NLC,用掃描電鏡觀察納米粒形態,結果見圖1。所制備納米粒類球形,粒徑比較均勻。
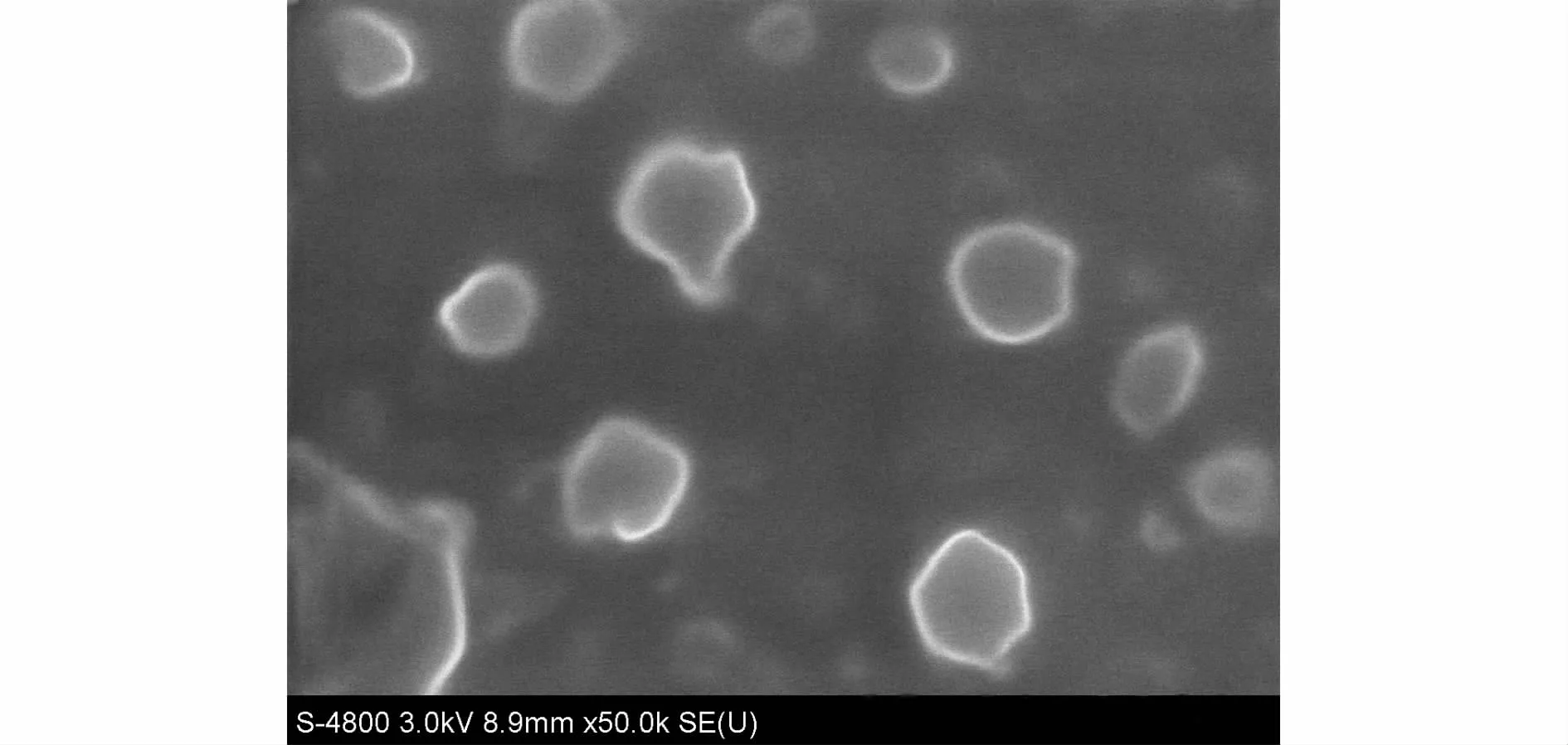
圖1 掃描電鏡結果Fig.1 Result of SEM
2.5 體外釋放情況
釋放試驗所得結果見圖2。
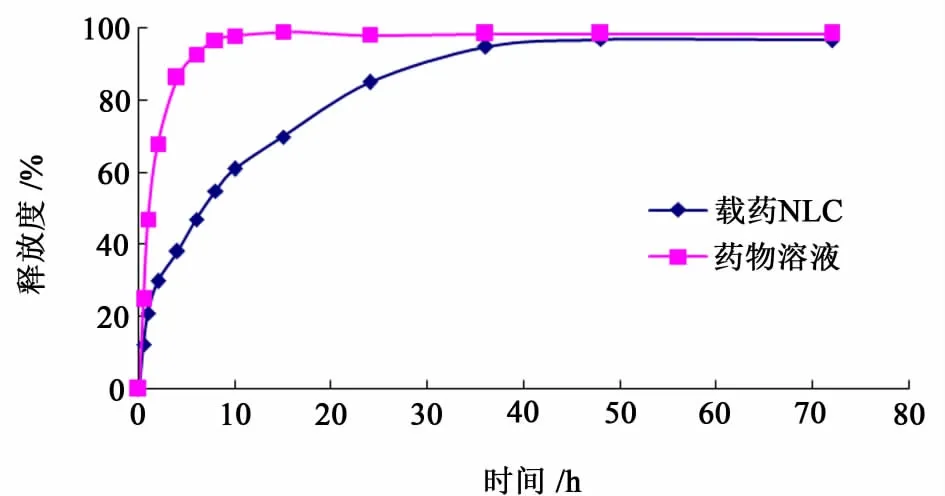
圖2 體外釋放實驗Fig.2 Results of in vitro release
藥物溶液在8 h內即已接近完全釋放,而載藥NLC在前10 h累積釋放率為63.58%,隨后緩慢釋放,最終在72 h時釋放達93.14%。由此推測,有部分藥物分布在納米球的表面,很快釋放出來。而位于納米球骨架內部的藥物則通過擴散釋放或者隨著納米球骨架溶蝕釋放的方式緩慢的釋放出來。
采用Higuchi模型擬合前24 h體外釋放曲線,得擬合曲線Q=0.162 t1/2+0.049,r=0.991。表明體外釋放行為較符合Higuchi模型,這與有關文獻的報道較為一致[8]。
3 結論
本研究采用高壓均質法制備了加載尼美舒利的納米結構脂質載體,采用單因素和正交設計考察處方與工藝因素對納米粒質量的影響。結果表明對包封率影響程度的相對大小為:藥脂比>油酸與GMS投料比>TPGS用量>均質壓力。確定的最適宜處方為油酸與 GMS投料比為3∶10,藥脂比為1∶40,TPGS用量為 1.4 g,均質壓力為90 MPa。 依據最適宜處方制備的納米粒粒徑為132.6±1.4 nm,包封率為82.35±1.23%。
所制備NLC呈類球形,粒徑較為均勻。體外釋放實驗顯示其具有先快速后緩慢釋放的釋藥特性,體外釋放曲線符合Higuchi模型。
[1]Müller R H,Shegokar R,Keck C M.20 years of lipid nanoparticles(SLN&NLC):Present state of development&industrial applications[J].Current Drug Discovery Technologies,2011,8:207-227
[2]Teeranachaideekul V,Muller R H,Junyaprasert V B.Encapsulation of ascorbyl palmitate in nanostructured lipid carriers(NLC):Effects of formulation parameters on physicochemical stability[J].International Journal of Pharmaceutics,2007,340:198-206
[3]Han F,Yin R,Che X,et al.Nanostructured lipid carriers(NLC)based topical gel of flurbiprofen:Design,characterization and in vivo evaluation[J].International Journal of Pharmaceutics,2012,439(1/2):349-357
[4]韓飛,劉洪卓,李三鳴.固體脂質納米粒和納米結構脂質載體在經皮給藥系統中的研究進展[J].沈陽藥科大學學報,2008,25(10):839-844 Han Fei,Liu Hongzhuo,Li Sanming.Recent advances of solid lipid nanoparticles and nano-structured lipid nanoparticles in transdermal drug delivery system[J].Journal of Shenyang Pharmaceutical University,2008,25(10):839-844(in Chinese)
[5]李智.超聲法制備紫杉醇固體脂質納米粒的研究[D].遼寧:沈陽藥科大學,2008 Li Zhi.Study of paclitaxel-loaded solid lipid nanoparticles by ultrasonic method[D].Liaoning:Shenyang Pharmaceutical University,2008(in Chinese)
[6]Jores K,MehnertW,Drechsler M,et al.Investigations on the structure of solid lipid nanoparticles(SLN)and oil-loaded solid lipid nanoparticles by photo correlation spectroscopy,field-flow fractionation and transmission electron microscopy[J].Journal of Controlled Release,2004,95:217-227
[7]Hu F,Jiang S,Du Y,et al.Preparation and characterization of stearic acid nanostructured lipid carriers by solvent diffusion method in an aqueous system[J].Colloids and Surfaces B:Biointerfaces,2005,45:167-173
[8]Teeranachaideekul V,Souto E B,Junyaprasert V B,et al.Cetyl palmitate-based NLC for topical delivery of Coenzyme Q10-development,physicochem ical characterization and in vitro release studies[J].European Journal of Pharmaceutics and Biopharmaceutics,2007,67(1):141-148
[9]Mehnert W,Mader K.Solid lipid nanoparticles:Production,characterization and applications[J].Advanced Drug Delivery Reviews,2012,64:83-101
[10]Siekmann B,Westesen K.Melt-Homogenized solid lipid nanoparticles stabilized by the nonionic surfactant tyloxapol.I.Preparation and particle size determination[J].Pharmaceutical and Pharmacological Letters,1994,3:194-197
[11]Mei Z,Chen H,Weng T,et al.Solid lipid nanoparticles and microemulsion for topical delivery of triptolide[J].Eurupean Journal of Pharmaceutics and Biopharmaceutics,2003,56:189-196
[12]Teeranachaideekul V,Souto E B,Junyaprasert V B,et al.Cetyl palmitate-based NLC for topical delivery of Coenzyme Q10-Development,physicochemical characterization and in vitro release studies[J].European Journal of Pharmaceutics and Biopharmaceutics,2007,67(1):141-148

