我國藥物臨床試驗機構的地域及專業分布
張華吉,鄒艷惠(1.國家食品藥品監督管理總局信息中心,北京 100053;.吉林省人民醫院,長春 13001)
藥物臨床試驗是新藥上市前在人體進行的安全性和有效性的科學評價過程。為了確保臨床試驗科學規范、數據準確可靠、受試者的安全和權益并加強臨床試驗監管,原國家食品藥品監督管理局于2003年8月頒布了《藥物臨床試驗質量管理規范》,又于2004年2月發布了《藥物臨床試驗機構資格認定辦法(試行)》,為我國藥物臨床試驗機構的建設奠定了法律基礎。近10年來,我國藥物臨床試驗機構的能力建設有了很大進步,特別是“十一五”“重大新藥創制”科技重大專項實施以來,國家進行了大量的投入,取得了巨大成就[1]。隨著我國自主創新藥物越來越多地進入臨床試驗,臨床試驗機構將面臨越來越多的挑戰,加深對臨床試驗機構的認識意義重大。經筆者對國家食品藥品監督管理總局網站藥物臨床試驗機構認定的公告數據[2]進行整理,將2005-2013年我國認定的藥物臨床試驗機構的地域及專業分布基本情況介紹如下。
1 我國藥物臨床試驗機構的認定情況
自2005年實施《藥物臨床試驗機構資格認定辦法(試行)》以來,國家藥品監管部門共發布了38 份藥物臨床試驗機構資格認定公告,涉及446 份公告號在內的403 家醫療機構的認定。2005年來每年新增認定的藥物臨床試驗機構情況見圖1。
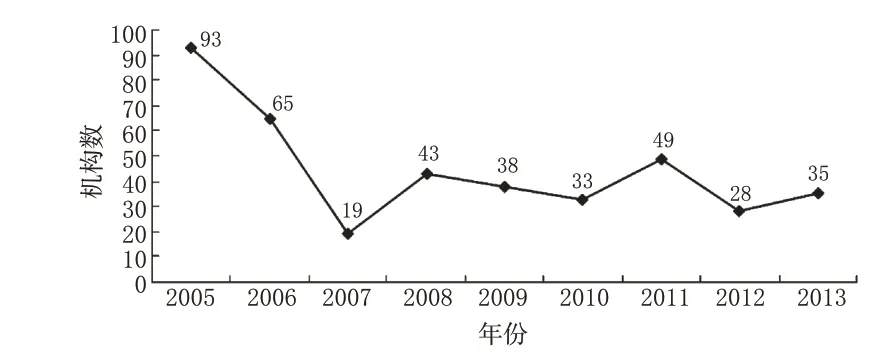
圖1 2005年來歷年新增認定的藥物臨床試驗機構情況Fig 1 Recognition of drug clinical trial institution since 2005
由圖1可見,自2008年以來,我國每年新增認定的藥物臨床試驗機構數量呈現基本穩定的態勢。2005-2007年的變化幅度較大,主要原因是《藥物臨床試驗機構資格認定辦法(試行)》規定:2005年3月1日前未獲得藥物臨床試驗資格的醫療機構以及原國家藥品臨床試驗基地,將不再具有承擔藥物臨床試驗的資格。因此,所有在此之前承擔藥物臨床試驗的152 家國家藥品臨床研究基地均需重新認定其藥物臨床試驗機構的資格,致使2005、2006年的藥物臨床試驗機構認定數量較高。
2 我國藥物臨床試驗機構的地區分布
2.1 東部省份獲得認定的藥物臨床試驗機構數量明顯占優
經統計403家藥物臨床試驗機構在各省份的分布情況,發現擁有臨床試驗機構數量在前10 位的省份除湘(第8 位)、鄂(第9位)兩省為中部省份外,其余均為東部省份,前10位省份合計認定267 家,占全部臨床試驗機構的66.3%。其中,京、粵、滬列臨床試驗機構數量的前3 位,約占全部臨床試驗機構總量的32.0%,這在一定程度上反映出我國衛生資源分布不平衡,與我國的醫療資源分布東部地區占優的情況基本相當[3]。臨床試驗機構的分布與地區經濟發展亦有直接關聯,經濟發達的東部地區衛生資源配置比較完善,更易于建設臨床試驗機構。各省份獲得認定的藥物臨床試驗機構數量見圖2。
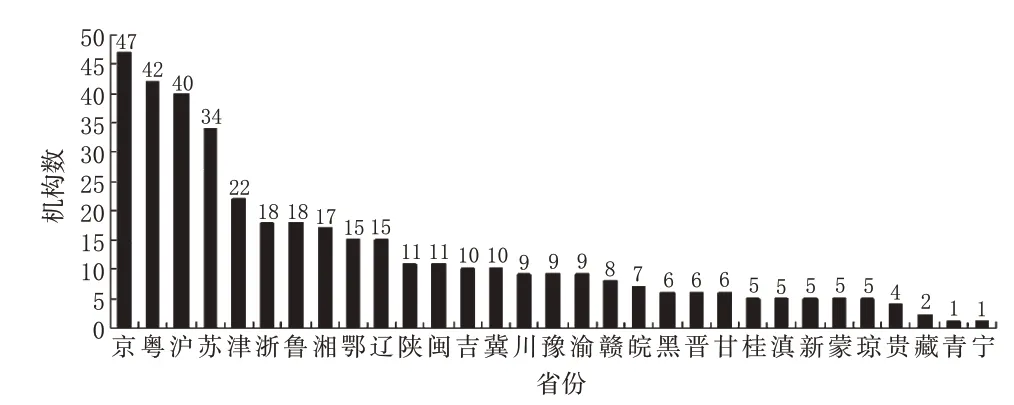
圖2 各省份獲得認定的藥物臨床試驗機構數量Fig 2 The number of clinical drug trial institutions in each province
2.2 臨床試驗機構主要集中在省會城市
多數省份的臨床試驗機構主要分布在省會城市,只有少數臨床試驗機構分布在省會以外的城市,顯示各省內部臨床試驗機構地域分布仍不均衡。403家臨床試驗機構中,分布在省會城市的有321 家,占80%;而非省會城市有82 家,占20%。臨床試驗機構全部分布在省會城市的省份多達11 個,占全部省份的35.5%。相對于其他省份,江蘇的臨床試驗機構在省內分布相對比較均衡,所擁有的34 家臨床試驗機構分布在省內10 個主要城市,但省會城市仍然占主導地位,共有15家,占全省臨床試驗機構總數的44.1%;其次分布相對均衡的是廣東,省會城市擁有27 家臨床試驗機構,占省內總數的64.3%。從全國整體數據顯示,臨床試驗機構仍然主要分布在省會城市,且省內地區分布仍不均勻。
3 我國藥物臨床試驗機構的專業分布
3.1 認定專業以西醫專業為主
截至目前,共認定的專業科室數量總計為2 982 個。其中,西醫專業2 364個,中醫(含民族醫學)專業618個。西醫專業科室數量占全部總認定數量的79.3%,占絕大多數;中醫專業僅占20.7%,遠遠低于西醫專業。
3.2 各地區認定專業科室數量分布情況
從獲批的專業科室數量來看,東部省份獲批專業數量依然占優。前10位省份中,除湘(第4位)、川(第9位)、鄂(第10位)外,其余省份均為東部省份。京、滬、粵等東部省份分別以101、72、62 個認定專業科室數量位居前3 位,明顯高于其他省份。各省份獲得認定的藥物臨床試驗專業科室數量見圖3。
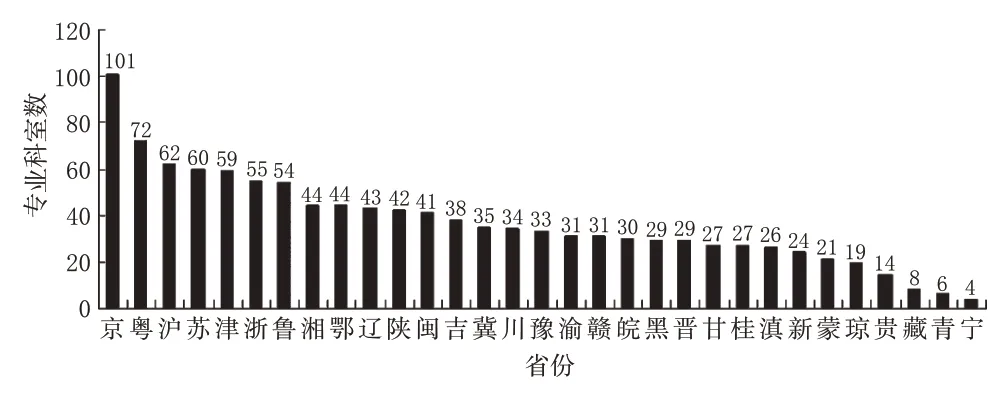
圖3 各省份獲得認定的藥物臨床試驗專業科室數量Fig 3 The number of accredited professional departments in each province
3.3 各專業認定情況
臨床試驗機構中,醫療技術水平較高的醫院所認定的專業也較多,且不同專業的認定數量差異較大。目前,共有150種專業獲得認定,其中心血管、消化、呼吸、腫瘤、神經內科、內分泌、腎病、血液病、骨科、普通外科分列各認定專業的前10位。藥物臨床試驗機構中認定的專業數量見圖4。
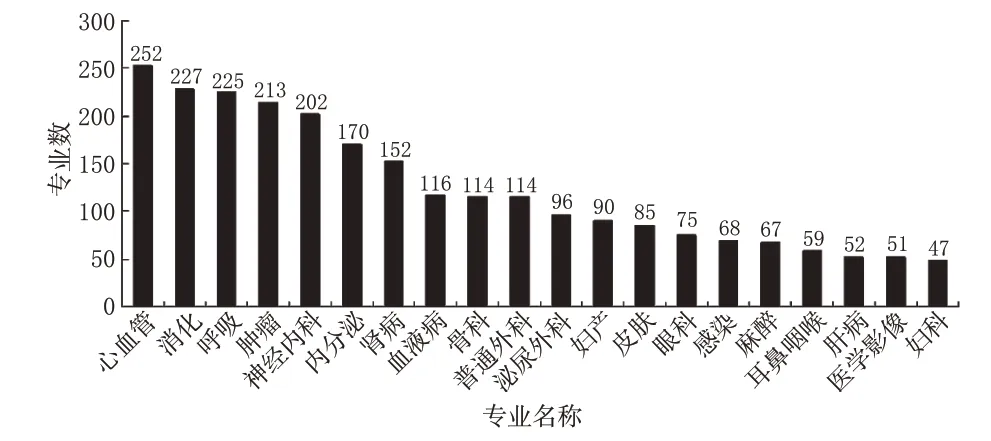
圖4 藥物臨床試驗機構中認定的專業數量Fig 4 The number of professional departments in clinical drug trial institutions
3.3.1 心血管專業。心血管作為一個較大的專業,在全國除青海外的其他30個省份均有臨床試驗機構的認定。北京認定最多,有28 家;其次是廣東、江蘇和上海,分別以25、23、22 家位列其后。位列前4 位省份認定機構數總數約占全部心血管專業認定機構數的38.9%,超過總數的1/3;其余26 個省份占了剩余的61.1%。共有252 家臨床試驗機構獲得心血管專業的認定,占全部403 家臨床試驗機構的62.5%,說明心血管專業在醫療工作中占有舉足輕重的地位。該數據同時也驗證了心血管疾病是當前發病率較高的疾病,心血管藥物面臨著巨大的市場需求。
3.3.2 消化、呼吸、腫瘤專業。消化專業在全國31個省份均有分布。北京、上海、江蘇、廣東分別以24、22、21、17家位列消化專業的前4位,占全部消化專業臨床試驗機構的37.0%。全國共有227家機構獲得消化專業的認定,占全部臨床試驗機構的56.3%。消化專業是僅次于心血管的第二大專業。
呼吸專業在全國31 個省份亦均有分布。北京、上海、江蘇、廣東分別以27、22、22、20 家位列呼吸專業的前4 位,占全部呼吸專業臨床試驗機構的40.4%。全國共認定225家,占全部臨床試驗機構的55.8%。
除青海、西藏、海南無腫瘤專業外,其余28 個省份均獲得腫瘤專業的臨床試驗機構的認定,廣東、北京、江蘇、上海分別以24、22、22、20家位列腫瘤專業的前4位,占全部腫瘤專業臨床試驗機構的41.3%。全國共認定213家醫院,占全部臨床試驗機構的52.9%。
3.3.3 民族醫學專業。民族醫學專業認定的主要是蒙醫和藏醫,共認定23 個專業科室,占全部認定專業科室數量的0.8%。所認定的臨床試驗機構分布在內蒙古、青海、西藏3個省份,其中內蒙古2家,青海、西藏各1家。認定的專業涉及風濕、婦產、肝膽、骨傷、呼吸、心血管、腦血管、內分泌、皮膚、腎病、消化、血液病等專業。
3.3.4 兒科、老年病專業。兒科藥物的臨床試驗一直是醫藥工作者研究的重點。臨床試驗機構中擁有兒科專業的有49家,占全部臨床試驗機構的12.2%,包含134個兒科專業科室,涉及兒科專業25個。其中,以小兒呼吸專業為最多,共認定21家,占全部兒科專業認定機構的42.9%;位列其后的是中醫兒科(18家)、小兒腎病(12家)、小兒血液病(11家)、小兒消化(10家)、小兒內分泌(9家)等專業。老年病專業共認定13家臨床試驗機構,其中中醫老年病專業6家,分布在江蘇、北京、吉林、浙江、湖南、遼寧、天津和甘肅等省份。
3.3.5 中醫專業。共認定119家機構的618個專業科室。119家機構中,62家為中醫專科醫院,基本是中醫藥院校附屬醫院或當地的中醫綜合醫院;57 家為含有中醫專業的以西醫為主的綜合性醫院,這些醫院分布在30個省份。其中,認定數量最多是上海,為15 家;其次是北京,為14 家;再次是廣東,為10家。認定的臨床醫療機構為中醫專科醫院的,廣東7家,北京、江蘇均為5家,上海、河南均為4家。
3.3.6 其他專業。戒毒專業認定8家臨床試驗機構,分布在北京、湖南、湖北、四川、廣東、云南。艾滋病(即獲得性免疫缺陷綜合征)專業認定10家臨床試驗機構,分布在北京、廣東、湖南、上海、浙江;其中中醫艾滋病專業1家,西醫專業9家;北京有5家醫療機構獲得艾滋病專業的認定,占該專業臨床試驗機構的50%。高原病在西藏認定1家醫院。抗輻射、抗毒、特種醫學與軍事醫學、熱帶病等少見疾病在北京各有1家醫院獲得認定。
4 臨床試驗機構發展中存在的問題
4.1 藥物臨床試驗機構數量遠低于醫院總量
截至2013年8月底,全國醫療衛生機構數達96.1萬個,其中醫院2.4萬個[4],而目前我國認定的藥物臨床試驗機構僅403家醫院,不到全部醫院的1.7%。與醫院總量相比,臨床試驗機構的數量還應有較大的增長空間,隨著各級醫院基礎設施的進一步完善,以及人員素質的進一步提高,應鼓勵有條件的醫院申請臨床試驗機構的認定。
4.2 藥物臨床試驗機構地域分布不均衡
目前所認定的臨床試驗機構,主要分布在經濟比較發達的省份,以東部省份居多,出現東多西少的現象;同時,各個省份的臨床試驗機構又主要聚集在省會城市及省內經濟比較發達的城市。這導致臨床試驗機構數量在全國各省份之間分布不均衡,各省份內部亦呈現分布不均衡的現象。
4.3 一些專業的認定數量明顯偏少
4.3.1 中醫專業。隨著世界各國之間經濟、科技交流與合作的逐步活躍,中醫中藥在國外的認知度也在不斷擴大,更多的中藥新藥將會上市,中醫專業的藥物臨床試驗將呈現遞增趨勢。當前所認定的119 家機構的618 個專業科室也僅占全部認定專業科室的20.7%。此外,一些綜合性醫院雖然設置了中醫科,但中醫并不是醫院工作重點,受到的關注扶持較少,更加制約了中醫專業臨床試驗機構的發展。
4.3.2 民族醫學專業。當前,我國已有31 個民族挖掘整理了本民族的醫學資料,其中,藏族、蒙古族、壯族、維族、朝鮮族、傣族、回族、苗族、瑤族、布依族、彝族、侗族、羌族、土家族、哈薩克族等民族設立了民族醫院[5]。目前,藥物臨床試驗機構中也只認定了藏族、蒙古族的民族醫學專業,而其他民族專業未見有臨床試驗機構的認定。我國民族醫藥有悠久的歷史,民族藥新藥開發有很大潛力,這就需要有相關民族醫臨床試驗機構的支持。2009年全國各地區民族醫院總計是191家[6],而目前只有4家民族醫院獲得民族醫學專業的認定,臨床試驗機構的認定數量依然偏少。
4.3.3 兒科專業。全國共有49家醫療機構獲得兒科專業的臨床試驗機構認定,與我國龐大的兒童人群及兒科疾病狀況極不適應。長期以來,臨床使用的兒科藥物大多未經過專門的兒科臨床試驗證實,只是通過成人藥物臨床試驗,再按照醫師的臨床經驗為兒童給藥。然而兒童的身體狀況、生理機能,尤其是一些重要臟器和系統,如肝、腎、神經和內分泌功能與成人的差異較大,藥動學和藥效學有其獨特的規律,因此開發兒科新藥須以兒童人群為臨床試驗研究對象。與成人臨床試驗相比,兒童藥物臨床試驗受試者召集難度大、臨床試驗花費高,且兒科藥物市場規模不大,因而對制藥企業的經濟驅動力較小,有資質且對兒科藥物臨床試驗感興趣的研究者少[7]。這導致很多藥物在開展多中心臨床試驗時,可選擇的藥物臨床試驗機構較少,難以滿足兒科新藥臨床試驗的開展。
5 改進臨床試驗機構分布狀況的構想
5.1 鼓勵醫療機構參與認定,提高臨床試驗機構數量
隨著全球新藥研發的進一步加速,新藥臨床試驗尤其是多中心臨床試驗的開展將越來越多。亞洲擁有豐富的疾病資源和患者資源,擁有巨大的藥品消費市場,很多跨國制藥企業將臨床試驗的重心轉移到了亞洲[8],因此我國更要鼓勵醫院積極參與臨床試驗機構的認定,加大認定機構數量,以適應越來越多的臨床試驗的需求。
醫院開展藥物臨床試驗,可使醫院的學術水平緊跟醫學、藥學研究前沿,促進醫療機構自身的發展和壯大。對于實力較強的醫療機構因未申請藥物臨床試驗機構認定而無法參加新藥的臨床試驗,從某種意義上講,也是一種資源的浪費[9]。建議有關部門大力宣傳醫療機構開展藥物臨床試驗的重要意義,鼓勵醫院參加藥物臨床試驗機構的認定,以滿足日益增加的新藥研發需求。
5.2 加強欠發達地區的醫療資源投入,平衡地區間差異
現有藥物臨床試驗機構地域分布很不均衡,經濟發達地區占有絕對優勢;經濟欠發達地區因軟、硬件條件的限制,其擁有的藥物臨床試驗機構數量寥寥無幾。因此,為平衡地區間醫療資源,推動轄區醫院積極開展臨床試驗機構的認定是提高醫院競爭力、豐富醫療資源的好辦法。在滿足藥物臨床試驗機構基本要求的前提下,推動經濟欠發達地區藥物臨床試驗機構建設和臨床專業科室的建設,使醫療資源配置相對均衡。同時,經濟欠發達地區的疾病資源豐富,對制藥企業開展臨床試驗低成本召集受試者也是一種吸引力,為這些地區發展藥物臨床試驗機構奠定了基礎。
5.3 增加一些專業科室的認定數量
中醫、中藥是祖國的瑰寶,是具有較高成長性的領域。國家中醫藥管理局于2012年發布了中醫藥事業發展“十二五”規劃,對中醫中藥的發展有作出重大部署[10]。然而,現有臨床試驗機構數據顯示中醫(含民族醫學)專業的藥物臨床試驗機構和專業科室數量明顯低于西醫專業。隨著中醫中藥行業的發展,中藥、民族藥新藥的研究和開發將越來越多,對臨床試驗的需求會越來越大。因此,醫院應重視中醫專業科室的建設,促進醫院中醫科室認定藥物臨床試驗機構工作開展。同時,國家在大力發展中藥、民族藥的進程中應加大力度扶持中醫、民族醫學專業藥物臨床試驗機構的設置。
隨著兒科新藥研發的進展,兒科藥物的臨床試驗的需求將進一步擴大。我國目前開展的兒科臨床試驗數量尚不多,除了與兒童專用新藥的自主研發能力相對較弱外,還與我國兒童藥物臨床試驗機構的不足有關。兒科藥物的臨床試驗機構不足將制約著兒童藥物臨床試驗的發展。要在我國建立系統和完善的兒科臨床試驗管理體系,還需進行大量的工作,臨床試驗機構的建設和認定就是其中的重要內容。
綜上所述,現有藥物臨床試驗機構呈現地區、專業的不均衡。因此,應鼓勵醫療機構參與臨床試驗機構的認定,增加臨床試驗機構和相關專業科室的認定數量,做到統籌兼顧,平衡臨床試驗機構資源,為新藥的臨床驗證打好基礎。
[1]石遠凱,莫紅楠,孫燕.實施臨床試驗準備階段質量控制的意義與方法[J].中國藥物評價,2013,30(4):193.
[2]國家食品藥品監督管理局.藥物臨床試驗機構認定公告[EB/OL].(2013-09-25)[2013-12-30].http://www.cfda.gov.cn/WS01/CL0069/.
[3]陳惠.2012《中國藥品市場報告》:醫療資源多在東部[EB/OL].(2013-01-14)[2013-12-30].http://health.sohu.com/20130114/n363414226.shtml.
[4]中華人民共和國衛生和計劃生育委員會.2013年8月底全國醫療衛生機構數[EB/OL].(2013-10-17)[2013-12-30].http://www.nhfpc.gov.cn/mohwsbwstjxxzx/s7967/201310/65581817c2a94b2faa1887bf84ca83aa.shtml.
[5]趙秀麗,單愛蓮,王淑民,等.我國藥物臨床試驗機構資格認定現狀[J].中國臨床藥理學雜志,2011,21(10):809.
[6]衛生部.2010中國衛生統計年鑒[EB/OL].(2010-10-08)[2013-12-30].http://www.moh.gov.cn/publicfiles/business/htmlfiles/zwgkzt/ptjnj/year2010/index2010.html.
[7]王曉玲.兒童藥物臨床試驗的國內外現狀研究[J].中國藥物評價,2013,30(3):167.
[8]付曉陽,孫利華.制藥公司對臨床試驗的干預作用[J].中國醫藥導刊,2013,15(4):733.
[9]武小軍,李欣.我國藥物臨床試驗機構的發展與現狀[J].中國藥物經濟學,2009(2):36.
[10]國家中醫藥管理局.國家中醫藥管理局關于印發中醫藥事業發展“十二五”規劃的通知[EB/OL].(2012-06-06)[2013-12-30].http://www.satcm.gov.cn/web2010/zhengwugongkai/jihuaguihua/zhuanxiangguihua/2012-06-06/15737.html.

