正交設計試驗優選去甲斑蝥素在大鼠肝細胞中代謝的影響因素Δ
王曉輝,高 萍,李光遠,王 瑛,陶遵威,李毅敏(天津市醫藥科學研究所,天津 300020)
去甲斑蝥素(Norcantharidin,NCTD)是斑蝥素的衍生物。與斑蝥素相比,其對泌尿系統的刺激性顯著降低,并具有獨特的升高白細胞總數的作用,也是我國首先合成的新型抗腫瘤藥物[1]。其衍生物眾多而且很多衍生物都表現出抗腫瘤活性[2],其新型制劑研發工作也取得一些進展[3]。但由于NCTD 自身化學性質活潑、代謝快速以及代謝產物的復雜性,導致其代謝機制和代謝物的深入研究非常困難,限制了NCTD開發應用。
利用細胞株對藥物進行代謝的研究方法可以排除體內因素的干擾,為整體藥物研發提供可靠的試驗數據。對體內代謝率低、毒性大以及缺少靈敏檢測方法的藥物來說,細胞代謝法更是首選的研究方法。由于細胞對藥物的代謝受到細胞接種密度、給藥濃度等多種因素影響,所以本文設計正交設計試驗研究NCTD 在大鼠肝細胞(Buffalo rat liver,BRL)中代謝的相關影響因素,以提高代謝效率、獲得最佳培養方案,為后續及相關研究提供科學依據。
1 材料
1.1 儀器
GC-17A 氣相色譜儀[中國(上海)島津有限公司];Infinite M200酶標儀[帝肯(上海)貿易有限公司];Legend Micro17R高速離心機(美國Therme Electron Corportion公司,離心半徑:78 mm);TMS-PH-3倒置顯微鏡[尼康儀器(上海)有限公司]。
1.2 藥品與試劑
NCTD 對照品(中國食品藥品檢定研究院,批號:100414-200501,純度:100%);NCTD原料藥(南京景竹生物科技有限公司,批號:JZ130421A,純度:99%);達爾伯克改良伊格爾(DMEM)培養基(美國Gibco公司,批號:12800-027)。
1.3 細胞
大鼠BRL細胞(國家科學院典型培養保藏委員會細胞庫)。
2 方法與結果
2.1 檢測NCTD對BRL細胞的半數抑制濃度(IC50)
參考相關資料[4],將BRL 細胞按照25 000、50 000、75 000個/ml 3 種密度進行接種,用培養液將NCTD 配成10.0、7.14、5.10、3.64、2.60、1.86、1.33、0.949、0.678、0.484 μg/ml 10 個質量濃度,培養48 h,用MTT法檢測細胞抑制率,重復3次。結果3種細胞接種密度下的IC50分別為(6.04±0.22)、(5.82±0.31)、(6.07±0.18)μg/ml,其平均值5.98 μg/ml即為NCTD對BRL細胞的IC50。
2.2 檢測NCTD相對含量的方法
2.2.1 色譜條件。色譜柱:DM-1 毛細管色譜柱(30 m×0.25 mm,0.25 μm);流動相:氮氣,流速:1 ml/min;檢測器:氫離子火焰檢測器(FID);柱溫:200 ℃;進樣口溫度:250 ℃;檢測器溫度:280 ℃;無分流;進樣量:1 μl。
2.2.2 樣品的處理。收集各組培養液,加入10%三氯乙酸[10%三氯乙酸:培養液(0.6 ∶1)]除蛋白,以10 000 r/min離心5 min,取上清液濃縮干燥,將固體干燥物用200 μl水定容,靜置30 min充分溶解,取上清液濾過作為待測樣品。
2.2.3 方法專屬性考察。分別將NCTD對照品、空白培養液、培養液+NCTD對照品,經“2.2.2”項下處理后,按“2.2.1”項下色譜條件檢測,記錄色譜。結果空白培養液對NCTD 色譜峰幾乎無干擾,色譜圖見圖1。
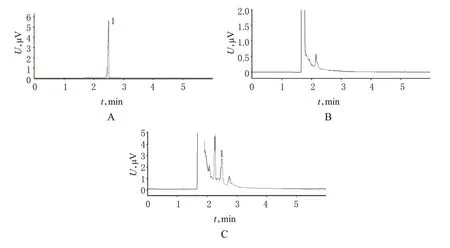
圖1 氣相色譜圖A.對照品;B.空白培養液;C.培養液+NCTD對照品;1.NCTDFig 1 GC chromatogramsA.substance control;B.blank culture medium;C.culture medium sample+NCTD control;1.NCTD
2.2.4 精密度試驗。配制質量濃度分別為0.200 0、0.800 0、3.200 μg/ml 的NCTD 培養液樣品,按“2.2.2”項下方法處理后進樣。同日內測定5次,得日內RSD為(2.58±0.37)%;每日測定1次,連續測定5 d,得日間RSD為(5.10±0.55)%。
2.2.5 檢測限考察。以信噪比為3 時,NCTD 的檢測限為10 ng/ml。
2.3 正交設計試驗優選最優培養條件
根據“2.1”項下方法與結果,參考相關文獻[5-6],選取細胞接種密度(A)、給藥濃度(B)、培養時間(C)為考察因素。因素A、C 的考察水平參考文獻選取3 個水平;因素B 考察水平以NCTD 對BRL 細胞的IC50為參考,選取3 個水平,具體數值見表1。
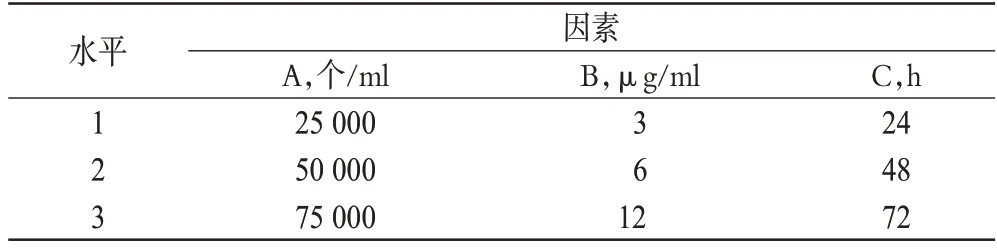
表1 正交設計試驗因素與水平Tab 1 Factors and levels of orthogonal test
按照4因素3水平L9(34)正交試驗表進行試驗,培養體系置于37 ℃、5%二氧化碳及飽和濕度條件下培養相應時間,以培養體系中NCTD的相對含量的峰面積為評價指標。正交設計試驗結果及極差分析見表2,方差分析結果見表3。
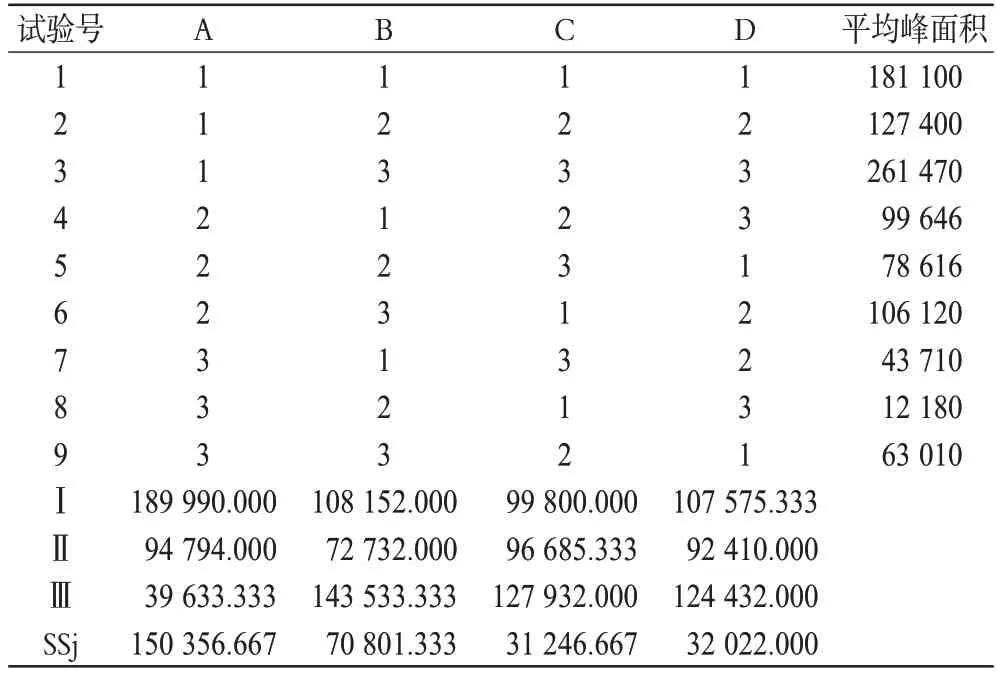
表2 正交設計試驗結果與極差分析(n=3)Tab 2 Results of orthogonal test and analysis of range(n=3)
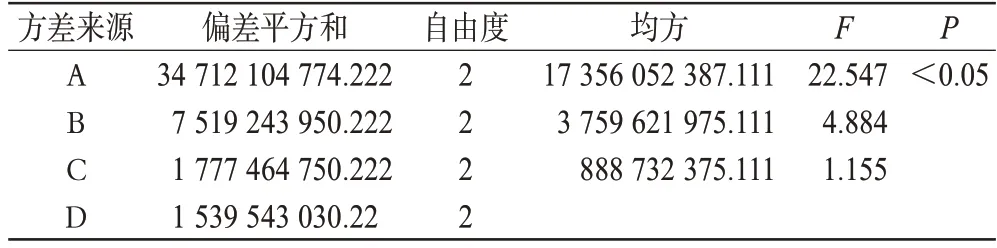
表3 正交設計試驗的方差分析Tab 3 Results of orthogonal test and analysis of variance
由表2、表3可知,各因素對培養體系中NCTD相對含量的影響順序為A>B>C。其中,因素A 有顯著性影響(P<0.05),選擇水平3;而因素B、因素C 各水平間差異不大,從培養效率方面考慮,均選擇水平2。故最優培養條件為A3B2C2,即接種密度為75 000個/ml,給藥濃度為6 g/ml,培養時間為48 h。根據最優條件培養,試驗重復3次,檢測其體系中NCTD的相對含量的峰面積為10 567±664。
3 討論
有資料報道NCTD 對人肝癌細胞Bel-7402、HL-7702 的IC50分別為18.84、22.66 μg/ml[7],對海拉癌細胞Hela 的IC50為261 μg/ml[8],對人胃癌細胞BGC-823的IC50為7.85 μg/ml[9]。本研 究 中NCTD 對BRL 細 胞 的IC50為5.98 μ g/ml,由 此 表 明NCTD對不同細胞株的抑制率是不一樣的,所以在對不同細胞株試驗研究時,應該對其抑制率進行研究。通過預試驗,筆者將NCTD對BRL細胞IC50的0.5、1、2倍作為正交設計試驗的給藥濃度,即3、6、12 μg/ml。
由于NCTD分子結構中不含共軛結構,無強生色團,導致NCTD 無紫外特征吸收峰,所以使用紫外檢測法進行體內藥動學研究和體外代謝產物研究時會受較多干擾,達不到檢測要求。本試驗建立氣相色譜法測定培養基中NCTD 藥物濃度,并對該方法進行方法學考察研究。結果表明,該方法符合生物樣品的分析要求,可為NCTD的體內外藥動學研究、臨床給藥監測以及開發高效低毒的NCTD衍生物和新劑型等提供簡單快捷的檢測方法。體外代謝是利用各種體外代謝模型對候選化合物進行高通量篩選,可以對代謝過快或生成毒性代謝物的候選化合物進行結構改良,也可以通過模擬或合成活性代謝物的結構得到新的候選化合物。與體內代謝研究相比,體外代謝研究可在新藥研發早期利用候選化合物的體外代謝參數合理預測候選化合物的體內藥動學行為,指導后期藥效學、藥動學以及安全性評價的模型選擇,縮小體內研究的篩選范圍,具有廣闊的應用前景[10]。
通過正交設計試驗研究發現,接種密度對以代謝快慢具有顯著的影響且影響最大;而給藥濃度和培養時間沒有顯著性,通過直觀分析看到給藥濃度的影響次之,培養時間影響最小。當接種密度為75 000個/ml、給藥濃度為6 g/ml、培養時間為48 h時,在培養液中剩余NCTD含量是最低的,說明在此條件下,NCTD 在BRL 細胞中代謝效率最高。NCTD 在BRL 細胞中代謝最優培養條件的研究結果可為NCTD體外代謝產物的相關研究提供可靠的科學數據和必要的前提條件。
[1]余濤,劉曼曼,侯風剛,等.去甲斑蝥素抗腫瘤分子機制研究進展[J].遼寧中醫藥大學學報,2012,14(4):73.
[2]李賀敏,彭國平,陳農,等.新型斑蝥素羧酸衍生物的合成及其抗癌活性[J].合成化學,2013,21(5):518.
[3]牛硯濤,武冬雪,董文娜,等.去甲斑蝥素新型制劑研究進展[J].中國藥學雜志,2013,48(9):663.
[4]魏偉,吳希美,李元建.藥理實驗方法學[M].4版.北京:人民衛生出版社,2010:1 568-1 569.
[5]楊慈清,李小英.Hepal-6細胞的最佳培養條件研究[J].安徽農業科學,2010,38(28):15 507.
[6]王爽,梁偉伶,劉斯斯,等.正交試驗法優選HepG2 細胞最佳培養條件[J].中國現代醫學雜志,2007,17(13):1 603.
[7]胡瑋,章良,王欽,等.去甲斑蝥素N-乳糖酰殼聚糖納米粒的肝靶向抗腫瘤藥效學評價[J].中國新藥雜志,2010,19(19):1 814.
[8]劉洪月,楊紅,吳秀鳳,等.葉酸修飾去甲斑蝥素隱形泡囊的制備、表征及體外藥效學評價[J].中國新藥雜志,2013,22(18):2 174.
[9]王晨宇,李猛,王天陽,等.DHA 聯合去甲斑蝥素對人胃癌細胞BGC-823增殖及凋亡的影響[J].世界華人消化雜志,2013,21(11):1 008.
[10]吳慧,彭英,孫建國,等.體外代謝在新藥早期評價中的應用與發展[J].藥學學報,2013,48(7):1 071.

