廢水中硝態(tài)氮來(lái)源、轉(zhuǎn)化及去除方法
趙 群
(山東省環(huán)境保護(hù)科學(xué)研究設(shè)計(jì)院, 山東 濟(jì)南 250013)
1 廢水中硝態(tài)氮的來(lái)源
2 硝態(tài)氮在處理過(guò)程中的轉(zhuǎn)化
硝態(tài)氮是氮元素的高價(jià)態(tài)化合物(+3和+5價(jià)),所以硝態(tài)氮的轉(zhuǎn)化往往是氮素的還原即反硝化.當(dāng)氧氣含量非常低時(shí),硝酸鹽開(kāi)始替代氧氣作為電子受體,有機(jī)物、硫化物、氫氣等提供電子,還原硝氮物質(zhì).以有機(jī)物作為電子供體時(shí),參與的微生物為異養(yǎng)菌,硫化物、氫氣等無(wú)機(jī)物作為電子供體時(shí),參與的微生物為自養(yǎng)菌.自然界中具有反硝化能力的細(xì)菌廣泛存在于廢水中.硝氮還原為氮?dú)鈱?shí)際上是分步進(jìn)行的,大量研究表明,硝酸根的異化代謝路徑如下[6]:
低pH值(pH<7)有利于形成氮氧化物;高pH值(pH>7)有利于形成氮?dú)?氮氧化物仍為環(huán)境污染物質(zhì),因此,反硝化液的pH值應(yīng)維持在pH>7以上,以使硝酸鹽代謝的最終產(chǎn)物以氮?dú)獾男问揭莩?
硝酸鹽的同化代謝途徑目前尚不完全清楚,但一般認(rèn)為大致遵循以下規(guī)律:
有機(jī)氮→細(xì)胞
其細(xì)胞產(chǎn)率大約為每還原1 g的硝氮,產(chǎn)生約0.4 g的細(xì)胞物質(zhì).一般細(xì)胞物質(zhì)可表示為C5H7NO2,其中N僅為0.04 g,因此,在硝酸鹽的代謝過(guò)程中,氣態(tài)氮是其代謝的主要最終產(chǎn)物.
3 常用的處理方法
常用的脫氮方法有化學(xué)脫氮(零價(jià)鐵和鎂還原,離子交換,反滲透,電滲析、催化脫氮)和生物脫氮[7-8].世界衛(wèi)生組織(WHO)建議采用生物脫氮和離子交換法脫氮,而離子交換、反滲透和電滲析則被美國(guó)環(huán)保署(EPA)認(rèn)為是最可行的處理被硝酸鹽污染水的方法.但這些脫氮的方法均有其優(yōu)點(diǎn)和缺點(diǎn),見(jiàn)表1.

表1 去除硝氮方法的優(yōu)缺點(diǎn)
3.1 離子交換法
離子交換法是指讓含有硝酸鹽廢水通過(guò)強(qiáng)堿性陰離子交換樹(shù)脂,樹(shù)脂中的氯離子或碳酸氫根離子被硝酸根交換下來(lái),從而去除廢水中硝氮的一種方法.飽和后的樹(shù)脂可通過(guò)高濃度的氯化鈉或碳酸氫鈉溶液再生.Komgold指出海水可以做為陰離子交換樹(shù)脂的再生液[9].常規(guī)的強(qiáng)堿性陰離子交換樹(shù)脂對(duì)陰離子選擇性是碳酸氫根最弱,其次是氯離子,而對(duì)硫酸根選擇能力最強(qiáng),硝酸根次之.但去除含有高濃度硫酸根溶液的硝酸鹽時(shí),情況變得非常復(fù)雜.因此很有必要開(kāi)發(fā)一種專門(mén)去除硝酸根的樹(shù)脂.當(dāng)樹(shù)脂中銨根周?chē)奶荚釉黾訒r(shí),樹(shù)脂對(duì)硝酸根的選擇性增加.如樹(shù)脂中銨根周?chē)募谆灰一娲螅跛岣鄬?duì)于硫酸根的選擇性系數(shù)從100增加至1000.另外增加樹(shù)脂或其鍵合官能團(tuán)的憎水性也能提供樹(shù)脂對(duì)硝酸鹽的選擇性.但離子交換法再生時(shí)產(chǎn)生高鹽廢水的處置和成本是其應(yīng)用過(guò)程中必須考慮的問(wèn)題.有人用高濃度二氧化碳溶液再生樹(shù)脂從而避開(kāi)產(chǎn)生高鹽廢水,但有關(guān)成本問(wèn)題仍需進(jìn)一步開(kāi)發(fā)[10-12].
3.2 反滲透
反滲透過(guò)程中,含有正負(fù)離子的廢水通過(guò)一個(gè)半透膜,水能夠通過(guò)半透膜,而硝酸根和其它離子被保留從而達(dá)到去除硝酸鹽目的.施加的壓力一般在2070~10350 kPa,半透膜通常由醋酸纖維素構(gòu)成,也可有聚酰胺纖維或復(fù)合膜構(gòu)成,這些膜對(duì)任何離子均沒(méi)有選擇性透過(guò)性,所以可以有效降低水的礦化度.但反滲透也伴隨著一些問(wèn)題,如結(jié)垢、膜壓縮以及隨時(shí)間膜被老化等.這些問(wèn)題將導(dǎo)致可溶性鹽、有機(jī)物、懸浮顆粒物在膜上沉積,所以反滲透法需要對(duì)廢水進(jìn)行前處理[8].
3.3 吸附
由于吸附設(shè)計(jì)簡(jiǎn)單,操作方便,通常被用于去除廢水中不同類(lèi)型的有機(jī)物和無(wú)機(jī)物.吸附技術(shù)目前已成功應(yīng)用于去除氟離子、硝酸根離子、溴離子、高氯酸根離子.需要注意的是吸附劑的選擇對(duì)達(dá)到理想去除率非常重要.目前去除水中硝氮的吸附劑主要分以下幾類(lèi):碳基吸附劑、天然礦物吸附劑、農(nóng)業(yè)廢物類(lèi)吸附劑、工業(yè)廢物類(lèi)吸附劑、生物吸附劑等,見(jiàn)表2.

表2 去除硝氮的吸附劑
其中類(lèi)滑石類(lèi)吸附劑和改性殼聚糖對(duì)硝酸根的去除率相對(duì)于其它吸附劑最高,可以達(dá)到30~100 mg/g[13-15].農(nóng)業(yè)廢棄物經(jīng)過(guò)表面修飾后也能達(dá)到可觀的效果(如負(fù)載Zn的甘蔗渣、化學(xué)修飾的甜菜渣能達(dá)到30~60 mg/g)[16].一些工業(yè)廢棄物對(duì)硝氮吸附去除也有很大潛力,如赤泥(20~60 mg/g)[17].但在修飾這些材料時(shí),成本是必須考慮的問(wèn)題.吸附劑的選擇需要考慮硝氮初始濃度,其它競(jìng)爭(zhēng)離子及它們的濃度、吸附劑使用量?jī)?yōu)化,廢水pH調(diào)節(jié),操作與維護(hù)的便利性等問(wèn)題.選擇一種合適的去除硝氮吸附劑是一項(xiàng)復(fù)雜的過(guò)程,一種在實(shí)驗(yàn)室里表現(xiàn)出對(duì)硝氮高吸附去除率的吸附劑用于現(xiàn)場(chǎng)時(shí)可能受到別的因素如并存其它污染物的影響不再具有理想效果.所以篩選出一種合適的吸附技術(shù)是一個(gè)冗長(zhǎng)的過(guò)程.
3.4 化學(xué)還原
硝酸鹽也能通過(guò)化學(xué)途徑去除,即利用易被氧化的金屬或化合物將硝酸鹽還原為氨氮、氮氧化物或氮?dú)猓瑥亩_(dá)到脫氮的目的.化學(xué)還原硝酸鹽用到的還原劑分為活潑金屬(Al、Zn、Fe、Arndt合金、Devarda合金等),銨,硼氫化物,甲酸,肼和胲,氫氣,二價(jià)鐵,詳見(jiàn)表3[18].
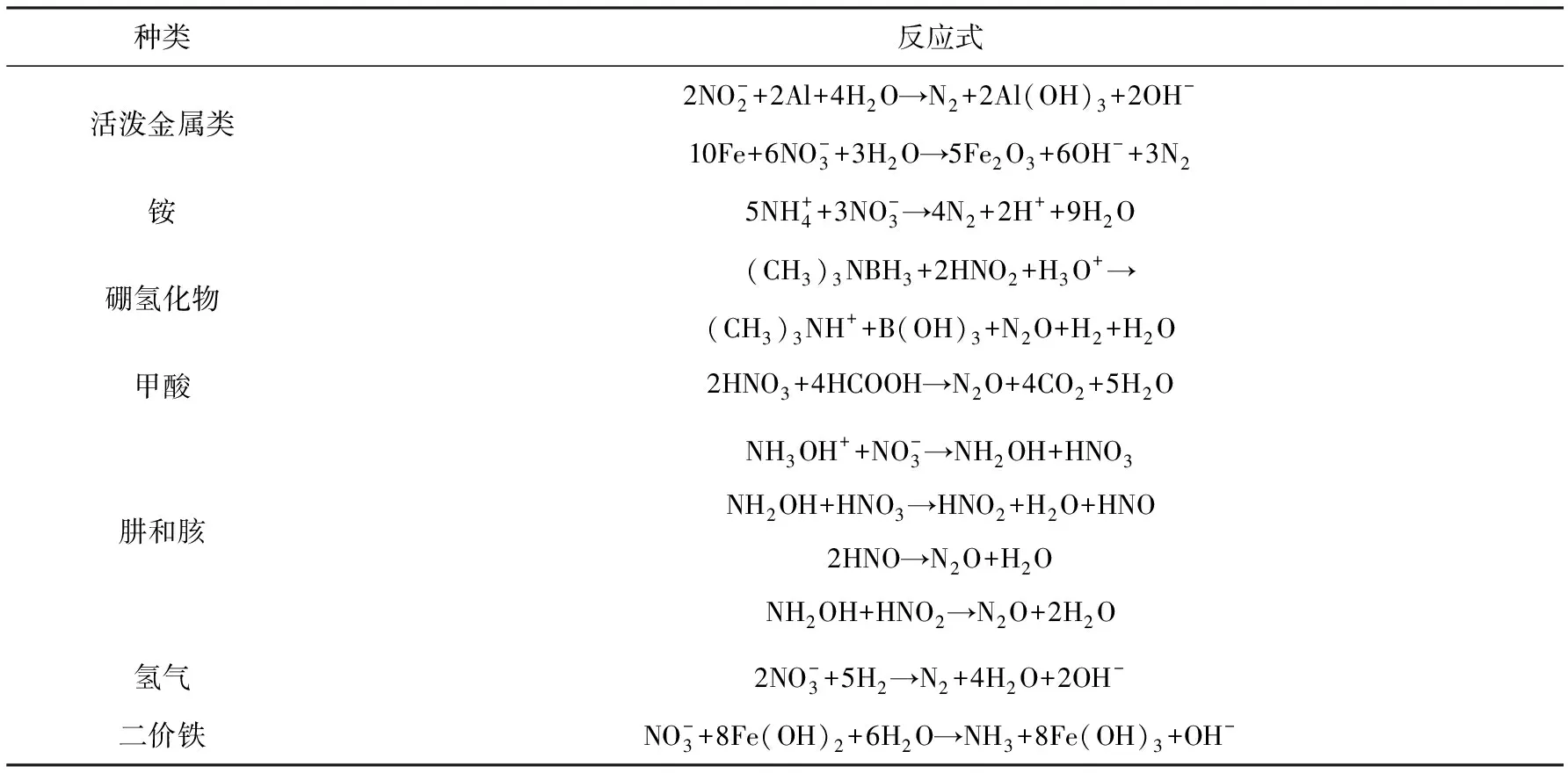
表3 去除硝氮的化學(xué)還原劑及反應(yīng)式
除了上述的還原劑還原廢水中的硝氮,通過(guò)能量的方式也能實(shí)現(xiàn)硝氮的還原.如電化學(xué)還原,通過(guò)原電池反應(yīng),使硝氮還原為一氧化氮.最新研究發(fā)現(xiàn)使用光能激發(fā)硝酸根或者促進(jìn)硝酸根與其它還原成分反應(yīng),實(shí)現(xiàn)硝氮的還原,見(jiàn)以下路徑:
用化學(xué)還原法去除水中硝氮時(shí),往往不能僅僅依靠一種還原方法,最好的途徑的聯(lián)合多種還原方法.如通過(guò)活潑金屬,能將硝氮還原為亞硝氮,之后可通過(guò)電化學(xué)還原將亞硝氮進(jìn)一步還原為氮?dú)饣虬?硼氫化物能與硝酸鹽反應(yīng)產(chǎn)生氨和氫氣,這時(shí)向其中加入Cu-Pd催化劑可使產(chǎn)生的氫氣進(jìn)一步還原硝酸鹽.
3.5 生物脫氮
生物脫氮按碳源的種類(lèi)可分為外加碳源(主要為甲醛)、內(nèi)源呼吸碳源(利用微生物自身的內(nèi)源呼吸以及其它微生物的水解產(chǎn)物為碳源)和廢水中固有碳源(廢水本身的BOD物質(zhì)為碳源)三種方式.當(dāng)廢水本身缺少或沒(méi)有BOD物質(zhì)時(shí),為了給反硝化反應(yīng)提供足夠的電子供體,則需外加部分或全部有機(jī)物.已經(jīng)證明,反硝化菌可以利用許多有機(jī)物作為碳源完成反硝化反應(yīng),但到目前為止,大多數(shù)研究主要集中于甲醇、乙醇、乙酸、葡萄糖等少數(shù)低碳有機(jī)物,其相應(yīng)的化學(xué)計(jì)量關(guān)系如下[6]:
7H2O+6OH-
9H2O+12OH-
6H2O+8OH-
18H2O+24OH-
由以上各式可以算出,反硝化菌每還原1 g硝氮,甲醇、乙醇、乙酸和葡萄糖的需要量分別為1.9、1.37、2.68和2.68 g.
細(xì)胞物質(zhì)作為有機(jī)碳源時(shí),微生物利用內(nèi)源呼吸進(jìn)行反硝化,而微生物自身隨著反硝化的進(jìn)行被消耗.化學(xué)計(jì)量關(guān)系為:
2N2+4OH-
每去除1 g硝氮需硝化1.61 g的細(xì)胞物質(zhì),同時(shí)在此過(guò)程還產(chǎn)生0.25 g銨態(tài)氮.
當(dāng)廢水中的BOD物質(zhì)作為反硝化過(guò)程中的有機(jī)碳源時(shí),硝氮起著與好氧氧化中分子氧完全相同的功能.在反硝化過(guò)程中,1 mol硝酸根接收5 mol的電子,即1 g硝氮相當(dāng)于2.86 g氧,每去除1 g硝氮,需消耗廢水中2.86 g BOD.
4 結(jié)論與展望
目前應(yīng)用于廢水中硝酸鹽去除的技術(shù)主要要離子交換技術(shù)、反滲透技術(shù)、吸附、化學(xué)還原修復(fù)和生物脫氮等技術(shù).其中生物脫氮具有高效低耗的特點(diǎn),但會(huì)導(dǎo)致水中含有細(xì)菌和殘留有機(jī)物,必須進(jìn)行后續(xù)處理;離子交換、反滲透和吸附屬于物理化學(xué)處理技術(shù),只是將硝酸鹽污染物進(jìn)行了濃縮或轉(zhuǎn)移,并沒(méi)有對(duì)其進(jìn)行徹底去除,同時(shí)產(chǎn)生高濃度再生廢液同樣需要處理;化學(xué)還原反硝化應(yīng)用負(fù)載型催化劑可將大部分硝酸鹽轉(zhuǎn)化為氮?dú)猓呋€原過(guò)程中需要以氫氣作為還原劑,而氫氣容易爆炸,不便于工程施用.因此,單獨(dú)靠一種方法去除廢水中的硝酸鹽往往會(huì)碰到各種難題,能結(jié)合處理需求和利用不同處理方法的特點(diǎn),揚(yáng)長(zhǎng)避短,才能發(fā)揮出這些除硝酸鹽方法的優(yōu)勢(shì).
國(guó)內(nèi)外對(duì)工業(yè)廢水硝態(tài)氮去除的研究積累了許多研究成果,許多技術(shù)已經(jīng)投入了實(shí)際應(yīng)用,但工業(yè)廢水硝態(tài)氮去除仍然是一項(xiàng)頗具挑戰(zhàn)性的工作.從成本角度看,投資和運(yùn)行費(fèi)用都還比較高,因此需要進(jìn)一步優(yōu)化現(xiàn)有的工藝和開(kāi)發(fā)新的工藝.從研究的角度看,許多研究針對(duì)某種硝態(tài)氮去除工藝、組合工藝,如物理處理和化學(xué)處理組合、物理處理和生物處理組合、化學(xué)處理和生物處理組合未受到足夠的重視.所以工業(yè)廢水中硝態(tài)氮去除仍然有許多工作需要投入.
[1] 徐芳香,陸雍森. 我國(guó)地下水中硝酸鹽污染防治及水源保護(hù)區(qū)劃分[J]. 污染防治技術(shù), 1999,12(1): 27-31.
[2] 馮紹元,鄭耀泉. 農(nóng)田氮素的轉(zhuǎn)化與損失及其對(duì)水環(huán)境的影響[J]. 農(nóng)業(yè)環(huán)境保護(hù), 1996, 15(6): 277-280.
[3] 張慶忠,陳欣,沈善敏. 農(nóng)田土壤硝酸鹽積累與淋失研究進(jìn)展[J]. 應(yīng)用生態(tài)學(xué)報(bào), 2002, 13(12): 233-238.
[4] 宋秀杰,丁庭華. 北京市地下水污染的現(xiàn)狀及對(duì)策[J]. 環(huán)境保護(hù), 1999(11): 44-47.
[5] 許國(guó)強(qiáng),曾光明,殷志偉,張劍峰. 氨氮廢水處理技術(shù)現(xiàn)狀及發(fā)展[J]. 湖南有色金屬, 2002, 2(4): 29-33.
[6] 張希衡, 廢水厭氧處理工程[M]. 北京: 中國(guó)環(huán)境科學(xué)出版社,1996.
[7] Amit Bhatnagara M S. A review of emerging adsorbents for nitrate removal from water[J]. Chemical Engineering Journal, 2011, 168: 493-504.
[8] Anoop Kapoor T V. Nitrateremoval from drinking water-review[J]. Journal of Environmental Engineering and Science, 1997,123: 371-380.
[9] Korngold E. Removal of nitrates from potable water by ion exchange[J]. Water Air Soil Pollution, 1973,2: 15-22.
[10] Hagen K, Holl W, Kretzschmar W. The CARIXIll process for removing nitrate, sulfate and hardness from water[J]. Aquatic Sciences, 1986, 5: 275-278.
[11] Holl W H, Kretzschmar W. Combined nitrate and hardness elimination by the CARIX ion exchange process[J]. Water Supply, 1988,6: 51-55.
[12] Wenli G, Wensheng H, HoB W H. Combined nitrate and hardness elimination from drinking water by the CARIX process[J]. Water SRT-Aqua, 1994, 43: 93-101.
[13] Chatterjee S, Lee D S, Lee M W,etal. Nitrate removal from aqueous solutions by cross-linked chitosan beads conditioned with sodium bisulfate[J]. Journal of Hazardous Materials, 2009, 166: 508-513.
[14] Chatterjee S, Woo S H. The removal of nitrate from aqueous solutions by chitosan hydrogel beads[J]. Journal of Hazardous Materials, 2009, 164: 1012-1018.
[15] Hosni K, Srasra E. Nitrate adsorption from aqueous solution by MII-Al-CO3layered double hydroxide[J]. Inorg. Mater, 2008, 44: 742-749.
[16] Orlando U S, Bases A V, Nishijima W,etal. A new procedure to produce lignocellulosic anion exchangers from agricultural waste materials[J]. Bioresource Technology, 2002, 83: 195-198.
[17] Cengeloglu Y,Tor A,Ersoz M,etal. Removal of nitrate from aqueous solution by using red mud[J]. Sep. Purif. Technol, 2006,51: 374-378.
[18] Fanning J C. The chemical reduction of nitrate in aqueous solution[J]. Coordination Chemistry Reviews, 2000, 199: 159-179.

