Fe3+對聚苯胺復合二氧化鈦光催化性能的影響
范文玉, 明 皓, 陳婉茹, 郝平平, 焦 陽
(1.沈陽化工大學 環境與安全工程學院, 遼寧 沈陽 110142; 2.沈陽市第十五中學, 遼寧 沈陽 110021)
TiO2因具有無毒、無害、無腐蝕性、可反復使用等特點而被廣泛應用到光催化降解有機污染物中.近年來的研究成果表明:TiO2光催化降解是一種具有廣泛應用前景的綠色環境治理技術[1].但納米TiO2光催化劑在水處理懸浮相光催化體系中存在著量子效率低、光催化性能差、吸附性差等缺點,嚴重制約著納米TiO2光催化劑的產業化和商業化[2].為了拓寬TiO2光催化材料的光譜響應范圍和提高光催化性能,人們通常采用貴金屬沉積、離子摻雜、半導體復合、表面光敏化和表面改性等方法[3].
在眾多的高分子聚合物中,聚苯胺(PANI)具有較高的電導率和良好的環境穩定性,且原料廉價易得,摻雜機制獨特,合成工藝簡便等,成為目前研究最多的一類導電高分子材料[4].而導電聚合物可以改性納米TiO2,提高其可見光利用率,亦引起了科研工作者的高度重視.
本實驗采用離子摻雜和半導體復合的方法[5],并通過水蒸氣-水解法和化學氧化聚合法分別制備了納米級TiO2粉體、不同摻雜比例的Fe3+-TiO2和PANI/Fe3+-TiO2復合材料[6].利用單因素實驗驗證了不同摻雜比例的Fe3+對TiO2和PANI/TiO2光催化活性的影響.結果表明:Fe3+的摻雜和聚苯胺的負載,均可以改進納米TiO2光催化劑的光催化性能.
目前紡織染料和其他商業染料已經成為近幾年環境修復的焦點[7],處理染料廢水的傳統方法在實際處理過程中存在處理不徹底、易造成二次污染、處理費用高等缺點,光催化作為一種處理廢水的新方法引起廣泛的重視[8].本實驗應用不同摻雜比例Fe3+改進的TiO2及PANI/TiO2粉體對KBF 染料模擬的染料廢水進行處理,并針對Fe3+對光催化劑的影響進行研究.
1 試驗部分
1.1 主要試劑和儀器
硝酸鐵,天津市福晨化學試劑廠;苯胺,天津市科密歐化學試劑有限公司,經二次減壓蒸餾;四氯化鈦,天津市蘇莊化學試劑廠,分析純;一定濃度的KBF 染料溶液.
D8 Advance X 射線衍射儀,德國布魯克公司;JSM-6360LV 高低真空掃描電子顯微鏡,日本電子株式會社;NEXUS 470紅外光譜儀,美國熱電公司;旋轉蒸發儀,上海亞榮生化儀器廠.
1.2 TiO2 粉體和Fe3+-TiO2 粉體的制備
將一定體積的TiCl4緩慢倒入無水乙醇中并快速攪拌,設置空氣流量0.6 L/min,加熱攪拌反應4 h,冷凝回流后,用無水乙醇反復洗滌、離心至上清液中無Cl-1.取出樣品,烘干,研磨,馬弗爐400 ℃ 焙燒,即得到白色納米TiO2粉體.
加熱攪拌反應前,在TiCl4與無水乙醇的淡綠色混合溶液中,按不同的Fe3+與四氯化鈦摩爾比例加入一定量的硝酸鐵,其他制備方法相同,即可得到Fe3+-TiO2系列粉體.
1.3 PANI/TiO2 和PANI/Fe3+-TiO2 粉體的制備
將一定量的苯胺、酸溶液和已制得的TiO2粉體或Fe3+-TiO2系列粉體混合均勻,5 ℃冰浴條件下充分攪拌.將一定質量的過硫酸銨溶于相同酸溶液中,對上述體系緩慢滴定20 min,此時過硫酸銨作為氧化劑,在酸性環境下使苯胺發生聚合反應.滴定結束后繼續攪拌4 h,使聚合反應均勻徹底.反應結束后,將樣品放置陰涼處12 h,使樣品形成凝膠狀態.取出樣品依次用酸溶液和蒸餾水洗滌,離心,烘干,并研磨到無大顆粒,即得到一系列PANI/Fe3+-TiO2粉體.
1.4 光催化降解實驗
在紫外光照射下,將一定濃度的KBF 染料溶液置于光催化降解裝置中,加入一定量的光催化劑樣品并快速攪拌,使粉體與染料溶液充分接觸.每隔一定時間取一定量的染料溶液經離心后測其吸光度.
2 結果與討論
2.1 光催化效果分析
光催化劑在紫外光條件下對染料廢水的吸附降解效果可以宏觀地反應出光催化劑的光催化性能.圖1、圖2分別為紫外光照射下不同摻雜比例(Fe3+與四氯化鈦的摩爾比分別為0.5 %、1 %、3 %、5 %,對應的Fe3+-TiO2、PANI Fe3+-TiO2粉體表示為0.5 %-Fe3+-TiO2、1 %-Fe3+-TiO2、3 %-Fe3+-TiO2、5 %-Fe3+-TiO2和0.5 %-PANI Fe3+-TiO2、1 %-PANI Fe3+-TiO2、3 %-PANI Fe3+-TiO2、5 %-PANI Fe3+-TiO2)的Fe3+-TiO2和PANI/Fe3+-TiO2對KBF 染料降解的ρ-t對比圖,可以看出隨時間變化,KBF 染料溶液質量濃度呈明顯下降趨勢.
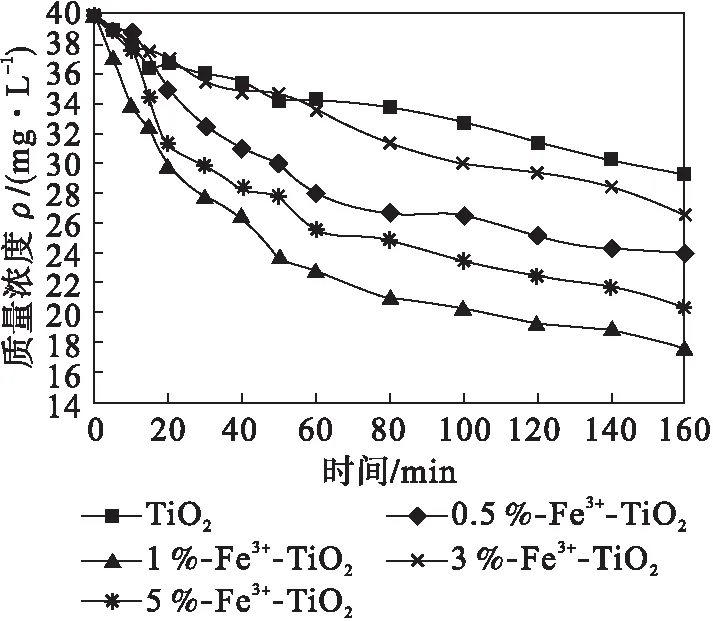
圖1 Fe3+-TiO2 系列粉體對KBF 染料的降解
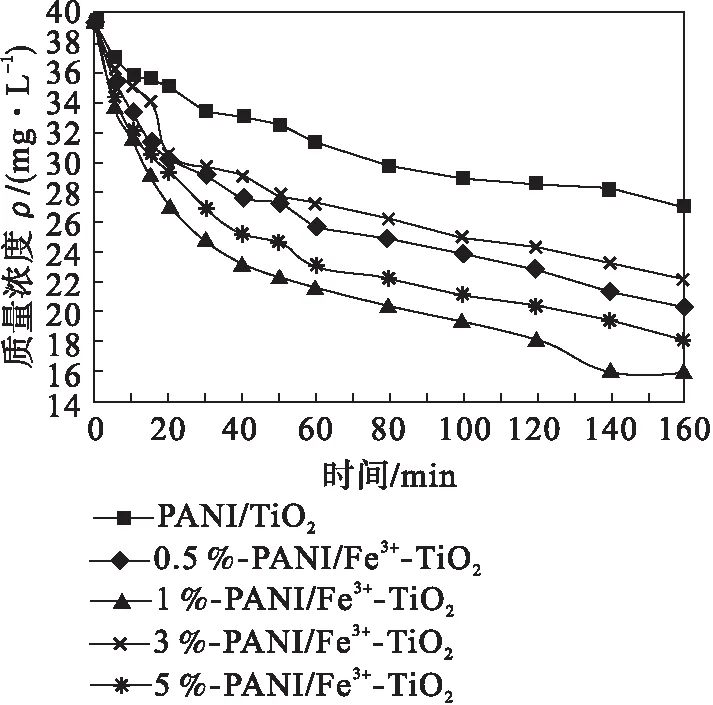
圖2 PANI/Fe3+-TiO2 系列粉體對KBF 染料的降解
采用一級方程擬合,通過ln(ρ/ρ0)與時間t的關系(其中ρ0為KBF染料的初始質量濃度,ρ為不同降解時間測得的KBF染料質量濃度,設C=ρ/ρ0),可得到不同光催化劑的光降解速率常數(見表1).
通過結果分析可知:單一TiO2粉體的光催化效果并不理想,聚苯胺的負載對光催化劑的性能有一定提高,Fe3+的摻雜使TiO2粉體和PANI/TiO2粉體的性能均有較大的提升.當Fe3+與四氯化鈦摩爾比為1 % 時,TiO2粉體和PANI/TiO2粉體表現出較好的光催化性能,其中光催化效果最好的是1 %-PANI/Fe3+-TiO2.說明Fe3+的摻雜和聚苯胺的負載,改善了TiO2粉體的光催化降解性能,提高了光催化活性.
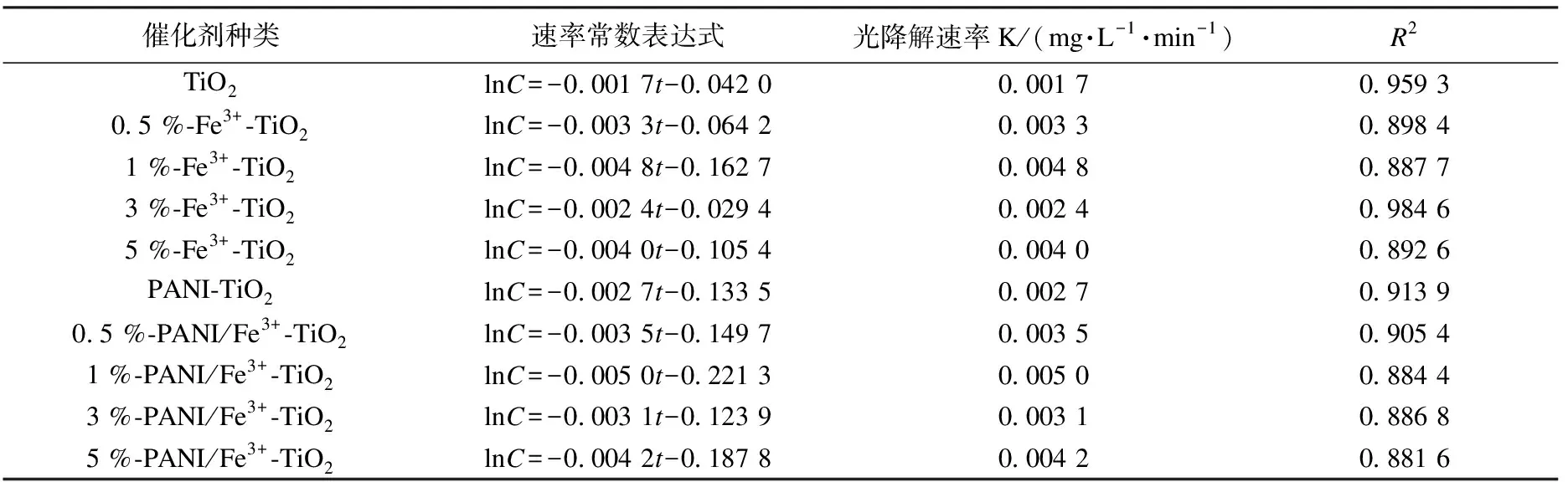
表1 不同光催化劑對KBF染料廢水的光降解速率
2.2 XRD 分析
同一種類型的光催化劑可能因為晶型不同而具有不同的催化性能[9].圖3為光催化劑的XRD 譜圖.PANI/TiO2的衍射角與TiO2的特征衍射峰值相差不大,1 %-PANI/Fe3+-TiO2的峰值較其他樣品有所增加,但譜圖樣式趨勢幾乎相同,衍射峰尖銳明顯,沒有出現PANI 的衍射峰.說明在Fe3+與PANI共同作用于TiO2時,樣品具有更好的結晶度和吸附力.合成過程中,TiO2的晶型并沒有改變,氧化劑過硫酸銨使苯胺在TiO2的顆粒表面發生聚合,表面效應會阻礙PANI 的結晶,但并沒有影響到TiO2的晶型結構.在現有水平下,只有少量金紅石產生,產生的晶型基本上都是銳鈦礦型[10].

圖3 光催化劑的XRD 譜圖
2.3 SEM 分析
圖4依次為TiO2粉體、1 %-Fe3+-TiO2、PANI/TiO2和1 %-PANI/Fe3+-TiO2的SEM形貌.從圖4中可以看出:光催化劑的粒徑可以達到納米級,摻雜PANI前的表觀形貌是不太規則的堆積狀,負載了PANI之后,粉體的表面形成大量微孔,在Fe3+和PANI 共同存在時,可以看出粉體呈更明顯的蜂窩狀分布.微孔的存在使光催化劑更容易與水溶液接觸,產生更多的表面羥基和羥基自由基,提高TiO2的光催化活性.另外,按不同的Fe3+與四氯化鈦摩爾比例制備的粉體,光催化劑的形貌亦出現很大的差別,查閱相關文獻可知:這可能與負載前驅體和負載機理不同有關[11].但聚合反應產生的大量微孔間接拓寬了TiO2的光譜響應范圍,進而提高了光量子效率.


圖4 光催化劑的SEM 照片
2.4 比表面積分析
通常粒子的粒徑越小,單位質量的粒子數越多,相應比表面積越大.比表面積是決定光催化反應基質吸附量的重要因素.當催化劑表面的活性中心密度一定時,表面積越大則活性越高.但有時具有較大的比表面積也會存在更多的載流子復合中心,導致光催化活性降低[12].
表2為TiO2、0.5 %-Fe3+-TiO2、1 %-Fe3+-TiO2、3 %-Fe3+-TiO2、5 %-Fe3+-TiO2粉體的比表面積對比.通過數據可以看出:1 %-Fe3+-TiO2和5 %-Fe3+-TiO2的多點BET比表面積明顯較TiO2粉體減小,而0.5 %-Fe3+-TiO2和3 %-Fe3+-TiO2的比表面積較TiO2粉體略有增大.實際的降解中,Fe3+的摻雜增加了光催化劑的光催化性能,這可能是因為Fe3+的摻雜可以將電子迅速轉移,降低TiO2光照產生的電子-空穴的幾率,改變了粒子的大小,提高了材料的量子尺寸,同時Fe3+和TiO2粒子間有較強的相互作用,可能增加對太陽光的利用效率,進而提高了光催化劑的光催化性能[13].
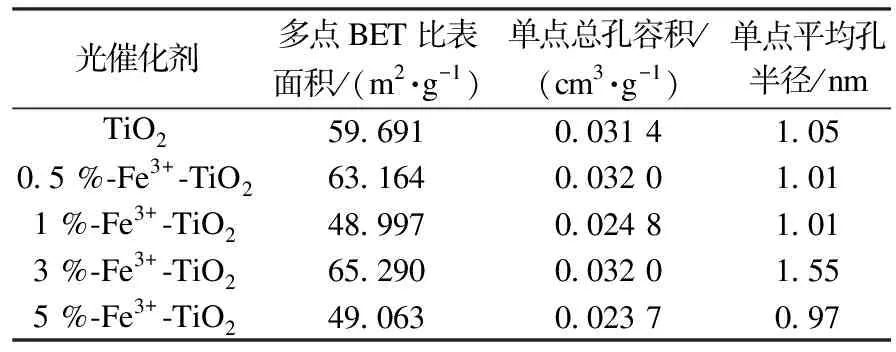
表2 光催化劑的比表面積
2.5 紅外光譜分析
由圖5傅里葉紅外光譜圖可知:在3 398 cm-1處的吸收峰對應于N—H 伸縮振動,其峰值很小,分子內的N—H 鍵數量不多.1 400~1 600 cm-1處的吸收峰來自于苯環的特征峰,1 598 cm-1處的吸收峰為醌式結構N==Q==N,1 386 cm-1處的吸收峰為苯式結構N—B—N,這兩個吸收峰的強度比可以反映復合物的氧化程度,表征苯式結構的峰不明顯,說明摻雜Fe3+后分子鏈的氧化程度并不高[14].在1 350 cm-1附近有弱峰,可能為Ti—OH 的特征吸收峰.TiO2的本征峰不容易看到.1 000 cm-1以下的吸收可以看作是 Ti—O 的lattice 吸收.
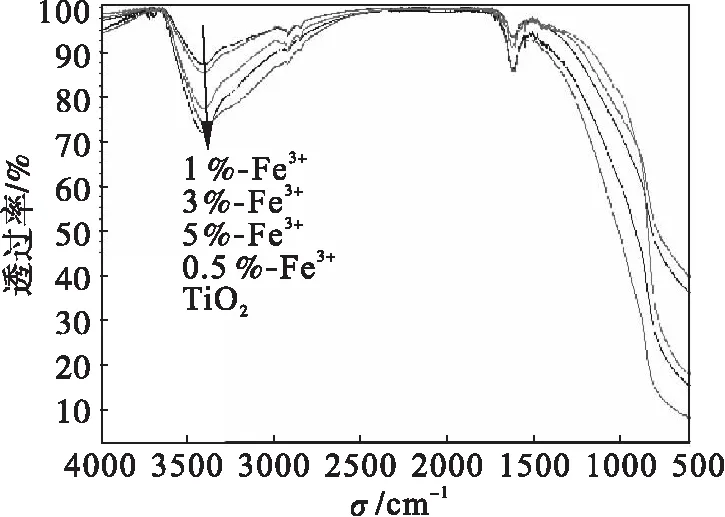
圖5 不同Fe3+濃度的紅外光譜
3 結 論
Fe3+的摻雜可以將電子迅速轉移,降低TiO2光照產生的電子-空穴的幾率,改變了粒子的大小,提高了材料的量子尺寸,進而改善了光催化劑的光催化性能;
通過光催化降解KBF 染料模擬的染料廢水實驗結果可知:其他單因素相同時,當Fe3+與四氯化鈦摩爾比為1 % 時,TiO2粉體和PANI/TiO2粉體表現出較好的光催化性能,其中光催化效果最好的是1 %-PANI/Fe3+-TiO2;
Fe3+的摻雜和聚苯胺的負載對納米TiO2光催化劑的改性,顯著改善了納米TiO2光催化劑的光催化性能,可有效降解KBF 染料.
參考文獻:
[1] 葉國梁.二氧化鈦的制備、表征及光催化降解甲醛的活性研究[D].福建:廈門大學,2009:6.
[2] 韓忠霄,殷蓉,李景印,等.聚苯胺改性負載型納米二氧化鈦的研究[J].無機鹽工業,2007,39(12):16-19.
[3] 李煒罡,霍冀川,劉樹信,等.負載型TiO2光催化劑研究進展[J].陶瓷學報,2004,25(2):133-138.
[4] 王彥宗,沈明歡,劉振營,等.聚苯胺-二氧化錫納米復合材料合成及表征[J].化工新型材料,2007,35(1):46-49.
[5] 馮光建,劉素文,修志亮,等.可見光響應型TiO2光催化劑的機理研究進展[J].稀有金屬材料工程,2009,38(1):185-188.
[6] Bessekhouad Yassine,Robert Didier,Jean Victor Weber.Synthesis of Photocatalytic TiO2Nanoparticles Optimization of the Preparation Conditions[J].Joumal of Photochemistry and Photobiology A:Chemistry,2003,157(1):47-53.
[7] Ganesh R,Boardman G D,Mochelson D.Fate of Azo Dyes in Sludges[J].Water Research,1994,28(6):1367-1376.
[8] 李俊妮.納米TiO2光催化在廢水處理中的應用[J].化工中間體,2012(2):48-53.
[9] 寇生中,胡聰麗.納米光催化劑TiO2/Fe3O4的制備及表征[J].應用化工,2008,37(1):67-70.
[10] 李凡修,陸曉華,梅平.金屬離子摻雜對納米TiO2晶型轉變影響作用機制的研究進展[J].材料導報,2006,20(9):13-17.
[11] 朱新鋒,楊家寬,肖波,等.負載型納米二氧化鈦光催化劑制備及其光催化性能研究[J].材料科學與工程學報,2004,22(6):863-866.
[12] 沈偉韌,趙文寬,賀飛,等.TiO2光催化反應及其在廢水處理中的應用[J].化學進展,1998,10(4):349-361.
[13] 于佳.PANI-TiO2復合方法的探索及光電性能研究[D].哈爾濱:黑龍江大學,2007.
[14] 劉秀琴,張云艷,常勇剛.孔介SiO2表面的氨基修飾及吸附性能研究[J].化學世界,2009(2):70-73.

