內鏡下治療消化道早癌及癌前病變效果
陳祝勇
(泰州市人民醫院消化內科,江蘇 泰州 225300)
醫學技術不斷發展,使得微創手術治療在醫學中的應用逐漸廣泛,并且取得的效果越來越理想,成為當前比較滿意治療方式[1]。如內鏡下黏膜剝脫術(endoscopic mucosal stripping,ESD)與內鏡下黏膜切除術(endoscopic mucosal resection,EMR),他們在國外的應用不僅十分普遍,而且技術十分成熟,在我國大部分醫院中也有所涉及,尤其是他們在消化道早期腫瘤的治療中有十分重要的地位[2]。總的來說,ESD治療技術是由EMR治療技術發展而來,屬于治療早期消化道腫瘤比較安全與有效的一種新技術,具有切除范圍大、方便病理學評估等優勢[3]。為了進一步分析內鏡下治療消化道早癌及癌前病變的方式及效果,本研究對收治的25例消化道癌變患者采用EMR與ESD進行治療研究,現報道如下。
1 資料與方法
1.1一般資料 選取泰州市人民醫院消化內科2011年2月至2013年2月收治的25例消化道癌變患者為研究對象,全部經我院內鏡中心治療,男16例,女9例;年齡44~84(58.9±4.7)歲;病變性質包括胃早癌、直腸側向發育性腫瘤、胃息肉及結腸息肉;病變大小及部位分布詳見表1。所有患者在術前均進行腹部超聲掃查,顯示均無病灶轉移,而對早癌患者進行超聲內鏡檢查,顯示病變部位全部在黏膜層,并未侵入肌層。
1.2方法 本研究采用的內鏡為奧林巴斯CF-Q260AI,同時還涉及的器材有注射針、鈦夾、熱活檢鉗、鉤刀(HOOK刀)、圈套管、末端絕緣手術刀(IT刀)、透明帽、愛博(ERBE)工作站等[4]。
1.2.1ESD治療 病變部位利用靛胭脂進行染色,染色之后確定病變部位的邊界,并用氬氣在病灶的邊界處進行標記;將1∶10 000的腎上腺素靛胭脂生理鹽水利用注射針在黏膜下進行多點注射,使病變可以充分抬舉,用HOOK刀順著病灶邊緣的標記外側將黏膜切開,并用IT刀將黏膜下層剝離,在剝離時應進行多次黏膜注射,這樣可以盡量將病變完整剝除,若有部分病灶較大則利用圈套器進行分片切除;在整個治療過程中,應做好止血處理,一般選擇氬氣刀或熱活檢鉗進行止血與處理創面。
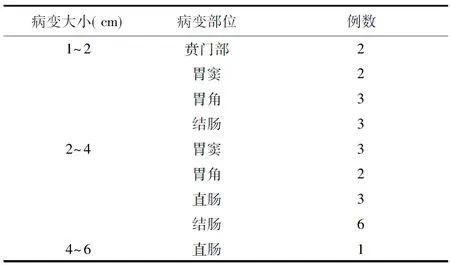
表1 25例消化道癌變患者病變大小及部位分布情況
1.2.2EMR治療 針對長蒂息肉,采取1∶10 000腎上腺素靛胭脂生理鹽水進行注射,完畢后將圈套盡量往管腔側靠近并行息肉切除,創面應采用金屬夾夾閉;部分蒂較粗的息肉則應以金屬夾將其基底夾閉。
1.3術后處理 所有患者術中切除病灶取出后皆保存待檢,送到相關部門進行病理診斷,對癌變類型進行判斷與分析。此外,術后對所有患者進行6~12個月隨訪,對手術部位的情況進行觀察分析。
2 結 果
2.1手術情況 25例患者病變全部被切除,切除率為100%,其中采用EMR切除病灶總計10例、采用ESD分片切除3例、采用ESD完整切除病灶12例。EMR手術時間33~56(40.3±4.8) min,ESD手術時間47~150(80.3±9.1) min。
2.2術后病理診斷情況 術后病理結果顯示:4例胃息肉,5例胃早癌,6例直腸側向發育性腫瘤,10例結腸息肉(表2)。
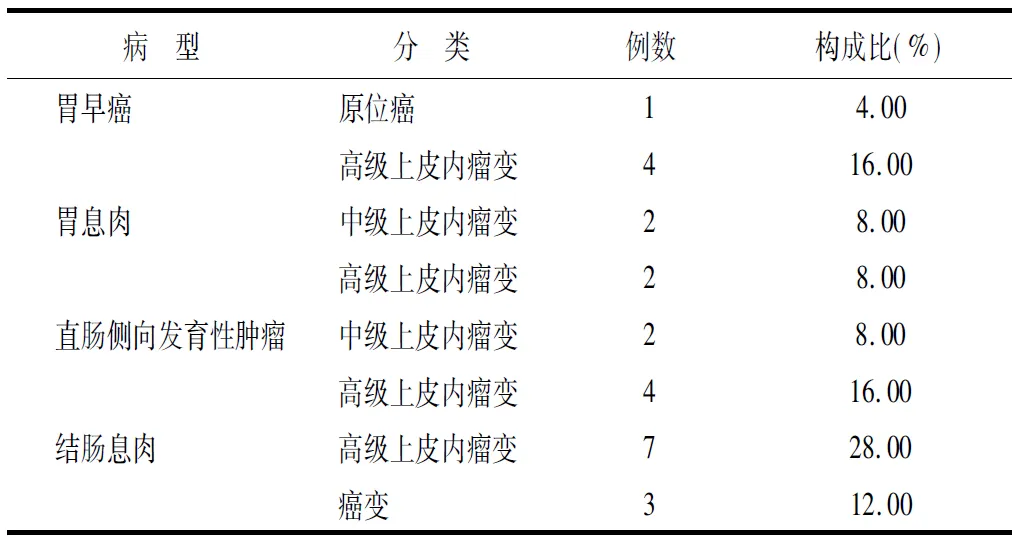
表2 25例消化道癌變患者術后病理診斷情況
2.3治療結果 25例患者經過EMR與ESD治療后,一次切除率為96.00%(24/25),出血率為12.00%(3/25),穿孔率為8.00%(2/25),出血患者與穿孔患者給予積極的處理皆效果良好。25例患者均進行6~12個月隨訪,隨訪復發率為0。在ESD與EMR治療中均出現不同程度的出血,但采取熱活檢鉗與氬氣刀及金屬夾進行止血后,成功。術后,EMR治療患者胃部病變并未出現遲發性出血,但1例直腸側病變患者發生遲發性出血,采取冰鹽水去甲腎上腺素、金屬夾、氬氣刀等處理,達到止血效果。ESD術后出血2例,對癥處理后1 d內得到緩解。所有患者術后均采用禁食與抗炎及止血補液等治療,胃部病變患者加用制酸藥處理,患者均取得比較良好的效果。此外,2例患者穿孔嚴重,采取金屬夾一般都能夾閉,術后結合內科處理,取得良好的效果。
3 討 論
就當前來看,消化內鏡下微創手術治療在消化道良性病變、消化道早期腫瘤及癌前病變等方面都有十分廣泛的應用。研究發現,內鏡下治療早期腫瘤取得的效果較外科根治術治療沒有顯著性差異,也就是能取得相似的治療效果,比較滿意[5]。如上海長海醫院[6]將其用在早期腫瘤患者中,一次性整塊切除率高達97.7%(42/43),而組織學的完全治愈率高達95.3%(41/43)。隨著近年來ESD設備與技術不斷發展與進步,相關的適應證也不斷放寬,甚至在一些黏膜下層與固有肌層病變也能利用該類手術行黏膜下剔除術,而且效果比較明顯。
就以往臨床ESD治療情況來看,術后并發癥主要為穿孔與出血(嚴重并發癥比較少見),其中出血相較于穿孔又更為常見,大部分在術中或者術后24 h發生,而且出血對于ESD治療是無法避免的,只是技術的好壞則取決于出血的有效控制[7]。因此,應嚴格進行出血的預防與控制,其對策應從術前準備著手,如抗凝出血、及時處理術中出血、術后出血預防的內鏡處理等,同時做好術中出血應對,嚴格按照實際情況及相關規范操作準備及應用不同的器械。為了減少剝離過程中的出血,應做好以下幾點:黏膜下小血管,采用勾刀頭進行直接電凝;較粗黏膜下層血管,采用熱活檢鉗對血管進行鉗夾之后,進行外拉,當熱活檢鉗完全脫離管壁之后才能采用電凝止血。在實際操作中,若上述各種方法止血效果不佳或者不成功者,則用金屬夾將出血點夾閉,但這會對后面操作產生一定的影響,因此應慎重使用。整個病變被完整切除后,一般采用氬等離子電凝技術對創面小血管進行電凝處理(必要時采用金屬夾)。從穿孔來看,ESD術中或術后出現的穿孔都比較小,一般采用金屬夾即可夾閉,之后結合內科治療,就可以避免外科手術治療,從而減少不必要的痛苦。因此,ESD治療不僅要盡量減少穿孔的發生,而且要盡量減少穿孔引發的外科手術治療。
本研究采用ESD治療的患者術中皆有不同程度的出血,但術后并無嚴重并發癥發生,僅有2例出血,經氬氣刀、熱活檢鉗及金屬夾等止血方式皆能成功。而在EMR治療患者中,術中出血不太明顯,胃部病變患者術后未發生遲發性出血,而直腸側向發育性腫瘤患者中則出現遲發性出血,均為鮮血便,腸鏡下可見創面出現活動性出血,采用氬氣刀、金屬夾等均可止血。本研究患者在術后皆進行抗炎、禁食及止血補液等治療,而且胃部患者也給予制酸藥物治療,個別結腸息肉可能癌變的患者采取外科腹腔鏡下追加手術治療,取得了良好的效果。
總之,對于消化道早癌及癌前病變患者,采用ESD與EMR治療能取得良好的效果,除安全有效外,復發率也較低、患者痛苦少且恢復快,同時對于病理評估也有積極的意義。
[1] 徐威,姚平,徐美東,等.內鏡下治療消化道早癌及癌前病變20例臨床分析[J].臨床和實驗醫學雜志,2011,10(2):129-130.
[2] 賈國法,單紅,吳麗穎,等.內鏡黏膜下剝離術治療消化道早期癌及癌前病變[J].中華消化雜志,2012,32(6):409-411.
[3] 令狐恩強,卜保國,盧忠生,等.內鏡下治療伴發靜脈曲張的上消化道早癌患者的出血風險[J/CD].中華腔鏡外科雜志:電子版,2011,4(5):349-351.
[4] 盧忠生,令狐恩強,黃啟陽,等.內鏡黏膜下剝離術治療消化道早期癌及癌前病變[J].中華消化內鏡雜志,2008,25(11):578-583.
[5] 孫曦,張修禮,盧忠生,等.消化道早癌及癌前病變內鏡下切除與外科手術切除的效價對比研究[J].中華消化內鏡雜志,2013,30(1):15-17.
[6] 施新崗,李兆申,徐丹鳳,等.內鏡黏膜下剝離術在早期胃癌治療中的應用[J].中華消化雜志,2009,29(10):670-673.
[7] 王海洋,袁志萍,施瑞華,等.內鏡黏膜下剝離術治療早期胃癌及癌前病變的臨床評價[J].中華消化內鏡雜志,2012,29(3):169-170.

