高效液相色譜法測定養血生發膠囊中羌活醇和異歐前胡素的含量*
劉慶煥,傅 予,王文彤
(天津市醫藥科學研究所,天津 300020)
高效液相色譜法測定養血生發膠囊中羌活醇和異歐前胡素的含量*
劉慶煥,傅 予,王文彤
(天津市醫藥科學研究所,天津 300020)
[目的]建立高效液相色譜法(HPLC)測定養血生發膠囊中羌活醇和異歐前胡素的含量測定方法。[方法]色譜柱:Agilent Zorbax Eclipse XDB-C18(250 mm×4.6 mm,5 μm),流動相:乙腈-0.1%磷酸水溶液(45∶55),流速:1 mL/min,檢測波長:310 nm,柱溫:25℃。[結果]羌活醇和異歐前胡素分別在0.204~1.224 μg(r=0.999 7)和0.103~0.616 μg(r= 0.999 8)線性關系良好,平均回收率分別為99.24%(RSD=0.74%)和99.86%(RSD=1.36%)。[結論]該方法簡便易行、重復性好,可用于養血生發膠囊中羌活醇和異歐前胡素的質量控制。
養血生發膠囊;羌活醇;異歐前胡素;高效液相色譜法
養血生發膠囊收載于《中國藥典》2010年版一部,由制何首烏、熟地黃、羌活、當歸等9味中藥組成,具有養血補腎、祛風生發的功效[1]。藥理研究表明,養血生發膠囊對碳酸鉈引起的脫毛與體質量減輕具有明顯的保護作用[2],并能增加C57BL/6脫發模型小鼠毛囊組織中血管內皮生長因子(VEGF)表達、毛囊血管數及毛囊數,促進毛發生長[3]。目前《中國藥典》標準中僅對君藥何首烏2,3,5,4′-四羥基二苯乙烯-2-O-β-D-葡萄糖進行了含量測定。為了更加全面地評價養血生發膠囊的質量,本研究建立了養血生發膠囊中羌活醇和異歐前胡素的含量測定方法,為全面控制其質量提供參考依據。
1 儀器與試藥
儀器與色譜柱:島津LC-10ATvp高效液相色譜儀,二極管陣列檢測器。
試劑:甲醇(分析純,天津市化學試劑批發公司),磷酸(分析純,天津市化學試劑批發公司),乙腈(色譜純,迪馬科技有限公司),水為娃哈哈純凈水。
對照品:羌活醇(中國藥品生物制品檢定所購置,批號:111820-201001),異歐前胡素(中國藥品生物制品檢定所購置,批號:110827-200407)。
試驗藥品:養血生發膠囊(藥廠中試樣品,批號:J01094,J01095,J01096)。
2 方法與結果
2.1 色譜條件 色譜柱:Agilent ZORBAX Eclipse XDB-C18(250 mm×4.6 mm,5 μm),流動相:乙腈-0.1%磷酸水溶液(45∶55),流速:1 mL/min,檢測波長:310 nm,柱溫:25℃。理論塔板數以羌活醇計應不低于4 500,以異歐前胡素計應不低于7 000。對照品、供試品及陰性溶液色譜見圖1~3。
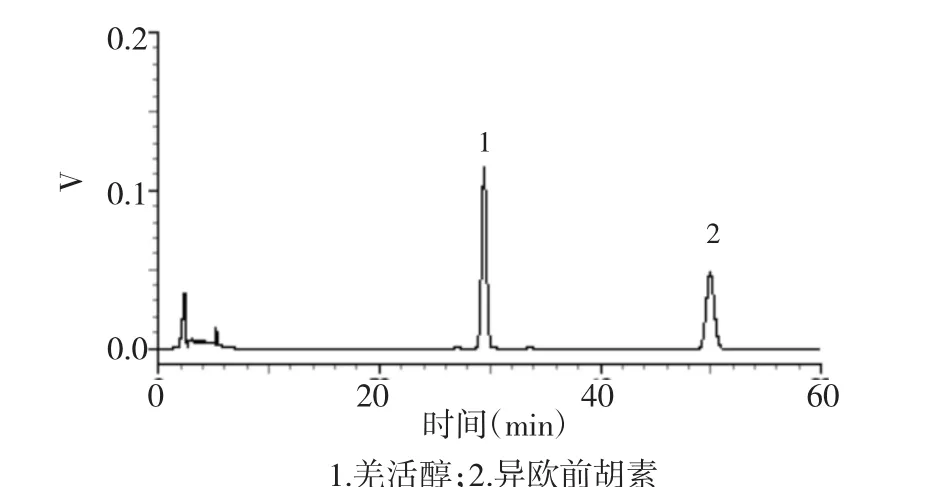
圖1 對照品溶液色譜圖Fig.1 HPLC chromatogram of standard substance
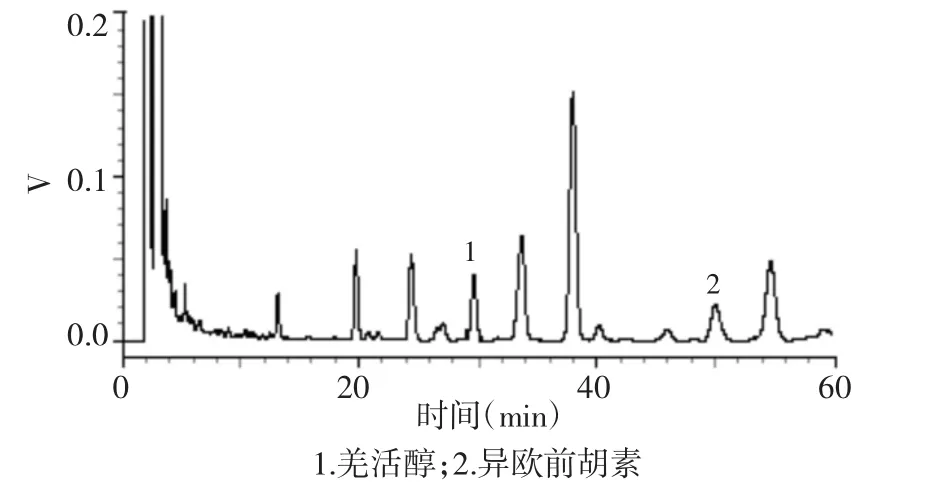
圖2 供試品溶液色譜圖Fig.2 HPLC chromatogram of sample
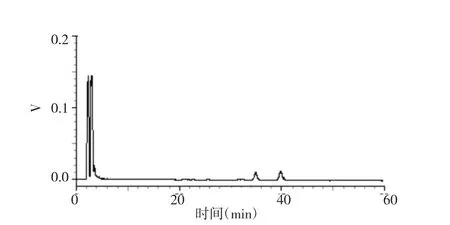
圖3 陰性溶液色譜圖Fig.3 HPLC chromatogram of negative control
2.2 溶液的制備
2.2.1 混合對照品溶液的制備 取羌活醇與異歐前胡素對照品適量,精密稱定,加甲醇制成每1 mL含羌活醇60 μg、異歐前胡素30 μg的混合溶液,即得。
2.2.2 供試品溶液的制備 取本品約10 g,研細,精密稱定,置具塞錐形瓶中,精密加入甲醇100 mL,稱定質量,超聲處理(250 W,40 kHz)30 min,放冷,再稱定質量,用甲醇補足減失的質量,搖勻,濾過,取續濾液,過0.45 μm微孔濾膜,即得。
2.2.3 陰性樣品溶液的制備 按處方配比,取除羌活外其他藥材,按2010版《中國藥典》[制法]項下的工藝制成膠囊劑[1],再按“2.2.2”供試品溶液制備方法,制得陰性樣品溶液。
2.3 線性關系考察 取羌活醇和異歐前胡素對照品適量,精密稱定,加甲醇制成每1mL含羌活醇10.2、20.4、30.6、40.8、51.0、61.2 μg的系列溶液。加甲醇制成每 1 mL含異歐前胡素為 5.13、10.26、15.39、20.52、24.65、30.78 μg的系列溶液,分別精密吸取上述溶液各20 μL,注入液相色譜儀,按“2.1”色譜條件分析,分別測定各自峰面積,以對照品進樣量(μg)為橫坐標,峰面積值為縱坐標,進行線性回歸,得羌活醇和異歐前胡素回歸方程分別為Y^=3×106X-53 562(r=0.999 7),Y^=4×106X-61 058(r=0.999 8)。結果表明,羌活醇和異歐前胡素分別在0.204~1.224μg、0.103~0.616 μg范圍內呈良好線性關系。
2.4 精密度實驗 精密吸取對照品溶液20 μL,按“2.1”色譜條件分析,連續進樣6次,對照品中羌活醇峰面積值的RSD為0.86%,異歐前胡素峰面積值的RSD為0.82%。
2.5 重復性實驗 取同一批樣品(批號J01094),研細,取6份,按照“2.2.2”供試品溶液制備操作,按“2.1”色譜條件分析,測定,計算含量。樣品中羌活醇和異歐前胡素含量的RSD分別為0.41%和0.96%。
2.6 穩定性實驗 取同一批樣品(批號J01094),研細,取1份,按照“2.2.2”供試品溶液制備操作,按“2.1”色譜條件分析,精密吸取供試品溶液20 μL,分別于0、2、4、6、9、24 h進樣,測定羌活醇的RSD為1.22%,異歐前胡素的RSD為1.90%,結果表明,供試品溶液在24 h內基本穩定。
2.7 加樣回收率實驗 取同一批樣品(批號J01094),研細,取9份,每份約5 g,精密稱定,分別按照5 g樣品中所含被測成分的50%、100%、150%精密加入羌活醇與異歐前胡素對照品溶液50 mL,每一個水平平行3份,按照“2.2.2”供試品溶液制備操作,制得供試品溶液,按“2.1”色譜條件分析,計算回收率,結果平均回收率分別為99.24%和99.86%,RSD分別為0.74%和1.36%,見表1和表2。
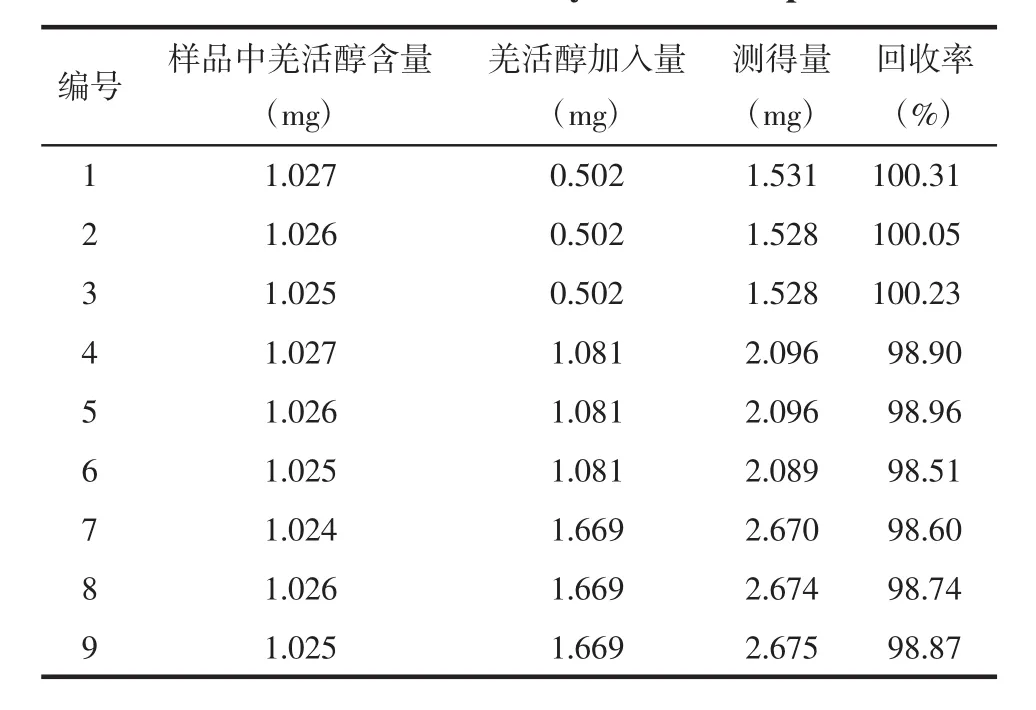
表1 羌活醇回收率實驗結果Tab.1 Results of recovery tests of notopterol
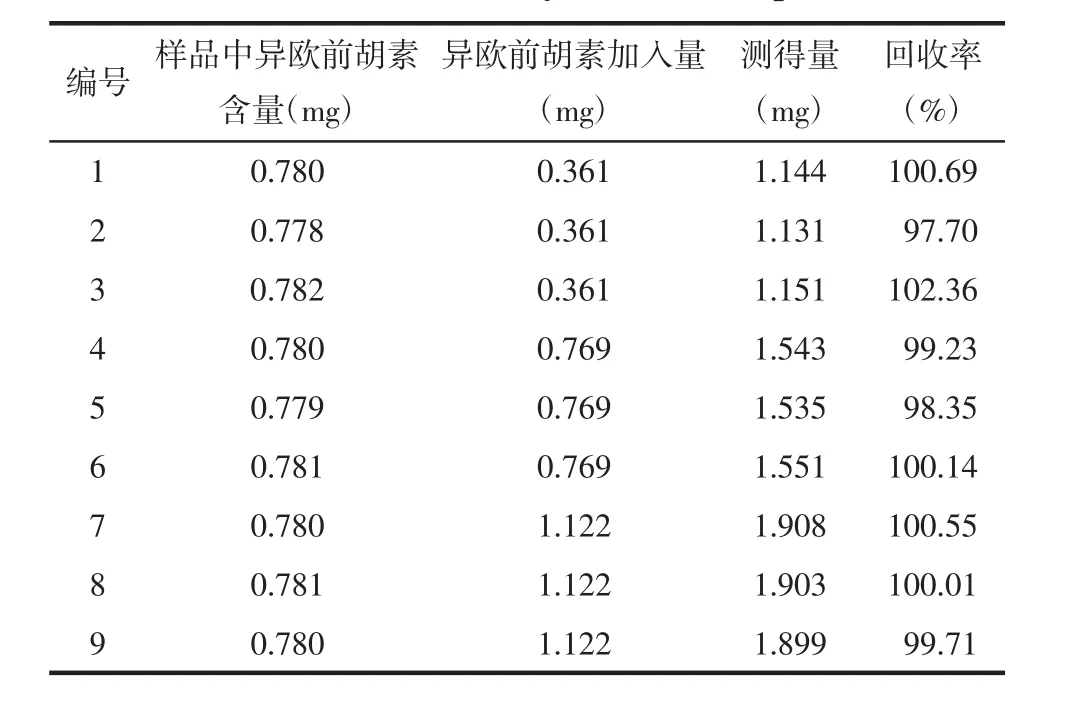
表2 異歐前胡素回收率實驗結果Tab.2 Results of recovery tests of isoimperatorin
2.8 樣品測定 取3份不同批號制劑,按照“2.2.2”供試品溶液制備操作,按“2.1”色譜條件分析,測定,計算樣品中羌活醇與異歐前胡素含量,結果見表3。
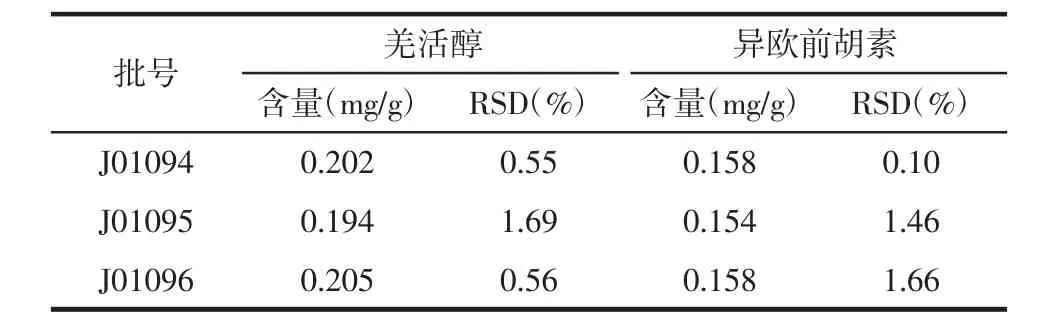
表3 養血生發膠囊中羌活醇與異歐前胡素的含量測定結果(n=3)Tab.3 Results of content determination of notopterol and isoimperatorin(n=3)
3 討論
3.1 流動相的選擇 參照《中國藥典》2010年版一部羌活項下含量測定方法,考察了不同組成的流動相(乙腈-水、乙腈-磷酸水和乙腈-甲酸水)系統。結果發現兩種酸水系統均能改善峰型,而乙腈-磷酸水系統較乙腈-醋酸水系統分離效果更好。
3.2 提取方法的優化 為使被測化合物提取效果最佳,考察了不同提取方法(超聲、回流)、不同提取溶劑(甲醇、乙醇)和不同提取時間(15、30、45、60 min)等因素對提取效率的影響,最終確定甲醇超聲30min提取效果最好。
羌活含有揮發油、香豆素、有機酸等活性成分[4]。目前多為針對羌活藥材活性成分檢測的研究[5-11],而對其制劑的報導較少[12-13],本實驗建立了養血生發膠囊中羌活醇和異歐前胡素的含量測定方法,為全面控制其質量提供了參考依據。
[1]國家藥典委員會.中華人民共和國藥典(一部)[S].北京:化學工業出版社,2010:946.
[2]劉世明,邊天羽.養血生發膠囊的藥理實驗研究[J].天津中醫藥, 1987,4(4):12-15.
[3] 陳芙蓉,岳 南,只德廣,等.養血生發膠囊對C57BL/6小鼠毛發生長的影響及機制[J].現代藥物與臨床,2010,25(2):137-140. [4]金盼盼.藥用植物羌活的研究進展 [J].安徽農業科學,2011,39 (2):815-816,903.
[5]高建邦,宋平順,郁 霞.HPLC法同時測定羌活中異歐前胡素和阿魏酸含量[J].中藥材,2010,33(2):231-233.
[6]周 毅,蔣舜媛,孫 輝,等.羌活中揮發油和異歐前胡素的含量測定[J].中國中藥雜志,2007,32(7):566-569.
[7]古麗娜·沙比爾,郭洪祝,郭 慧,等.HPLC法測定羌活中阿魏酸、羌活醇、苯乙基阿魏酸醋和異歐前胡素[J].中草藥,2006,37 (6):937-940.
[8]楊安東,馬 艷,王 笳,等.人工栽培羌活中異歐前胡素的含量測定[J].中國藥房,2006,17(15):1172-1173.
[9]朱美曉,陳 燕,易進海,等.羌活藥材薄層色譜鑒別與含量測定[J].時珍國醫國藥,2011,22(1):116-117.
[10]李春麗,周玉碧,周國英,等.野生與栽培羌活藥材揮發油含量及組分的比較分析[J].分析試驗室,2012,31(1):29-34.
[11]劉衛根,王亮生,周國英,等.羌活不同部位有機酸和香豆素類化合物含量的比較研究[J].藥物分析雜志,2012,32(11):1950-1956,1967.
[12]趙渤年,丁曉彥,劉 青.HPLC法測定九味羌活丸中異歐前胡素的含量[J].山東醫藥,2008,42(26):94-95.
[13]何 丹,楊 林,張景勍.超高效液相色譜法測定九味羌活顆粒中歐前胡素和異歐前胡素的含量[J].中國醫院藥學雜志,2013,33 (24):2053-2055.
Determination of notopterol and isoimperatorin in Yangxue Shengfa capsules by HPLC
LIU Qing-huan,FU Yu,WANG Wen-tong
(Tianjin Institute of Medical Science,Tianjin 300020,China)
[Objective]To establish the method for determining notopterol and isoimperatorin in Yangxue Shengfa capsules.[Methods] Chromatography column:Agilent Zorbax Eclipse XDB-C18was used;the mobile phase consisted of acetonitrile-0.1%phosphoric acid(45∶55);the flow rate was 1.0 mL/min;the detection wavelength was 310 nm;the column temperature was set at 25℃.[Results]The calibration curve showed a good linear correlation in the range of 0.204~1.224 μg(r=0.999 7)for notopterol and 0.103~0.616 μg(r=0.999 8) for isoimperatorin.The average recoveries of notopterol and isoimperatorin were 99.24%(RSD=0.74%)and 99.86%(RSD=1.36%). [Conclusion]The method is simple,accurate and specific for the quality control of Yangxue Shengfa capsules.
Yangxue Shengfa capsule;notopterol;isoimperatorin;HPLC
R284
A
1672-1519(2014)11-0693-03
2014-06-16)
(本文編輯:高 杉,馬曉輝)
10.11656/j.issn.1672-1519.2014.11.15
天津市中醫藥管理局中醫、中西醫結合科研課題資助項目(11083)。
劉慶煥(1984-),女,研究實習員,主要從事中藥化學與質量標準研究。

