赫賽汀聯合化療藥物在轉移性乳腺癌治療中的療效觀察
陳建華
(河南省信陽市中心醫院門診西藥房,河南 信陽 464000)
赫賽汀聯合化療藥物在轉移性乳腺癌治療中的療效觀察
陳建華
(河南省信陽市中心醫院門診西藥房,河南 信陽 464000)
目的 探討赫賽汀聯合化療藥物治療轉移性乳腺癌的臨床療效及安全性。方法 將96例人類表皮生長因子受體-2(HER-2)過度表達的轉移性乳腺癌患者隨機分為治療組(48例)和對照組(48例)。治療組給予赫賽汀+NVB+DDP,對照組僅給予赫賽汀。每4周為1個療程,至少進行2個療程,觀察患者的療效、Karnofsky評分及不良反應。結果 治療組的總有效率為72.9%,顯著高于對照組52.1%,差異有統計學意義(P<0.05)。治療后,兩組Karnofsky評分均顯著提高(P<0.05);兩組治療后比較,治療組Karnofsky評分明顯高于對照組,差異有統計學意義(P<0.05)。治療組的心臟毒性程度顯著低于對照組,差異有統計學意義(P<0.05)。結論 赫賽汀與NVP等化療藥物聯合治療HER2陽性轉移性乳腺癌療效確切,且心臟毒性較輕。
轉移性乳腺癌;赫賽汀;人類表皮生長因子受體-2;化療
轉移性乳腺癌的平均生存時間僅為18~24個月[1],化療是目前最為有效的治療手段。有研究顯示,有15%~20%的乳腺癌患者存在人類表皮生長因子受體-2(HER-2)基因擴增及蛋白質過度表達,且其與患者的預后密切相關[2]。赫賽汀作為一種以癌基因為靶點的分子靶向藥物,現已廣泛應用于HER2過度表達的轉移性乳腺癌,但其單藥治療時存在一定的心臟毒性。本研究采用赫賽汀聯合化療藥物治療HER2過度表達的轉移性乳腺癌患者,取得良好療效,報道如下。
1 資料與方法
1.1 一般資料
選擇2008年1月至2011年12月間我院收治92例的HER-2過度表達的乳腺癌轉移患者。入組標準:①均經手術或病理檢查確診,且均為女性;②免疫組織化學法檢測HER-2呈中、高陽性表達,且通過Fish檢測為陽性;③年齡≤70歲,Kamofsky評分≥60分,預計生存期超過3個月,近1個月內均為接受其他放化療。年齡43~68歲,平均(51.3± 13.2)歲;肺轉移53例,肝轉移22例,淋巴結轉移17例。96例患者均為術后首次出現復發、轉移。按照手術方式將所有患者分為治療組和對照組,每組各48例。兩組患者年齡、轉移部位等差異無統計學意義(P>0.05),具有可比性。
1.2 方法
治療組的具體化療方案:赫賽汀首次給予4 mg/kg負荷量靜脈滴注,之后2 mg/kg靜脈滴注,每周1次,連續使用;順鉑(DDP)70 mg/m2靜脈滴注3 h,第1~3天;異長春花堿(NVB)25 mg/m2靜脈滴注15 min,第1、5天。每4周為1個療程,至少應用2個療程。對照組僅給予赫賽汀,劑量及用法同治療組。治療期間,定期復查血常規、心電圖、心臟超聲及肝腎功能,并檢測左心室射血分數(LVEF)。若患者出現癥狀性充血性心力衰竭(CHF),或無癥狀性LVEF降低,與基線相比>15%或低于正常下限,則中止治療。所有患者每8周復查腫瘤變化情況,并進行療效評估。
1.3 觀察指標
根據WHO制定的實體瘤療效評價標準進行評估,分為完全緩解(CR)、部分緩解(PR)、穩定(SD)及進展(PD),其中以CR+PR計算有效率。采用Karnofsky評分標準評估患者化療前后的生活質量,同時按WHO抗癌藥物不良反應評價標準進行安全性評估,分為0~Ⅳ度。心臟毒性定義為:①有癥狀的CHF伴LVEF下降≥10%;②無癥狀的CHF伴LVEF下降≥15%或LVEF下降不足10%但降至基線的45%以下。1.4 統計學方法
應用SAS 8.2軟件進行統計分析。計數資料比較采用χ2檢驗或秩和檢驗,計量資料比較采用t檢驗,P<0.05為差異有統計學意義。
2 結 果
2.1 臨床療效
治療組的總有效率為72.9%,顯著高于對照組52.1%,差異有統計學意義(P<0.05)。見表1。
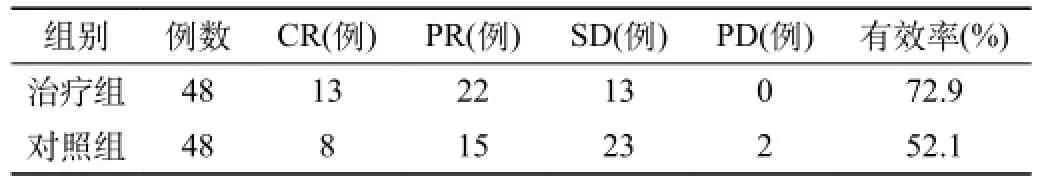
表1 兩組臨床療效比較
2.2 生活質量評分比較
治療前,兩組Karnofsky評分差異無顯著性(P>0.05);治療后,兩組Karnofsky評分均顯著提高(P<0.05);兩組治療后比較,治療組Karnofsky評分明顯高于對照組,差異有統計學意義(P<0.05)。見表2。
表2 兩組患者治療前后生活質量評分比較()
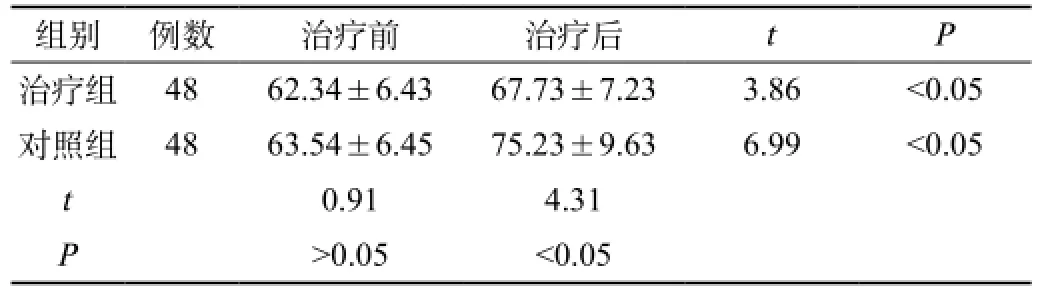
表2 兩組患者治療前后生活質量評分比較()
組別 例數 治療前 治療后 t P治療組 48 62.34±6.43 67.73±7.23 3.86 <0.05對照組 48 63.54±6.45 75.23±9.63 6.99 <0.05t0.91 4.31P>0.05 <0.05
2.3 不良反應比較
兩組主要不良反應為骨髓抑制(血小板減少、粒細胞減少及貧血),消化道反應(惡心嘔吐、腹瀉)及心臟毒性。治療組的心臟毒性程度顯著低于對照組,差異有統計學意義(P<0.05),而兩組骨髓抑制、胃腸道反應無顯著性差異(P>0.05)。見表3。
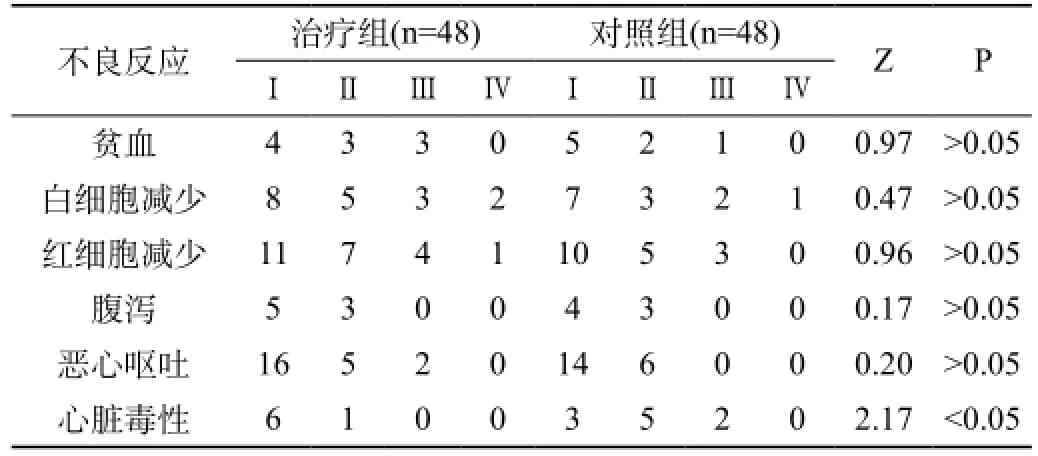
表3 兩組不良反應比較(例)
3 討 論
乳腺癌是女性常見的惡性腫瘤之一,嚴重影響婦女的身心健康。近年來HER-2作為一種促癌基因愈發引人關注,其可參與細胞生長、分化和存活的調控,且HER-2過度表達被認為是乳腺癌轉移和復發的高危因素[3]。研究發現,HER-2陽性的乳腺癌惡性程度與侵襲性較高,對內分泌治療和放療不敏感,且易對化療藥物產生耐藥性,預后較差[4,5]。赫賽汀是一種針對HER-2蛋白的高純度蛋白重組DNA衍生的人源化單克隆抗體,可通過阻斷HER-2蛋白表達而達到抑制腫瘤細胞增殖的目的[6]。但由于赫賽汀存在一定的心臟毒性,故其安全性和耐受性已成為學者關注的焦點[7]。
赫賽汀單藥使用時的主要不良反應是心臟毒性,表現為無癥狀LVEF下降,其他不良反應包括惡心、頭痛、脫發及中性粒細胞缺乏癥等。本研究中,兩組骨髓抑制、胃腸道反應無顯著性差異(P>0.05)。治療組的心臟毒性程度顯著低于對照組,差異有統計學意義(P<0.05),提示該方案可有效減少化療的毒副反應,尤其是赫賽汀所致心臟毒性,提高患者對化療的耐受力。但為防止嚴重的不良反應發生,在治療時仍需監測患者的心功能、血常規等相關生命指標。
總之,赫賽汀與NVB、DDP等化療藥物聯合較單用赫賽汀更為有效,且藥物不良反應明顯降低。鑒于本研究樣本量較小,觀察時間較短,其遠期療效及安全性還有待進一步研究證實。
[1] 王瀟瀟,周中梅,袁中玉,等.多西紫杉醇聯合卡培他濱治療轉移性乳腺癌的臨床研究[J].癌癥,2007,26(4):407-410.
[2] 張還珠,劉芯,李瑩,等.曲妥珠單抗聯合蒽環類脂質體治療HER2陽性轉移性乳腺癌(附1例報道并文獻復習)[J].廣州醫學院學報,2009,37(3):49-53.
[3] 劉春萍,逯翀,田元,等.血清HER-2/neu胞外域在復發轉移性乳腺癌患者解救化療中的臨床意義[J].中華實驗外科雜志,2009, 26(4):422-424.
[4] Dent S,Verma SH,Latreille J,et a1.The role of HER-2 targeted therapies in woman with HER-2 overexpressing metastatic breast cancer[J].Curt Oncol,2009,16(4):25-35.
[5] 王永鳳,韓建軍,劉月梅.赫賽汀聯合紫杉醇治療HER-2過表達轉移性乳腺癌[J].山東醫藥,2009,49(46):74-75.
[6] 徐峰,胡蓮,廖志勇.赫賽汀與化療藥物聯合應用治療轉移性乳腺癌進展[J].中國腫瘤生物治療雜志,2003,10(2):140-142.
[7] 王莉萍,沈坤煒,沈鎮宙.赫賽汀在乳腺癌新輔助治療與輔助治療中的新進展[J].中華腫瘤雜志,2006,28(4):241-243.
R737.9
B
1671-8194(2014)18-0152-02

