陰道內DHA脂肪酸應用對危險妊娠早產的影響
康士珍
(河南浚縣衛賢鎮衛生院,河南 鶴壁 456238)
陰道內DHA脂肪酸應用對危險妊娠早產的影響
康士珍
(河南浚縣衛賢鎮衛生院,河南 鶴壁 456238)
目的 觀察經陰道應用二十二碳六烯酸(docosahexaenoic acid,DHA)改善早產危險孕婦妊娠時間長短和新生兒體質量的作用。方法 采用隨機化研究觀察方法,納入早產高危險孕婦74例,38例為治療組,36例為對照組。治療組經陰道給予DHA 1 g每天1次,從妊娠1~37周。主要終點為妊娠時間長短,次要終點為新生兒體質量。結果 分娩時孕齡治療組為(38.6±1.05)孕周,對照組為(37.6±0.84)孕周(P=0.006)。完成治療的孕婦分娩時新生兒體質量治療組為(3082.1±293)g,對照組為(2699.3±150)g(P<0.001)。結論 早產高危孕婦經陰道應用DHA增加妊娠時間長度和新生兒體質量。
早產;高危妊娠;DHA;陰道用藥
早產是導致圍生兒病死率和患病的重要原因,由此引起新生兒病死率為28%[1]。分娩時的孕齡和新生兒病死率和患病率之間呈反相關[2]。自發性早產危險與宮頸長度呈反比關系,宮頸越短發生早產危險越高[3,4]。另一重要的預測自發早產因素是產科病史,尤其是先前的自發性早產病史。一旦確定為危險的早產孕婦,臨床醫師可能會采取終止或減弱子宮收縮措施。但是,保胎藥物延長妊娠時間和改善圍生兒結局的證據不足[5],可能達到短期受益的藥物是皮質激素改善胎兒肺成熟度。此外,一些保胎藥可對母體或胎兒產生不良影響。有研究表明,必需脂肪酸對于延長孕齡有重要作用[6-8],延緩自發性早產時間,降低早產復發危險,改善新生兒結局。亞油酸(linoleic acid,LA)和亞麻酸(linolenic acid,LnA)是必需脂肪酸,可由膳食獲取。膳食LA是多不飽和脂肪酸n-6(polyunsaturated fatty acids,PUFAs)前體,LnA為PUFAs n-3前體。正常情況下n-6∶n-3的比值為1∶1,而膳食中二者比例失調則不能滿足n-3的需要,特別是二十二碳六烯酸(docosahexaenoic acid,DHA)。事實上,歐米伽(ω)-3脂肪酸是人體必需且僅從膳食攝取。 妊娠母體DHA需求增加。妊娠期間DHA需求量尚不清楚,雖然研究證明ω-3脂肪酸在胎兒神經發育的重要作用,對于妊娠時間長短和新生兒體質量及炎癥方面亦有重要影響。妊娠婦女獲得足夠量的ω-3脂肪酸需要多種膳食來源以滿足機體消耗。研究報道表明ω-3在高危險妊娠預防或降低早產復發危險、先兆子癇和胎兒生長改善等方面有重要作用[9,10]。本研究的目的在于觀察陰道內DHA脂肪酸應用對危險妊娠早產的影響。
1 資料與方法
1.1 研究設計和對象
研究采用前瞻性隨機對照研究方法,時間自2008年1月至2011年12月止。入選對象為所有妊娠婦女且有早產危險者,包括有IUGR病史、胎兒死亡和先兆子癇病史。排除標準:①非活胎;②胎膜早破病史;③妊娠出血;④應用前列腺素抑制劑;⑤多胎;⑥魚類過敏;⑦定期攝取魚油;⑧陰道衣原體、支原體、檢查陽性,細菌性陰道炎;⑨陰道畸形。孕齡計算根據妊娠頭3個月超聲掃描。
1.2 研究方法
研究對象隨機分為兩組:治療組經陰道給予DHA 1 g,每天1次,自妊娠第1~37周。對照組給予相似形式的安慰劑。
1.3 隨訪觀察
所有患者自報告任何相關并發癥,臨床條件加重患者,則撤離研究組給予保胎治療。所有孕婦隨訪至分娩。患者的基礎特征、分娩時間、新生兒體質量及其他任何并發癥均加以記錄。
1.4 統計學處理
連續性變量以平均值±標準差表示,非連續性變量以中位值(四分區間范圍,interquartile range,IQR)表示,分類變量應用卡方或Fisher's檢驗,連續變量比較采用t檢驗和Mann-Whitney U-檢驗。取P<0.05為差異有統計學意義。統計學軟件為SPSS16.0。
2 結 果
共74例患者納入研究。38例為治療組,36例為對照組。對照組14例患者因臨床癥狀加重而撤離研究組。兩組患者的基礎特征見表1,兩組的基本特征差異無統計學意義。
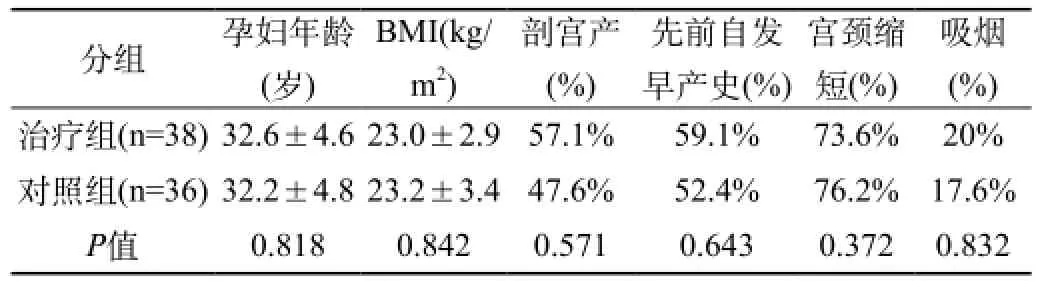
表1 兩組患者的基礎特征比較
分娩時平均孕齡治療組為(38.6±1.05)孕周,對照組為(37.6± 0.84)孕周(P=0.006)。完成治療的孕婦分娩時新生兒體質量治療組為(3082.1±293)g,對照組為(2699.3±150)g(P<0.001)。
3 討 論
本研究結果顯示,與對照組相比,對于高危的妊娠經陰道給予DHA可顯著延長妊娠時間,增加新生兒體質量。一些研究表明,ω-3補充可能會影響分娩過程,延遲分娩發動,降低早產復發危險,動物試驗顯示其有保胎作用[9]。雖然其確切機制尚不清楚,但是涉及類十二烷酸介導子宮肌層收縮變化和結締組織重建,類十二烷酸受體變化,或這些脂肪酸對胎膜的影響如改變信號傳送途徑或調整離子介導的收縮。特別是亞麻酸(n-6)是前列腺素的重要來源,是分娩過程的必需部分。n-3脂肪酸可降低分娩過程促發物質如類十二烷酸的活化,特別是前列腺素F和E;增加子宮肌層松馳物質如前列腺環素的活化[9,10]。
根據本研究結果及先前文獻資料,可以認為DHA應用后由PUFA產生的前列腺環素對子宮肌肉細胞和血管造成直接影響,或許,陰道內給予不僅可避免首過效應,因此藥物劑量更能完全達到藥物濃度,而且也直接作用于宮頸。增加ω-3攝取和其他脂肪酸比例相適應致使ω-6的合成下調,從而降低PGE2和PEF2α生成,對宮頸有修正作用。前列腺環素PGI2和PGI3,對子宮肌層具有松馳作用。對于妊娠時間的其他影響可能與子宮肌層電生理活動有聯系,ω-3可能使規律性收縮發動延遲,影響妊娠時間的長短。
總之,本研究結果提示對于早產高危險患者經陰道給予DHA顯著降低早產發生率,可改善胎兒發育。
[1] Menon R.Spontaneous preterm birth,a clinical dilemma: etiologic,pathophysiologic and genetic heterogeneities and racial disparity[J].Acta Obstet Gynecol Scand,2008,87(6):590-600.
[2] Olsen SF,Secher NJ,Tabor A,et al.Randomised clinical trials of fish oil supplementation in high risk pregnancies. Fish Oil Trials In Pregnancy (FOTIP)Team[J].BJOG,2000,107(3):382-395.
[3] Horvath A,Koletzko B,Szajewska H.Effect of supplementation of women in high-risk pregnancies with long-chain polyunsaturated fatty acids on pregnancy outcomes and growth measures at birth: a meta-analysis of randomized controlled trials[J].Br J Nutr,2007,98(2):253-259.
[4] Szajewska H,Horvath A,Koletzko B.Effect of n-3 long-chain polyunsaturated fatty acid supplementation of women with lowrisk pregnancies on pregnancy outcomes and growth measures at birth: a meta-analysis of randomized controlled trials[J].Am J Clin Nutr,2006,83(6):1337-1344.
[5] 張侃,何鳳慈,曾琳,等.必需脂肪酸對新生大鼠腦發育與學習記憶功能的影響[J].中國臨床康復,2004,8(4):624-625.
[6] 張侃,曾琳,龍在云,等.必需脂肪酸對新生大鼠小腦細胞構筑結構的影響[J].第三軍醫大學學報,2005,27(13):1355-1356.
[7] Sung WK,Ronald DM.Functional Amino Acids and Fatty Acids for Enhancing Production Performance of Sows and Piglets. Asian-Aust[J].J Anim Sci,2007,20(2) :295-306.
[8] Olsen SF.Is supplementation with marine omega-3 fatty acids during pregnancy a useful tool in the prevention of preterm birth?[J].Clin Obstet Gynecol,2004,47(4):768-774.
[9] Baguma-Nibasheka M,Brenna JT,Nathanielsz PW.Delay of preterm delivery in sheep by omega-3 long-chain polyunsaturates[J].Biol Reprod,1999,60(3):698-701.
[10] Larqué E,Demmelmair H,Berger B,et al.In vivo investigation of the placental transfer of 13C-labeled fatty acids in humans[J].J Lipid Res,2003,44(1):49-55.
R714
B
1671-8194(2014)18-0166-02

