緩激肽對轉化生長因子-β1誘導的肺動脈平滑肌細胞遷移的影響*
馮文靜,趙剛,徐西振,趙俊杰,董若蘭,凃玲,姚濟華
(1.華中科技大學同濟醫學院附屬同濟醫院老年醫學科,武漢 430030;2.山東大學附屬省立醫院心血管內科,濟南 250021;3.華中科技大學同濟醫學院附屬同濟醫院心血管內科,武漢 430030)
緩激肽對轉化生長因子-β1誘導的肺動脈平滑肌細胞遷移的影響*
馮文靜1,趙剛2,徐西振3,趙俊杰1,董若蘭1,凃玲1,姚濟華1
(1.華中科技大學同濟醫學院附屬同濟醫院老年醫學科,武漢 430030;2.山東大學附屬省立醫院心血管內科,濟南 250021;3.華中科技大學同濟醫學院附屬同濟醫院心血管內科,武漢 430030)
目的 觀察緩激肽對轉化生長因子-β1(TGF-β1)誘導的肺動脈平滑肌細胞(PASMCs)遷移的影響及其可能機制。方法原代培養PASMCs,應用Transwell小室檢測緩激肽對PASMCs跨膜遷移能力的影響,同時應用劃痕修復實驗檢測緩激肽對PASMCs橫向遷移能力的影響。結果TGF-β1顯著增加了跨膜遷移的PASMCs數目(P<0.05),緩激肽顯著減少了PASMCs的跨膜遷移(P<0.05),而B2受體抑制劑(HOE-140)對緩激肽抑制TGF-β1誘導的PASMCs的跨膜遷移作用無顯著改變(P>0.05)。緩激肽顯著降低PASMCs的劃痕愈合指數(P<0.05),而HOE-140對緩激肽抑制TGF-β1誘導的PASMCs的橫向遷移能力無顯著改變(P>0.05)。結論緩激肽可以抑制TGF-β1誘導的PASMCs跨膜和橫向遷移能力,而這一效應可能不通過緩激肽B2受體介導。
緩激肽;肺動脈平滑肌細胞;轉化生長因子-β1;遷移
肺動脈高壓是一類嚴重的進展性疾病,其主要特征是肺血管阻力進行性升高,持續發展可導致患者右心衰竭而死亡[1]。肺血管重構是肺血管阻力進行性升高的重要病理生理基礎,肺動脈平滑肌細胞(pulmonary arterial smooth muscle cells,PASMCs)由中層至內膜層的遷移,導致了肺動脈中膜增厚和非肌性血管肌化,最終導致血管硬化和阻塞,從而使肺動脈壓力持續升高[2]。研究表明,多種肺動脈高壓動物模型均存在PASMCs中轉化生長因子-β1(transforming growth factor-β1,TGF-β1)表達增加并刺激PASMCs遷移,促進肺血管重構的發生和發展[3]。
緩激肽(bradykinin,BK)是一種血管活性九肽,通過自分泌-旁分泌機制釋放,與受體結合后發揮擴張血管、降低血壓、增加局部血流、調節平滑肌松弛和收縮、增加血管通透性等多種生物學效應[4]。研究表明,激肽釋放酶可以通過增加緩激肽水平從而抑制血小板源性生長因子誘導的大鼠主動脈平滑肌細胞遷移[5],然而,BK是否能抑制TGF-β1誘導的PASMCs遷移及其可能的分子機制尚不清楚。因此,筆者研究肺血管重構的病理生理機制,旨在探討BK對TGF-β1誘導的PASMCs遷移的影響,為臨床肺血管重構的治療提供新的理論依據。
1 材料與方法
1.1 試劑 豬肺動脈購自武漢市血清制品廠,胎牛血清(fetal bovine serum,FBS)、達爾伯克必需基本培養液(Dulbecco′s minimum essentialmedium,DMEM)、胰酶均購自Hyclone公司。10%DMEM為含有10%胎牛血清、0.146 g·L-1L-谷氨酰胺、1×105U·L-1青霉素和1×105U·L-1鏈霉素的DMEM培養液。BK、TGF-β1、緩激肽B2受體抑制劑HOE-140購自美國Sigma公司。牛血清清蛋白購自碧云天生物技術研究所。Transwell小室購自美國Corning公司,其余試劑均為國產分析純試劑。
1.2 方法
1.2.1 原代培養PASMCs 無菌操作下取豬肺動脈,分離肺組織中的3~4級肺小動脈,鈍性分離法剝除肺動脈外膜后,立即用大量含有雙抗的磷酸鹽緩沖液(phosphate buffered solution,PBS)沖洗。縱向剪開肺動脈,刮除肺動脈內皮細胞,并用PBS清洗掉殘留的肺動脈內皮細胞。將肺動脈中膜組織在含有少量10%FBS的DMEM培養液中剪成1 mm3大小的組織塊后轉移到細胞培養瓶中,翻轉培養瓶,置于37℃、5%二氧化碳培養箱中倒置培養4~6 h。組織塊貼壁后補充適量含10%FBS的DMEM培養液并輕輕翻轉培養瓶,正置培養5~7 d,可見少量細胞從組織塊邊緣爬出。每2~3 d更換培養液,換液時去除漂浮的組織塊。用0.02%乙二胺四乙酸-0.25%胰蛋白酶消化傳代,實驗采用第2~6代細胞。
1.2.2 PASMCs鑒定 分別采用倒置相差顯微鏡下觀察和免疫熒光染色檢測抗α-平滑肌肌動蛋白(αsmoothmuscle actin,α-SMA)的方法[6]對所培養的細胞進行鑒定,從而明確是否為PASMCs。細胞純度在95%以上用于實驗。
1.2.3 實驗分組 培養板中的細胞隨機分為6組:對照組、溶媒組、TGF-β1組、TGF-β1+HOE-140組、TGF-β1+BK組及TGF-β1+BK+HOE-140組,干預前換0.4%FBS的DMEM培養液同步化處理12 h。為研究可能機制,給予BK前1 h加用緩激肽B2受體抑制劑HOE-140(10-5mol·L-1)、BK干預作用30min后,加入TGF-β1(10 ng·mL-1)。每次實驗至少重復3次。
1.2.4 Transwell小室檢測PASMCs的跨膜遷移能力細胞跨膜遷移能力按文獻所述的方法進行[7]。常規胰酶消化收集PASMCs,1 000 r·min-1離心(德國賀利氏Fresco臺式高速離心機)10 min,用無血清DMEM培養液重懸PASMCs,使細胞密度達到5×105·mL-1,每個Transwell小室均勻滴加細胞懸液200μL(1×105個),下室加入無血清DMEM培養液600μL。按照上述實驗分組和干預時間點將BK、HOE-140加入Transwell上室,TGF-β1作為誘導遷移的細胞趨化因子加入Transwell下室誘導PASMCs遷移。將24孔板置于37℃、5%CO2培養箱中孵育6 h。干預結束后用棉簽輕輕擦去上室內的細胞,并用4%多聚甲醛固定30 min,0.1%結晶紫室溫下染色10 min,純化水漂洗干凈,顯微鏡下隨機選取5個高倍視野(×200)計數每個Transwell小室遷移的細胞數目并攝相。
1.2.5 劃痕修復實驗檢測PASMCs的橫向遷移能力 細胞劃痕修復實驗按文獻所述的方法進行[8]。將PASMCs接種于6孔板,加入含10%FBS的DMEM培養液繼續培養,待細胞長至完全融合時,用無菌的200μL槍頭在6孔板的底面上沿直線輕輕進行劃痕,用PBS洗3次將懸浮的細胞洗掉,加入無血清DMEM培養液繼續培養并按分組加入相應的藥物干預,分別在0,24 h于倒置顯微鏡下(×100)觀察細胞遷移情況,隨機選擇劃痕區5個視野攝相,測量不同時間點的劃痕寬度,比較各組間劃痕愈合的差異并計算劃痕愈合指數。劃痕愈合指數=(初始劃痕寬度-愈合后劃痕寬度)/初始劃痕寬度。
2 結果
2.1 PASMCs形態及鑒定 肺動脈中膜組織塊移植于培養瓶后,培養5~7 d可見少量細胞從組織塊邊緣爬出,細胞呈不規則多角形,并逐漸伸展成梭形或長梭形。部分區域可見PASMCs融合呈梭形重疊生長,呈現典型的“谷與峰”樣特征。免疫熒光染色結果見圖1所示,95%以上細胞抗α-SMA陽性,細胞質顯示呈綠色熒光標記的肌動蛋白結構,細胞核呈橢圓形位于細胞中央被染成藍色。
2.2 BK對TGF-β1誘導的PASMCs跨膜遷移能力的影響 按上述實驗分組和干預方法,應用Tanswell檢測BK對TGF-β1誘導的PASMCs跨膜遷移能力的影響。如圖2,3所示,與對照組和溶媒組比較,TGF-β1組PASMCs跨膜遷移的細胞數目顯著增加(P<0.05)。與TGF-β1組比較,TGF-β1+BK組顯著減少了TGF-β1誘導的PASMCs跨膜遷移的細胞數目(P<0.05)。而合用緩激肽B2受體抑制劑HOE-140后,BK抑制TGF-β1誘導的PASMCs的遷移作用無顯著改變。說明BK可以抑制TGF-β1誘導的PASMCs的跨膜遷移能力,而這一效應可能不通過緩激肽B2受體介導。
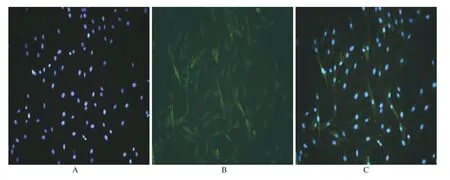
圖1 PASMCs免疫熒光染色(×200)A.細胞核;B.細胞質α-SMA染色陽性;C.PASMCs組合圖Fig.1 Immunofluorescent staining on PASMCs(×200)A.nucleus;B.positiveα-SMA expression in cytoplasm by staining;C.merged PASMCs
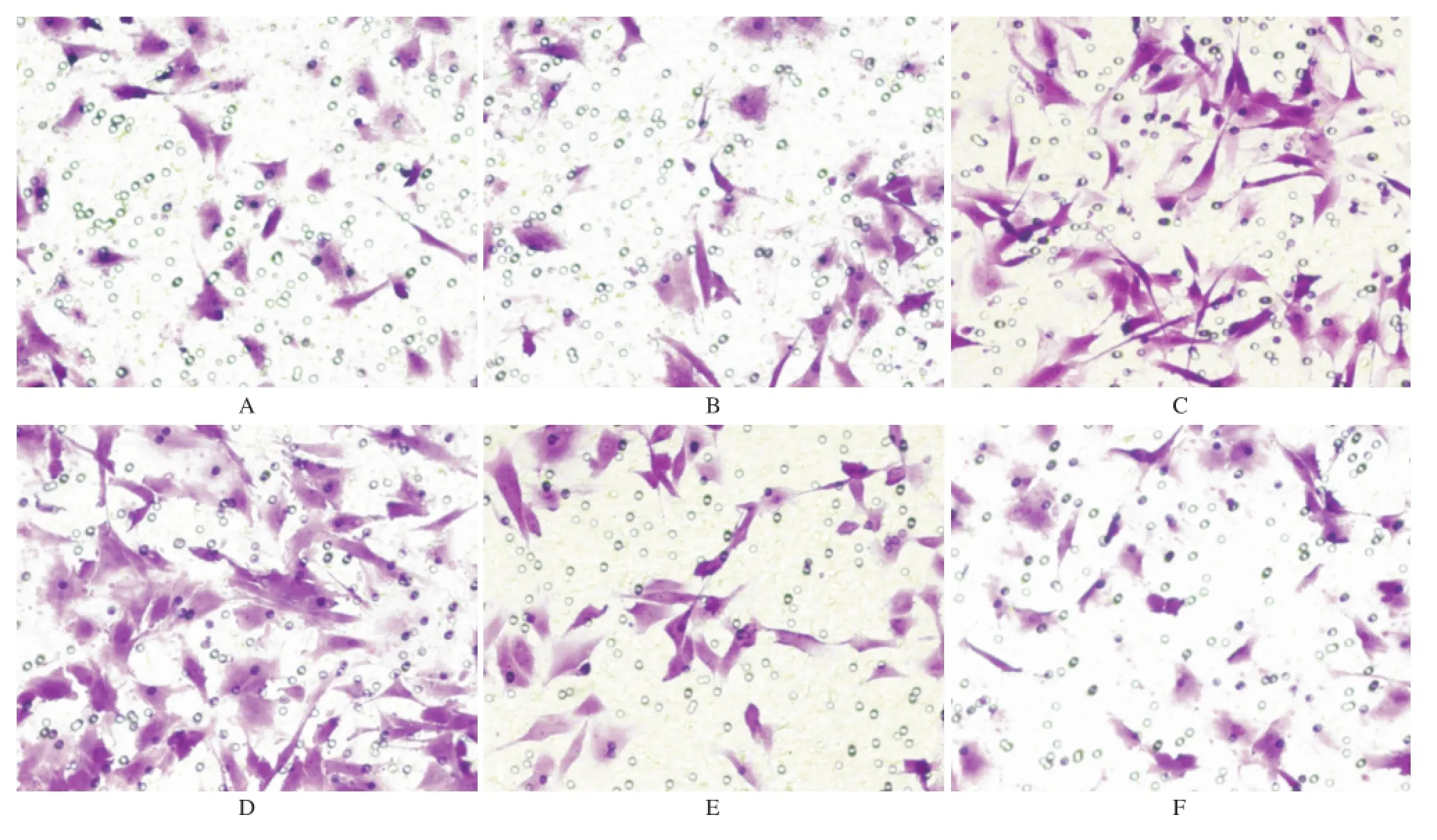
圖2 6組細胞遷移圖(×200)A.對照組;B.溶媒組;C.TGF-β1組;D.TGF-β1+HOE-140組;E.TGF-β1+BK組;F.TGF-β1+BK+HOE-140組Fig.2 Transition diagram of six groups of cells(×200)A.control group;B.vehicle group;C.TGF-β1group;D.TGF-β1plus HOE-140 group;E.TGF-β1plus BK group;F.TGF-β1,BK plus HOE-140 group
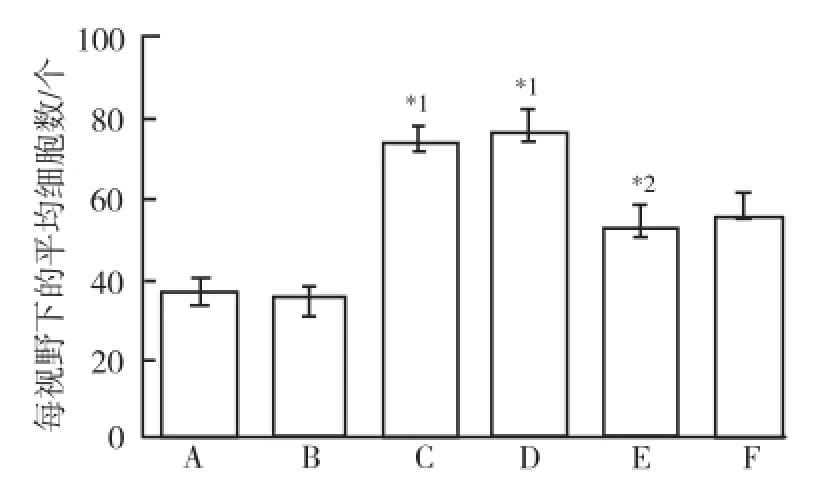
圖3 6組細胞每視野下的平均細胞數目直方圖A.對照組;B.溶媒組;C.TGF-β1組;D.TGF-β1+HOE-140組;E.TGF-β1+BK組;F.TGF-β1+BK+HOE-140組;與對照組和溶媒組比較,*1P<0.05;與TGF-β1組比較,*2P<0.05Fig.3 Histogram of average cell number under per visual field in six groups of cellsA.control group;B.vehicle group;C.TGF-β1group;D.TGF-β1plus HOE-140 group;E.TGF-β1plus BK group;F.TGF-β1,BK plus HOE-140 group;compared with the control group and vehicle group,*1P<0.05;compared with TGF-β1group,*2P<0.05
2.3 BK對TGF-β1誘導的PASMCs橫向遷移能力的影響 按上述實驗分組和干預方法,應用劃痕修復實驗檢測BK對TGF-β1誘導的PASMCs橫向遷移能力的影響。如圖4,5所示,單層細胞劃痕實驗24 h后,與對照組和溶媒相比較,TGF-β1組PASMCs劃痕愈合指數顯著增加(P<0.05)。與TGF-β1組比較,TGF-β1+ BK組PASMCs劃痕愈合指數顯著降低(P<0.05)。而合用緩激肽B2受體抑制劑HOE-140后,BK抑制TGF-β1誘導的PASMCs的橫向遷移作用無顯著改變。說明BK可以抑制TGF-β1誘導的PASMCs的橫向遷移能力,而這一效應可能不通過緩激肽B2受體介導。
3 討論
肺血管重構主要包括肺動脈內膜損害、中膜肥厚和外膜增厚,肺血管內皮細胞凋亡參與肺動脈高壓發病的重要起始環節[9]。SAKAO等[10]研究發現,凋亡的肺血管內皮細胞可以分泌一系列細胞因子(血管內皮生長因子、TGF-β1等)作用于PASMCs,促進肺血管重構。STURROCK等[11]研究發現,肺動脈高壓發病過程中TGF-β1表達顯著增加。多種肺動脈高壓動物模型均存在PASMCs中TGF-β1表達增加并刺激PASMCs遷移,促進肺血管重構的發生和發展[3]。PASMCs由中層至內膜層的遷移,導致肺動脈中膜增厚和非肌性血管肌化,最終導致血管硬化和阻塞[2]。本實驗應用TGF-β1誘導原代培養的豬PASMCs遷移,結果顯示: TGF-β1可以顯著誘導PASMCs遷移,這與文獻[3]報道一致,說明TGF-β1誘導PASMCs遷移模型制作成功,可以用于研究BK對TGF-β1誘導的PASMCs的遷移作用。
本實驗中,Tanswell結果顯示,TGF-β1顯著增加了跨膜遷移的PASMCs數目,BK顯著減少了TGF-β1誘導的PASMCs的跨膜遷移,而HOE-140對BK抑制TGF-β1誘導的PASMCs的跨膜遷移作用無顯著改變。劃痕修復實驗也顯示,BK顯著降低了TGF-β1誘導的PASMCs的劃痕愈合指數,而HOE-140對BK抑制TGF-β1誘導的PASMCs的橫向遷移能力無顯著改變。說明BK可以抑制TGF-β1誘導的PASMCs跨膜和橫向遷移能力,而這一效應可能不通過緩激肽B2受體介導。

圖4 6組細胞劃痕修復圖(×100)A.對照組;B.溶媒組;C.TGF-β1組;D.TGF-β1+HOE-140組;E.TGF-β1+BK組;F.TGF-β1+BK+HOE-140組Fig.4 Scratch-restoration of six groups of cells(×100)A.control group;B.vehicle group;C.TGF-β1group;D.TGF-β1plus HOE-140 group;E.TGF-β1plus BK group;F.TGF-β1,BK plus HOE-140 group

圖5 6組細胞愈合指數直方圖A.對照組;B.溶媒組;C.TGF-β1組;D.TGF-β1+HOE-140組;E.TGF-β1+BK組;F.TGF-β1+BK+HOE-140組;與對照組和溶媒組比較,*1P<0.05;與TGF-β1組比較,*2P<0.05Fig.5 Healing index histogram of six groups of cellsA.control group;B.vehicle group;C.TGF-β1group;D.TGF-β1plus HOE-140 group;E.TGF-β1plus BK group;F.TGF-β1,BK plus HOE-140 group;compared with the control group and vehicle group,*1P<0.05;compared with TGF-β1group,*2P<0.05
BK是激肽釋放酶-激肽系統(kallikrein-kinin system,KKS)中的重要活性物質,主要通過自分泌-旁分泌機制釋放,與受體結合后發揮擴張血管、降低血壓、增加局部血流、調節平滑肌松弛和收縮、增加血管通透性,改善腎功能等多種生物學效應[4]。B2受體是一種跨膜G-蛋白耦聯受體,廣泛表達于大多數組織。已有研究報道,重組腺病毒介導的人組織激肽釋放酶基因轉染可明顯抑制血小板源性生長因子誘導的自發性高血壓大鼠血管平滑肌細胞遷移[5]。本研究發現, BK抑制TGF-β1誘導的PASMCs的遷移作用,而HOE-140對BK抑制TGF-β1誘導的PASMCs的遷移作用不產生影響,因此推測BK抑制PASMCs的遷移作用不通過緩激肽B2受體介導。
綜上所述,BK可抑制TGF-β1誘導的PASMCs的遷移作用,這一效應不通過緩激肽B2R介導。這可能為肺血管重構的發生和發展提供了新的理論依據,為預防和治療肺血管重構提供了新的思路,但還有待于進一步對其具體機制進行研究。
[1]RABINOVITCH M.Molecular pathogenesis of pulmonary arterial hypertension[J].JClin Invest,2008,118(7): 2372-2379.
[2]KOURI F M,QUEISSER M A,KONIGSHOFF M,et al. Plas-minogen activator inhibitor type 1 inhibits smooth muscle cell proliferation in pulmonary arterial hypertension[J].Int JBiochem Cell Biol,2008,40(9):1872-1882.
[3]LONG L,CROSBY A,YANG X,et al.Altered bone morphogenetic protein and transforming growth factor-beta signaling in ratmodels of pulmonary hypertension:potential for activin receptor-like kinase-5 inhibition in prevention and progression of disease[J].Circulation,2009,119(4): 566-576.
[4]MAURER M,BADER M,BASM,et al.New topics in bradykinin research[J].Allergy,2011,66(11):1397-1406.
[5]余惠珍,謝良地,朱鵬立,等.人組織激肽釋放酶基因轉移對血管平滑肌細胞遷移的影響[J].南方醫科大學學報,2010,30(4):746-749.
[6]TIAN X,VROOM C,GHOFRANIH A,et al.Phosphodiesterase 10A upregulation contributes to pulmonary vascular remodeling[J].PLoSOne,2011,6(4):e18136.
[7]MERLO S,FRASCA G,CANONICO P L,et al.Differential involvementof estrogen receptor alpha and estrogen receptor beta in the healing promoting effect of estrogen in human keratinocytes[J].JEndocrinol,2009,200(2):189-197.
[8]XU C,GUIQ,CHENW,et al.Small interference RNA targeting tissue factor inhibits human lung adenocarcinoma growthin vitroandin vivo[J].J Exp Clin Cancer Res, 2011,30(1):63-65.
[9]TEICHERT-KULISZEWSKA K,KUTRYK M J,KULISZEWSKIM A,et al.Bone morphogenetic protein receptor-2 signaling promotes pulmonary arterial endothelial cell survival:implications for loss-of-function mutations in the pathogenesis of pulmonary hypertension[J].Circ Res, 2006,98(2):209-217.
[10]SAKAO S,TARASEVICIENE-STEWART L,WOOD K,et al.Apoptosis of pulmonary microvascular endothelial cells stimulates vascular smooth muscle cell growth[J].Am J Physiol Lung Cell Mol Physiol,2006,291(3):362-368.
[11]STURROCK A,CAHILL B,NORMAN K,et al.Transforming growth factor-beta1 induces Nox4 NAD(P)H oxidase and reactive oxygen species-dependent proliferation in human pulmonary artery smoothmuscle cells[J].Am J Physiol Lung Cell Mol Physiol,2006,290(4):661-673.
DOI 10.3870/yydb.2014.01.003
Effects of Bradykinin on Migration of Pulmonary Artery Smooth Muscle Cells Induced by TGF-β1
FENGWen-jing1,ZHAO Gang2,XU Xi-zhen3,ZHAO Jun-jie1,DONG Ruo-lan1,TU Ling1,YAO Ji-hua1
(1.Department of Geriatrics,Tongji Hospital,Tongji Medical College,Huazhong University of Science and Technology,Wuhan 430030,China;2.Department of Cardiology,Shandong Provincial Hospital,Shandong University,Jinan 250021,China;3.Department of Cardiology,Tongji Hospital,Tongji Medical College, Huazhong University of Science and Technology,Wuhan 430030,China)
Objective To study the effects of bradykinin(BK)on pulmonary artery smooth muscle cells(PASMCs) migration induced by transforming growth factor-β1(TGF-β1)and their possible mechanisms.MethodsThe transmembrane migration of BK on primary PASMCs with TGF-β1treatmentwas exam ined by transwell assay,and the lateralm igration of BK on primary PASMCs with TGF-β1was determined by healing of surface scratch assay.ResultsTGF-β1significantly increased the number of PASMCs migrating across the membrane(P<0.05).BK significantly reduced TGF-β1-induced PASMCs transmembranemigration(P<0.05),which was not prevented by the B2 receptor(B2R)inhibitor HOE-140(P>0.05). Furthermore,BK significantly reduced TGF-β1-induced PASMCs lateralmigration(P<0.05),while the effectwas not blocked by the B2R inhibitor HOE-140(P>0.05).ConclusionBK can significantly inhibit TGF-β1-induced PASMCs transmembrane and lateralmigration.However the inhibitory effects ofmigrationmay notbemediated by bradykinin B2 receptor.
Bradykinin;Pulmonary artery smoothmuscle cell;Transforming growth factor-β1;Migration
R972;R965
A
1004-0781(2014)01-0008-05
2013-04-10
2013-06-27
*國家自然科學基金資助項目(30971247, 81170111)
馮文靜(1986-),女,山東日照人,博士,從事肺動脈高壓的發病機制及藥物對其保護作用研究。電話:027-83662533,E-mail:wenjing.8687@163.com。
姚濟華(1965-),男,湖北武漢人,副教授,學士,研究方向:肺動脈高壓發病機制與治療。電話:027-83662606,E-mail:jhyaott@hotmail.com。

