聚氨酯泡沫塑料法從粉煤灰中回收鎵研究
王莉平,劉建,崔玉卉
(長安大學環境科學與工程學院化工系,陜西西安 710054)
鎵在國防科學、高性能計算機的集成電路、光電二極管等方面有著廣泛應用,并被稱為“電子工業糧食”。目前世界上每年鎵的需求量150~220 t,并正以每年12%的速度增長。我國金屬鎵的儲量占世界儲量的80% ~85%[1],鎵在地殼中約占萬分之一點五,數量不小,但沒有形成集中的單質金屬礦,提取也十分困難。鎵作為稀有分散金屬,為一種伴生礦,其富集分離方法一般有如下幾種:含鎵的廢液中回收鎵、含鋅的礦物中提取鎵、硫化銅礦中回收鎵、鋁冶煉過程中提取鎵、粉煤灰或有色金屬冶煉廠的爐渣中回收鎵等。粉煤灰中鎵的含量為12 ~230 μg/g[2],和其它礦物相比,極具回收價值。
本研究基于鹽酸溶液中鎵以穩定配陰離子存在,含胺基團可與質子形成銨陽離子,兩者相互作用,形成締合物。實驗通過在酸介質中聚氨酯泡沫塑料對粉煤灰中鎵的吸附性能和解析性能的研究,得到粉煤灰中回收鎵的工藝條件,獲得了一種新的有別于樹脂吸附或萃取[3]的有顯著應用前景的粉煤灰中回收鎵的工藝方法。
1 實驗部分
1.1 試劑與儀器
三氧化二鎵,分析純;粉煤灰,西安熱電廠及渭河電廠提供;高密度聚氨酯泡沫塑料,工業品。
721分光光度計;MSE225P-OCF-DU型電子分析天平;HY-2型調速多用振蕩器;PHS-3C型精密pH計。
1.2 粉煤灰預處理
準確稱取灰樣5.0 g,置于瓷坩堝中,加無水碳酸鈉5.0 g,攪勻,放入700℃高溫爐中熔融5 min。取出冷卻,將坩堝放入250 mL燒杯中,加沸水25 mL浸取,加入濃鹽酸25 mL,將氫氧化物沉淀溶解,并稍過量,洗出坩堝。在電熱套中蒸發至完全干涸,攪拌并搗碎鹽類,再低溫烘干,使硅酸脫水。取下稍冷,用6 mol/L鹽酸溶解,并轉入50 mL容量瓶中,以6 mol/L鹽酸稀釋至刻度,搖勻,備用。
1.3 實驗方法
1.3.1 吸附過程原理 在鹽酸介質中,Ga3+可和Cl-形成配陰離子。
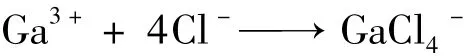
泡塑中酰胺基團可與質子(H+)形成銨陽離子。

配陰離子和銨陽離子形成締合物,從而實現鎵的吸附和固液分離。

1.3.2 吸附實驗 取干燥錐形瓶,加泡塑0.050 0 g,酸性條件下,加定量鎵溶液,置于振蕩器上振蕩2 h,至吸附平衡,測定濾液中的鎵含量,計算吸附率。

式中,C0、C1分別表示溶液中鎵離子的初始濃度和吸附平衡濃度。
1.4 分析方法
粉煤灰及實驗溶液中的鎵含量用羅丹明B顯色萃取分光光度法測定[4]。
2 結果與討論
2.1 聚氨酯泡塑吸附鎵的工藝條件
2.1.1 酸介質對吸附率的影響 在錐形瓶中各加入泡塑 0.500 0 g,分別加入 H2SO4、HCl、HNO3,各加500 μg/mL的鎵標液0.5 mL,稀釋至酸溶液中的H+濃度為2~6 mol/L,溶液總體積為25 mL,液固比為50∶1(mL/g),加蓋后放在恒溫振蕩器上,室溫下振蕩2 h。用干燥的移液管移取吸附后殘液1.0 mL,放入干燥的比色管中,用1∶1(V/V)鹽酸將其稀釋至10 mL,測其吸光度。不同酸介質與吸附率的關系,見圖1。
由圖1可知,硝酸、硫酸、鹽酸3種酸性介質中,鹽酸的吸附效果最好,隨鹽酸濃度的增加,吸附率增大;在酸濃度為6 mol/L時,鹽酸的吸附效率為99%;濃度>6 mol/L時,接近100%,效果最好。綜合考慮,選用6 mol/L的鹽酸作為泡塑吸附介質。

圖1 酸介質對吸附率的影響曲線Fig.1 Effect curve of the acid medium on adsorbing rate of gallium
2.1.2 鹽酸介質濃度對吸附率影響 實驗條件C0=10 μg/mL,V=25 mL,t=2 h,T=20 ℃,mPU=0.500 0 g,液固比 =50∶1(mL/g),以濃鹽酸稀釋實驗溶液中H+濃度為3~8 mol/L,室溫下振蕩吸附2 h。吸附殘液測其鎵含量,不同酸濃度下的吸附率見圖2。

圖2 酸濃度對吸附的影響Fig.2 Effect of the acid concentration on adsorbing rate of gallium
由圖2可知,6 mol/L鹽酸濃度吸附效果最佳。
2.1.3 吸附時間對吸附率的影響 考察了在不同吸附時間條件下吸附的效果,其他條件不變,結果見圖3。
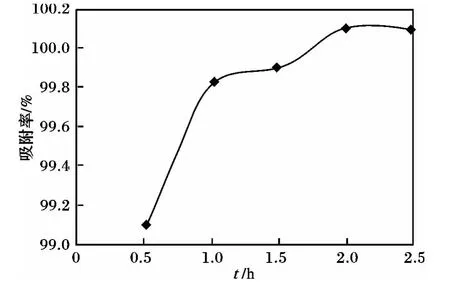
圖3 吸附時間對吸附影響Fig.3 Effect of time on adsorbing rate of gallium
由圖3可知,在1.0 h之內,吸附率與時間成正比例關系;1.0~1.5 h,吸附率的增加速度緩慢;1.5 h后吸附率趨于平衡。確定吸附時間2 h為宜。
2.1.4 固液比對吸附率的影響 固定鎵溶液濃度和體積,改變泡塑用量,考察不同固液比下吸附率。25 mL的10 μg/mL鎵溶液室溫下加蓋后振蕩2 h,結果見圖4。
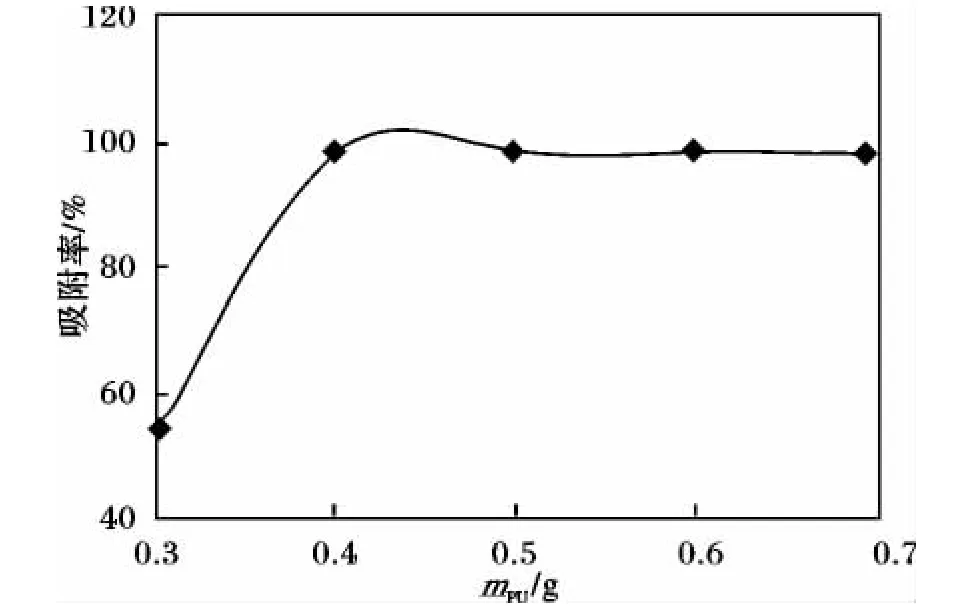
圖4 泡塑質量對吸附的影響Fig.4 Effect of the amount of PC on adsorbing rate of gallium
由圖4可知,當泡塑質量>0.500 0 g鎵的吸附率不小于 98.4%。綜合考慮,選擇泡塑質量0.500 0 g,即固液比 =1∶50(g/mL)。
2.1.5 飽和吸附量 實驗條件為 V=25 mL,t=2 h,T=20 ℃,mPU=0.500 0 g,CHCl=6 mol/L 以鎵的濃度為橫坐標,單位質量的泡塑吸附的鎵的量為縱坐標作圖見圖5。

圖5 靜態吸附曲線Fig.5 Isotherm curve of Ga adsorption
由圖5可知,隨鎵的量的增加,單位質量的泡塑吸附的鎵的量增加較快。達飽和吸附后,由于同離子效應的影響,鎵濃度的增加反而使得單位質量的泡塑吸附鎵的量有所減少。市售高密度聚氨酯泡沫塑料的飽和吸附量為46.7 mg/g-PU。
2.1.6 溫度對吸附的影響 考察了不同溫度條件下泡塑對鎵的吸附率影響,實驗過程按2.1.1節,實驗條 件:C0=10 μg/mL,V=25 mL,t=2 h,mPU=0.500 0 g,CHCl=6 mol/L,結果見表 1。
由表1可知,溫度對吸附率的影響很小。綜合考慮各種因素后,確定吸附溫度為室溫。
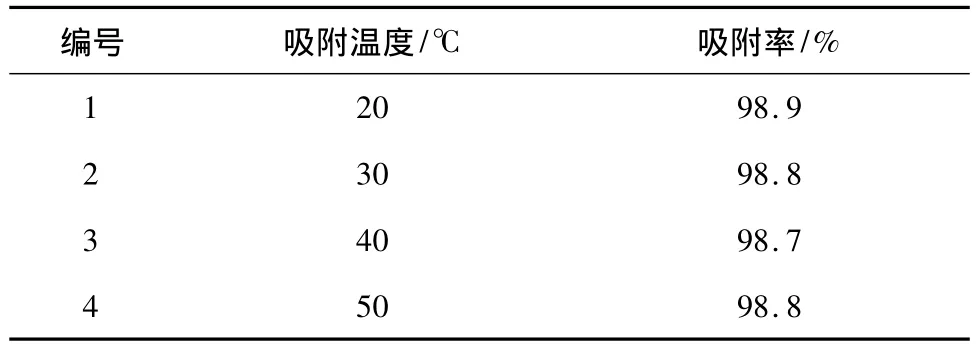
表1 溫度對吸附的影響Table 1 Effect of temperature on adsorbing rate of gallium
2.1.7 共存離子對吸附率的影響 實驗考察了粉煤灰中含量較大的Fe3+、Al3+、Mg2+及Ca2+四種共存離子干擾情況。在錐形瓶中,各加入泡塑0.500 0 g,分別加入含鎵500 μg/mL 溶液25 mL,溶液由鹽酸調節至6 mol/L HCl濃度,同時按鎵濃度的10~50倍(記為M/Ga)依次分別加入共存離子,室溫下加蓋振蕩2 h。測殘液的吸光度值,計算相應的吸附率。
實驗結果表明,Fe3+存在時,對吸附影響顯著,吸附率明顯下降。在鹽酸介質中,Fe3+被還原為低價狀態,不被吸附;Ca2+、Al3+、Mg2+也不被泡塑吸附。由此可知,Fe3+、Al3+、Mg2+、Ca2+四種共存離子對鎵的吸附率影響不大,表明該方法具有實際應用價值。
2.2 泡塑吸附回收粉煤灰中鎵
對電廠的煙道粉煤灰進行焙燒、浸出,并測定其鎵含量,測量吸附和洗脫后的吸光度,結果見表2。

表2 粉煤灰中鎵的吸附回收Table 2 Adsorption recovery of gallium in coal fly ash
由表2可知,西安熱電廠干灰的清液和樣液中鎵含量均最大;渭河電廠干灰雖清液中鎵含量較低,但樣液中含量高;渭河電廠濕灰和西安熱電廠濕灰清液和樣液中鎵含量均較低。用泡塑進行3次吸附和洗脫,西安熱電廠干灰洗脫率為53%,被泡塑吸附的鎵很大一部分不能被氯化銨洗脫,因此不適于用泡塑法提取鎵;而渭河電廠干灰雖然鎵含量較低,但在相同條件下洗脫率較高,為71.7%,能有效的回收鎵,適于用泡塑法提取鎵。因此選用渭河電廠干灰提取鎵為宜。泡塑可進行多次吸附解析,具有很好的重復利用性。
3 結論
聚氨酯泡沫塑料能夠作為吸附材料,在6 mol/L的鹽酸溶液中可有效吸附鎵,吸附的鎵可用0.5 mol/L NH4Cl溶液定量洗脫。
[1]劉騰.中科鎵英問鼎半導體新材料世界老大[N].財經日報,2002-02-07.
[2]Jung C H,Osako M.Leaching characteristics of rare metal elements and chlorine in fly ash from ash melting plants for metal recovery[J].Waste Management,2009,29(5):1532-1540.
[3]曾青云.從粉煤灰中提取金屬鎵的實驗研究[D].北京:中國地質大學,2007.
[4]李連仲.巖石礦物分析 (第一分冊)[M].3版.北京:地質出版社,1991:29-35,70-80,716-722.

