Fe3O4@NiSiO3磁性納米粒子對剛果紅的吸附性能研究
陳曉影,婁大偉 ,連麗麗,祝 波,任 紅,金 麗,胡 鳳,楊巧玲
(1.吉林化工學院化學與制藥工程學院,吉林吉林 132022;2.吉林大學化學學院,吉林長春 130012)
染料在人們的日常生活中起著非常重要的作用,也推動了我國經濟的迅速發展.天然染料為美化人們生活做出了不可磨滅的貢獻,由于合成染料色澤鮮艷,廉價而逐步取代了天然染料,但是合成染料在印染過程中排放的廢水難以生物降解,并且一些染料中間體是有毒的、致癌的.用常規的方法難以進行污水處理,對環境造成了嚴重的污染.
近年來,磁分離技術已被應用到水處理行業中,它是一種借助磁場力對不同磁性物質進行分離的技術[1].Fe3O4磁性納米粒子因其獨特的磁學特性,在生物醫學領域、環境分析等領域具有廣闊的應用前景,近年來備受關注[2].其具有較高的比表面積,強烈的聚集傾向,可以通過表面修飾降低納米粒子的表面能,得到分散性能良好的功能化磁性納米粒子.同時,適當的表面修飾還可以調節磁性納米粒子的生物相容性和反應特性,從而滿足其在生物技術以及醫學等不同方面的應用需求[3-7].
本文以陰離子染料剛果紅為例,探討了Fe3O4@NiSiO3磁性納米粒子吸附染料剛果紅的動力學和熱力學影響.
1 實驗部分
1.1 儀器與試劑
722可見分光光度計(上海新茂儀器有限公司);甲醇(分析純,天津市永大化學試劑有限公司)
1.2 實驗方法
脫附實驗:稱取適量Fe3O4@NiSiO3磁性納米粒子于反應器中,然后加入50 mL剛果紅濃度為50 mg/L的溶液,待吸附平衡后取出過濾,測定溶液中剛果紅剩余濃度,分析Fe3O4@NiSiO3磁性納米粒子吸附容量,再于60℃條件下烘干后投入50 mL蒸餾水中,同時投加適量甲醇,置于恒溫水浴振蕩器中,適時測定溶液中的剛果紅濃度,計算吸附率.
1.3 Fe3O4@NiSiO3磁性納米粒子的制備
將制得0.10 g Fe3O4@SiO2[8]分散于20 mL 二次水中,將 1 mmolNiSiO4·6H2O、10mmolNH4·Cl加入20 mL的二次水中混合均勻,同時加入1.0 mL28%的NH3·H2O.將以上兩種溶液通過超聲波振動混合均勻轉移到50 mL的水熱合成釜中,在140℃下反應10 h.自然冷卻至室溫,獲得的磁性粒子用去離子水和無水乙醇清洗,烘干即得到Fe3O4@NiSiO3粉末.
2 結果與討論
2.1 吸附動力學
如表1所示,為了深入了解吸附過程的特性,將數據用準一級和準二級動力學模型進行擬合[9-10].其相應線性形態如下:
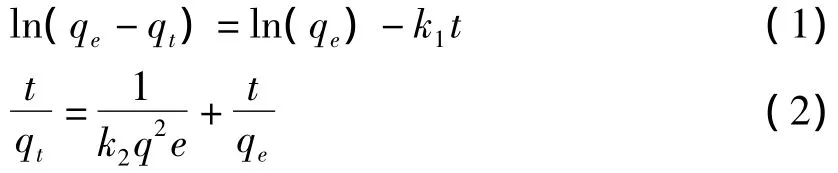
式中,qe(mg/g)與qt(mg/g)分別是平衡時與時間t(min)時單位吸附劑吸附的剛果紅的量.k1(1/min)與k2(g/mg·min)分別是準一級和準二級速度常數.表1給出了準一級和準二級動力學模型擬合的動力學參數和相關系數(R2).可見準二級動力學模型的R2值遠高于準一級動力學模型,而且依據準二級模型計算的qe值(qe,cal)與實驗值(qe,exp)比較接近.
從圖1可以看出,t/qt與t呈很好的線性關系,此類現象比較常見[11-12],原因是在計算準一級模型的各參數之前需要通過實驗確定平衡吸附量qe,而這在實際過程中很難做到.然而準二級方程包含了吸附的所有過程(外部液膜擴散、表面吸附和顆粒內擴散等),可真實、全面地反映剛果紅溶液在固體表面的吸附.
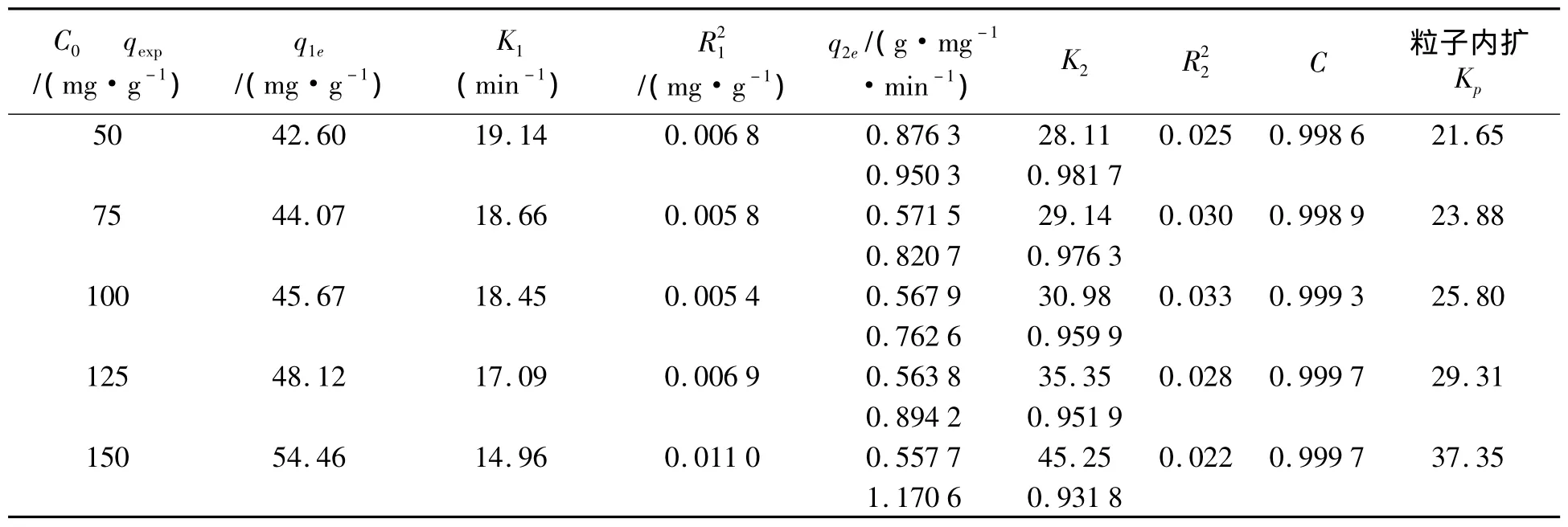
表1 Fe3O4@NiSiO3磁性納米粒子吸附剛果紅溶液的動力學參數
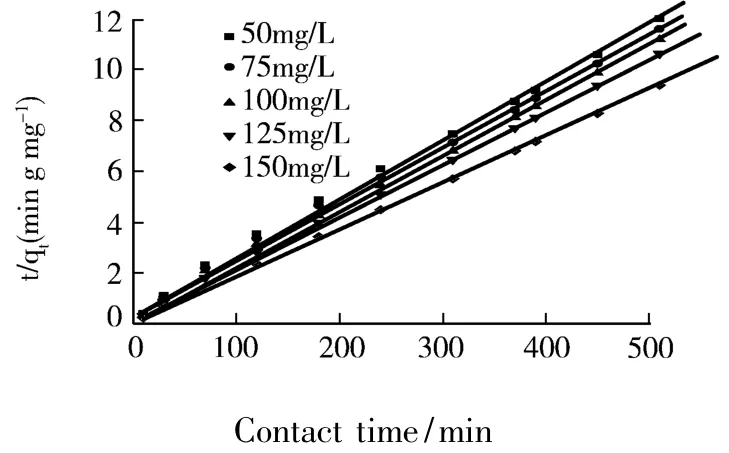
圖1 剛果紅溶液在磁性Fe3O4@NiSiO3上吸附的二級動力學模型
2.2 Weber-Morris動力學模型
為了確定剛果紅溶液在吸附過程中的實際速率控制步驟,采用Weber-Morris方程[13](公式3)對動力學數據進行分析:

式中,ki是粒子內擴散速度常數(mg/g·min1/2),C是反映邊界層效應的常數(mg/g).qt對t1/2的圖形列于圖2,相應的動力學參數列于表1.
圖2出現多線性的圖形,表明吸附過程涉及兩個或兩個以上的步驟[14].初始區域發生的是擴散吸附階段,歸于吸附質跨液膜到吸附劑外表面的擴散(外擴散).第二個區域是漸進的吸附階段,對應于吸附質從吸附劑的外表面到達吸附劑的孔隙或內表面的毛細管擴散(內擴散).因此,外擴散和顆粒內擴散過程共同影響著磁性Fe3O4@NiSiO3對剛果紅溶液的吸附.從圖2也可看出雖然qt對t1/2的回歸為線性,但曲線沒有通過原點,因此,顆粒內擴散并不是唯一的速率限制步驟,而是由外擴散和粒子內擴散共同控制[15].
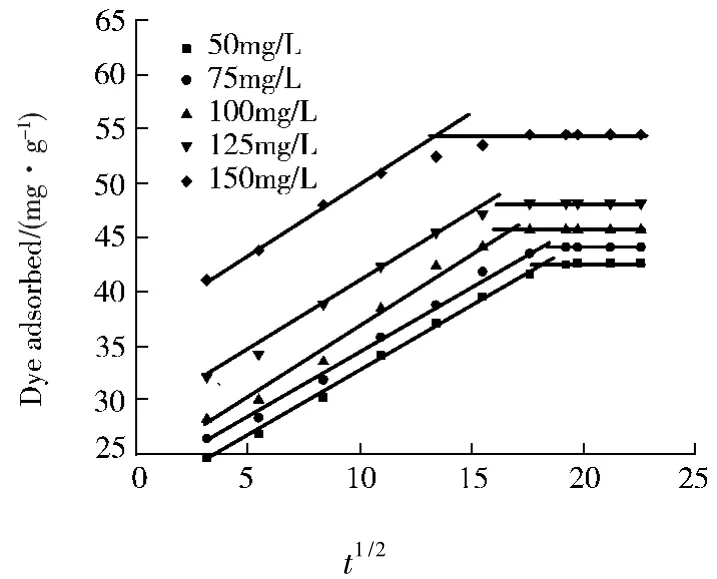
圖2 剛果紅溶液在磁性Fe3O4@NiSiO3上吸附的粒子內擴散圖像
2.3 吸附等溫線
吸附等溫線描述了溶質是如何與吸附劑發生相互作用的,常用Langmuir模型和Freundlich模型描述平衡吸附數據.Langmuir等溫線模型假定吸附表面為均相(所有吸附位點具有相同的吸附親合勢)[16],而 Freundlich等溫線是關于非均相表面的吸附經驗關系式[17].Langmuir與Freundlich吸附等溫線模型表示如下:
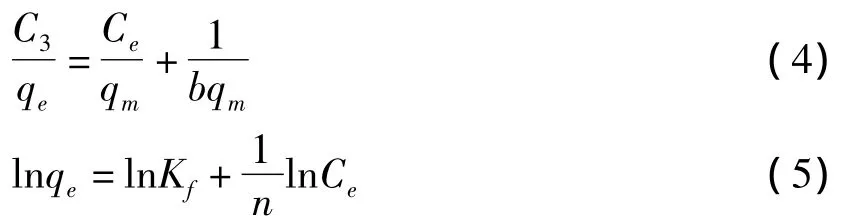
式中,qm是最大的單層吸附容量(mg/g);Ce是甲硝唑的平衡濃度(mg/L);qe是平衡濃度下單位重量的磁性Fe3O4@NiSiO3對剛果紅的吸附量(mg/g);b是Langmuir常數(L/mg),它與結合位點的親和性相關.Freundlich等溫線常數可從溫度293、303、313、323K 下 qe對 Ce的圖形確定;參數Kf是吸附容量的大致指標(L/mg),n是吸附強度(g/L).表2給出了在293K下將吸附平衡數據擬合于 Langmuir和 Freundlich模型得到的參數(303、313和323K下的參數值與293K下的參數有類似趨勢,故省略).根據表2中的數據,Freundlich模型的相關系數(R2)位于0.97~0.98之間,明顯大于Langmuir模型的R2值.所以Freundlich模型比Langmuir模型更好地描述了剛果紅在磁性Fe3O4@NiSiO3上的吸附.對于等溫過程,Langmuir模型傾向于描述單分子層吸附,即每個吸附位點只吸附一個吸附質微粒,當所有吸附位置都被占據后就達到動態吸附平衡.由此可推斷水中剛果紅在磁性Fe3O4@NiSiO3上的吸附機理并不傾向于單分子層吸附,而是涉及到更為復雜的吸附機理.在Freundlich模型中,常數n與吸附推動力的強弱有關.

表2 剛果紅溶液在磁性Fe3O4@NiSiO3上的吸附等溫線參數
分離因子式(6)是一個與Langmuir等溫線基本特性有關的無量綱的常數,

式中,C0是吸附質的最大初始濃度(mg/L),b(L/mg)是 Langmuir吸附常數.在 293、303、313 和323K下,對應的RL值都介于0到1之間,表明剛果紅的吸附是有利的.RL值反映吸附等溫線的形狀,表示在給定吸附質的濃度范圍內,某吸附劑對吸附質發生吸附現象的可行性.例如,當RL>1時表示不利于吸附;0<RL<1表示可以進行;RL=1表示吸附過程是線性的;而RL=0表示吸附過程是不可逆的.
2.4 吸附熱力學
從下列方程式計算熱力學參數:

式中,R是普適氣體常數(8.314 J/mol·K),T 是熱力學溫度(K),Kc是分布系數.吸附過程的吉布斯自由能變量(⊿G0)可由不同溫度下的lnKc值計算,而Kc值則由以下方程式計算:


根據方程式(9),將lnKc對1/T繪圖得到圖3,由其得直線的斜率與截距分別計算出⊿H0和⊿S0參數.
式中,Ce是吸附平衡狀態下的吸附質的濃度;qe是在平衡濃度下單位量的Fe3O4@NiSiO3吸附剛果紅溶液的質量(mg/g).吸附過程的焓變量(⊿H0)和熵變量(⊿S0)由以下方程式計算:
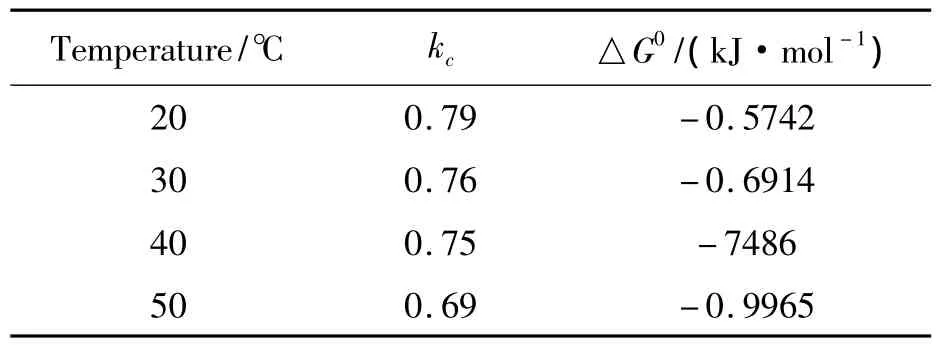
表3 不同溫度下磁性Fe3O4@NiSiO3對吸附剛果紅溶液的熱力學參數
熱力學參數列在表3中.ΔG0是負值,表明反應是自發的過程.當焓變值在 -20 kJ/mol到40 kJ/mol之間是物理吸附,當焓變值在-400 kJ/mol與-80 kJ/mol之間是化學吸附.ΔH0(12.92 kJ/mol)說明吸附是吸熱的,并且為物理吸附.ΔS0(32.91 KJ/mol/K)為正,說明反應是不可逆的,解吸不易發生.
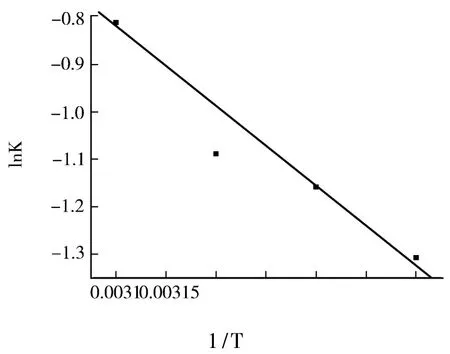
圖3 Fe3O4@NiSiO3吸附剛果紅的熱力學模型
2.5 脫附實驗
Fe3O4@NiSiO3磁性納米粒子吸附染料剛果紅的再生性能很好.如表4所示,前十次的吸附率均為90.00%以上.

表4 Fe3O4@NiSiO3磁性納米粒子吸附染料剛果紅的再生性能
4 結 論
(1)動力學研究表明,吸附過程服從準二級模型,吸附的總體速度受到外質量傳遞和粒子內擴散二者的影響.
(2)熱力學研究表明,吸附過程是自發的吸熱反應,是不可逆的物理吸附反應.
(3)脫附實驗表明Fe3O4@NiSiO3磁性納米粒子有很好的再生性能.
[1] 王鳳平.磁性納米粒子的研究進展[J].納米科技,2010.4.
[2] 熊雷.Fe304磁性納米粒子表面修飾研究進展[J].材料導報,2008.5.
[3] 李玉寶.納米生物醫藥材料[M].北京:化學工業出版社,2004.141.
[4] Liong M,Lu J,Kovochich M,Xia T,Ruehm SG,Nel A,et al.Multifunctional inorganic nanoparticles for imaging,targeting,and drug delivery[J].ACS Nano.2008,2(8):89-96.
[5] Sen T,Sebastianelli A,Bruce IJ.Mesoporous silicamagnetite nanocomposite:fabrication and applications in magnetic bioseparations[J].J Am Chem Soc,2006,128(7):130-131.
[6] Deng YH,Qi DW,Deng CH,Zhang XM,Zhao DY.Superparamagnetic highmagnetization microspheres with an Fe3O4@SiO2core and perpendicularly aligned mesoporous SiO2shell for removal of microcystins[J].J Am Chem Soc,2008,130:28-29.
[7] Liu J,Sun ZK,Deng YH,Zou Y,Li CY,Guo XH,et al.Highly water-dispersible biocompatible magnetite particles with low cytotoxicity stabilized by citrate groups[J].Angew Chem Int Ed 2009,48:5875-5879.
[8] Z.Y.Ma,Y.P.Guan,H.Z.Liu,J.Magn.Magn[J].Mater.2006,301:469-477.
[9] Zhang,L.W.;Petersen E.J.;Zhang W.;Chen Y.S.;Cabrera M.;Huang Q.G[J].Environ.Pollut.,2012,166-75.
[10] Saleh,T.A.;Agarwal,S.;Gupta,V.K[J].Appl.Catal.,B:Environmental,2011,106:46.
[11] Fasfous,I.I.;Radwan,E.S.;Dawoud,J.N[J].Appl.Surf.Sci.2010,256:7246.
[12] Arasteh,R.Masoumi,M.Rashidi,A.M.Moradi,L.Samimi,V.Mostafavi,S.T[J].Appl.Surf.
[13] Shi Y.;Kong,X.Z.;Zhang,C.M.;Chen,Y.M.;Hua,Y.F.Chem.Eng.J.2013,113:215-216.
[14] Chen,G.C.;Shan,X.Q.;Zhou,Y.Q.;Shen,X.E.;Huang,H.L.;Khan,S.U.J.Hazard[J].Master.,2009,169:912.
[15] Badriya,A.R.;Chedly,T.;Nidal,H.Chem.Eng.J[J].2012,183:294.
[16] Zhang,P.K.;Li,W.Sep.Purif[J].Technol.,2010,70:367.
[17] Gautham,P.J.;Clement,T.P.J[J].Contam.Hydrol.,2012,46:129-130.

