芬太尼椎管內麻醉的鎮痛效果及錐體外系反應的臨床研究
馬 瑾,徐繼淵,尹 翠
0 引言
芬太尼為阿片類受體激動劑,屬強效的麻醉性鎮痛藥,其作用機制尚不清楚。可能是通過阿片受體作用于中樞神經系統內而起效。阿片類藥可選擇性地抑制某些興奮性神經的沖動傳遞,發揮競爭性抑制作用,從而解除對疼痛的感受和伴隨的心理行為反應[1]。但其也會產生一定的副作用。本研究觀察應用芬太尼進行椎管內麻醉產生的錐體外系反應及其作用機制。
1 資料與方法
1.1 一般資料 選擇我院2011年1月至2013年12月擇期手術的患者80例,其中男32例,女48例,年齡18~69歲,平均年齡36.5歲,體重48~73 kg,其中下肢手術18例,腹部手術39例,盆腔手術18例,淺表腫塊切除術5例。術前患者均檢查肝腎功能、凝血指標,均無異常。所有納入研究的患者均無嚴重高血壓,24 h內均未使用過非甾體類鎮痛藥物,無長期或正在使用麻醉性鎮痛藥物及其他精神類藥品。術前隨機將80例患者分為A、B兩組,每組40例,兩組患者的性別、年齡、體重差異均無統計學意義(P>0.05)。
1.2 方法 所有患者術前需禁食8 h以上、禁飲4 h,均不使用術前用藥。患者進入手術室后開放外周靜脈通路,常規監測血壓、脈搏、血氧飽和度(SpO2)及心電圖,并給予鼻導管吸氧3 L/min。根據手術部位選擇行蛛網膜下隙阻滯、硬膜外間隙阻滯或腰硬聯合阻滯。A組患者使用0.5%左旋布比卡因對其進行麻醉,A組患者均不使用芬太尼;B組患者在上述用藥基礎上逐次加入芬太尼,單次給藥劑量50 μg進行麻醉,待麻醉平面完善后開始手術。B組患者術后仍使用低劑量芬太尼進行維持鎮痛。
1.3 芬太尼對多巴胺(DA)的影響 對各組患者采取外周血5 mL,離心后提取血清并置于-40 ℃冰箱中待測。血清中DA含量采用高效液相熒光法測定。
1.4 術后評價 術后從患者清醒開始計時,分別于5 min(T1)、10 min(T2)、20 min(T3)、30 min(T4)、60 min(T5)記錄患者一般情況,如血壓、呼吸、心率,并注意有無錐體外系反應,生理病理反射是否存在。術后鎮痛效果評價:采用視覺模擬評分法(VAS法)[2]對術后患者進行評分,無痛者評為0分,輕度疼痛者評為1~3分,中度疼痛者評為4~7分,劇烈疼痛者評為8~10分。
1.5 統計學分析 采用SPSS 19.0統計軟件進行統計學分析,組間比較采用兩獨立樣本資料的Z檢驗,組內比較采用方差分析,P<0.05 為差異有統計學意義。
2 結果
2.1 術后1 h兩組鎮痛效果比較 術后1 h兩組鎮痛效果比較差異有統計學意義(P<0.05),見表1。

表1 術后1 h兩組鎮痛效果比較
2.2 兩組患者術后各時間段一般情況比較 兩組患者術后T1、T2、T3、T4、T5時刻平均動脈壓、呼吸、心率比較差異均有統計學意義,見表2。
2.3 兩組術后錐體外系反應及病理生理反射情況 A組發生并發癥1例,表現為乏力、嗜睡,1例患者出現病理反射;B組3例發生錐體外系反應,表現為精神緊張、呼吸急促、肌肉震顫、肌張力增高等;2例患者生理反射消失,3例患者出現病理反射。芬太尼導致錐體外系反應的發生率為7.5%。見表3。
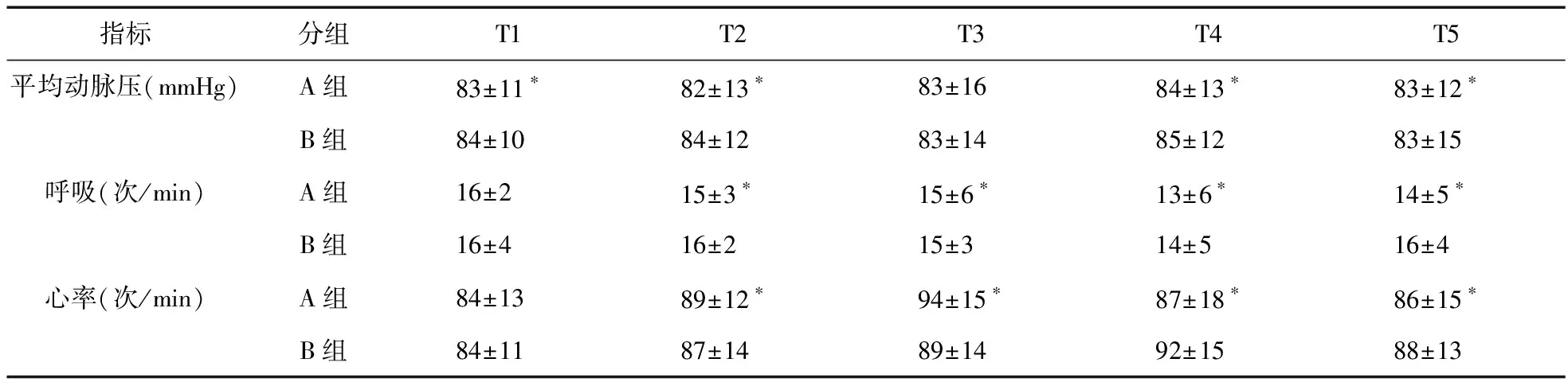
表2 兩組患者術后各時間段一般情況比較

表3 兩組患者術后發生椎體外系反應及病理生理反射情況(例)
2.4 對血清DA的影響 筆者曾進行過的動物實驗發現,病態下以及發生錐體外系反應時,血清中DA受體的表達明顯上升,差異有統計學意義(P<0.05)。見表4。
3 討論
術中及術后使用芬太尼進行鎮痛時,可減輕術后患者的疼痛感覺;使用芬太尼可導致錐體外系反應的發生,但發生率較低,本次研究顯示其發生率為7.5%。其作用機制可能為芬太尼透過硬脊膜和蛛網膜(或直接注入蛛網膜下間隙),并在腦脊液中擴散,隨后彌散透過軟脊膜,到達脊髓表面,最后與脊髓背角的阿片受體結合,以致達到鎮痛效應。

表4 不同實驗組別動物模型DA受體表達情況比較(例)
椎管內麻醉是指將藥物注入椎管內的某一腔隙,可逆性阻斷或減弱脊神經傳導功能或興奮性的一種麻醉方法[3]。椎管內麻醉主要是阻斷脊神經根。椎管內麻醉主要包括硬脊膜外腔阻滯、蛛網膜下腔阻滯及腰硬聯合阻滯[4]。硬脊膜外腔阻滯具有術后恢復快、并發癥少、對呼吸循環系統干擾少等優點,但因老年人對藥物的起效時間較短,阻滯平面較寬,故應用于老年人時需減少麻醉藥物用量或采用小劑量粉刺給藥以達到安全穩定的目的。然而蛛網膜下腔阻滯具有麻醉起效快、短時間內即可固定麻醉平面的優點,一旦達到麻醉效果,只需靜脈追加全麻藥物完成手術即可,但此麻醉對呼吸循環系統的影響較大,倘若手術時間過長,較難控制,并且蛛網膜下腔阻滯后患者可能出現術后嚴重頭痛,這是蛛網膜下腔阻滯術后患者最感痛苦的并發癥。相關文獻報道[5-6],硬膜外麻醉和蛛網膜下腔阻滯不僅具有抑制應激反應的作用,而且還能穩定血液動力學,減少術中出血并降低術后血栓栓塞的發生率。硬膜外麻醉聯合腰麻兼有腰麻和硬膜外麻醉的雙重特點,是一種新發展的麻醉技術,適合用于下肢手術的麻醉[7]。但椎管內麻醉仍存在一定的并發癥[8]:①患者可出現局麻藥的全身毒性反應,主要表現為中樞神經系統和心腦血管系統毒性。②患者可出現低血壓、蕁麻疹、支氣管痙攣、咽喉水腫以及血管神經性水腫等局麻藥物過敏反應。③患者還可出現短暫性神經綜合征、感染、惡心、嘔吐、尿潴留等不良反應。發生椎管內麻醉意外的原因主要包括人為因素,例如麻醉師穿刺手法不準確,穿刺技術不夠熟練,操作不夠規范,消毒不完善;此外,行硬膜外麻醉時,誤入蛛網膜下腔可引起較嚴重的后果;另外,患者自身原因也可導致椎管內麻醉意外的發生,例如患者不能很好地配合,對于一些老年患者,還可能因為韌帶鈣化、骨質增生等導致的硬膜外間隙難于尋找,從而影響麻醉效果。
芬太尼為作用于中樞神經系統的鎮痛藥,其作用機制與嗎啡相似,亦有成癮性,但其作用速度較嗎啡快,作用強度也較嗎啡強,是嗎啡的60~80倍,但芬太尼使用后不釋放組胺,故對心血管功能的影響相對較小,也可以對氣管插管時的應激反應進行抑制。芬太尼對呼吸的抑制作用雖然較嗎啡弱,但若不掌握好靜脈注射的速度,也可出現不良反應。一般不良反應與嗎啡相似,可出現眩暈、惡心、嘔吐等癥狀;若長期使用可產生一定的藥物依賴性,但成癮性較嗎啡弱;另外,若大劑量使用或靜脈注射過快也可產生胸壁肌強直,從而出現呼吸抑制或延遲性呼吸抑制的顯像。該癥狀可通過應用納洛酮或肌松藥物對其產生的呼吸抑制進行拮抗[9]。
錐體外系是人體運動系統的重要組成部分之一,其主要功能是調節肌張力、維持軀體的運動姿勢,協調肌肉的運動及保持平衡。這種調節功能主要依賴于中樞神經遞質DA及乙酰膽堿之間的動態平衡,當各種原因造成DA減少或乙酰膽堿增多時,就會出現肌張力增高、動作遲緩、流涎、面容呆板、肌肉震顫、靜坐不能、反復徘徊等帕金森綜合征樣的癥狀;出現強迫性張口、伸舌、呼吸運動障礙、斜頸及吞咽困難等急性肌張力障礙的表現[10-11]。本研究未使用芬太尼的A組40例患者術中及術后均未發生錐體外系反應;使用芬太尼的B組40例患者,在術中未發現錐體外系反應,在術后使用芬太尼維持鎮痛時,有3例患者出現精神緊張、呼吸急促、肌肉震顫、肌張力增高的表現,該組使用芬太尼術后錐體外系反應的發生率為7.5%,芬太尼在椎管內致錐體外系反應的主要原因可能是由于引起患者腦部DA受體高表達引起。
參考文獻:
[1] 劉新偉,郭艷巍.芬太尼與地佐辛對老年骨科病人術后鎮痛效果的對比[J].中國老年學雜志,2011,31(22):4465-4466.
[2] 付蓮英,段淑云,萬水珍.視覺模擬評分法在病人滿意度調查中的應用[J].中國護理管理,2008,8(9):68-69.
[3] 王佩,許睿,李樂,等.椎管內麻醉后產婦神經損傷的調查及相關原因分析[J].實用醫學雜志,2013,29(24):4113-4115.
[4] 孫勝,岳利民,董玉貴,等.微創化椎管內麻醉的研究進展[J].河北醫藥,2012,34(9):1387-1388.
[5] 周紅梅,周清河,肖旺頻.硬膜外阻滯聯合全麻對老年腹部手術應激反應的影響[J].中國中西醫結合外科雜志.2011,17(3):254-257.
[6] 劉奕君.地佐辛與芬太尼用于瑞芬太尼靜脈麻醉后痛覺過敏的比較[J].實用藥物與臨床,2012,15(10):647-649.
[7] 喬飛,展希,汪珺.舒芬太尼復合咪達唑侖輔助椎管內麻醉效果評價[J].實用藥物與臨床,2011,14(5):386-388.
[8] Espinosa-Aguilar M,Hernández-Palazón J,Fuentes-García D.Intraspinal and intracranial subarachnoid haemorrhage with severe cerebral vasospasm after spinal anaesthesia for assisted delivery[J].British Journal of Anaesthesia,2012,108(5):885-886.
[9] Matsuki Y,Mizogami M,Tabata M,et al.Suspected respiratory depression associated with use of a transdermal fentanyl patch[J].Pain Physician,2012,15:E533-E540.
[10]王桂龍,王志萍.超前應用曲馬多聯合小劑量芬太尼防治全麻蘇醒期躁動的臨床觀察[J].實用藥物與臨床,2012,15(4):213-215.
[11]Baldessarini RJ,Gardner DM.Incidence of extrapyramidal syndromes and tardive dyskinesia[J].Journal of Clinical Psychopharmacology,2011,31(3):382-384

